固体酸催化淀粉一锅法制备果葡糖浆的研究
2016-12-13陈晖晖蒋叶涛
陈晖晖, 蒋叶涛, 孙 勇, 林 鹿
(厦门大学 能源学院, 福建 厦门 361102)
·研究报告——生物质化学品·
固体酸催化淀粉一锅法制备果葡糖浆的研究
陈晖晖, 蒋叶涛, 孙 勇*, 林 鹿
(厦门大学 能源学院, 福建 厦门 361102)


果糖是葡萄糖的同分异构体,主要存在于水果浆汁和蜂蜜中,是一种天然的甜味剂,其作为甜味剂具有蔗糖不可比拟的性能优势,不仅甜味强且纯正,而且有营养、无毒副作用。另外果糖也是制备高附加值化学品最活跃的原料之一[1],如5-羟甲基糠醛(HMF)[2-4]、乙酰丙酸(LA)及其衍生高附加值化学品[5-7]。大量研究表明,酮糖(果糖)比醛糖(葡萄糖)更易转化为HMF和LA[2],效率更高,选择性更好[1]。果糖有着广泛的食品和工业需求,但是果糖在自然界中的储量远不如葡萄糖丰富。目前生产果糖的主要方法是酶法和化学法。果糖的工业酶法生产主要有2种,一种是以蔗糖为原料生产果糖,蔗糖是由葡萄糖和果糖通过糖苷键连接的双糖,在酸或蔗糖转化酶的催化作用下能转化为葡萄糖和果糖,可分离得到果糖;另一种方法是以淀粉为原料,先将淀粉水解成葡萄糖,再经过固定化葡萄糖异构酶将葡萄糖异构化为果糖,得到混合着约58 %葡萄糖和42 %果糖的糖液,即为果葡糖浆(HFS)。果葡糖浆经色谱分离纯化,其中果糖含量可超过90 %,最后通过结晶工艺可产出结晶果糖[8]。虽然酶法反应条件温和、具有较高的专一性和反应活性,可以制得高纯度的果糖,但是酶价格昂贵,反应体系中的温度、 pH值和底物浓度都需要严格的控制,否则酶就容易变性失活[9-10]。为了弥补酶法的不足,放宽反应条件,使反应能在较高温度下进行以提高反应效率,越来越多的研究者致力于开发出绿色清洁、廉价高效的化学催化剂。淀粉先在酸催化作用下水解为葡萄糖,葡萄糖再通过酸或碱催化异构为果糖,而直接将淀粉转化为果糖的研究少有报道。研制能够直接将淀粉转化为果糖的催化剂是制备果糖的一个重要研究方向,而制得果葡糖浆就意味着制得了果糖,因此可以转而研究淀粉一步法制备果葡糖浆的催化剂,用于高效催化淀粉制备果糖。分子筛具有较大的比表面积、开放的三维孔道结构和优良的水热稳定性、能经受苛刻的再生条件,是常见的催化剂载体。本研究以超稳Y型分子筛(USY)等几种不同分子筛以及SiO2和硅胶负载硫酸,制备了负载型固体酸催化剂,用于淀粉一步转化制备果葡糖浆,比较了几种催化剂的催化效果;主要探讨了USY负载硫酸型固体酸催化剂催化淀粉转化为果葡糖浆的效果,以期为淀粉制备果葡糖浆提供一条新的途径。
1 实 验
1.1 原料、试剂与仪器
可溶性淀粉,红薯淀粉,厦门市绿茵试剂玻仪有限公司;硫酸,分析纯;SiO2、硅胶、超纯水。USY分子筛(含0.05 % Na2O)、 Hβ分子筛(硅铝物质的量比50)、 MCM-41分子筛,南开大学催化剂厂。
Parr 4848高压反应釜,美国Parr公司;Waters 2695高效液相色谱仪,美国Waters公司;理学Ultima IV X射线衍射仪,日本理学公司;ASAP-2020物理吸附仪,美国Micromeritics公司;Auto chem II 2920化学吸附仪,美国Micromeritics公司;Vario EL III元素分析仪,德国Elementar公司;0.22 μm有机滤膜,上海市新亚净水器件厂。
1.2 负载硫酸型固体酸的制备

1.3 固体酸催化淀粉制备果葡糖浆
将1.5 g淀粉、 30 g去离子水和一定量的催化剂加入到50 mL高压反应釜中,密封加热到目标温度,搅拌速度为400 r/min,开始反应;一段时间后,迅速冷却至室温,过滤分离得到液体产物和固体催化剂。液体产物经0.22 μm有机滤膜过滤后,用高效液相色谱仪分析;固体催化剂用去离子水反复清洗,干燥,400 ℃焙烧3 h,去除可能残留的淀粉和杂质,置于干燥器内备用。
1.4 产物分析及计算
产物采用HPLC进行分析,检测器为Waters 2414 RID,色谱柱为Bio-Rad Aminex HPX-87H,工作站为EmpowerTM3,流动相为5 mmol/L H2SO4,流动相速度0.6 mL/min,检测器温度30 ℃,柱温50 ℃,进样量10 μL,以外标法作为分析方法。
葡萄糖、果糖、 5-羟甲基糠醛(HMF)的得率分别以生成的葡萄糖、果糖、HMF的质量除以原料淀粉的质量乘以100 %计算得到。
1.5 催化剂的表征
1.5.1 XRD分析 采用X射线衍射仪分析,入射光源为Cu靶 (λ=0.154 06 nm),扫描范围5~70°,扫描速度10(°)/min,管电压40 kV,管电流40 mA。
1.5.2 物理吸附表征 在物理吸附仪上,采用N2静态吸附容量法测定比表面积和孔结构。吸附温度为液氮温度,样品吸附前在363 K下脱气1 h,623 K下脱气4 h。
1.5.3 程序升温脱附(TPD)表征 在化学吸附仪上,采用NH3程序升温脱附测定催化剂的表面酸性,载气为He,载气流速25 mL/min,检测器为TCD,桥电流150 mA,升温速率20 ℃/min,吸附温度120 ℃。
1.5.4 元素分析 催化剂的碳和硫元素组成采用元素分析仪进行测定。
2 结果与分析
2.1 催化剂及其制备条件对果葡糖浆得率的影响
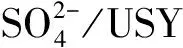
表 1 不同分子筛催化淀粉制备果葡糖浆

图 1 固体酸催化淀粉水解异构机理图

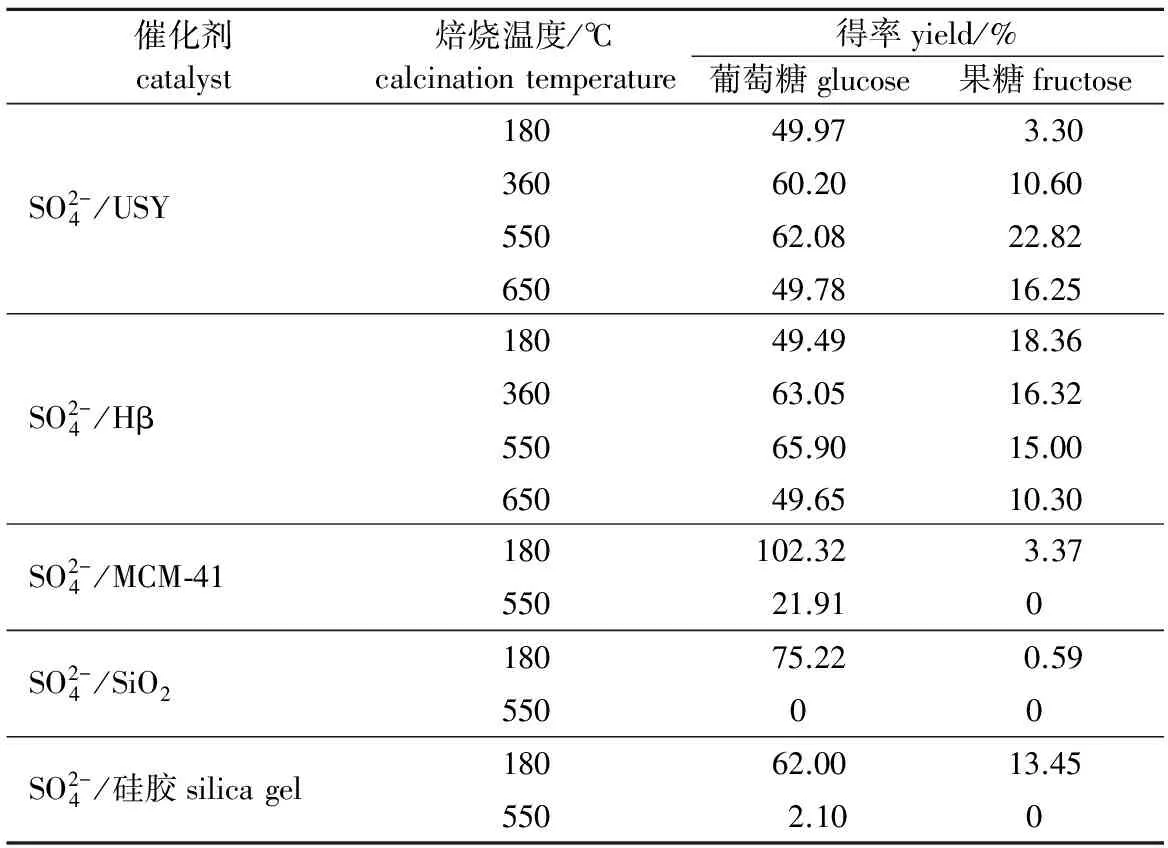
表 2 不同焙烧温度制备的催化剂对产物得率的影响
2.1.3 硫酸浓度 硫酸负载量也是影响果葡糖浆得率的重要因素之一。反应条件同2.1.1节,分别考察USY在浓度为0.5、 1.0、 1.5、 2.0和2.5 mol/L硫酸溶液中浸渍负载,在550 ℃焙烧温度下制备得到的催化剂的催化效果,结果如图2所示。可以看出硫酸负载量少时葡萄糖得率较高,但果糖得率不高。而负载量太高,会造成果糖继续催化降解为副产物如5-羟甲基糠醛(HMF),果葡糖浆得率(葡萄糖得率和果糖得率之和,下同)也不理想。USY在浓度为1.5 mol/L的硫酸溶液中进行负载制备的催化剂,果葡糖浆得率较高,为86.18 %,其中含58.34 %的葡萄糖和27.84 %果糖。
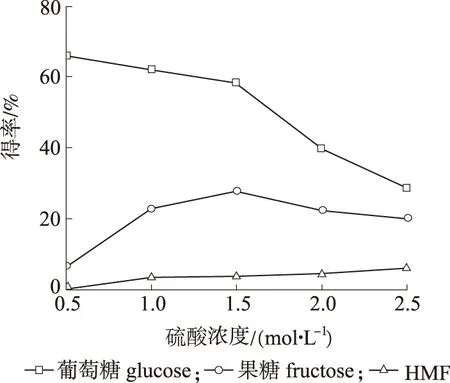
图 2 硫酸浓度对果葡糖浆得率的影响
2.2 反应条件对果葡糖浆得率的影响

图 3 反应温度对果葡糖浆得率的影响

图 4 反应时间对果葡糖浆得率的影响

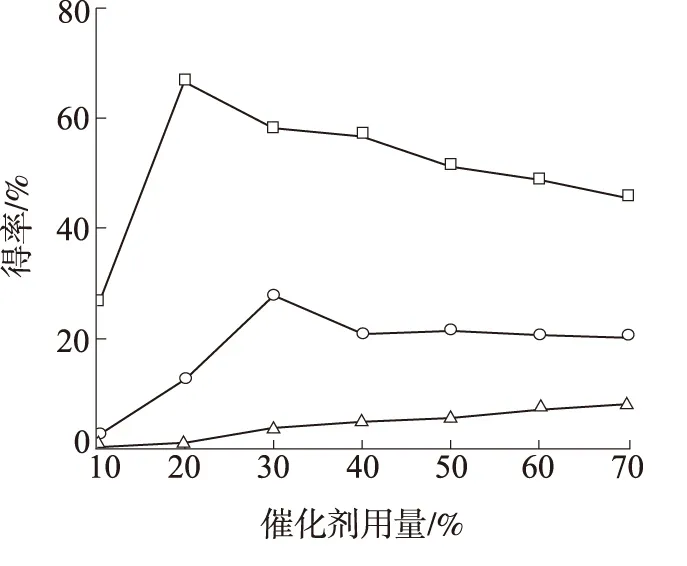
图 5 催化剂用量对果葡糖浆得率的影响Fig. 5 Effect of catalyst amount on HFS yield
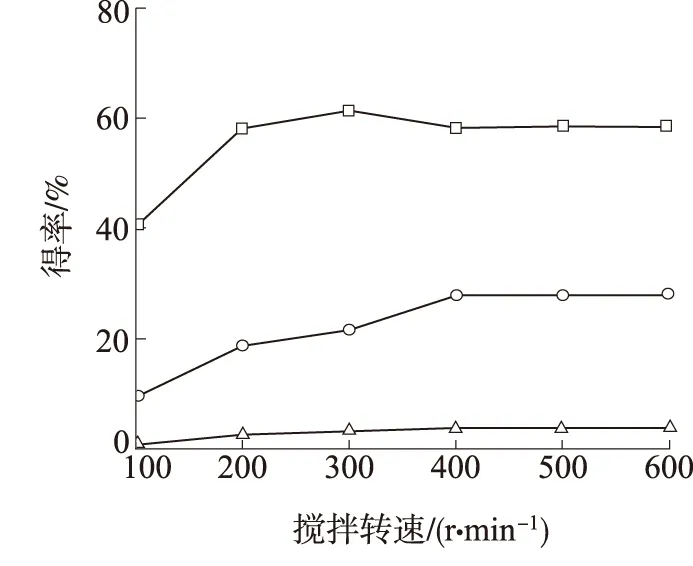
图 6 搅拌转速对果葡糖浆得率的影响Fig. 6 Effect of stirring rate on HFS yield

2.3 催化剂的重复使用性能
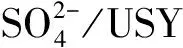
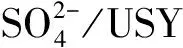
表 3 未焙烧、焙烧和简单活化的催化剂重复使用次数对果葡糖浆得率的影响
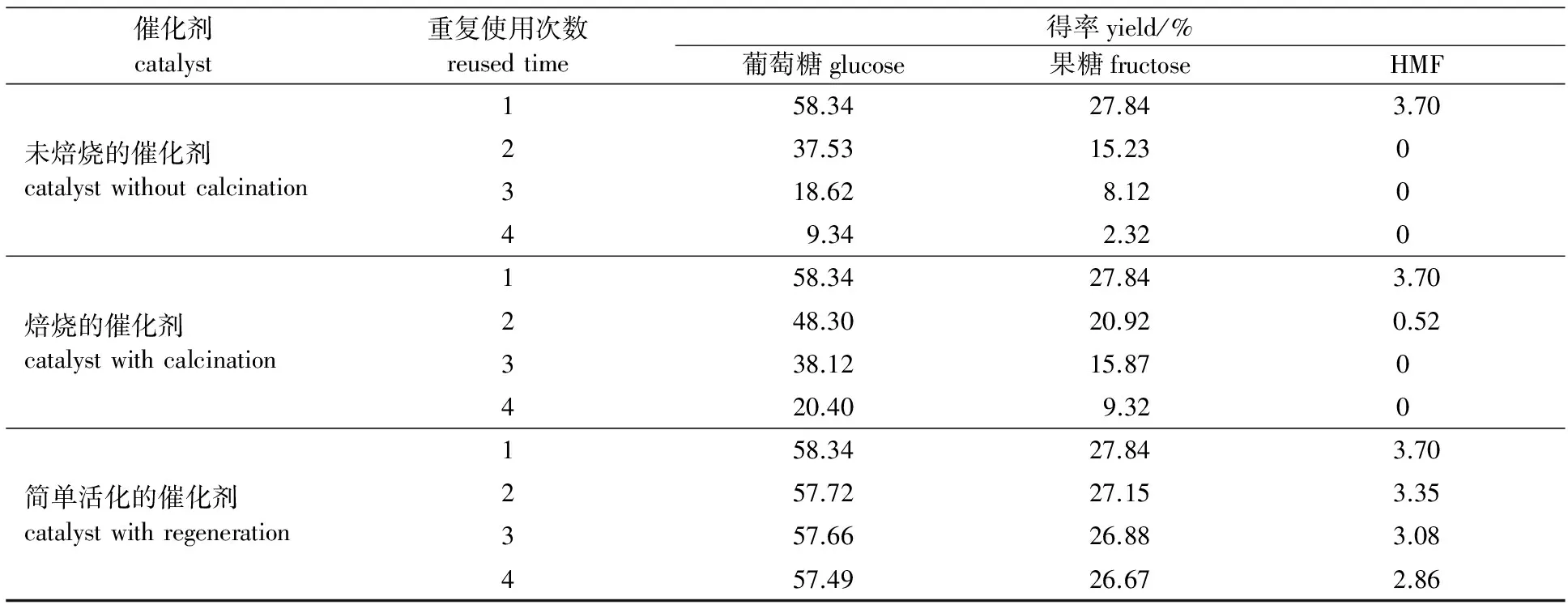
calcination and regeneration on the HFS yield
2.4 USY负载型催化剂的表征
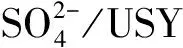
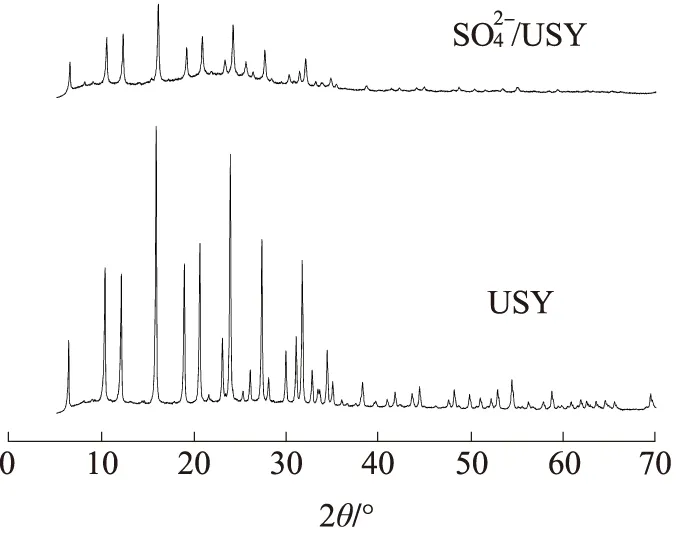
图 7 不同样品的XRD 谱图
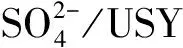
表 4 不同样品的比表面积和孔体积分析
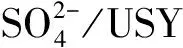

图 8 样品的NH3程序升温脱附曲线
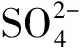
表 5 回收催化剂中碳硫元素含量

重复使用次数reusedtime碳元素carbon/%未焙烧withoutcalcination焙烧withcalcination简单活化withregeneration硫元素sulfur/%未焙烧withoutcalcination焙烧withcalcination简单活化withregeneration10.080.080.083.023.023.0220.890.060.062.422.212.9631.770.070.081.741.242.9042.960.060.050.920.682.85
3 结 论
[1]CORMA A,IBORRA S,VELTY A. Chemical routes for the transformation of biomass into chemicals[J]. Chemical Reviews,2007,38(36):2411-2414.
[2]TAKAGAKI A,OHARA M,NISHIMURA S,et al. A one-pot reaction for biorefinery:Combination of solid acid and base catalysts for direct production of 5-hydroxymethylfurfural from saccharides[J]. Chemical Communications,2009,210(41):6276-6278.
[3]TAKAGAKI A,TAKAHASHI M,NISHIMURA S,et al. One-pot synthesis of 2,5-diformylfuran from carbohydrate derivatives by sulfonated resin and hydrotalcite-supported ruthenium catalysts[J]. ACS Catalysis,2011,1(11):1562-1565.
[4]REN Qiu-he,HUANG Yi-zheng,MA Hong,et al. Conversion of glucose to 5-hydroxymethylfurfural catalyzed by metal halide in N,N-dimethylacetamide[J]. BioResources,2013,8(2):1563-1572.
[5]MEHDI H,FABOS V,TUBA R,et al. Integration of homogeneous and heterogeneous catalytic processes for a multi-step conversion of biomass:From sucrose to levulinic acid,γ-valerolactone,1,4-pentanediol,2-methyl-tetrahydrofuran,and alkanes[J]. Topics in Catalysis,2008,48(1/2/3/4):49-54.
[6]ZHANG Jun,WU Shu-bin,LI Bo. Advances in the catalytic production of valuable levulinic acid derivatives[J]. ChemCatChem,2012,4(9):1230-1237.
[7]SON P A,NISHIMURA S,EBITANI K. Synthesis of levulinic acid from fructose using Amberlyst-15 as a solid acid catalyst[J]. Reaction Kinetics,Mechanisms and Catalysis,2012,106(1):185-192.
[8]BUCHHOLZ K,SEIBEL J. Industrial carbohydrate biotransformations[J]. Carbohydrate Research,2008,343(12):1966-1970.
[9]YAN Z,HIDAJAT K,RAY A K. Optimal design and operation of SMB bioreactor:Production of high fructose syrup by isomerization of glucose[J]. Biochemical Engineering Journal,2004,21(2):111-121.
[10]FILHO F F. Handbook of food enzymology[J]. Revista Brasileira De Ciências Farmacêuticas,2004,40(2):269.
[11]ZHAO Jun,WANG Geng-geng,QIN Li-hong,et al. Synthesis and catalytic cracking performance of mesoporous zeolite Y[J]. Catalysis Communications,2016,73(2):98-102.
[12]ZHAO Jun,YIN Yan-chao,LI Yang,et al. Synthesis and characterization of mesoporous zeolite Y by using block copolymers as templates[J]. Chemical Engineering Journal,2016,284(1):405-411.
[13]TESTOVA N V,PAUKSHTIS E A,IONE K G. Some peculiarities in synthesis of nitrogen-containing heterocyclic compounds on zeolite catalysts[J]. Reaction Kinetics & Catalysis Letters,1991,44(1):243-249.
[14]QIAN Xiang-hong. Mechanisms and energetics for brønsted acid-catalyzed glucose condensation,dehydration and isomerization reactions[J]. Topics in Catalysis,2012,55(3/4):218-226.
[15]ANTAL M J,LEESOMBOON T,MOK W S,et al. Mechanism of formation of 2-furaldehyde fromD-xylose[J]. Carbohydrate Research,1991,217(2):71-85.
[16]ANTAL M J,MOK W S,RICHARDS G N. Mechanism of formation of 5-(hydroxymethyl)-2-furaldehyde fromD-fructose and sucrose[J]. Carbohydrate Research,1990,199(1):91-109.
[17]CHHEDA J N,ROMN-LESHKOV Y,DUMESIC J A. Production of 5-hydroxymethylfurfural and furfural by dehydration of biomass-derived mono- and poly-saccharides[J]. Green Chemistry,2007,9(4):342-350.
[18]周硼. 硫酸衍生固体酸—负载型硫酸及其盐和磺酸树脂催化性能的研究[D]. 大连:大连理工大学博士学位论文,2003.
One-pot Preparation of High Fructose Syrup Directly from Starch over Solid Acid Catalyst
CHEN Hui-hui, JIANG Ye-tao, SUN Yong, LIN Lu
(College of Energy,Xiamen University, Xiamen 361102, China)

2016-03-24
福建省自然科学基金(2016J01077);厦门大学校长基金(20720160087)
陈晖晖(1988— ),女,福建福鼎人,硕士生,从事生物质化学转化的研究;E-mail:864271545@qq.com
*通讯作者:孙 勇(1979— ),副教授,博士,从事生物炼制和生物能源化学的研究;E-mail:sunyong@xmu.edu.cn。
10.3969/j.issn.1673-5854.2016.06.004
TQ35
A
1673-5854(2016)06-0023-09
