癌抗原15-3酶促化学发光免疫分析方法的建立
2016-12-10程缤雁
程缤雁
(北京北方生物技术研究所有限公司,北京100076)
癌抗原15-3酶促化学发光免疫分析方法的建立
程缤雁
(北京北方生物技术研究所有限公司,北京100076)
目的 建立癌抗原15-3(CA15-3)酶促化学发光免疫分析方法。方法 利用双抗体夹心法建立CA15-3化学发光检测体系,分别对该体系的最低检测限、线性、分析特异性、准确度和精密度进行评估,并与进口全自动化学发光检测结果进行对比。结果 本方法灵敏度为0.26 U/mL,线性范围为0~300 U/mL,与CEA和CA125无交叉反应,添加回收率在97.0%~105.6%之间,分析内与分析间CV均小于10%,与进口全自动化学发光试剂同时检测160份样本的CA15-3浓度,检测结果的线性相关系数为0.987。结论 成功建立了CA15-3酶促化学发光免疫分析方法。该方法灵敏度高、重复性好,在临床应用中可替代进口化学发光检测试剂。
肿瘤标志物; 癌抗原15-3; 乳腺癌; 酶促化学发光法
癌抗原15-3(CA15-3)是一种粘蛋白型糖蛋白,相对分子质量约为400000,是目前应用最广泛的乳腺癌血清标志物[1]。CA15-3在乳腺癌早期灵敏度不足,阳性率仅为10.1%,随着病情进展灵敏度有所增加[2];发生转移时,70%的患者血清CA15-3会显著增高[3];乳腺癌患者在临床治疗有效的情况下,血清CA15-3测值会降低[4]。检测血清CA15-3浓度,对乳腺癌患者疗效观察和预后估计有重要的意义。酶促化学发光免疫分析方法具有灵敏度高、特异性好、检测范围宽等优点。本工作利用双抗夹心法建立了CA15-3酶促化学发光免疫分析方法,对国内乳腺癌的治疗和检测有重要的意义。
材料和仪器
1 主要仪器
化学发光仪:厦门天中达生物科技有限公司。
2 主要材料与试剂
CA15-3单克隆抗体:Hytest公司产品;辣根过氧化物酶(HRP):Sigma公司产品;化学发光板:NUNC公司产品;去激素血清、小牛血清:天津康源生物技术有限公司产品;血清样本由北京中同蓝博临床检
验所提供。
3 方法
3.1 固相抗体包被板的制备 用0.02mol/L PB(pH 7.4)稀释CA15-3单抗至终浓度为4 μg/mL,100μL/孔加入化学发光板中,置于4℃过夜。次日甩弃包被液,再加入蔗糖封闭液150μL/孔,置于37℃温育。2h后,甩弃封闭液,将包被板自然晾干。
3.2 辣根过氧化物酶标记抗体的制备 参照郭春祥等[5]简易高碘酸钠法制备辣根过氧化物酶(HRP)标记的 CA15-3抗体。将0.5 mg HRP溶于0.25 mL蒸馏水中,向其中缓慢滴加100 μL NaIO4(0.1mol/L)溶液,4℃搅拌20min后在HAc-NaAc缓冲液(1 mmol/L,pH 4.4)中透析过夜。次日,将碳酸缓冲液(0.0 5 mol/L,pH 9.6)透析的 CA15-3单抗缓慢滴加到活化的酶溶液中,室温避光搅拌。2h后,加入50 μL NaBH4中止反应,将溶液在 4℃静置2h后转入透析袋,在磷酸缓冲液(0.02mol/L,pH7.4)中透析过夜。次日取出,加入等体积甘油,分装后在-20℃长期保存。
3.3 校准品的制备 用去激素血清将CA15-3纯品分别稀释为5、20、80、160、300 U/mL。用CA 15-3全自动化学发光试剂盒测定各点浓度,标识为S1~S5,作为CA15-3校准品。1 mL/瓶分装,-20℃冻存。
3.4 分析程序 向CA15-3包被板孔中依次加入150 μL样本稀释液、20 μL校准品或样品,37℃温育30min后用洗涤液冲洗3次并拍干;每孔加入100 μL酶标抗体,37℃温育30min后用洗涤液冲洗3次并拍干;加入100 μL发光底物液,3~10min后测量每孔光子数。以光子数为纵坐标,校准品浓度为横坐标进行双对数作图,拟合校准品曲线方程。将样本的发光计数代入方程,即可计算出样本中CA15-3的浓度。样本稀释液为含20%小牛血清的磷酸盐缓冲液(0.02 mol/L,pH 7.4)。
4 数据分析方法
采用Excel 2003分析。
结 果
1 酶标抗体工作浓度的选择
制备酶标抗体稀释比例分别为1∶10000、 1∶20000、1∶40000、1∶80000的溶液,在包被浓度为4 μg/mL时,观察不同浓度HRP-CA15-3对校准品曲线的影响,结果如图1所示。根据校准品曲线的线性相关系数,选择酶标抗体的工作浓度为1∶20000。
2 包被浓度的选择
制备包被浓度分别为 2μg/mL、4μg/mL、8μg/mL的CA15-3固相抗体板,HRP-CA15-3浓度为1∶20000时,观察不同包被浓度对校准品曲线的影响,结果如图2所示。包被浓度为4 μg/mL和8 μg/ mL时,校准品曲线的线性相关系数均为0.999,以节约原料为原则,选择包被浓度为4 μg/mL。
3 反应条件的确定
3.1 加样量 样本稀释液加样体积为150 μL
时,选取10 μL、20 μL、50 μL校准品加样体积进行对比分析,结果如图3所示。考虑到加样准确性和校准品曲线的线性相关系数,本分析方法选用20 μL校准品,150 μL样本稀释液进行反应。
3.2 反应时间 本分析方法采用两步法,加入稀释液和样本后分别温育0.5h、1h、2h、3h、4h,在第二步温育1h时,对比分析第一步反应温育时间对发光计数的影响。由图4可以看出,第一步反应0.5h即可达到平衡,故选取第一步温育时间为0.5h。在第一步温育0.5h时,加入酶标抗体分别温育0.5h、1h、2h、3h,对比分析第二步温育时间对发光计数的影响。由图5可以看出,第二步反应0.5h也可达到平衡。故本分析方法选取0.5h+0.5h的反应模式,满足了市场快速检测的需求。
4 方法学鉴定
4.1 校准品曲线及最低检测限 同时测定20孔S0,计算其发光计数(RLU)的均值x和标准差s,以x±2s为Y值,代入校准品曲线公式,计算出相对应的浓度值为0.26 U/mL,即为本方法的最低检测限。
4.2 线性 将一份CA15-3高值样本用样本稀释液倍比稀释,测定值如表1所示。稀释度与测定值的相关方程为 Y=1232.9X+5.8,r=0.998,表明本分析方法在0~300 U/mL范围内线性关系良好。样本稀释曲线如图6所示。
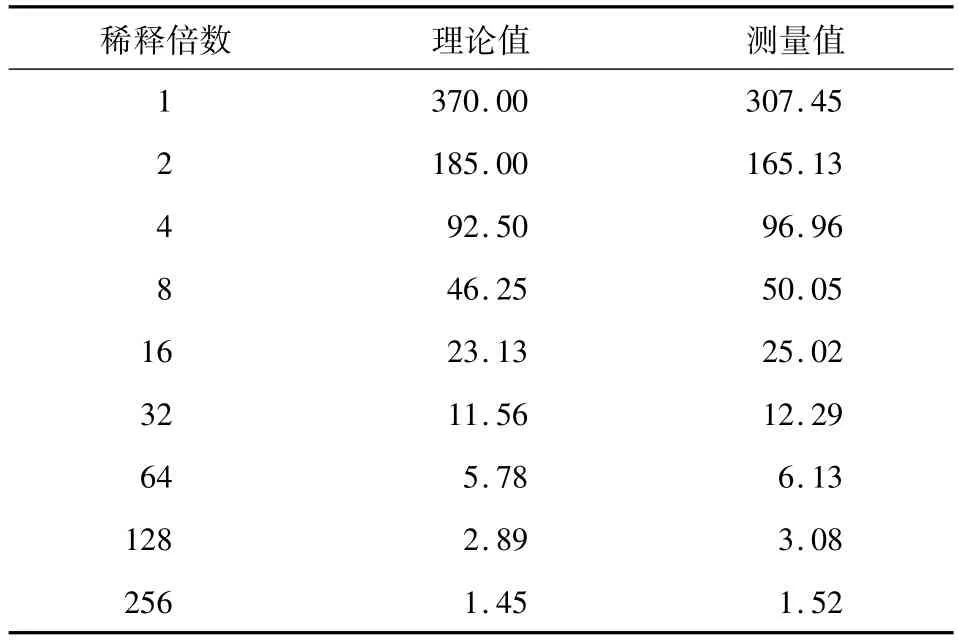
表1 不同稀释倍数血样测定结果(U/mL)
4.3 分析特异性 用去激素血清分别配制浓度为1000 ng/mL的CEA和1000 U/mL的CA125溶液,本方法测定结果分别为0.18 U/mL和0.22 U/mL。
4.4 准确度 向两份含不同浓度CA15-3的血清中加入已知量的校准品,对其测量并计算添加回收率,即为本分析系统的准确度。实验结果如表2和表3所示。本方法的回收率为97.0%~105.6%。
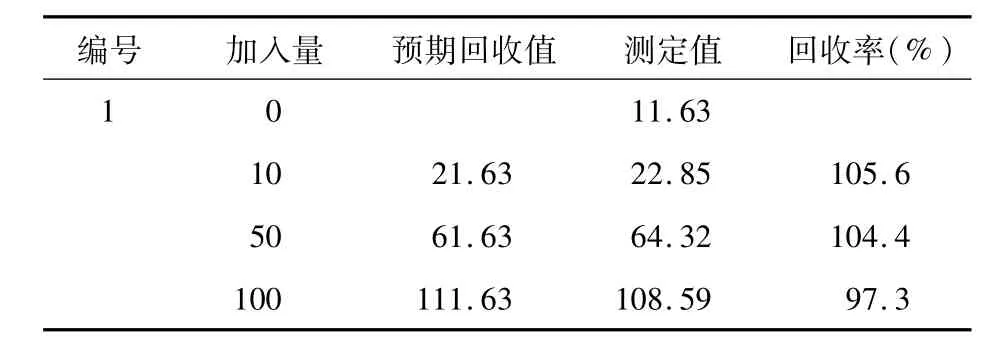
表2 1#样本添加回收实验(U/mL)
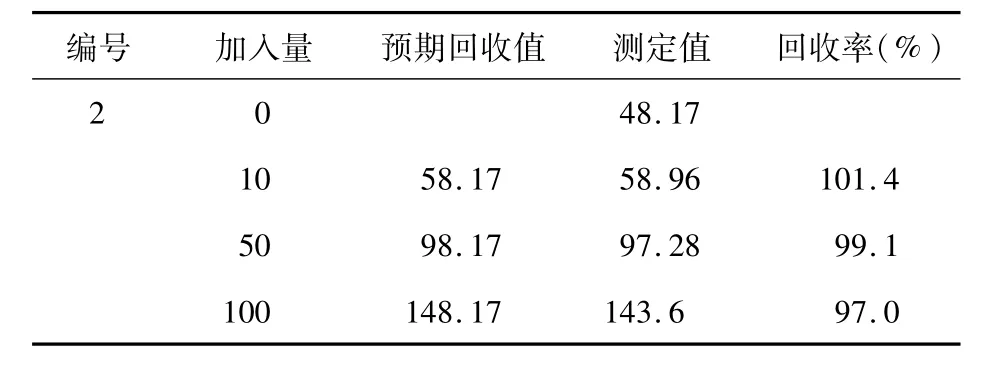
表3 2#样本添加回收实验(U/mL)
4.5 分析内与分析间精密度 对高、中、低三份样本,分别在同次实验中平行测量20孔,计算分析内精密度;分别在10次实验中重复测量,计算分析间精密度。结果如表4和表5所示。
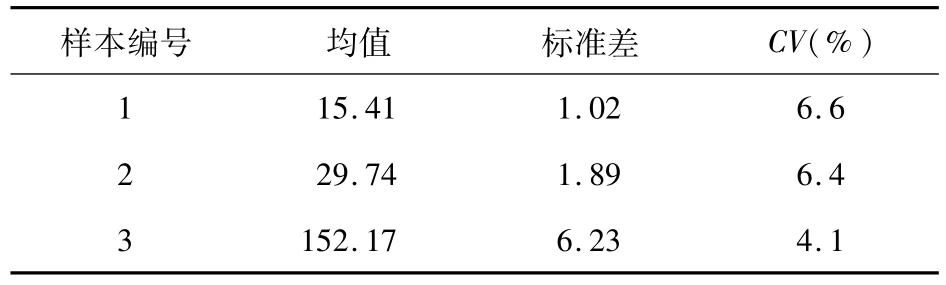
表4 分析内精密度结果(n=20,U/mL)
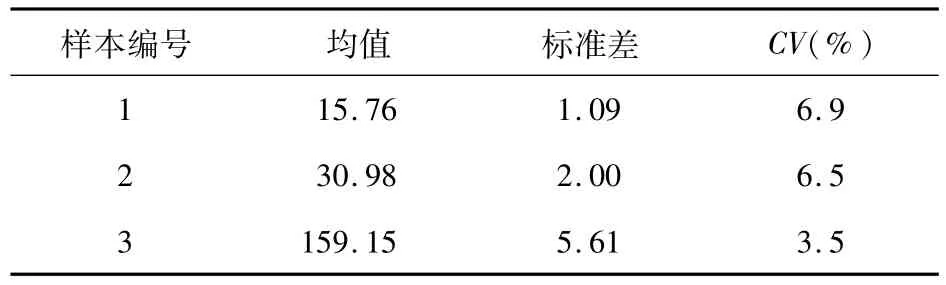
表5 分析间精密度结果(n=10,U/mL)
4.6 相关性实验 使用ADVIA Centaur CA15-3 ReadyPack全自动化学发光试剂(西门子医学诊断产品有限公司,批号:043160)与本方法同时测定160份样本的CA15-3浓度,相关性见图7,相关性方程为:Y=0.968X+1.538,r=0.987。
结 论
血清CA15-3含量对乳腺癌患者的疗效观察和预后估计具有重要的意义。本研究利用双抗体夹心法研制的CA15-3酶促化学发光免疫分析试剂盒,最低检测限为0.26 U/mL,在0~300 U/mL范围内线性关系良好,与高浓度CEA和CA125无交叉反应,分析内、分析间CV均小于10%,与进口全自动化学发光试剂检测结果的线性相关系数为0.987。此外,本试剂盒无需进行样本稀释,方便临床检验操作;反应时间仅需一小时,能够满足快速检测的市场需求。在临床工作中具有广阔的应用前景。
[1]Duffy M J,Evoy D,McDermott E W.CA15-3:Uses and limitation as a biomarker for breast cancer.Clin Chim Acta,2010,411(23-24):1869-1874.
[2]Sandri M T,Salvatici M,Botteri E,et al.Prognostic role of CA15.3 in 7942 patients with operable breast cancer.Breast Cancer Res Treat,2012,132(1):317-326.
[3]Ohuchi N,Sato S,Akimoto M,et al.The correlation between the immunohistochemical expression of DF3 antigen and serum CA15-3 in breast cancer patients.Jpn J Surg,1991,21(2):129-137.
[4]Brouckaert O,Laenen A,Wildiers H,et al.The prognostic role of preoperative and(early)postoperatively change in CA15.3 serum levels in a single hospital cohort of primary operable breast cancers.Breast,2013,22(3):254-262.
[5]郭春祥,郭锡琼.介绍一种简单、快速、高效的辣根过氧化物酶标记抗体的过碘酸钠法.上海免疫学杂志,1983,3(2):97-100.
(张增武编辑)
《标记免疫分析与临床》杂志继续入选2016版“中国科技期刊(核心版)”目录
《标记免疫分析与临床》杂志继续入选“中国科技期刊(核心版)”目录。在此,《标记免疫分析与临床》杂志社向一直以来关心和支持本刊的各位编委、专家教授、作者以及读者表示由衷的感谢!
《标记免疫分析与临床》以从事检验医学、临床医学、核医学体外检测技术以及科研工作的人员为读者对象,突出科学性、创新性和实用性,紧追国内外相关领域的发展趋势。刊登标记免疫分析、核素诊断与治疗等领域的理论、应用与方法等方面的研究成果和经验总结,以及与免疫分析有关的分子生物学、生物化学、微生物学、临床检验学、细胞生物学等领域内的新进展、新技术,抗体理论和抗体标记技术等方面的文章。
《标记免疫分析与临床》创刊以来,在各位编委、专家学者、作者等同仁的共同努力下,在各位读者的支持下,经历了由季刊、双月刊到月刊的蜕变,影响因子逐年升高,2016版《中国科技期刊(核心版)》目录中,本刊核心影响因子为0.541,《中国科技期刊(扩刊版)》目录中,影响因子为0.978。
我们感谢并期待大家一如既往的支持与关注!
《标记免疫分析与临床》杂志社
2016年10月18日
Development of a Chemiluminescent Immunoassay for Cancer Antigen 15-3
CHENG Bin-yan
(Beijing North Institute of Biological Technology,Beijing100076,China)
Objective To evaluate using chemiluminescent immunoassay(CLIA)system to detect serum cancer antigen 15-3(CA 15-3).Methods The system was evaluated in its limit of detection,linearity,analytical specificity,accuracy and repetitiveness.A total of 160 clinical specimens were detected and evaluated.Results The limit of detection was 0.26 U/mL and the recovery rate for accuracy was 97.0%-105.6%.The assay had a good linear relationship between 5-300 U/mL and had no cross reaction with CEA and CA125.All samples were detected by two CLIA systems,and the results were consistent and trusted.Conclusion The CLIA system for detecting CA15-3 has been established,which has satisfied sensitivity,repeatability,and will be widely used in clinical testing.
Tumor marker; Cancer antigen 15-3; Breast cancer; Chemiluminescence enzyme immunoassay
10.11748/bjmy.issn.1006-1703.2016.11.031
2016-05-20;
2016-06-11
