香豆素-3-羧酸的制备及光谱性质研究
2016-12-08杨文生
杨文生
(榆林学院化学与化工学院,陕西榆林719000)
香豆素-3-羧酸的制备及光谱性质研究
杨文生
(榆林学院化学与化工学院,陕西榆林719000)
本文以水杨醛、丙二酸二乙酯为原料合成香豆素-3-羧酸乙酯,进而合成香豆素的重要衍生物香豆素-3-羧酸,对其结构进行了表征,并通过紫外光谱和荧光光谱研究了溶剂极性、溶液酸度及溶剂中甲醇含量所产生的影响,最后计算了荧光量子产率,得出香豆素-3-羧酸为弱荧光物质。
合成;溶剂极性;溶液酸度;荧光量子产率
香豆素及其衍生物广泛分布在高等植物中,其基本组成苯并a-吡喃酮为重要的芳香杂环化合物,分子结构中C=C和C=O双键形成较大的共轭体系,分子中的内脂结构增强了分子的刚性,使整个分子具有良好的热力学和光学稳定性,容易进行结构修饰及各种功能官能团的导入。这种特殊结构使其具有良好的生理活性,如衍生物有抗肿瘤[1]、抗HIV[2]、抗凝血[3]、抗氧化[4]、抗细菌[5]、降血压[6]的作用;而且有较好的光学活性,如荧光量子产率高[7]、stokes位移大[8]、光稳定性好、光物理及光化学性质可调,是荧光探针及荧光染料设计中优秀的候选荧光团。
香豆素及其衍生物在医药[9]、香料[10]、荧光染料[11]、荧光增白剂[12]、光电材料[13]、荧光探针[14]等方面有着广泛的应用。香豆素-3-羧酸是香豆素的重要衍生物,也是合成香豆素的重要中间体,具有重要的研究意义。
本文由水杨醛与丙二酸二乙酯在二乙胺(取代传统的六氢吡啶)催化下合成香豆素-3-羧酸乙酯,在此基础上合成荧光化合物香豆素-3-羧酸,通过元素分析、红外光谱对产物的结构进行了表征,并研究了紫外吸收和荧光发射等光谱性质。合成路线如下:
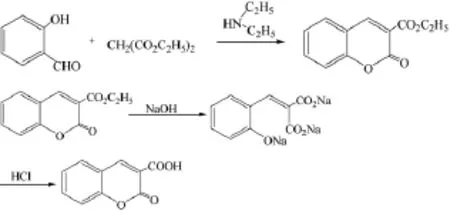
1 实验部分
1.1主要仪器与试剂
970CRT荧光分光光度计(上海仪电科学仪器股份有限公司);岛津UV-2450型紫外分光光度计(日本岛津);Broker红外光谱仪(布鲁克光谱仪器公司);PE-2400型元素分析仪(美国Perkin-Elmer公司);电子天平(上海上平仪器公司);显微熔点测定仪(北京泰克仪器有限公司)。
水杨醛(上海阿拉丁试剂公司);丙二酸二乙酯(上海国药基团);二乙胺、冰乙酸、乙醇、甲醇、二氯甲烷、乙酸乙酯、环己烷、L-色氨酸(天津科密欧试剂公司);所用试剂均为分析纯,所用水为二次蒸馏水。
1.2合成与表征
1.2.1香豆素-3-羧酸乙酯的合成在准备好的干燥的100mL圆底烧瓶中,加入4.2mL水杨醛,6.8mLl丙二酸二乙酯,25mL无水乙醇,0.5mL二乙胺(代替六氢吡啶)和2D HAc,放入几粒沸石后,装上回流冷凝管,上口接一个无水CaCl2干燥管,在水浴上加热回流2h,温度控制在70℃左右。反应完毕后,待溶液稍冷后,将反应物倒入30mL水中,于冰水中冷却结晶,析出大量晶体,结晶完全后,进行过滤,每次用经冰冷却后的50%乙醇4~5mL洗涤2~3次,所得粗产物用25%的乙醇溶液重结晶,产物为白色晶体,产率86%,m.p.92.2~93.1℃(文献值:92~93℃)。IR(KBr),v,cm-1:3065(Ar-H);1776(C=O);1608,1565,1451(C=C);1208,1132,1024(C-O)。元素分析,C12H10O4,实测值(计算值),%:C66.14(66.06);H4.48(4.59);O29.44(29.36)。
1.2.2香豆素-3-羧酸的合成在准备好的100mL圆底烧瓶中加入上一步合成的香豆素-3-羧酸乙酯4g,NaOH 3g,95%无水乙醇20mL和水10mL,加入几粒沸石,装上回流冷凝管,加热温度控制在70℃左右,在水浴条件下加热直至酯完全溶解后,继续回流操作约30min。放置一会使溶液稍冷后,将得到的反应混合物在不断搅拌下转移至有50mL水与10mL浓HCl的烧杯中,很快析出大量晶体,将其放入冰浴中冷却,待结晶完全后,进行抽滤,使用少量准备好的冰水洗涤晶体,再用水重结晶,压干,于干燥箱中干燥,产物为白色针状晶体,产率93%,m.p.191.4~192.8℃(文献值:191~193℃)。IR(KBr),v,cm-1:3429(O-H);3057(Ar-H);1748,1684(C=O);1612,1568,1422(C=C);1208,1042(C-O)。元素分析,C10H6O4,实测值(计算值),%:C 63.23(63.16);H 3.24(3.16);O33.76(33.68)。
1.3香豆素-3-羧酸的光谱性质
1.3.1香豆素-3-羧酸在不同极性溶剂中的紫外光谱分别以二氯甲烷、乙醇、乙酸乙酯及环己烷为溶剂配制浓度为1.0×10-5mol·L-1的香豆素-3-羧酸溶液,在紫外分光光度计上测定吸收光谱。
1.3.2香豆素-3-羧酸在不同极性溶剂中的荧光光谱与上述条件相同,分别以乙醇、乙酸乙酯、二氯甲烷及环己烷为溶剂配制浓度为1.0×10-5mol· L-1的香豆素-3-羧酸溶液,以紫外吸收的最大吸收波长为激发波长,测定不同溶剂中香豆素-3-羧酸的荧光发射光谱。
1.3.3香豆素-3-羧酸在不同酸度溶液中的荧光光谱配制浓度相同(C=1.0×10-5mol·L-1)且pH值不同的香豆素-3-羧酸溶液,测试pH值为1~13时的荧光发射光谱。
1.3.4香豆素-3-羧酸在不同甲醇含量的溶剂中的荧光光谱改变溶剂中甲醇的含量,测试甲醇含量为10%-90%时香豆素-3-羧酸的荧光发射光谱。
1.3.5香豆素-3-羧酸的荧光量子产率分别测试适当浓度的香豆素-3-羧酸与L-色氨酸的吸收光谱和发射光谱,以L-色氨酸为参比(在甲酸中280nm时荧光量子产率为0.14),并使吸收光谱的最大吸收波长处的吸光值小于0.05,依据荧光量子产率的计算公式ΦX=ΦS(AS/AX)(FX/FS)(nX/nS)2计算香豆素-3-羧酸的荧光量子产率。
2 结果与讨论
2.1溶剂极性对香豆素-3-羧酸紫外光谱的影响
实验结果见图1。

图1 不同极性溶剂对香豆素-3-羧酸紫外吸收光谱的影响Fig.1Effect of different polar solvents on the UV absorption spectra of coumarin-3-carboxylic Acid
由图1可知,是经归一化的吸收光谱,表明最大吸收波长位于紫外波长区域,随着溶剂极性的增大,最大吸收波长出现蓝移,这是由于非成键的n电子与极性溶剂相互作用形成氢键,从而降低了基态能量,使得n→π*的能量增大,紫外吸收光谱因而发生蓝移。
2.2溶剂极性对香豆素-3-羧酸荧光光谱的影响
实验结果见图2。

图2 不同极性溶剂对香豆素-3-羧酸荧光发射光谱的影响Fig.2Effect of different polar solvents on the fluorescence emission spectra of coumarin-3-carboxylic acid
由图2可知,随着有机溶剂极性的变化,荧光强度的大小出现明显的不同,荧光发射峰最大相差5倍,这主要由于香豆素-3-羧酸分子的基态与激发态与有机溶剂分子间存在不同程度的相互作用,并对激发态和基态能量差产生影响。
2.3溶液酸度对香豆素-3-羧酸荧光光谱的影响
实验结果见图3、4。

图3 溶液酸度对香豆素-3-羧酸荧光发射光谱的影响Fig.3Effect of solution acidity on the fluorescence emission spectra of coumarin-3-carboxylic acid

图4 溶液酸度对香豆素-3-羧酸荧光强度的影响Fig.4Effect of solution acidity on the fluorescence intensity of coumarin-3-carboxylic acid
由图3、4可知,pH值为1~3时,随pH值的增大香豆素-3-羧酸溶液荧光强度明显增强,pH值为3时达到最大,pH值为4~7时,荧光强度急剧下降,pH值在7之后几乎没有荧光。由此推测随溶液pH值的升高,香豆素-3-羧酸分子逐步发生了质子离解和水解:
酸性很强时,香豆素-3-羧酸的羰基氧发生质子化(1),此时荧光较强;pH值在3左右,羰基氧上的质子逐步电离,所形成的中性分子具有最强的荧光(2);当pH值继续增大时,分子中羧基质子电离,形成负离子,导致羧基吸电子能力降低,这时荧光很弱(3);当溶液变为碱性时,分子出现水解并打开内脂环,从而破坏分子的原有共轭结构,减少了刚性,此时无荧光(4)。
2.4溶剂中甲醇含量对香豆素-3-羧酸荧光光谱的影响
实验结果见图5、6。
随着溶剂中甲醇含量的增加,最大发射波长有轻微的蓝移,甲醇含量为10%至40%时,荧光强度显著增强,含量为40%时荧光强度最大,当甲醇含量为40%至90%时,荧光强度逐步减弱,由此可知,实验中甲醇含量以40%为适宜含量。
2.5香豆素-3-羧酸的荧光量子产率

由香豆素-3-羧酸和L-色氨酸的吸收光谱可知AX=0.042,AS=0.035;二者的发射光谱可知FX=24050,FS=294677,参比L-色氨酸的溶剂甲酸的折射率nS=1.3714,香豆素-3-羧酸的溶剂水的折射率nX=1.3333,L-色氨酸在甲酸中280nm时荧光量子产率为ΦS=0.14,依据公式ΦX=ΦS(AS/AX)(FX/FS)(nX/nS)2,计算香豆素-3-羧酸的荧光量子产率为0.009,表明香豆素-3-羧酸为弱荧光化合物,虽然香豆素-3-羧酸分子具有共轭结构和一定的刚性,但3位取代基(-COOH)为吸电子基团,能够很大程度上抑制荧光的增强,因此,香豆素-3-羧酸的荧光很弱。
3 结论
合成了香豆素的重要衍生物香豆素-3-羧酸,研究了不同溶剂极性对香豆素-3-羧酸的紫外吸收光谱和荧光发射光谱的影响,以及溶液酸度和溶剂中甲醇含量对荧光强度的影响。结果表明,随着溶剂极性的增大吸收光谱有蓝移现象;发射光谱荧光强度随溶剂极性的变化发生很大差异;随着溶液pH值的升高,香豆素-3-羧酸出现质子离解和水解;溶剂中甲醇含量为40%时荧光强度最高;最后计算荧光量子产率为0.009,表明香豆素-3-羧酸为弱荧光物质。
[1]Chen H,Li S,Yao YC,et al.Design,synthesis,and anti-tumor activities of novel triphenylethylene-coumarin hybrids,and their interactions with Ct-DNA[J].Bioorg.Med.Chem.Lett.,2013,23:4785-4789.
[2]Kudo E,Taurn M,Matsuda K,et al.Inhibition of HIV-l replication by a tricyclic coumarin GUT-70 in acutely and chronically infacted cells[J].Bioorg.Med.Chem.Lett.,2013,23:606-609.
[3]TUMMNOP J Competitive inhibition ofHIV-1 Protease bywarfarin derivatives[J].Biochem BioPhys Res Commun.,1994,201(1):290-294.
[4]Melagraki G,Afantitis A,Igglessi-Markopoulou O,et al.Synthesis and evaluation of the antioxidant and antiinflammatory acttivity of novelcoumarin-3-aminoa mi des and their alphalipoic acid adducts[J].Enr.J.Med.Chem.,2009,44:3020-3026.
[5]Patel MM,Mali MD,Pater SK.Bernthsen synthesis,antimicrobial activities and cytotoxicity of acridine derivatives[J].Bioorg.Med. Chem.Lett.,2010,20:6324-6326.
[6]Yang JR,Li Qp,Rao MR.Protective effects of praeruptorin C and nifedipine on ischemia-reperfused injury in working rat hearts[J]. Acta Pharm.Sin.,1992,27(10):729-733.
[7]TURKI H,ABID S,FERY-FORGUES S.et al.Optical properties of newfluorescentiminocoumarins:Part1[J].Dyesandpigments,2007,73(3):311-316.
[8]ELANGOVAN A,LIN J-H,YANG S-W,et al.Synthesis and Electrogenerated Chemiluminescence of Donor-Substituted Pheny lethynylcoumarins[J].The Journal of Organic Chemistry,2004,69(23):8086-8092.
[9]S D Joshi,H M Vagdevi,V P Vaidya,et al.Synthesis of new 4-pyrrol-1-yl benzoic acid hydrazide analogs and some derived oxadiazole,trazole and pyrrole ringsystems:Anovel class ofpotential antibacterial and antitubercular agents[J].Eur J Med Chem,2008,43(9):1989-1996.
[10]Abraham K,Wohrlin F,Lindtner O,et al.Toxicology and risk assessment of coumarin:focus on human data[J].Mol.Food.Res.,2010,54:228-239.
[11]Bulut M,Erk C.Improved synthesis of some hydroxycoumarins[J].Dyes and Pigment,1996,30:99-104.
[12]Sekar N,Fluorescent colorants containing two coumarin units[J]. Colourage,2004,51:61.
[13]Ren X,Kondakova ME,Giesen D J,et al.Coumarin-based,electron-trapping iridium complexes as highly efficient and stable phosphorescent emitters for organic light-emitting diodes[J].Inorganic chemistry,2010,9(4):1301-1303.
[14]Lin Q,Bao C,Cheng S,et al.Target-activated coumarin phototriggers specifically switch on fiuorescence and photocleavage upon bonding to thiol-bearing protein[J].Journal of the American Chemical Society,2012,134(11):5052-5055.
Study on preparation and spectroscopic properties of coumarin-3-carboxylic acid
YANG Wen-sheng
(School of Chemistry and Chemical Engineering,Yulin University,Yulin 719000,China)
In this paper the coumarin-3-carboxylic acid ethyl ester was synthesized with salicylaldehyde,diethyl malonate as raw material,and then the coumarin-3-carboxylic acid which is the important derivative of coumarin was also synthesized,the structure of which were characterized,and the effects of solvent polarity、acidity of the solution and methanol content in the solvent were studied by UV and fluorescence spectra.Finally,the fluorescence quantum yield was calculated,the results showed that coumarin-3-carboxylic acid was a weak fluorescent substance.
synthesis;solvent polarity;solution acidity;fluorescence quantum yield
O621.3
A
10.16247/j.cnki.23-1171/tq.20161182
2016-03-29
杨文生(1974-),男,汉族,河北行唐人,博士,讲师,主要从事荧光染料和荧光探针研究。
