高血压对老年帕金森病患者非运动症状的影响
2016-12-06宋征宇岳秉宏
宋征宇 岳秉宏
(河北北方学院附属第一医院神经内三科,河北 张家口 075000)
高血压对老年帕金森病患者非运动症状的影响
宋征宇 岳秉宏
(河北北方学院附属第一医院神经内三科,河北 张家口 075000)
目的 探讨高血压对老年帕金森病(PD)患者非运动症状的影响。方法 随机选择原发性老年PD患者85例,按是否伴有高血压分为PD伴高血压组和PD组,入组前给予PD非运动症状评估量表 (NMSQuest),问卷评分,记录每位患者的评分结果。常规药物治疗1年后,再次NMSQuest问卷评分,比较结果。结果 PD伴高血压组入组前评分为(21.7±2.3)分,PD组为(17.5±3.0)分,两组差异显著(P<0.05)。1年后PD伴高血压组为(25.7±2.4)分,PD组为(20.9±1.8)分,两组差异显著(P<0.05)。两组NMSQuest问卷量表中认知功能、焦虑抑郁等方面差异显著(P<0.05),自主神经功能的项目无统计学差异(P>0.05)。结论 高血压加重了老年PD患者的非运动症状。
帕金森病;高血压;非运动症状
帕金森病(PD)的非运动症状(NMS)被认为是影响患者生活质量的重要原因〔1〕。氧化应激对PD的发生发展有重要作用。有足够的证据显示PD患者处于氧化应激状态〔2〕。而高血压是老年人最常见的基础疾病,是导致机体氧化应激及衰老的最重要因素之一。因此,推测高血压可能对PD患者NMS有一定影响。同时此类相关研究未见报道。本文探讨高血压与老年PD患者NMS的潜在关系。
1 资料与方法
1.1 一般资料 2012年10月至2014年3月老年PD患者85例。PD伴高血压组41例,男21例,女20例;年龄61~76〔平均(66.1±5.1)岁〕;平均病程(3.8±2.2)年;Hoehn-Yahr分期(2.8±0.5)。PD组44例,男24例,女20例;年龄60~75岁,平均(68.2±6.3)岁;平均病程(3.0±2.1)年;Hoehn-Yahr分期(3.6±0.2)。两组患者年龄、病程及Hoehn-Yahr分期无统计学差异。入组标准:① 每日服用左旋多巴,其他药物包括司来吉兰、金刚烷胺、吡贝地尔、普拉克索等;高血压药物包括氨氯地平、硝苯地平、依那普利。②患者有NMS主诉;③Hoehn-Yahr分期Ⅰ~Ⅳ期。排除标准:① 尽量排除帕金森综合征(PS近期无异动现象)。②Hoehn-Yahr分期V期。③尽量排除其他可能影响评分的疾病(如抑郁症)、新发急性血管病及其他重大疾病者。④伴有其他内外科基础病的患者,如心力衰竭、肺心病、糖尿病等。⑤依从性较差的患者。
1.2 研究方法 PD病情评价采用Hoehn-Yahr分期。NMS评价采用PD NMS30(NMSQuest)问卷评分,记录2次各项评分。
1.3 统计学方法 选用SPSS19.0软件进行t及χ2检验。
2 结 果
入组时PD伴高血压组平均评分(21.7±2.3)分明显高于PD组平均评分(17.5±3.0)分(t=7.192,P<0.05)。1年后,PD伴高血压组评分(25.7±2.4)分明显高于PD组评分(20.9±1.8)分(t=10.435,P<0.05)。随访1年后与PD组比较,PD伴高血压组在体现痴呆及焦虑抑郁的多项指标方面差异的有统计学意义(P<0.05)。两组在体现自主神经功能的多项指标无统计学差异(P>0.05)。见表1。
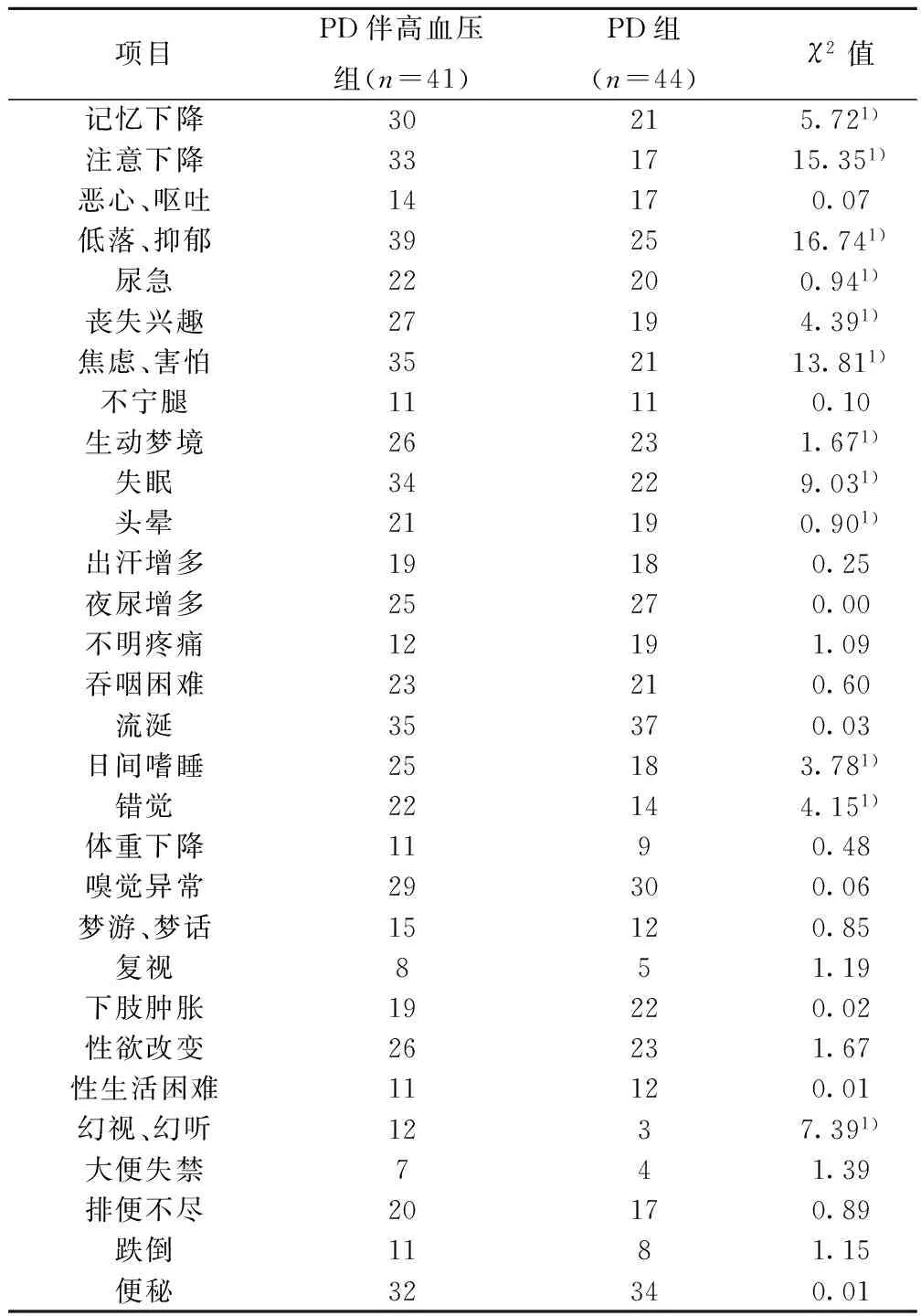
表1 两组随访1年后NMSQuest各项评分比较(n)
1)P<0.05
3 讨 论
从病因学上讲,NMS的发生往往呈多因素,与PD的病程、疾病的严重程度、伴随情况、年龄等都可能有关。NMS在PD的早期诊断和治疗中占据重要地位〔3〕,NMS和患者的生活质量密切相关。NMS对患者的影响体现在〔4〕:70%以上的PD患者有睡眠障碍;伴随痴呆障碍的患者可能会走失;部分症状与抑郁症的外在特点重叠,给抑郁的诊断带来一定的困难等。国外一项研究显示,对于老年PD患者来说,NMS对个人感受以及日常生活的影响明显高于运动症状〔5〕。
本研究采用可靠性和有效性均较为肯定的NMSQuest〔6〕,结果显示伴有高血压的老年PD患者更容易出现不同类型的更为严重的NMS,且PD伴高血压患者记忆力下降、注意力下降更明显。我们考虑可能是由于高血压本身由于小动脉硬化能够导致认知功能障碍。且PD患者由于神经递质改变等因素大多伴有轻度认知障碍或者痴呆,故可能两者有累积效应。本研究同时发现PD伴高血压患者更多地出现焦虑和抑郁,究其原因,可能是PD、高血压均是慢性疾病,不能够完全治愈,患者需要长期带病生存。由于高血压本身并发症较多,PD患者如果合并高血压,心理压力较大,同时加之神经递质存在失衡,故焦虑抑郁等指标有较大变化。这与国外的研究相一致〔7〕。我们同时发现两组在提示自主神经功能的多项指标无统计学差异,考虑原因如下:PD自主神经障碍是由于中枢一些控制自主神经功能核团的变性和损害导致,病理生理过程较复杂,涉及如迷走背核、疑核及其他通过下行通路控制交感节前神经元的延髓核团。除此之外,还包括胆碱能、单胺能等核团变性所致的中枢自主神经网络系统的损害〔8〕。目前所知,高血压对于自主神经影响的研究多集中于心脏自主神经。对于中枢的研究多来自于血管病的研究,其病理过程涉及复杂机制未完全知晓,故认为随着病程的进展,以及诸如年龄、药物等未知因素影响,两者均出现自主神经功能障碍,表现为两组患者无明显差异。
既往研究表明几乎所有类型的高血压患者均存在氧化应激增强〔9〕,高血压患者中活性氧簇明显较正常人增高。同时,在许多动物模型中都证实氧化应激与血压增高之间存在明显的关系。由于慢性心理应激与高血压发病密切相关。而PD患者多伴有焦虑、抑郁等不良心理状态。故高血压与PD可能相互促进。高血压患者或高血压动物模型均有多巴胺受体合成减少和其介导的利尿利钠能力的下降。在高血压动物模型中,多巴胺D3类受体与老年高血压有明显的相关性〔10〕。中枢神经系统的多巴胺D2类受体基因破坏后都表现为明显高血压〔11〕。同时多巴胺D2样受体激动剂可增加尿钠排泄、扩张阻力血管,并可抑制交感神经末梢释放去甲肾上腺素,降低血压〔12〕。高血压可以激活血管紧张素及还原型辅酶Ⅱ依赖性氧化酶,产生更多的超氧化物,加重体内氧化应激程度,同时,活化的还原型辅酶Ⅱ依赖性氧化酶导致更多的多巴胺能细胞死亡,在PD进展中发挥重要作用〔13〕。我们推测高血压可能通过以下途径影响PD病理过程。第一,长期高血压,导致小动脉硬化,中脑黑质慢性缺血,导致多巴胺细胞凋亡,促进PD发生。第二,高血压使含氧体内自由基增加,保护性谷胱甘肽减少,线粒体损伤〔14〕,机体保护性因素减少,加速PD发生发展。第三,由于高血压为慢性疾病,长时间的血压增高,对单胺类神经递质可能产生较大的影响,从而促进PD发展。综上,可以解释高血压对PD患者的NMS产生影响的病理过程。
本研究提示,高血压对PD患者NMS的发展在客观评分中确实有影响,故可以认为,高血压导致的机体功能障碍促进了老年PD患者的病情发展。我们需要关注的是PD患者可能很早就出现NMS,如果同时合并高血压,且患者在规律服用降压药的时候,在5年后或者10年后是否仍有影响,不得而知。量表主观性强,患者本身的偏差和记录偏差可能也会对结果产生一定的影响。
严重的NMS降低了老年PD患者生活信心〔15〕,如果合并高血压,则进一步加重患者对生活的忧虑,感觉前途暗淡。作为临床医师我们需要高度关注PD患者尤其是老年患者合并其他基础病的问题,需要系统了解患者的既往史并制定相应的治疗方案,提高患者的生活质量。
1 Cilia R,Cereda E,Klersy C.Parkinson′s disease beyond 20 years〔J〕.J Neurol Neurosurg Psychiatry,2014;86(8):849-55.
2 Gaki GS,Papavassiliou AG.Oxidative stress-induced signaling pathways implicated in the pathogenesis of Parkinson′s disease〔J〕.Neuromol Med,2014;16(2):217-30.
3 董 青,李焰生.帕金森病非运动症状的研究进展〔J〕.临床神经病学杂志,2009;21(3):310.
4 Thanvi BR,Munshi SK,Vijaykumar N,etal.Neuropsychiatric non-motor aspects of Parkinson′s disease 〔J〕.Postgrad Med J,2003;79(936):561-5.
5 Santos-García D,dela Fuente-Fernández R.Impact of non-motor symptoms on health-related and perceived quality of life in Parkinson′s disease〔J〕.J Neurol Sci,2013;332(1-2):136-40.
6 中华医学会神经病学分会运动障碍及帕金森病学组·帕金森病治疗指南〔J〕.中华神经科杂志,2O06;39(6):409-12.
7 Skorvanek M,Gdovinova Z,Rosenberger J,etal.The associations between fatigue,apathy and depression in Parkinson′s disease〔J〕.Acta Neurol Scand,2014;6(10):1111-22.
8 Verbaan D,Marinus J,Visser M,etal.Patient-reported autonomic symptoms in Parkinson disease 〔J〕.Neurology,2007;69(4):333-41.
9 Fortuno A,Oliván S,Beloqui O,etal.Association of increased phagocytic NADPH oxidase-dependent superoxide production with diminished nitric oxide generation in essential hypertension〔J〕.J Hypertens,2004;22(11):2169-75.
10 Johnson TL,Tulis DA,Keeler BE,etal.The dopamine D3 receptor knockout mouse mimics aging-related changes in autonomic function and cardiac fibrosis〔J〕.PLoS One,2013;8(8):74116.
11 Lyzogub VH,Dolynna OV,Bogdan TV.State of the dopamine system activity,as one of factors for the development of arterial hypertension and obesity 〔J〕.Lik Sprava,2012;47(3-4):41-7.
12 李晓曦,杨智伟.多巴胺D2受体基因敲除对鼠肾上腺素和内皮素B受体依赖性高血压的影响〔J〕.中华医学杂志,2002;82(10):703-7.
13 Labandeira-Garcia JL,Rodriguez-Pallares,Rodríguez-Perez AI,etal.Brain angiotensin and dopaminergic degeneration:relevance to Parkinson′s disease 〔J〕.Am J Neurodegener Dis,2012;1(3):226-44.
14 曾春雨,杨志伟,吴丽娟,等.D3多巴胺受体基因敲除小鼠高血压产生机制的探讨〔J〕.中华心血管病杂志,2005;33(12):1132-6.
15 Zis P,Rizos A,Martinez-Martin P,etal.Non-motor symptoms profile and burden in drug naive versus long-term Parkinson′s disease patients〔J〕.J Parkinsons Dis,2014;4(3):541-7.
〔2015-04-15修回〕
(编辑 苑云杰/曹梦园)
宋征宇(1979-),男,硕士,主治医师,主要从事锥体外系疾病研究。
R742.5
A
1005-9202(2016)21-5287-03;
10.3969/j.issn.1005-9202.2016.21.032
