改性方法对核桃浓缩蛋白凝胶性的影响
2016-12-05胡雪娇陈永浩张春红郝艳宾齐建勋董宁光
胡雪娇 陈永浩 张春红 郝艳宾 齐建勋 董宁光
(1. 北京市农林科学院林业果树研究所,北京 100093;2. 北京市落叶果树工程技术研究中心,北京 100093;3. 沈阳农业大学食品学院,辽宁 沈阳 110866)
改性方法对核桃浓缩蛋白凝胶性的影响
胡雪娇1,2,3陈永浩1,2张春红3郝艳宾1,2齐建勋1,2董宁光1,2
(1. 北京市农林科学院林业果树研究所,北京 100093;2. 北京市落叶果树工程技术研究中心,北京 100093;3. 沈阳农业大学食品学院,辽宁 沈阳 110866)
分别采用物理及化学方法对核桃浓缩蛋白进行改性,通过测定改性后蛋白中游离巯基、二硫键含量及表面疏水性指数等指标,研究不同的改性方法及条件对核桃浓缩蛋白质凝胶性的影响,以获得具有形成强凝胶潜力的蛋白质,确定适宜的改性条件,并对改性前后蛋白凝胶质构性进行分析。结果表明:物理改性(超声处理)的适宜条件为超声功率840 W,超声时间6 min;化学改性(还原剂亚硫酸钠)的适宜条件为还原剂加入量0.625 mmol/L,处理时间60 min。经超声改性后的核桃浓缩蛋白,其凝胶性能最优。
核桃;蛋白质;改性;凝胶性;质构性
核桃又名胡桃、羌桃,是世界四大干果之一,也是中国重要的木本油料来源。据统计[1],2011年中国核桃产量已占世界核桃年产量的48.36%,远超过其它国家,产量的增加为其深加工及核桃油生产提供了充足的原料来源。核桃粕是核桃榨油的副产物,核桃仁的油脂含量约为60%~70%,而一般榨油方法的出油率在50%~90%[2],因此,每吨核桃仁榨油后,大约会产生370~700 kg核桃粕。蛋白质是核桃粕的主要成分,在核桃粕中的含量为30%~40%。核桃蛋白富含18种氨基酸,其中的8种人体必需氨基酸含量和比例合理,是一种优质蛋白资源[3-4],但往往因为核桃粕的废弃而造成资源浪费。
植物蛋白在肉制品、饮料、焙烤食品等产品的加工中应用广泛,尤以大豆蛋白的应用最多[5]。核桃蛋白不仅营养价值高,而且可消化率达87.2%,生物价达98.77%[6],以核桃蛋白取代大豆蛋白添加到食品中,不仅能够增加食品的营养价值,还可使食品呈现出独特的质构特性和感官品质。然而,核桃蛋白在榨油过程中往往发生了不同程度的变性,其较低的凝胶性会使火腿肠等肉制品的成型性差,易散开,限制了核桃蛋白在此类食品中的应用[7]16,88。目前,对核桃蛋白功能特性的研究主要集中在溶解性、乳化性和起泡性方面[4],而对于植物蛋白凝胶性的研究多见于大豆蛋白和花生蛋白的研究中[8-10],对核桃蛋白凝胶特性的研究尚未见报道。本研究以核桃粕中提取制备的核桃浓缩蛋白为原料,拟分别采用物理、化学方法对其进行改性,通过测定蛋白中游离巯基(—SH)、二硫键(—S—S—)的含量及表面疏水性指数(S0)和质构特征,来判断核桃浓缩蛋白凝胶性质的变化,以期获得凝胶强度较好的核桃浓缩蛋白,为其在食品特别是肉制品中的应用提供试验依据,促进核桃加工副产物的再利用,并为食品加工提供优质的植物蛋白来源。
1 材料与方法
1.1 试剂与材料
核桃浓缩蛋白:实验室自制,采用二次乙醇浸提法,将核桃粕粉碎并过60目筛后与75%乙醇溶液以1/10(g/mL)混合均匀,振荡浸提60 min,以4 200 r/mim离心20 min,去上清液,将沉淀与90%乙醇以1/8(g/mL)混合均匀,振荡浸提30 min,离心后将沉淀冷冻干燥,即得核桃浓缩蛋白,置于冰箱备用。
无水亚硫酸钠:分析纯,天津市福晨化学试剂厂;
5,5-二硫二硝基苯甲酸(DTNB)、三氯乙酸、三羟甲基氨基甲烷(Tirs)、甘氨酸(Glycine)、乙二胺四乙酸(EDTA)、β-巯基乙醇、1-苯胺基-8-苯磺酸(ANS)、考马斯亮蓝R250等:分析纯,索莱宝生物技术有限公司。
1.2 主要设备
质构仪:TA-XT2i型,英国Stable Micro System公司;
原位冷冻干燥机:LGJ-30型,北京松源华兴科技发展有限公司;
超声波细胞粉碎机:JY98-ⅢDN型,宁波新艺超声设备有限公司;
紫外可见分光光度计:UV-3802型,尤尼柯仪器有限公司;
荧光分光光度计:F96PRO型,上海棱光技术有限公司;
恒温双向磁力搅拌器:90-3型,上海振荣科学仪器有限公司;
pH计:PHS-3C型,上海精密科学仪器有限公司。
1.3 试验方法
1.3.1 核桃浓缩蛋白的纯化 参照吴海文[7]21-22的方法。
1.3.2 超声改性处理条件的确定
(1) 超声处理强度的确定:8 %蛋白悬浮液磁力搅拌均匀后,置于超声波细胞粉碎机内,将变幅杆末端插入液面2 cm处,并使其位于容器中心位置。分别在360,480,600,720,840,960,1 080 W功率下处理1 min,冷冻干燥后得到改性核桃浓缩蛋白,测定蛋白中游离巯基、二硫键的含量及表面疏水性指数。
(2) 超声处理时间的确定:样品处理同上,在1.3.2(1)的最佳功率下对蛋白分别处理1,2,4,6,8 min,冷冻干燥后得到改性蛋白,测定蛋白中游离巯基、二硫键的含量及表面疏水性指数。
1.3.3 还原剂亚硫酸钠处理条件的确定
(1) 亚硫酸钠浓度的确定:取9.6%的核桃浓缩蛋白悬浮液25 mL加入一组烧杯中,然后向每个烧杯中分别加入5 mL浓度为0.250,0.375,0.500,0.625,0.750,0.875 mmol/L的还原剂亚硫酸钠溶液,将其置于室温下振荡反应30 min。冷冻干燥后得到改性蛋白,测定蛋白中游离巯基、二硫键的含量及表面疏水性指数。
(2) 亚硫酸钠处理时间的确定:取9.6%的核桃浓缩蛋白悬浮液25 mL加入一组烧杯中,然后向每个烧杯中加入1.3.3(1)中最佳浓度的亚硫酸钠溶液5 mL,将其置于室温下分别振荡反应15,30,45,60,90,120 min。冷冻干燥后得到改性蛋白,测定蛋白中游离巯基、二硫键的含量及表面疏水性指数。
1.3.4 游离巯基和二硫键含量的测定 参照文献[11]。在10 mL含有8 mol/L尿素的Tris—Gly(pH 8.0)的缓冲溶液(每升溶液含10.418 g Tris,6.756 g Glycine,1.169 g EDTA)中混合振荡溶解1 h后离心(10 000 r/min,10 min),保留上清液。
(1) 游离巯基(SHF)的测定:取3 mL上清液加入120 μL Ellman’s试剂(400 mg DTNB溶于100 mL Tris—Gly缓冲溶液中),混匀后静置5 min,利用紫外分光光度计测定412 nm处吸光值。游离巯基含量按式(1)计算:
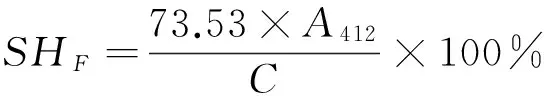
(1)
式中:
SHF——游离巯基含量,μmol/g;
73.53——106/(1.36×104),其中1.36×104为Ellman’s试剂巯基的摩尔吸光系数;
A412——412 nm处吸光值;
C——样品蛋白浓度,mg/mL。
(2) 总巯基(SHT)的测定:取3 mL上清液,加入1%β-巯基乙醇30 μL,对样品处理2.5 h后,再加入12%三氯乙酸4 mL进行蛋白沉淀处理1.5 h后离心(10 000 r/min,10 min),然后弃除上清液,利用12%三氯乙酸洗涤沉淀3次,再将沉淀溶于3 mL Tris—Gly缓冲溶液中,取出2 mL溶液以游离巯基的测定方法进行测定。
(3) 二硫键的含量:按式(2)计算:
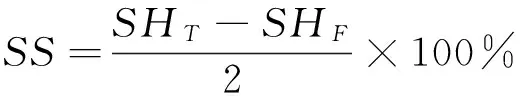
(2)
式中:
SS——游离巯基含量,μmol/g;
SHT——总巯基含量,μmol/g;
SHF——游离巯基含量,μmol/g。
1.3.5 表面疏水性指数的测定方法 采用ANS荧光探针法[12],当ANS与蛋白中膜或者相对疏水区域键合时,发出荧光,利用此特性来检测蛋白的表面疏水性指数。将蛋白样品溶于0.01 mol/L的磷酸缓冲溶液中,配制成1 mg/mL的蛋白液,然后离心(10 000 r/min,20 min)。取上清液利用考马斯亮蓝法测定上清液中的蛋白浓度,再利用0.01 mol/L的磷酸缓冲溶液将上清液分别稀释到0.200,0.100,0.050,0.025 mg/mL。取不同浓度的样品4 mL,分别加入20 μL浓度为0.008 mol/L的ANS溶液(使用0.01 mol/L,pH 7.0的磷酸缓冲溶液配制),混匀后静置10 min利用荧光分光光度计测定其荧光强度,本试验采用的发射波长为390 nm,激发波长为470 nm。最后以荧光强度对蛋白质浓度做出曲线图,曲线的初始斜率即为蛋白质样品的表面疏水性指数。
1.3.6 核桃浓缩蛋白最低胶凝点的测定 取0.4~1.6 g蛋白样品溶于10 mL的去离子水或0.1 mol/L的NaCl溶液中,将样品配制成了4~16 g/mL的蛋白液,用1 mol/L的NaOH调节pH至7.0后,室温下磁力搅拌60 min,用封口膜封口,置于90 ℃水浴中加热30 min,取出后迅速用冰水使其冷却至室温,置于4 ℃冰箱保存18 h。取出后对凝胶情况进行观察:将试管倒置,若凝胶不流出来则定义为“+”,为可形成自持凝胶的样品;相反则为“-”,不能形成凝胶。以此来判断能够形成凝胶的最低蛋白浓度,即最低凝胶点。
1.3.7 核桃浓缩蛋白凝胶质构性的测定 利用TA-XT2i型质构仪对核桃浓缩蛋白凝胶的硬度、弹性及黏结力进行测定。测定参数:探头:P0.5;每个数据采集时间:40 s;运行模式:TAP;测试前速度:2 mm/s;测试速度:0.8 mm/s;测试后速度:2 mm/s;下压距离:50%;力量源:50 kg;测试温度:室温。每个处理设置3次重复进行测定,平均值为最终测定结果。
2 结果与讨论
2.1 超声处理对凝胶性的影响
2.1.1 超声功率的对凝胶性的影响 由图1可知,当超声功率在360~840 W时,随着功率的增大,游离巯基含量总体呈现先上升后下降趋势;在超声功率为600 W和720 W时,游离巯基含量略有降低,但与480 W功率下的游离巯基含量差异不显著,二硫键含量呈先下降后上升趋势。由图2可知,表面疏水性指数呈现出与游离巯基含量相应的变化趋势。这是由于在超声波作用下蛋白分子之间及内部的非共价键及二硫键断裂,从而使蛋白中的游离巯基含量增加,提高了蛋白的表面疏水性指数,同时保存了蛋白质中游离巯基的含量,并使其能够在速凝阶段持续发挥作用[13-14]。而当继续增加超声功率后,游离巯基含量及表面疏水性指数缓慢下降,二硫键含量迅速上升,这可能是超声波声强过大,空化泡在声波膨胀相内还来不及发生崩溃或是太高的声强产生的大量空泡通过反射声波而减少了能量的传递[13]。因此在功率为840 W时,游离巯基含量及表面疏水性指数均达最高值,分别为19.25 μmol/g和14.35,二硫键含量降为最低值5.43 μmol/g。
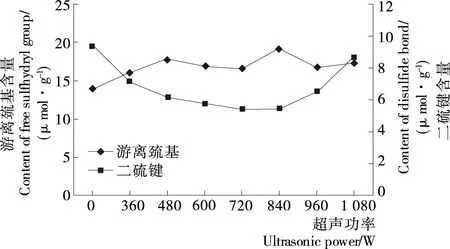
图1 超声处理强度对蛋白游离巯基和二硫键含量的影响
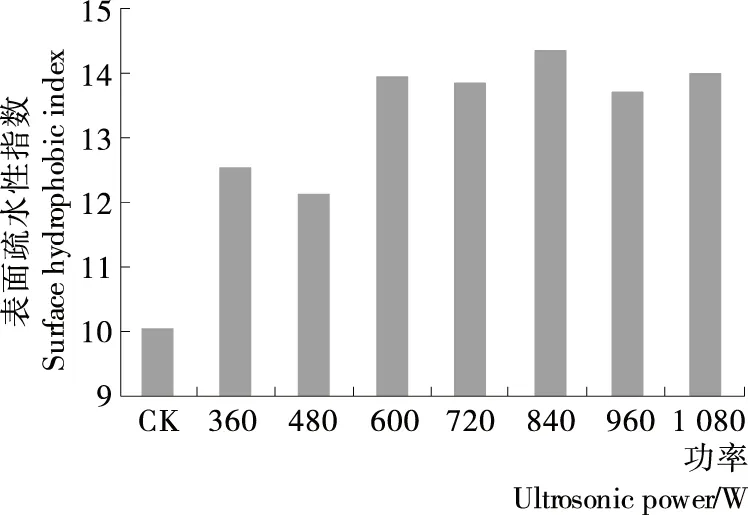
图2 超声处理强度对蛋白表面疏水性指数的影响
2.1.2 超声时间对凝胶性的影响 确定超声功率为840 W后,继续考察不同超声时间(1~8 min)对蛋白速凝性的影响。由图3、4可知,当超声时间在1~6 min时,游离巯基含量始终呈逐渐上升的趋势,二硫键则是逐渐下降,在2~6 min内下降尤为明显。当时间为6 min时,表面疏水性指数也达到最大值。继续延长处理时间到8 min时,游离巯基及二硫键含量均与6 min时无显著变化,但随着超声时间的延长,会使物料温度持续上升,导致分子链断裂,最终引起大分子链降解。因此超声处理时间6 min为最佳,此时的游离巯基含量为19.95 μmol/g,二硫键含量为5.50 μmol/g,表面疏水性指数为14.96。
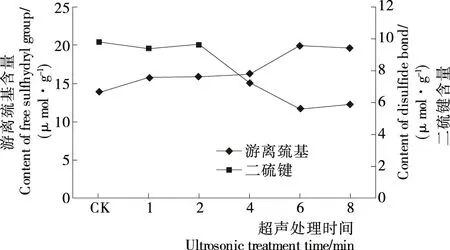
图3 超声处理时间对蛋白游离巯基和二硫键含量的影响
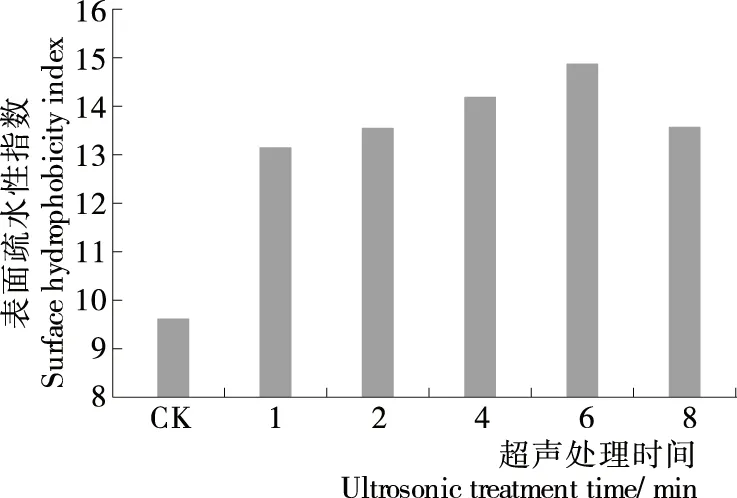
图4 超声处理时间对蛋白表面疏水性指数的影响
2.2 亚硫酸钠处理对凝胶性的影响
2.2.1 亚硫酸钠加入量的确定 由图5、6可知,当亚硫酸钠的加入量(≤0.625 mmol/L)比较低时,蛋白质中游离巯基的含量增加迅速,二硫键含量的下降趋势也很明显,这是由于还原剂的使用打破了蛋白中的二硫键。加入量为0.625 mmol/L时,蛋白质的游离巯基含量为23.65 μmol/g,与原始核桃浓缩蛋白相比提高了73.26%;二硫键含量为4.90 μmol/g,与原始核桃浓缩蛋白相比降低了37.82%;此时蛋白质的表面疏水性指数为17.15,与原始核桃浓缩蛋白相比提高了77.72%。之后,继续增加亚硫化钠的添加量,而蛋白质的游离巯基含量、二硫键含量及表面疏水性指数均没有显著性的变化(P>0.05)。因此,亚硫酸钠适宜加入量为0.625 mmol/L。
2.2.2 亚硫酸钠处理时间的确定 在加入量固定在0.625 mmol/L的条件下,由图7、8可知,当处理时间为15~60 min时,蛋白质游离巯基含量和表面疏水性指数均呈缓慢增加的趋势,二硫键含量则呈缓慢下降趋势。在处理时间为60 min时,蛋白质游离巯基含量为23.95 μmol/g,表面疏水性指数达到16.90,与原始核桃浓缩蛋白相比分别提高了75.38%和75.13%,二硫键含量降至4.93 μmol/g,与原始核桃浓缩蛋白相比降低了48.49%。继续延长处理时间,则发现游离巯基含量及表面疏水性指数开始缓慢下降,二硫键缓慢上升,这可能是亚硫酸钠处理是在振荡条件下进行的,振荡作用增加了蛋白分子间的相互摩擦碰撞的机会,巯基从蛋白中游离出来后,又形成了二硫键交联。因此,亚硫化钠处理适宜时间为60 min。
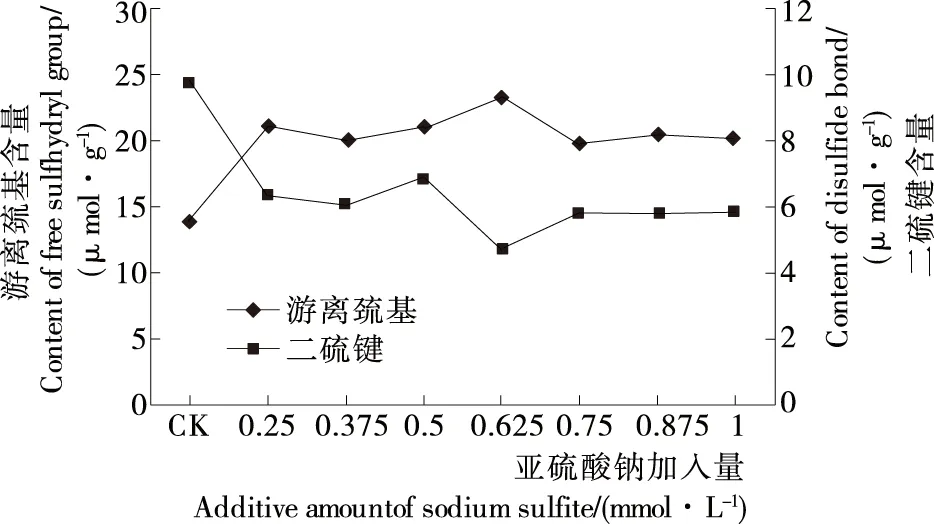
图5 亚硫酸钠加入量对蛋白游离巯基和二硫键含量的影响
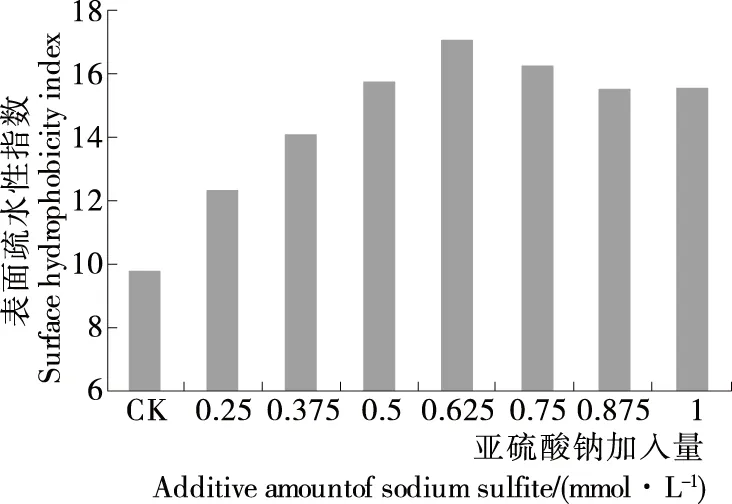
图6 亚硫酸钠加入量对蛋白表面疏水性指数的影响
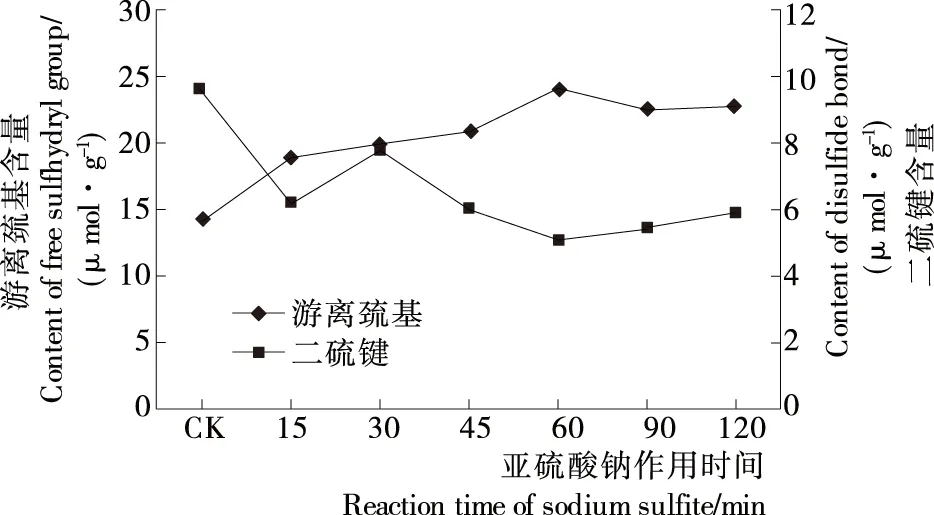
图7 亚硫酸钠作用时间对蛋白游离巯基和二硫键含量的影响
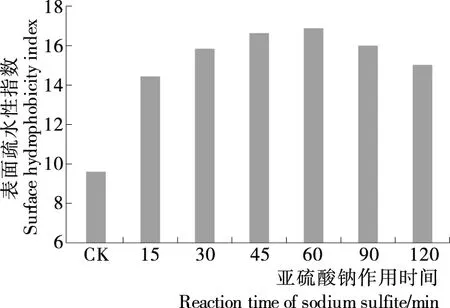
图8 亚硫酸钠加入量对蛋白表面疏水性指数的影响
Figure 8 Effect of additive amount of sodium sulfite on the surface hydrophobicity index of protein
2.3 改性方法对核桃浓缩蛋白最低凝胶点的影响
由于食品体系中pH值大多在中性范围内,因此本研究考察了在中性(pH 7.0)条件下蛋白浓度对胶凝性的影响,结果见表1。
由表1可知,当pH 7.0时,改性前后的蛋白质最低凝胶点是不同的,原始蛋白在浓度为12%时能够形成自持凝胶;而经超声改性后的蛋白在浓度为10%时就能形成较好的自持凝胶;经还原剂亚硫酸钠改性的蛋白在浓度为10%时能够形成半流动性固体,在12%时能形成很好的自持凝胶。由此可见,改性后的核桃浓缩蛋白更容易形成凝胶,其中,超声处理的核桃浓缩蛋白速凝性更为明显。超声处理和还原剂亚硫酸钠处理使蛋白质原来紧密有序的结构变成了松散的结构,疏水基团部分暴露,游离巯基含量增多,因此,一定浓度的蛋白溶液经过热诱导的过程,较易形成热稳定性凝胶。
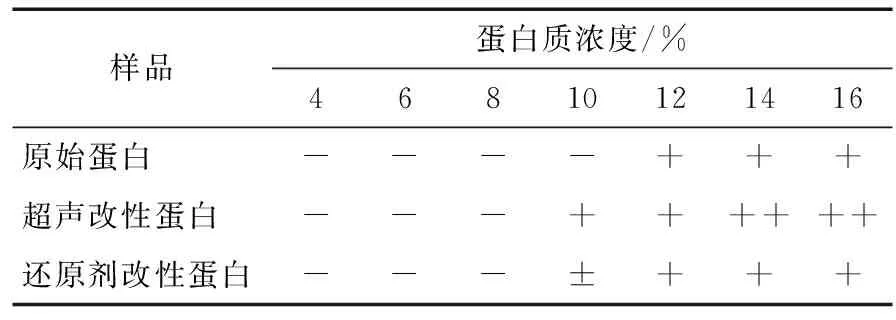
表1 蛋白浓度对胶凝性的影响†
† “-”表示没有自持凝胶形成;“+”表示有自持凝胶形成。
2.4 改性方法对核桃浓缩蛋白凝胶质构特性的影响
蛋白质的凝胶特性主要表现在拥有高硬度、弹性和黏结力,这一性质在肉制品加工中极为重要[15]。由表2可知,改性方法对核桃浓缩蛋白的凝胶硬度具有显著影响,并且经过改性的蛋白凝胶硬度要显著高于改性前的蛋白,尤以超声改性后的凝胶硬度最大,比原始蛋白增加了149.85%,比还原剂改性的蛋白增加了26.22%,而经还原剂改性的蛋白凝胶硬度比原始蛋白增加了97.95%;经不同改性方法处理的蛋白凝胶的弹性并没有显著差异,但改性后的蛋白凝胶的弹性均显著高于原始蛋白,超声改性蛋白的凝胶弹性比原始蛋白增加了66.67%,还原剂改性蛋白的凝胶弹性比原始蛋白增加了78.95%;经不同改性方法处理的蛋白凝胶的黏结力没有显著差异,但改性后的蛋白凝胶的黏结力要显著高于原始蛋白,超声改性蛋白的凝胶黏结力比原始蛋白增加了92.5%,还原剂改性蛋白的凝胶黏结力比原始蛋白增加了80%。综合上述结果,能够说明超声改性对核桃浓缩蛋白凝胶性的改善作用更大。
表2 改性方法对核桃浓缩蛋白凝胶质构性的影响†
Table 2 Effects of different modification methods on the texture characteristics of walnut protein concentrate
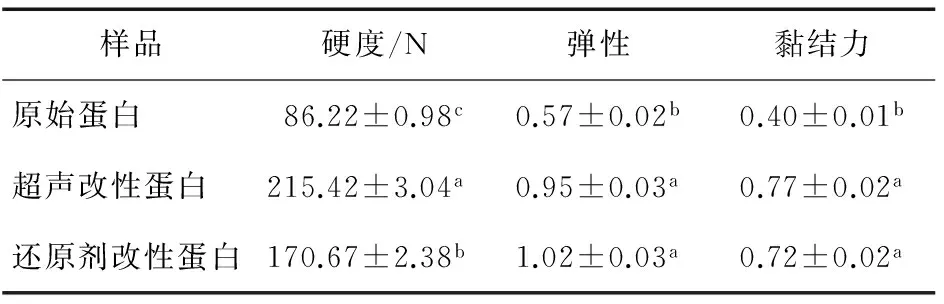
样品硬度/N弹性黏结力原始蛋白86.22±0.98c0.57±0.02b0.40±0.01b超声改性蛋白215.42±3.04a0.95±0.03a0.77±0.02a还原剂改性蛋白170.67±2.38b1.02±0.03a0.72±0.02a
† 同列不同字母表示在P<0.05时差异显著性。
3 结论
超声波处理和亚硫酸钠改性均可打破核桃浓缩蛋白的二硫键,提高游离巯基含量,从而提高核桃浓缩蛋白形成凝胶的特性。改性后的蛋白凝胶硬度、弹性、黏结力等质构特征均显著优于改性前,超声改性对蛋白凝胶速凝性和硬度提高尤为显著。由于化学改性存在化学成分和副产物残留,因此,超声改性处理在提高核桃浓缩蛋白的凝胶性方面更具有应用前景。
[1] 张婷婷. 不同施肥处理对核桃生长、产量和坚果品质的影响[D]. 杨凌: 西北农林科技大学, 2016: 1.
[2] 施显赫, 王丰俊, 欧阳杰. 核桃油制取方法和质量评价研究进展[J]. 食品工业科技,2013, 34(8): 395-399.
[3] MAO Xiao-ying, HUA Yu-fei. Composition, structure and functional properties of protein concentrates and isolates produced from walnut(JuglansregiaL) [J]. International Journal of Molecular Sciences, 2011, 13(2): 1 561-1 581.
[4] 沈敏江, 刘红芝, 刘丽, 等. 核桃蛋白质的组成、制备及其功能特性研究进展[J]. 中国粮油学报, 2014, 29(1): 123-128.
[5] 周杰, 陈韬. 大豆蛋白的功能特性及其在肉制品中的应用[J]. 肉类工业, 2009(11): 46-49.
[6] 杜蕾蕾, 郭涛, 万辉, 等. 核桃蛋白的分离纯化及功能性质的研究[J]. 中国油脂, 2009, 34(5): 21-24.
[7] 吴海文. 花生浓缩蛋白的制备凝胶形成机理及其应用研究[D]. 北京: 中国农业科学院, 2009.
[8] 孟小波, 华欲飞, 孔祥珍. 加热改性醇法大豆浓缩蛋白凝胶性的研究[J]. 中国油脂, 2008, 33(10): 25-28.
[9] 姚玉静, 杨晓泉, 唐传核, 等. 酰化对大豆分离蛋白凝胶性质的影响[J]. 食品与机械, 2008, 24(5): 9-11.
[10] 王丽, 王强, 刘红芝, 等. 花生品质对其蛋白质凝胶性的影响[J]. 农业工程学报, 2012, 28(17): 260-267.
[11] BEVERIDGE T, TOMA S J, NAKAI S D. Determination of SH- and SS-groups in some food proteins using Ellman’s reagent[J]. Journal of Food Science, 1974, 39(1): 49-51.
[12] 邵俊花, 吴菊清, 周光宏, 等. 巯基和疏水性对蛋白质乳化及凝胶特性的影响[J]. 食品科学, 2013, 34(23): 155-159.
[13] 林静韵, 李琳, 李坚斌, 等. 马铃薯淀粉糊在超声场中凝胶质构特性的变化研究[J]. 食品科学, 2007, 28(8): 120-123.
[14] 张华江, 迟玉杰. 两种改性技术提高大豆分离蛋白凝胶性能的研究[J]. 中国粮油学报, 2008, 23(4): 56-59.
[15] 郝红涛, 赵改名, 柳艳霞, 等. 肉类制品的质构特性及其研究进展[J]. 食品与机械, 2009, 25(3): 125-128.
Effects of different modification methods on gelation of walnut protein concentrate
HUXue-jiao1,2,3CHENYong-hao1,2ZHANGChun-hong3HAOYan-bin1,2QIJian-xun1,2DONGNing-guang1,2
(1.InstituteofForestryandPomology,BeijingAcademyofAgricultureandForestryScience,Beijing100093,China;2.BeijingEngineeringResearchCenterforDeciduousFruitTrees,Beijing100093,China;3.FoodScienceCollege,ShenyangAgriculturalUniversity,Shenyang,Liaoning110866,China)
In this study, walnut protein concentrate was modified through physical and chemical Methods respectively. After modification, free sulfhydryl group, disulfide bond content and surface hydrophobic of walnut protein concentrate were determined and the effects of different modification methods on gelation were explored. In order to obtain walnut protein concentrate with stronger gelation potential, the appropriate modification conditions were determined and textural characteristics of protein gel were also analyzed before and after modification. The results showed that the appropriate condition of physical modification(ultrasonic processing) was being treated using ultrasonic power at 840 W for 6 min. The proper condition of chemical modification (reducing agent sodium sulfite) was being reduced using a 0.625 mmol/L reductant for 60 min. It turned out that the ultrasonic modification was the more appropriate method to obtain the optimum gel performance of walnut protein concentrate.
walnut; protein; modification; gelation; texture property
北京市科技新星计划项目(编号:Z131105000413021)
胡雪娇,女,沈阳农业大学在读硕士研究生。
陈永浩(1979—),男,北京市农林科学院副研究员,博士。E-mail:cyh2010@126.com
郝艳宾(1963—),男,北京市农林科学院研究员,博士。
2015-05-29
10.13652/j.issn.1003-5788.2016.10.004
E-mail:jinhetaojht@263.net
