3LiBH4/CeF3体系的放氢性能及机制
2016-12-01王春阳黄维军柳东明
顾 润, 张 明, 王春阳, 黄维军, 柳东明
(安徽工业大学材料科学与工程学院, 马鞍山 243002)
3LiBH4/CeF3体系的放氢性能及机制
顾 润, 张 明, 王春阳, 黄维军, 柳东明
(安徽工业大学材料科学与工程学院, 马鞍山 243002)
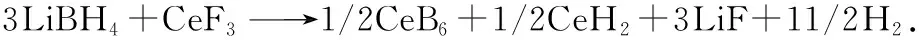
硼氢化锂; 氟化铈; 放氢性能; 放氢机制
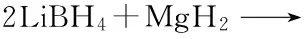
Nakamori等[12]发现, 将金属氯化物MCln(M=Ca, Sc, Ti, V, Cr, Mn, Zn或Al)与LiBH4以一定摩尔比球磨5 h后, 可以生成相应的硼氢化物M(BH4)n, 并且M电负性越大, M(BH4)n的分解温度越低, 但当M电负性大于1.5时(M=Al, Mn或Zn), 在生成H2的同时会伴随有B2H6的产生. Au等[13]研究发现, 2LiBH4/TiCl3, 2LiBH4/ZnF2及2LiBH4/TiF3体系的放氢温度与纯LiBH4相比有了显著降低. Fang等[14]和Guo等[15]的研究结果表明, TiF3的加入使得LiBH4的放氢热力学和动力学性能均得到改善. Zhang等[16]研究了(Ce, La)(Cl, F)3对LiBH4的降稳效应, 其研究结果表明, 3LiBH4/(Ce, La)(Cl, F)3体系的放氢温度为220~320 ℃, 在球磨过程中, CeCl3和LaCl3与LiBH4反应分别形成Ce(BH4)3和La(BH4)3, 而在后续加热过程中Ce(BH4)3和La(BH4)3分解放氢. 反应为
(1)
目前, 对放氢过程中CeF3或LaF3与LiBH4之间的相互作用以及放氢温度降低的原因尚不明确. 本文研究了3LiBH4/CeF3体系的放氢性能及反应机制, 并对放氢性能改善的原因进行了分析.
1 实验部分
1.1 试剂与仪器
LiBH4粉末(纯度95%)和CeF3粉末(纯度99.9%)购自美国Alfa Aesar公司.
米开罗那(中国)有限公司Super 1220/750/900型手套箱; 南京大学仪器厂QM-3SP2型行星球磨机; 日本铃木商社全自动压力-组成-温度(PCT)测试仪; 日本理学公司Rigaku D/Max 2500VL/PC型X射线衍射仪(XRD), CuKα辐射源, 工作电压50 kV, 工作电流200 mA, 采取步进式扫描方式, 步长0.02°, 积分时间1 s; 美国赛默飞世尔科技公司Nicolet 6700型傅里叶变换红外光谱仪(FTIR).
1.2 样品的制备
在氩气保护的手套箱内, 按摩尔比3∶1称量LiBH4和CeF3粉末, 混合均匀后倒入250 mL不锈钢球磨罐内, 在球磨机上对3LiBH4+ CeF3混合粉末进行不同时间(2, 10或16 h)的球磨处理, 即得到样品3LiBH4/CeF3(BM-2 h), 3LiBH4/CeF3(BM-10 h)和3LiBH4/CeF3(BM-16 h). 不加入CeF3, 仅对LiBH4粉末进行2 h的球磨处理, 所得样品记为LiBH4(BM-2 h). 球磨机的操作条件为: 球料比30∶1, 转速400 r/min, 每30 min正反转交替一次.
2 结果与讨论
2.1 3LiBH4/CeF3体系的升温放氢性能及反应机制
图1给出了3LiBH4/CeF3体系经不同时间球磨后的升温放氢曲线. 可以看出, 不同球磨时间样品的升温放氢曲线基本重合, 即球磨时间对体系的放氢行为影响不大. 体系在295 ℃左右快速放氢, 并基本完成放氢过程, 总放氢量为4.1%(质量分数). 同时, 图1还给出了纯LiBH4球磨2 h后的放氢曲线, 通过比较可见, 3LiBH4/CeF3体系的放氢温度远低于纯LiBH4, 这与Zhang等[16]的研究结果基本一致.
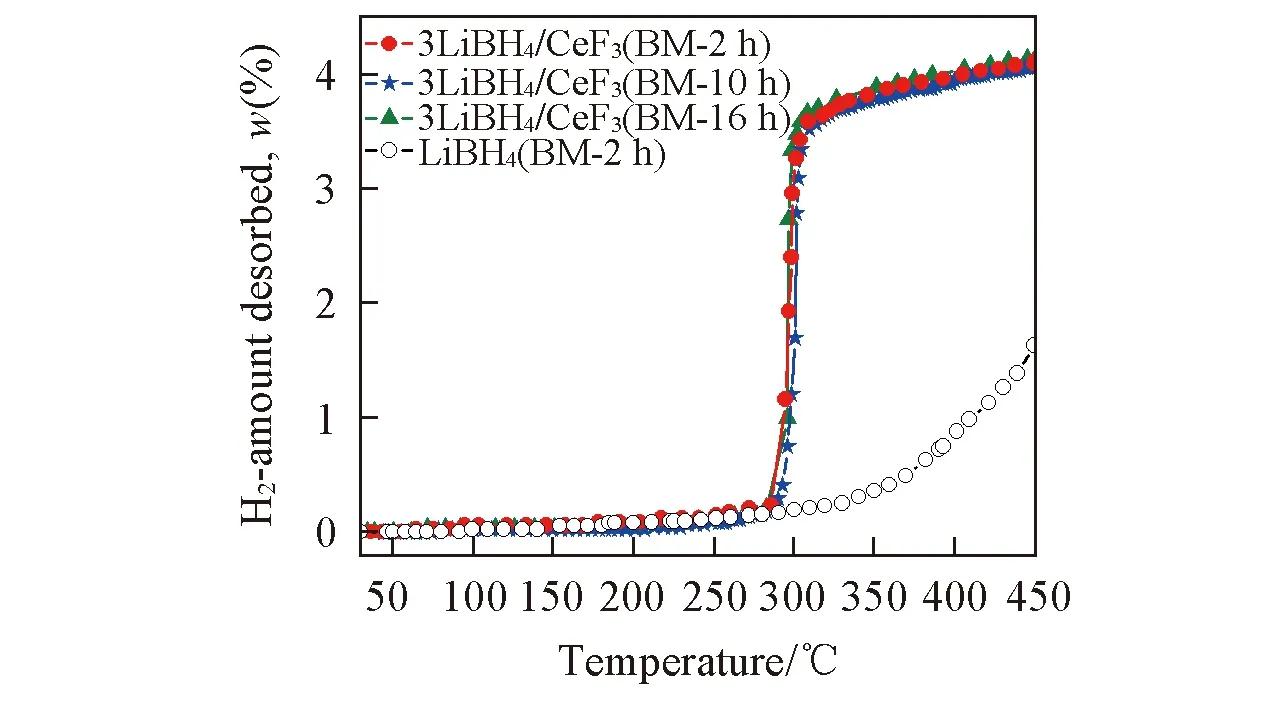
Fig.1 Hydrogen desorption curves of the 3LiBH4/CeF3 system ball-milled for different time
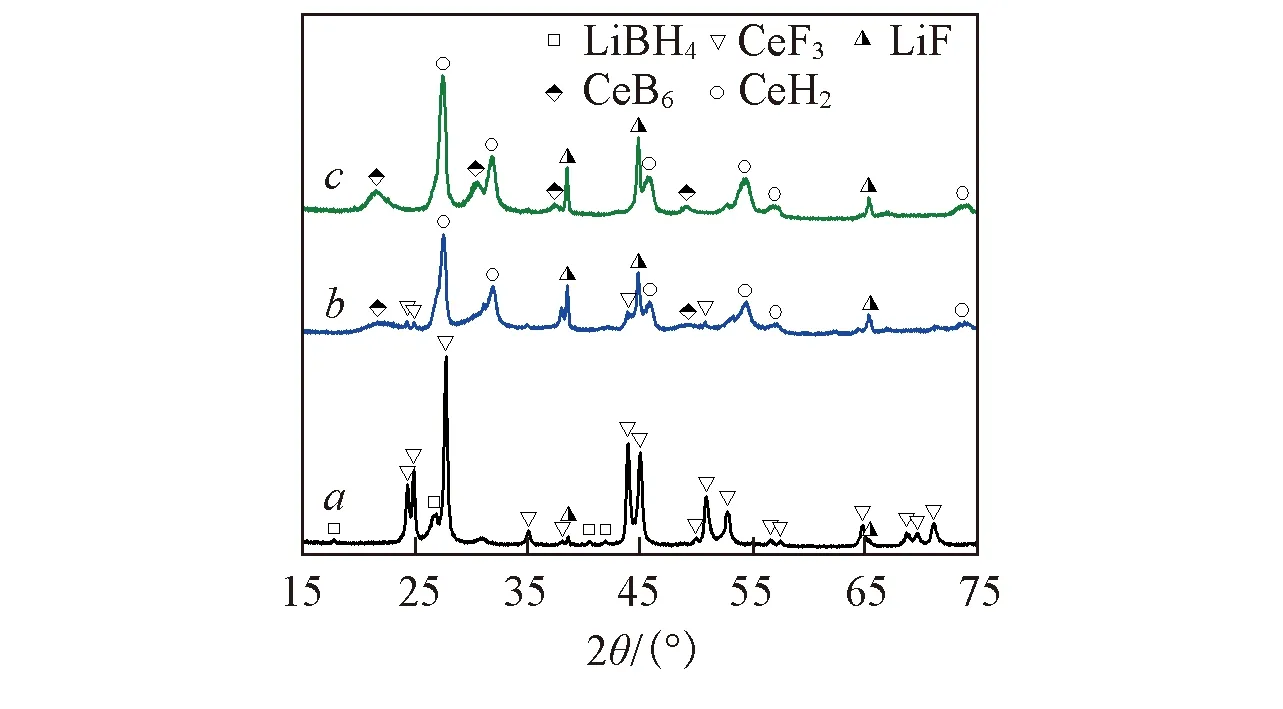
Fig.2 XRD patterns of the 3LiBH4/CeF3(BM-2 h) system dehydrogenated at 250(a), 350(b) and 450 ℃(c), respectively
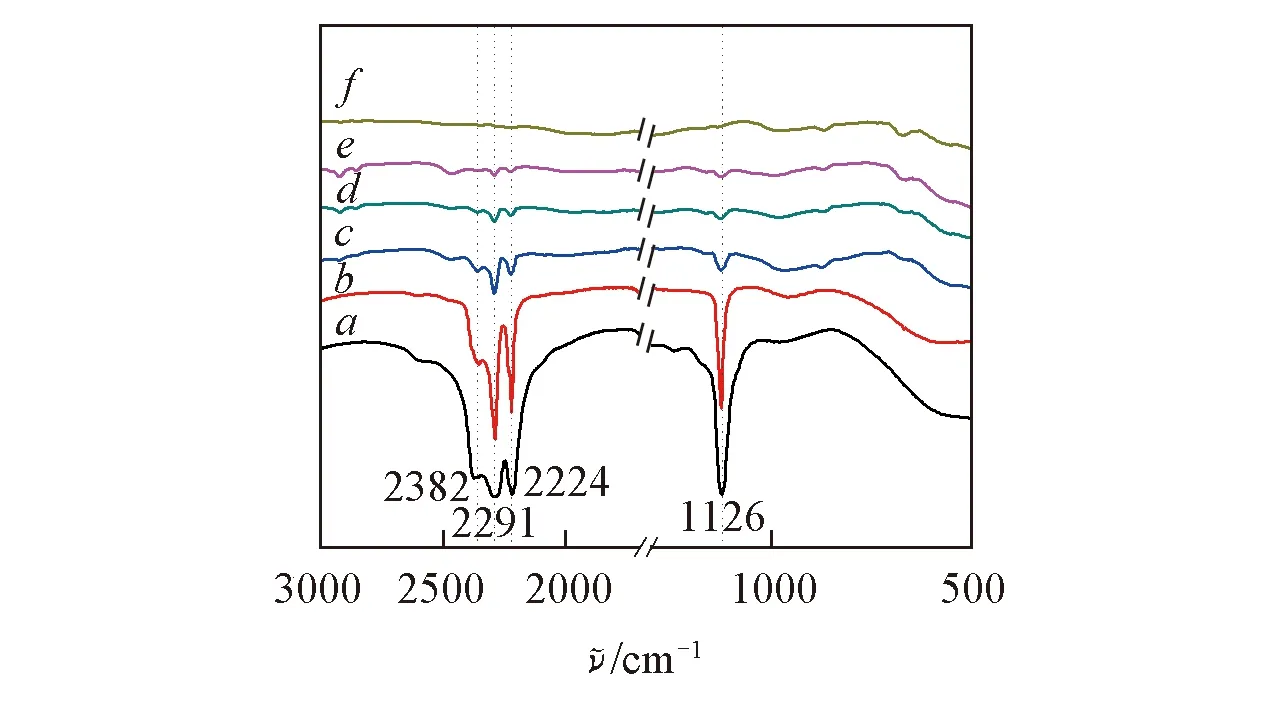
Fig.3 FTIR spectra of the 3LiBH4/CeF3(BM-2 h) system before(a) and after(b—f) heating at different temperaturesHeating temperature/℃: b. 250; c. 300; d. 350; e. 400; f. 450.
为了研究3LiBH4/CeF3体系的放氢过程, 图2给出了球磨2 h的体系不同温度放氢产物的XRD谱图. 由图2谱线a可知, 3LiBH4/CeF3体系在250 ℃的物相组成基本为初始成分LiBH4和CeF3. 当加热到350 ℃时, CeF3的衍射峰强度明显变弱, 同时出现了CeB6, CeH2和LiF的衍射峰(图2谱线b). 当温度升至450 ℃时, 从图2谱线c可见, CeF3的衍射峰完全消失, 放氢产物由CeB6, CeH2和LiF 3种物相组成.
图3为3LiBH4/CeF3体系球磨及加热到不同温度的FTIR图谱. 由图3谱线a可知, 球磨2 h后的样品在2382, 2291, 2224及1126 cm-1处有明显的对应于LiBH4中B—H键的伸缩和弯曲振动的特征吸收峰. 当加热至250 ℃时, 如图3谱线b所示, 3LiBH4/CeF3体系的FTIR谱图与球磨后的FTIR谱图基本一致. 当加热至300 ℃时, 图3谱线c中B—H键吸收谱带的强度明显减弱, 但位置没有发生明显变化, 说明此时LiBH4开始分解但并没有生成Ce(BH4)3. 随着温度继续升高, B—H键吸收谱带的强度逐渐降低, 到450 ℃时完全消失(见图3谱线f), 表明LiBH4已完全分解, 这与图1中的升温放氢结果基本一致.
根据以上分析可以判断, 3LiBH4/CeF3体系在球磨和加热过程中并未出现如3LiBH4/CeCl3体系中Ce(BH4)3形成和分解放氢的现象, 其放氢过程主要来源于CeF3与LiBH4之间的直接反应, 该反应可表示为
(2)
根据式(2)可以计算出3LiBH4/CeF3体系的理论放氢量为4.2%, 该值与图1中的实际放氢量(4.1%)非常接近.
2.2 3LiBH4/CeF3体系的放氢热力学
图4为3LiBH4/CeF3体系在290 ℃放氢的p-c曲线. 可以看出, 在0~7 MPa范围内, 体系的放氢p-c曲线中存在一个明显的平台, 平台压约为3.17 MPa. 纯LiBH4放氢反应的焓变(ΔH0—)和熵变(ΔS0—)分别约为74 kJ/mol H2和115 J/(K·mol)[3], 代入van’t Hoff方程:
lnpH2=-ΔH0—/(RT)+ΔS0—/R
式中:pH2为H2的分压;R为气体常数;T为绝对温度. 由此可以算出纯LiBH4在290 ℃时的放氢平台压约为0.014 MPa, 远低于3LiBH4/CeF3体系. 通常对于氢化物, 放氢平台压越高, 放氢的热力学驱动力越大, 氢化物的稳定性就越低. 可见, 与纯LiBH4相比, CeF3的加入大大降低了体系放氢的热力学稳定性, 从而导致3LiBH4/CeF3体系具有较低的放氢温度.
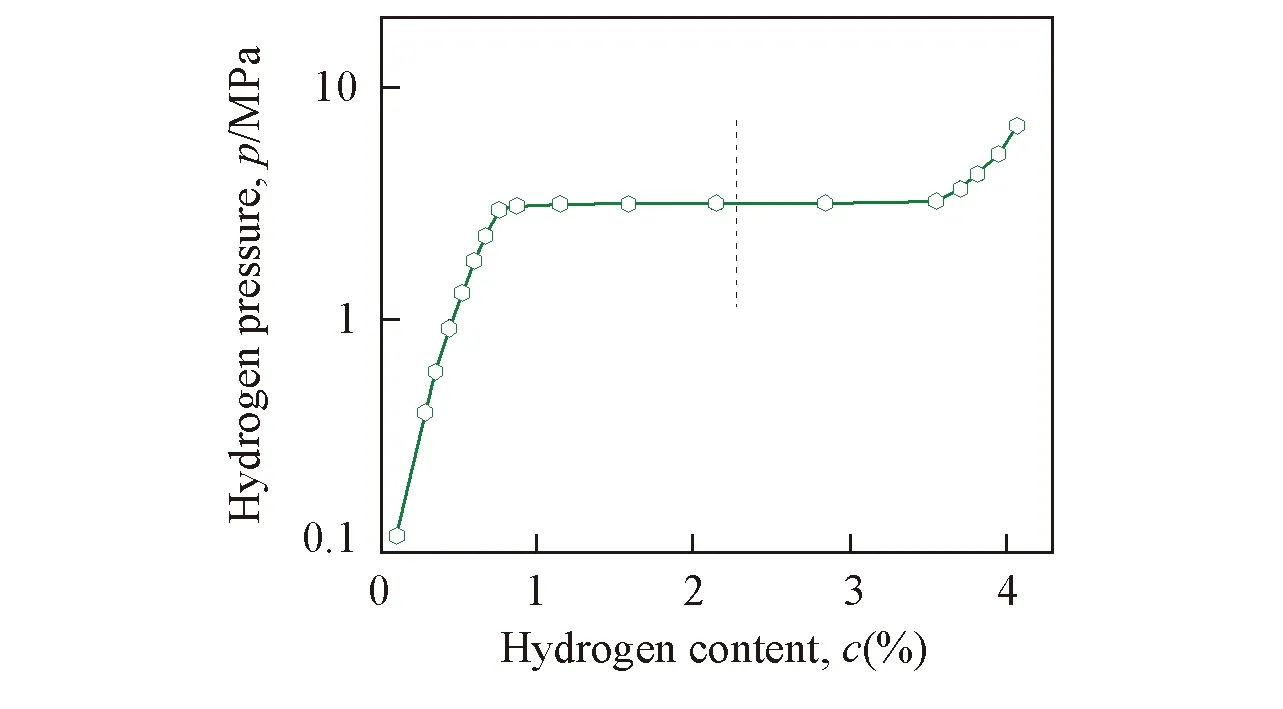
Fig.4 Dehydrogenation p-c isotherm of the 3LiBH4/CeF3 system at 290 ℃
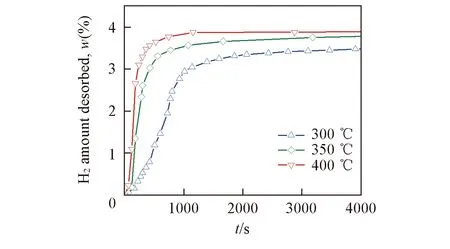
Fig.5 Isothermal dehydrogenation curves of the 3LiBH4/CeF3 system at different temperatures
2.3 3LiBH4/CeF3体系的放氢动力学性能
图5给出了3LiBH4/CeF3体系在不同温度下的放氢动力学曲线. 可见, 300 ℃时体系在1200 s内大约放出3.1%的氢气; 随着放氢温度的升高, 体系的放氢速率逐渐增大, 400 ℃时, 600 s内放氢量即可达到3.7%, 1000 s后放氢便趋于稳定. 为了进一步揭示3LiBH4/CeF3体系的放氢动力学机制, 利用动力学模型对该体系的放氢动力学曲线进行分析, 该模型可以表述为
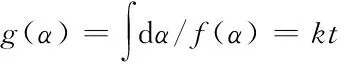
(3)
式中:α为t时刻的反应分数, 由该时刻的放氢量除以总放氢量(4.1%)得到;g(α)和f(α)为功能函数, 代表不同反应机制;k为速率常数. 采用不同的功能函数[17,18]对图5中的实验数据进行拟合, 发现在较宽的α范围内函数[-ln(1-α)]1/2对t具有较好的线性拟合度, 即3LiBH4/CeF3体系的放氢过程主要由二维形核和长大机理来控制.
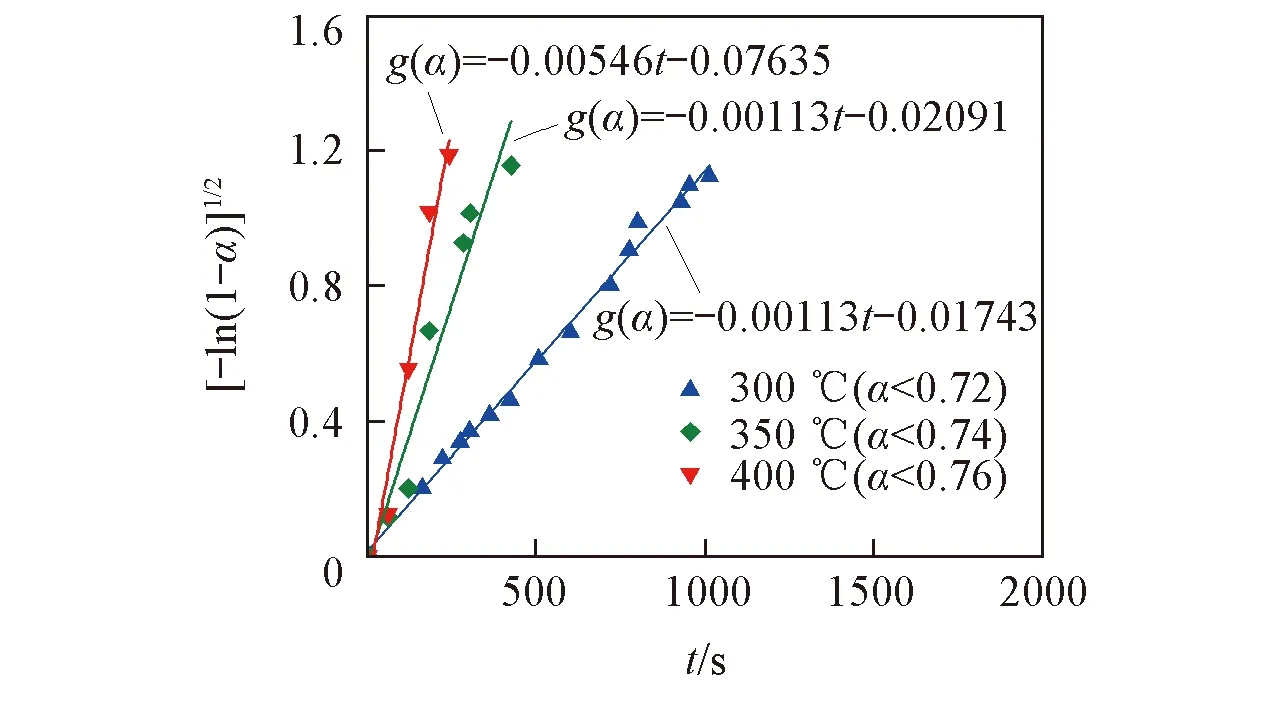
Fig.6 Plots of [-ln(1-α)]1/2 vs. t for the 3LiBH4/CeF3 system dehydrogenated at different temperatures
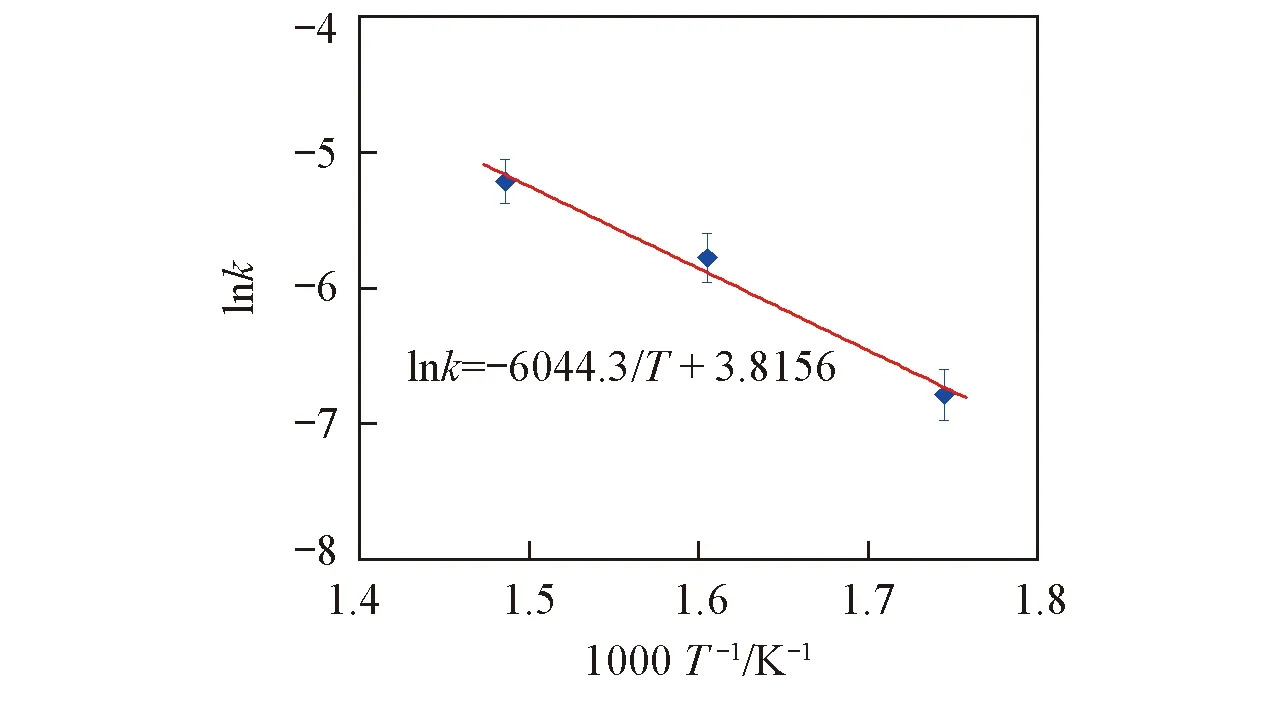
Fig.7 Arrhenius curve for the dehydrogenation of the 3LiBH4/CeF3 system
图6示出了不同温度下函数[-ln(1-α)]1/2与t的线性关系. 根据图6中拟合直线的斜率可以得到不同温度下的速率常数k, 继而可以通过Arrhenius方程[式(4)]获得放氢过程的表观活化能
(4)
式中: k0是指前因子, R是气体常数, T是绝对温度. 图7给出了lnk与1/T间的关系曲线. 可以看出,lnk和1/T之间具有良好的线性关系. 由直线的斜率(-Ea/R)可以算得3LiBH4/CeF3体系的放氢表观活化能Ea=50kJ/mol, 该值明显低于纯LiBH4的放氢反应活化能111~156kJ/mol[2,19,20], 这是3LiBH4/CeF3体系放氢性能改善的另一个原因.
3 结 论
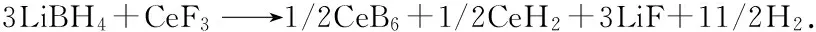
[1]ZüttelA., Mater. Today, 2003, 6(9), 24—33
[2]ZüttelA.,RentschS.,FischerP.,WengerP.,SudanP.,MauronP.,EmmeneggerC., J. Alloys Compd., 2003, 356/357, 515—520
[3]MauronP.,BuchterF.,FriedrichsO.,RemhofA.,BielmannM.,ZwickyC.N.,ZüttelA., J. Phys. Chem. B, 2008, 112(3), 906—910
[4]FangZ.Z.,KangX.D.,LuoJ.H.,WangP.,LiH.W.,OrimoS., J. Phys. Chem. C, 2010, 114(51), 22736—22741
[5]GongX.J.,ChengL.P.,XuB.E.,ZengY.L.,LiX.Y.,MengL.P., Chem. J. Chinese Universities, 2013, 34(8), 1929—1935(巩雪敬, 成丽苹, 许保恩, 曾艳丽, 李晓艳, 孟令鹏. 高等学校化学学报, 2013, 34(8), 1929—1935)
[6]CaiW.T.,WangH.,JiaoL.F.,WangY.J.,ZhuM., Int. J. Hydrogen Energy, 2013, 38(8), 3304—3312
[7]ZhangH.,ZhouY.X.,SunL.X.,CaoZ.,XuF.,LiuS.S.,ZhangJ.,SongL.F.,SiX.L.,JiaoC.L.,WangS.,LiZ.B.,LiuS.,LiF., Chem. J. Chinese Universities, 2012, 33(4), 78l—785(张慧, 周奕汐, 孙立贤, 曹忠, 徐芬, 刘淑生, 张箭, 宋莉芳, 司晓亮, 焦成丽, 王爽, 李志宝, 刘双, 李芬. 高等学校化学学报, 2012, 33(4), 78l—785)
[8]GuoL.J.,JiaoL.F.,LiL.,WangQ.H.,LiuG.,DuH.M.,WuQ.,DuJ.,YangJ.Q.,YanC.,WangY.J.,YuanH.T., Int. J. Hydrogen Energy, 2013, 38(1), 162—168
[9]JinS.A.,LeeY.S.,ShimJ.H.,ChoY.W., J. Phys. Chem. C, 2008, 112(25), 9520—9524
[10]VajoJ.J.,SkeithS.L.,MertensF., J. Phys. Chem. B, 2005, 109(9), 3719—3122
[11]KouH.Q.,SangG.,ChenL.X.,XiaoX.Z.,DengS.S.,HuangZ.Y., Chem. J. Chinese Universities, 2013, 34(10), 2347—2352(寇化秦, 桑革, 陈立新, 肖学章, 邓帅帅, 黄志勇. 高等学校化学学报, 2013, 34(10), 2347—2352)
[12]NakamoriY.,LiH.W.,KikuchiK.,AokiM.,MiwaK.,TowataS.,OrimoS., J. Alloys Compd., 2007, 446/447, 296—300
[13]AuM.,JurgensenA.R.,SpeneerW.A.,AntonD.L.,PinkertonF.E.,HwangS.J.,KimC.,BowmanR.C., J. Phys. Chem. C, 2008, 112(47), 18661—18671
[14]FangZ.Z.,MaL.P.,KangX.D.,WangP.J.,WangP.,ChengH.M., Appl. Phys. Lett., 2009, 94(4), 044104
[15]GuoY.H.,YuX.B.,GaoL.,XiaG.L.,GuoZ.P.,LiuH.K., Energy Environ. Sci., 2010, 3(4), 464—469
[16]ZhangB.J.,LiuB.H.,LiZ.P., J. Alloys Compd., 2011, 509(3), 751—757
[17]ZhangY.,TianQ.F.,ZhangJ.,LiuS.S.,SunL.X., J. Phys. Chem. C, 2009, 113(42), 18424—18430
[18]LiY.,ZhouG.,FangF.,YuX.,ZhangQ.,OuyangL.,ZhuM.,SunD., Acta Mater., 2011, 59(4), 1829—1838
[19]GrossA.F.,VajoJ.J.,AttaS.L.,OlsonG.L., J. Phys. Chem. C, 2008, 112(14), 5651—5657
[20]KatoS.,BielmannM.,BorgschulteA.,HerzogV.Z.,RemhofA.,OrimoS.I.,ZüttelA., Phys. Chem. Chem. Phys., 2010, 12(36), 10950—10955
(Ed.: S, Z, M)
† Supported by the National Natural Science Foundation of China(No.51371008).
Dehydrogenation Property and Mechanism of 3LiBH4/CeF3System†
GU Run, ZHANG Ming, WANG Chunyang, HUANG Weijun, LIU Dongming*
(SchoolofMaterialsScienceandEngineering,AnhuiUniversityofTechnology,Maanshan243002,China)
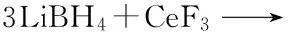
LiBH4; CeF3; Dehydrogenation property; Dehydrogenation mechanism
10.7503/cjcu20150848
2015-11-04.
日期: 2016-01-24.
国家自然科学基金(批准号: 51371008)资助.
O643
A
联系人简介: 柳东明, 男, 博士, 教授, 主要从事储氢材料研究. E-mail: ldm_ahut@163.com
