双柱串联–便携式气相色谱法测定室内空气中苯系物*
2016-11-30潘扬昌莫达松黄璐璐梁勇谢安杰覃仁港
潘扬昌,莫达松,黄璐璐,梁勇,谢安杰,覃仁港
(广西壮族自治区分析测试研究中心,南宁 530022)
双柱串联–便携式气相色谱法测定室内空气中苯系物*
潘扬昌,莫达松,黄璐璐,梁勇,谢安杰,覃仁港
(广西壮族自治区分析测试研究中心,南宁 530022)
建立双柱串联–便携式气相色谱测法定室内空气中苯系物的方法。利用仪器内部自带的Tenax吸附剂在0.5 L/min流量下采集空气样品100 s,然后仪器迅速升温至400℃左右,对吸附剂进行热解吸进样,以微亚离子检测器(MAID)对室内空气中7种苯系物进行测定。结果表明,色谱条件为MXT–200/MXT–WAX金属毛细管柱串联色谱柱,柱温90℃,柱压103 425 Pa时,分离效果最好,且运行时间短。各组分在19.26~306.7 μg/m3范围内与色谱峰面积的平方根线性关系良好,相关系数r大于0.995。方法检出限为6.40~15.9 μg/m3,空白加标回收率为92%~114%,测定结果的相对标准偏差为6.1%~13.7%(n=6)。采用双柱串联便携式气相色谱法测定室内空气中苯系物具有快速、准确、方便等优点。
苯系物;室内空气;便携式气相色谱法;双柱串联;微亚离子检测器
苯系物是室内装修污染较为严重的一类化合物[1],它们对人体的危害越来越受到人们的关注[2–3]。近年来,许多学者已经对苯系物的风险性以及致病机理做了大量研究工作,比如苯系物在人体内的代谢产物研究,苯系物的协同效应研究等[4–7]。苯系物对人的中枢神经系统以及血液系统具有毒害作用,与白血病的高发有着较大的相关性[8–9]。有关研究表明,苯系物与癌症的发生有着密切联系[10–11]。目前用于分析苯系物的方法有气相色谱法(GC)、气相色谱–质谱法(GC–MS)、离子迁移谱法、高效液相色谱法等[12–13]。空气中苯系物的现行国家标准检测方法有溶剂解吸或热解吸气相色谱法[14–15],这些方法准确度及精密度都很高,但样品需要采集,分析时间较长,成本较高,实际应用受到一定限制。便携式气相色谱能弥补这些不足,它不仅具有气相色谱的基本功能,而且体积小,便于携带,分析样品时间较短,可以现场分析样品,因而可以减少检测人员的工作量以及降低检测成本。目前便携式气相色谱主要应用在环境应急监测中[16],在室内空气中应用较少。笔者采用便携式气相色谱仪,配置微亚离子检测器(MAID),对苯系物进行检测。仪器内部还配置了预浓缩器,对于低浓度的样品可以延长采气时间,这样可以降低检出浓度。样品经过预浓缩器浓缩后可以快速加热升温至400℃左右而达到快速进样的目的,而且检测灵敏度高。
1 实验部分
1.1 主要仪器与试剂
便携式气相色谱仪:CMS 100型,美国因富康公司;
多元气体校准仪:146i型,稀释倍数5~2 500倍,美国热电公司;
微型注射器:10 μL,1 mL,美国安捷伦公司;
配气袋:3 L,上海颐乐经贸有限公司;
甲醇、苯、甲苯、对二甲苯、间二甲苯、邻二甲苯、乙苯、苯乙烯:色谱纯,德国CNW科技公司。
1.2 标准气体配制方法
(1)气袋清洗。将3 L气袋清洗干净,必要时可注入1 μL甲醇,然后充满零气,再用真空泵抽干净,重复3~5次。
(2)标准气体的制备。将清洗好的气袋准确注入一定体积零气,然后用微型注射器量取一定量苯、甲苯、对二甲苯、间二甲苯、邻二甲苯、乙苯和苯乙烯。完全气化后,再用1 mL注射器准确量取一定量的储备气注入另一只已准确注入一定体积零气的气袋中。同时记录气温、气压,并由此计算标准气体的浓度。
1.3 色谱条件
色谱柱:MXT–WAX金属毛细柱(30 m×0.53 mm,1.00 μm,美国RESTEK公司)和MXT–200金属毛细柱(30 m×0.53 mm,1.00 μm,美国RESTEK公司)串联;柱箱温度:90℃;柱压:103 425 Pa;检测器:微亚离子检测器;载气:氩气;预浓缩器的吸附剂:CARBXEN;采样时间:100 s;热解吸时间:4 s;色谱图延迟时间:180 s。
1.4 实验方法
利用仪器内部自带的Tenax吸附剂在0.5 L/min流量下采集空气样品100 s,然后仪器会迅速升温至400℃左右,对吸附剂进行热解吸进样,按1.3色谱条件对室内空气中7种苯系物进行测定。
2 结果与讨论
2.1 色谱条件优化
保持采样时间为100 s,解吸时间为4 s不变。对色谱条件进行优化,包括色谱柱的选择,柱温、柱压的优化。
2.1.1 MXT–200金属毛细柱色谱条件优化
参考GB/T 18204.2–2014 《公共场所卫生检验方法第2部分:化学污染物》附录C[17],首先使用MXT–200金属毛细柱进行优化试验,试验结果如图1、图2所示。
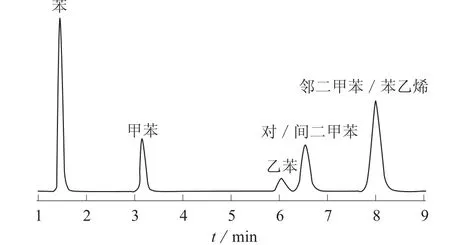
图1 柱温70℃、柱压68 950 Pa,MXT–200金属毛细柱色谱图
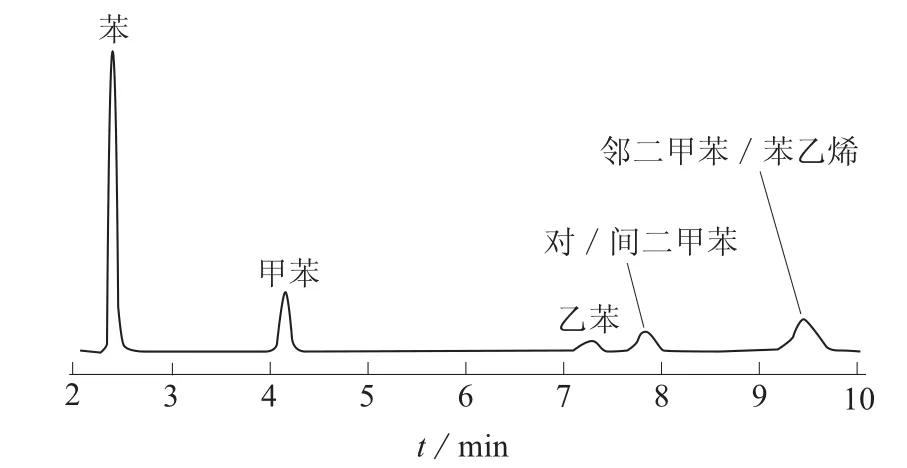
图2 柱温50℃、柱压55 160 Pa,MXT–200金属毛细柱色谱图
由图1、图2看出,7种苯系物未能完全分离,通过进单标样对比发现,对二甲苯和间二甲苯不能分离,苯乙烯和邻二甲苯也不能分离。降温降压都未能分离,而且造成峰形变差,因此色谱条件无法继续优化。GB/T 18204.2–2014 《公共场所卫生检验方法 第2部分:化学污染物》附录C[17]中给出的便携式气相色谱分析条件中所使用的色谱柱是MXT–200金属毛细柱,但是分析组分中并未包含苯乙烯,按照该条件对二甲苯进行分析时,苯乙烯会造成干扰。
2.1.2 MXT–WAX金属毛细柱色谱条件优化
为了能达到分离的目的,选择了MXT–WAX金属毛细柱再次进行优化试验,试验结果如图3、图4所示。
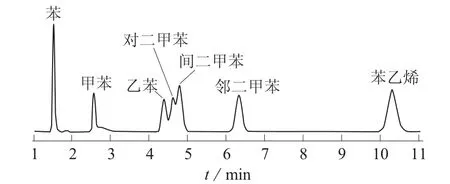
图3 柱温70℃、柱压68 950 Pa,MXT–WAX金属毛细柱色谱图
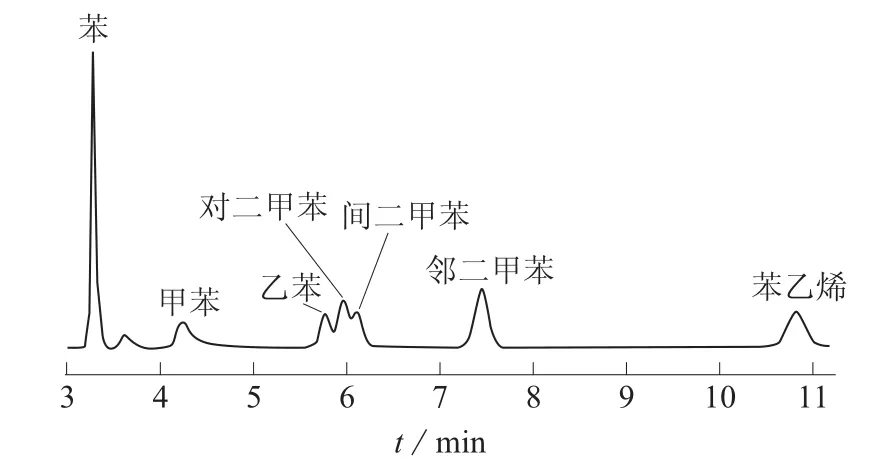
图4 柱温50℃、柱压55 160 Pa,MXT–WAX金属毛细柱色谱图
由图1~图4看出,MXT–WAX金属毛细柱分离效果较MXT–200金属毛细柱要好,但是乙苯、对二甲苯和间二甲苯3个组分有部分重叠,即使将柱温降到50℃,柱压降到55 160 Pa,也不能完全分离,而且峰形开始有拖尾,对定性定量都产生不良影响,因此该色谱柱也不适用。
2.1.3 双柱串联色谱条件优化
在没有合适的色谱柱的情况下,将MXT–WAX金属毛细柱和MXT–200金属毛细柱串联起来进行试验,分离效果见图5、图6。
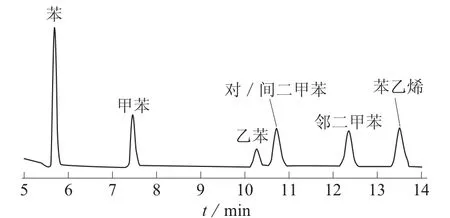
图5 柱温70℃、柱压68 950 Pa,双柱串联色谱图
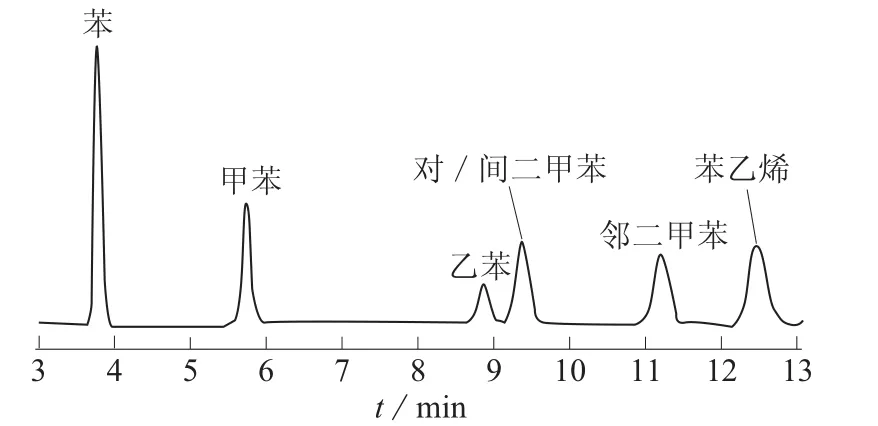
图6 柱温90℃、柱压103 425 Pa,双柱串联色谱图
从图5、图6可看出,无论是柱温70℃、柱压68 950 Pa,还是柱温90℃、柱压103 425 Pa,双柱串联的分离效果均很好,除了对二甲苯和间二甲苯不能分离外,其它组分分离都很好,这应该是两根色谱柱串联在一起后达到了取长补短的效果。《室内空气质量标准》[18]中二甲苯是以3个组分的总和作为指标的,因此对二甲苯和间二甲苯不能分离并不影响检测结果。考虑到分离效果、节省时间以及峰形,选择柱温90℃,柱压103 425 Pa。在这个条件下,分析时间可以缩短到10 min左右,且得到峰形很好的色谱图。
2.2 线性方程、线性范围与相关系数
按1.2配制系列标准气体,苯:19.53,39.06,58.59,78.12 μg/m3;甲 苯:19.26,38.52,57.78,77.04 μg/m3; 乙苯:38.53,77.06,115.6,154.1 μg/m3;对/间二甲苯:76.68,153.4,230.0,306.7 μg/m3;邻 二 甲 苯:39.12,78.24,117.4,156.5 μg/m3; 苯乙烯:40.27,80.54,120.8,161.1 μg/m3。按实验方法进样分析,以苯系物的质量浓度为横坐标,峰面积的平方根为纵坐标绘制标准曲线,得线性回归方程及相关系数见表1。由表1可知,各组分的相关系数r均大于0.995,说明线性良好。由回归方程的斜率可看出,苯和甲苯的斜率较大,说明其灵敏度较高,其它苯系物灵敏度则较低。
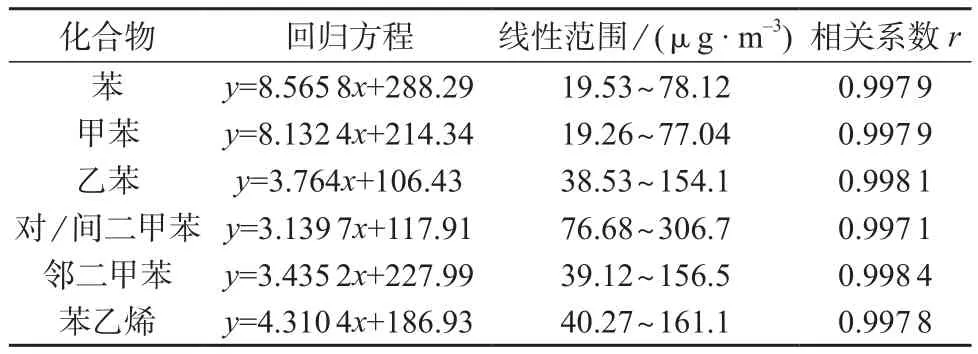
表1 线性方程与线性范围
2.3 方法检出限
对一定浓度(预计检出限的3~5倍)的样品进行重复测定7次,由此计算方法检出限及测定下限。
方法检出限:MDL=s·t(n–1,1–α=0.99),s为n次测量值的标准偏差,t(n–1,1–α=0.99)为自由度n–1、置信水平0.99的t检验值。测定下限一般为方法检出限的4倍[19]。查表得t(6,0.99)=3.143,1–α=0.99为置信水平,各个目标物的方法检出限和测定下限见表2。从表2中可看出,各组分的方法检出限在6.40~15.9 μg/m3之间,测定下限在25.6~63.6 μg/m3之间,满足室内空气中苯系物的检测要求。
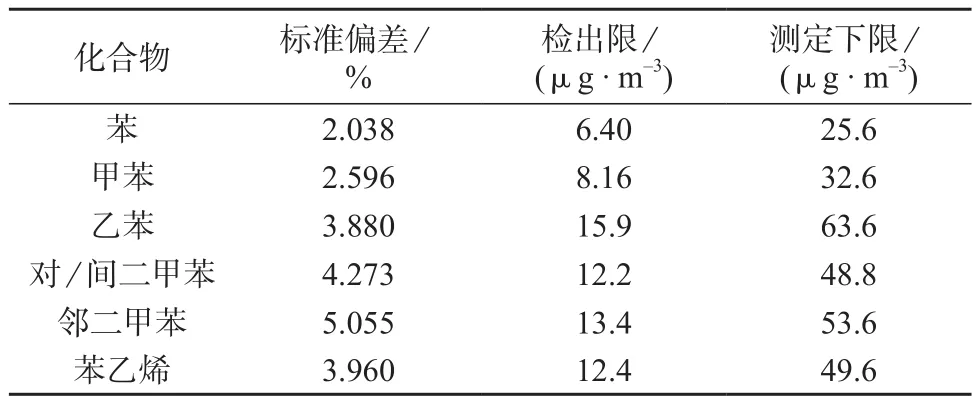
表2 方法检出限和测定下限
2.4 精密度试验
按实验方法测定表3中3种浓度的样品各6次,结果见表3。由表3可见,各组分测定结果的相对标准偏差为6.1%~13.7%(n=6),表明方法具有较高的精密度,可以满足室内空气中苯系物的检测要求。
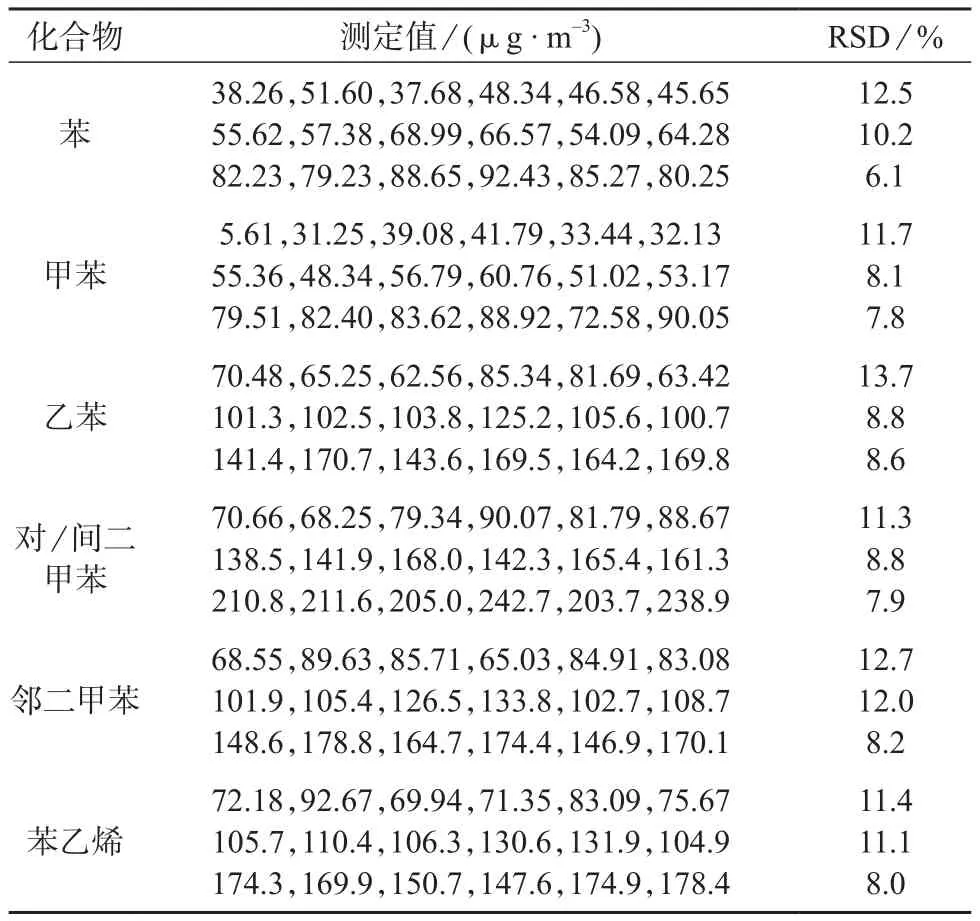
表3 精密度试验结果
2.5 回收试验
按实验方法测定表4中3个空白加标样品,结果见表4。由表4可见,各组分测定结果的平均空白加标回收率为92%~114%,表明方法准确度较高,满足分析要求。
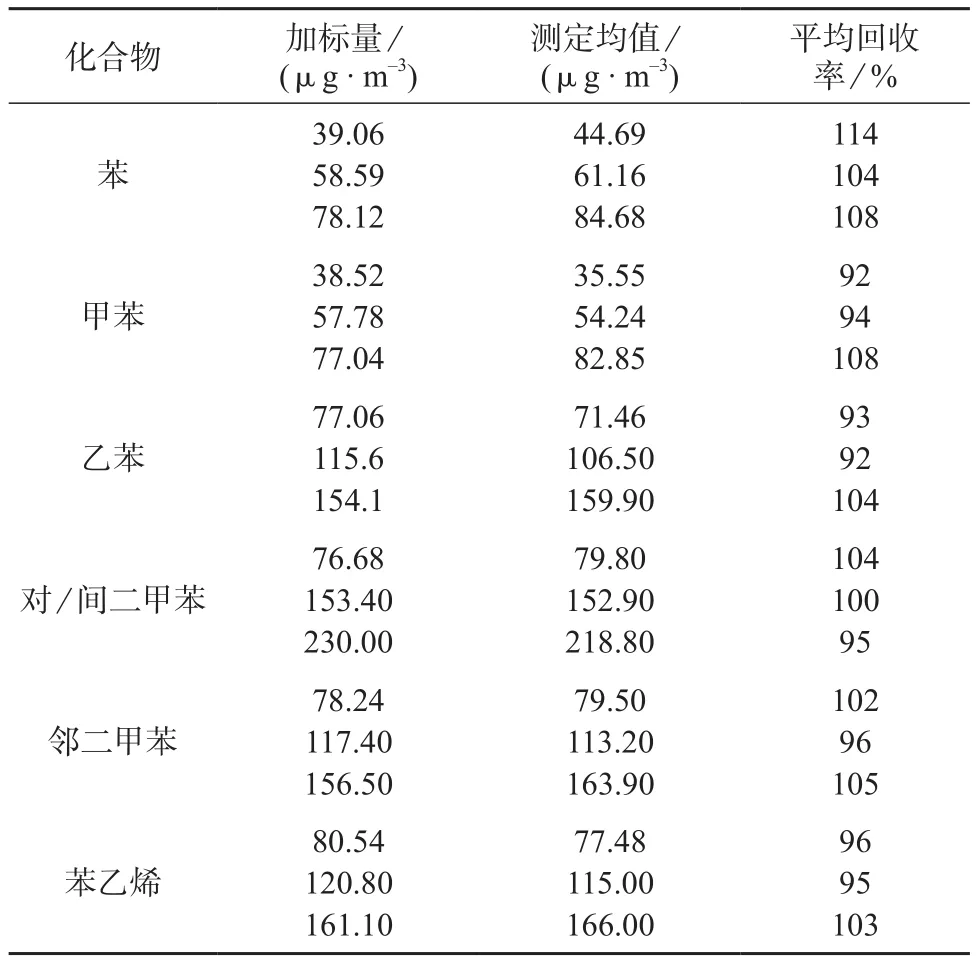
表4 回收试验结果(n=6)
3 结语
采用双柱串联–便携式气相色谱仪建立了室内空气中苯系物的测定方法,在最优色谱条件下各组分得到了很好的分离,运行时间较短,可以解决单柱分离效果差的难题,且线性范围、方法检出限、准确度和精密度均比较理想,与典型的气相色谱法相比,具有快速、准确、方便等优点。
[1] 莫达松,叶开富,罗平,等.装修对室内空气质量的影响及室内空气污染的防治[J].化学分析计量,2012,21(5): 30–33.
[2] Standeker S,Novak Z,Knez Z. Removal of BTEX vapours from waste gas streams using silica aerogels of different hydrophobicity[J]. Journal of hazardous materials,2009,165(1–3): 1 114–1 118.
[3] Billionnet C,Sherrill D,Maesano A. Estimating the health effects of exposure to multi-pollutant mixture[J]. Ann Epi-demi01,2012,22: 126–141.
[4] Zhang X D,Huang G H. Assessment of BTEX-induced health risk under multiple uncertainties at a petroleum-contaminated site: An integrated fuzzy stochastic approach[J]. Water Resources Research,2011,47(12): 4 154–4 158.
[5] Zhang Y J,Mu Y J,Liu J F,et a1. Levels,sources and health risks of carbonyls an BTEX in the ambient air of Beijing,China[J].Environmental Sciences,2012,24(1): 124–130.
[6] Dural E,Mergen G,Isiner B,et al. Determination of BTEX metabolites in urine and plasma of occupationally exposed workers non-exposed individuals[J]. Toxicology Letters,2011,205(1): S122–S122.
[7] Mazzeo D E C,Femandes T C C,Matin-Morales M A. Cellular damages in the Allium cepa test system,caused by BTEX mixture prior and after biodegradation process[J]. Chemosphere,201l,85(1): 13–18.
[8] Henderson L,Brusick D,Ratpan F,et a1. A review of the genotoxicity of ethyl-benzene[J]. Mutation Research Reviews in Mutation Research, 2007,(635): 81–89.
[9] Atkinson T J. A review of the role of benzene metabolites and mechanisms in malign transformation: Summative evidence for a lack of research in nonmyelogenous cancer types[J]. International Journal of Hygiene and Environmental Health,2009,212: 1–10.
[10] Aksoy M. Malignancies due to occupational exposure to benzene[J].American Journal of Industrial Medicine,1985(7): 395–402.[11] Brief R S,Lynch J,Bernath T,et a1. Benzene in the workplace[J]. American Industrial Hygiene Association Journal,1980,(41): 616–623.
[12] 肖小华,蔡积进,胡玉玲,等.固相微萃取–气相色谱/质谱联用分析室内空气中的苯系物[J].分析试验室,2010,29(5): 40–43.
[13] 傅小红,陈华,夏之宁.室内空气中苯系污染物检测研究进展[J].上海师范大学学报:自然科学版,2011,40(6): 619–623.
[14] HJ 584–2010 环境空气苯系物的测定活性炭吸附/二硫化碳解吸–气相色谱法[S].
[15] HJ 583–2010 环境空气苯系物的测定固体吸附热脱附–气相色谱法[S].
[16] 刘晔,陈尘,王古月.便携式气相色谱–质谱仪在应急监测中的应用[J].环境监控与预警,2010,2(3): 14–17.
[17] GB/T 18204.2–2014 公共场所卫生检验方法第2部分:化学污染物[S].
[18] GB/T 18883–2002 室内空气质量标准[S].
[19] 韦进宝,钱沙华.环境分析化学[M].北京:化学工业出版社,2002: 4–5.
Determination of BTEX in Room Air by Tandem Double Column–portable Gas Chromatography
Pan Yangchang , Mo Dasong, Huang Lulu, Liang Yong, Xie Anjie, Qin Rengang
(Guangxi Zhuang Autonomous Region Center for Analysis and Test Research, Nanning 530022, China)
Determination of benzene series(BTEX) in indoor air by tandem double column–portable gas chromatography was developed. The indoor air samples were collected 100 s by Tenax adsorbent for instrument in 0.5 L/min flow, and the instrument was quickly heated to 400℃for thermal desorption injection, and the seven kinds of BTEX were detected by micro argon ionization detector(MAID). The chromatographic conditions were as follows: MXT–200 and MXT–WAX metal capillary chromatographic column in series was used, the column temperature was 90℃, column pressure was 103 425 Pa. Under this condition, the separation effect was best, and the operation time was short. The mass concentration of each compounds and the square root of peak area had good linear relationship in the range of 19.26–306.7 g/m3, and the correlation coefficients were more than 0.995. The detection limit was 6.40–15.9 μg/m3, the recovery rate of the blank addition of each component was 92%–114%, and the relative standard deviation of determination results was 6.1%–13.7%(n=6). The method is rapid, accurate and convenient.
BTEX; indoor air; portable gas chromatography; double column series; micro argon ionization detector
O657.7
A
1008–6145(2016)06–0034–05
10.3969/j.issn.1008–6145.2016.06.008
*广西壮族自治区直属公益性科研院所基本科研业务费专项(2014ACZ06)
联系人:潘扬昌;E-mail: 307138983@qq.com
2016–08–12
