进展期胃癌术中精准腹腔热灌注治疗的效果评价
2016-11-29贺阳宋展
贺阳 宋展
进展期胃癌术中精准腹腔热灌注治疗的效果评价
贺阳1宋展2
目的 探讨进展期胃癌术中精准腹腔热灌注治疗的临床效果。方法 对我院2012年3月~2013年3月接受D2根治性胃癌切除术的进展期胃癌患者80例的临床资料进行回顾性分析。术中行精准腹腔热灌注治疗者40例(研究组),术中仅行常规腹腔冲洗者40例(对照组),两组均于术后3~4周按mFOLFOX6方案行全身静脉化疗,对比两组术前、术后1个月肿瘤标志物CEA与CA19-9变化,术后3年腹腔局部复发率及生存率。结果 术后1个月CEA与CA19-9均有下降,但研究组下降更显著(P<0.05);研究组3年腹腔局部复发率低于对照组,3年生存率高于对照组,差异均有统计学意义(P<0.05)。结论 进展期胃癌术中精准腹腔热灌注治疗能显著降低患者外周血CEA、CA19-9的水平,降低3年腹腔局部复发率,提高3年生存率。
胃肿瘤;化疗疗法;肿瘤;局部灌注
目前,进展期胃癌治疗效果较差,为了提高患者的生存时间和生存质量,各临床研究中心对胃癌的综合治疗方案进行了不断的探索。近年来,腹腔热灌注治疗在治疗进展期胃癌中越来越受临床医师的关注和青睐。本研究对进展期胃癌行术中精准腹腔热灌注化疗,探讨其临床治疗的效果。
1 资料与方法
1.1一般资料
选择我院普通外科2012年3月~2013年3月收治的经病理证实的接受标准的D2根治性胃癌切除术的进展期胃癌患者80例作为研究对象,按入组顺序根据随机数字表法随机分配到术中行腹腔热灌注化疗者40例(研究组),术中仅行常规腹腔冲洗者40例(对照组),两组患者于术后3~4周后按mFOLFOX6方案行全身静脉化疗。入组患者均于术前行超声胃镜、CT或MRI等影像学检查提示:肿瘤浸润深度为T3~4,未发生其他脏器转移;腹腔热灌注化疗及全身静脉化疗前检测血常规、肝功能、肾功能均正常,Karnofsky评分≥70,年龄为18~70岁;无严重心、肺、脑疾病及出血倾向,既往均未接受过放疗或化疗。所有根治性手术均做到R0切除,淋巴结清扫范围均为D2水平,检出淋巴结总数目≥15枚。本研究经我院道德伦理委员会批准并经患者或家属知情同意。按照随机数字法将他们分为两组,各40例,对照组:男性患者23例、女性患者17例;年龄34~70岁,平均(54.2±5.9)岁;高分化腺癌5例、中分化腺癌8例、低分化腺癌20例、黏液腺癌5例、印戒细胞癌2例;Ⅲa期24例、Ⅲb期16例。研究组:男性患者21例、女性患者19例;年龄35~69岁,平均(54.5±5.7)岁;高分化腺癌6例、中分化腺癌9例、低分化腺癌19例、黏液腺癌4例、印戒细胞癌2例;Ⅲa期26例、Ⅲb期14例。在上述一般资料上组间比较差异无统计学意义(P>0.05),可对比。
1.2方法
研究组行D2胃癌根治术后于腹腔左、右膈下及盆腔两侧各置1条灌注管,放置于盆腔的灌注管分别从同侧上腹壁戳口引出,作为进水口;左、右膈下灌注管分别从同侧下腹壁戳口引出,作为出水口,缝合固定后逐层关腹。将5-Fu 1 500 mg+0.9%氯化钠注射液3 000~5 000 ml加入腹腔热灌注化疗专用袋内。启动腹腔热灌注化疗设备(BR-TRG-Ⅰ型体腔热灌注治疗系统),设定温度43℃,灌注速度350 ml/min,治疗时间60 min。灌注过程中监测患者的生命体征。对照组仅行标准的D2根治性胃癌切除术。
术后3~4周给予研究组和对照组患者mFOLFOX6方案行全身静脉化疗,共计12个周期。mFOLFOX6方案为:奥沙利铂(Oxaliplatin,OXA)100 mg/m2,静脉滴注,持续2 h,第1 d;亚叶酸钙(Leucovori,LV)400 mg/m2,静脉滴注,持续2 h,第1 d;氟尿嘧啶 (5-Fluorouracil,5-FU)400 mg/m2,静脉推注,第1 d;5-FU 2 400 mg/m2,静脉滴注,持续46 h;每间隔2周重复1次该方案。
1.3观察指标
两组患者术前、术后1个月肿瘤标志物CEA与CA19-9水平变化;术后3年腹腔局部复发率及术后3年生存率。CEA与CA19-9采取电化学发光分析仪测定,其中CEA正常范围为0~5 μg/L[1],而CA19-9正常范围为0~39 U/ml[2]。
1.4统计学方法
采用SPSS 17.0软件进行统计学分析,计数资料用百分比(%)表示,采用χ2检验,计量资料用(均数±标准差)(±s)表示,采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1术前、术后1个月肿瘤标志物含量比较
两组患者术后1个月肿瘤标志物含量均降低(P<0.05),但研究组降幅更为显著(P<0.05),详见表1。
表1 两组患者术前、术后1个月CEA与CA19-9比较(±s)
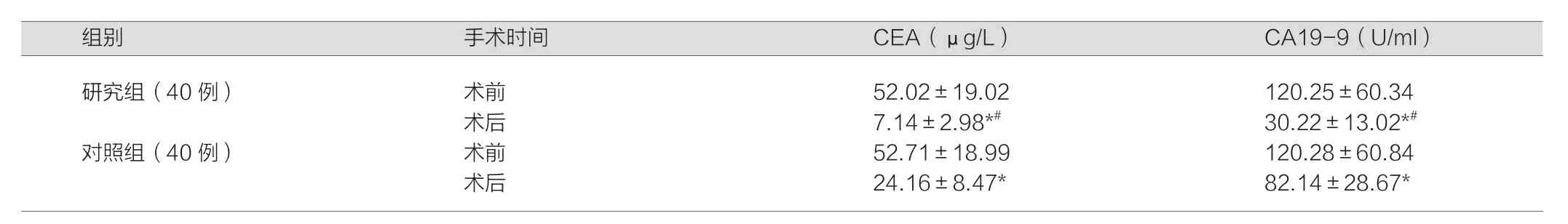
表1 两组患者术前、术后1个月CEA与CA19-9比较(±s)
注:与术前比较,*P<0.05;与对照组比较,#P<0.05
组别 手术时间 C E A (μ g / L ) C A 1 9 -9 (U / m l)研究组(4 0例) 术前 5 2 . 0 2 ± 1 9 . 0 2 1 2 0 . 2 5 ± 6 0 . 3 4术后 7 . 1 4 ± 2 . 9 8 *# 3 0 . 2 2 ± 1 3 . 0 2 *#对照组(4 0例) 术前 5 2 . 7 1 ± 1 8 . 9 9 1 2 0 . 2 8 ± 6 0 . 8 4术后 2 4 . 1 6 ± 8 . 4 7 * 8 2 . 1 4 ± 2 8 . 6 7 *
2.2术后3年腹腔局部复发率及生存率情况
研究组3年腹腔局部复发率为17.50%(7/40),对照组为47.50%(19/40),研究组的3年腹腔局部复发率低于对照组,差异具有统计学意义(P<0.05)。研究组术后3年生存率为80.00%(32/40),对照组为52.50%(21/40),研究组高于对照组(P <0.05),差异有统计学意义。
3 讨论
手术是胃癌最主要治疗手段,但根治性胃癌切除术后腹腔冲洗液中游离癌细胞阳性率高达24%~40%[3],术后腹腔局部复发和远处转移率较高[4]。腹腔热灌注腹腔化疗可清除游离癌细胞、亚临床病灶和微小癌结节。本研究结果显示:研究组的治疗效果优于对照组。
精准腹腔热灌注化疗有独特的优势[5]:第一,化疗药物经门静脉系统入肝,可提高肝脏局部药物浓度,使得门静脉与肝实质微小转移灶被清除;第二,使腹腔局部药物浓度高于静脉给药的20~1 000倍,其中5-Fu约为100倍[6],可使化疗药物与腹腔游离癌细胞充分接触,更好地清除腹腔内残留的癌细胞和微小转移灶;第三,热效应使毛细血管扩张增强,血流灌注增加,促进癌细胞膜稳定性降低,细胞的通透性增加,加速癌细胞凋亡[7]。血清CEA、CA19-9不仅有利于进展期胃癌的诊断及分期,而且联合动态监测胃癌患者术后的变化有利于早期发现胃癌的微小转移灶,在胃癌患者术后复发转移的“亚临床状态”进行干预,改善患者生活质量,延长患者生存期。从研究中可以看出,在术前不论是CEA还是CA19-9水平均高于正常范围,同类研究中证实这两种标志物会随着病情加重持续升高,且二者表达水平高低还和肿瘤大小、淋巴结、其他转移等有关[8]。经术中行精准腹腔热灌注化疗后,这两种标志物均有显著下降,但研究组下降更为明显,即术中加入腹腔热灌注治疗可更好地改善预后,同时研究组的术后3年腹腔局部复发率低于对照组,且3年生存率高于对照组。
[1]贺艳,陈佩仪,邹瞭南,等. 围手术期腹腔热灌注治疗进展期胃癌的疗效[J]. 广东医学,2012,33(18):2794-2796.
[2]宋展,钱国武,吕柯,等. 局部进展期胃癌术中腹腔热灌注化疗的疗效评价[J]. 中华普通外科杂志,2015,30(6):425-427.
[3]Yonemura Y,Kawamura T,Bandou E,et al. The natural history of free cancer cells in the peritoneal cavity[J]. Recent Results Cancer Res.,2007,169:11-23.
[4]崔海滨,白希永,葛怀娥,等. XRCC1 Arg399Gln基因多态性与进展期胃癌术后行腹腔热灌注化疗效果的相关性研究[J]. 现代中西医结合杂志,2015,24(12):1264-1266,1269.
[5]Van der Speeten K,Stuart OA,Sugarbaker PH. Pharmacology of perioperative intraperitoneal and intravenous chemotherapy in patients with peritoneal surface malignancy[J]. Surgical oncology clinics of North America, 2012,21(4):577-597.
[6]Rossi CR,Mocellin S,Pilati P,et al. Pharmacokinetics of intraperitoneal cisplatin and doxorubicin[J]. Surgical oncology clinics of North America,2003,12(3):781-794.
[7]李征,杨克虎,米登海,等. 进展期胃癌术后腹腔热灌注化疗有效性和安全性的系统评价[J]. 中国循证医学杂志,2011,11(12):1402-1408.
[8]董保国,谢桂生,王佳雷. 进展期胃癌术中腹腔热灌注化疗的效果分析[J]. 中国现代普通外科进展,2014,17(3):199-202.
Evaluation of Therapeutic Effect of Intraperitoneal Perfusion in Advanced Gastric Cancer
HE Yang1SONG Zhan21 Department of Graduate, Xinxiang Medical College, Xinxiang He’nan 453003, China, 2 Department of General Surgery, Nanyang Central Hospital, Nanyang He’nan 473000, China
Objective To study the advanced gastric cancer clinical effect of intraoperative precise celiac hot perfusion chemotherapy. Methods Clinical data of 80 patients with advanced gastric cancer who underwent D2 radical gastrectomy for gastric cancer were retrospectively analyzed in our hospital from March 2012 to March 2013. 40 cases of intraoperative accurate peritoneal perfusion treatment (study group), 40 patients who underwent routine peritoneal lavage (control group), two groups in the postoperative 3 to 4 weeks plan according to mFOLFOX6 for intravenous chemotherapy, compared two groups before and 1 months after surgery and tumor marker CEA the change of CA19-9, 3 years after surgery were local recurrence rate and survival rate. Results 1 months after the operation of CEA and CA19-9 were decreased, but the study group significantly decreased (P<0.05), study group 3 years local recurrence of abdominal cavity was lower than the control group, the 3 year survival rate was higher than the control group, the differences were statistically significant (P<0.05). Conclusion In advanced gastric cancer surgery, precise intraperitoneal perfusion can reduce the content of CEA and CA19-9 in peripheral blood, and decrease the local recurrence rate in 3 years, and increase the survival rate of 3 years.
Gastric cancer, Chemo therapy, Tumor, Local perfusion
R735
A
1674-9308(2016)30-0125-02
10.3969/j.issn.1674-9308.2016.30.081
1 新乡医学院研究生处,河南 新乡 453003;2 南阳市中心医院普通外科,河南 南阳 473000
宋展,E-mail:songzhanny@163.com
