用Flash DSC研究硝酸铵的相变特征与规律
2016-11-25任晓宁赵凤起高红旭轩春雷
任晓宁,赵凤起,高红旭,轩春雷,李 娜
(西安近代化学研究所燃烧与爆炸技术重点实验室,陕西 西安 710065)
用Flash DSC研究硝酸铵的相变特征与规律
任晓宁,赵凤起,高红旭,轩春雷,李 娜
(西安近代化学研究所燃烧与爆炸技术重点实验室,陕西 西安 710065)
采用闪速差示扫描量热法(Flash DSC)对硝酸铵(AN)的晶型转变与结晶特征进行研究,获得了相应转变过程的特征规律并根据Kissinger方程计算了相变动力学参数。结果表明,随着升温速率从100K/s增加到5000K/s,AN各相变的峰形在逐渐增宽,Ⅴ→Ⅳ型晶转起始温度显著向低温漂移,Ⅳ→Ⅲ型、Ⅲ→Ⅱ型、Ⅱ→Ⅰ型晶转起始温度略向高温漂移。从-10~-3500K/s的降温速率试验中,AN可逆的各级相变均存在显著“过冷”现象, AN的结晶峰温、Ⅰ→Ⅱ型、Ⅱ→Ⅲ型、Ⅲ→Ⅳ型晶转峰温均向低温方向偏移,AN在-10~-500K/s和-1000~-3500K/s两种降温速率范围下其结晶、Ⅰ→Ⅱ型晶转、Ⅱ→Ⅲ型晶转活化能值Ea分别为761.11、570.98、700.71kJ/mol和102.48、82.16、166.76kJ/mol,指前因子ln(A/s-1)分别为-213.27、-183.76、-267.25和-29.26、-26.71、-64.38。
硝酸铵;AN;闪速差示扫描量热法; Flash DSC;相变规律; 晶型转变; 结晶;热分析
引 言
含能材料中有许多多晶型化合物,如AN、AP、FOX-7、HMX、CL-20等,其应用研究一直备受关注[1-2]。硝酸铵(AN)作为火炸药用原材料,价格低廉、易制备,绿色无污染,具有化学安定性与热安定性良好、热感度与冲击感度低等特点,可用于低特征信号、低易损性和低污染固体推进剂中[3-5]。国外对AN的性能研究进行了大量报道[6-7],如AN吸湿性、安全性研究,AN热分解机理及固、液相产物分析等。研究表明[8-9],固体炸药的晶型不同,其热分解及安定性行为存在明显差异,与材料混合体系的热稳定性差异显著,在进行相容性判定时结果显著不同。化合物的晶型除受前处理方法的影响明显外,温度变化是另一显著影响因素,极快的降温速率使试样可产生新的结构性能。文献报道[10]AN在加热时具有5种晶型的多晶型转变行为,易导致火炸药产品应用过程中的体积、密度出现改变,最终导致能量改变,因此,研究AN的相变规律对优化工艺有重要意义。
目前,关于AN多晶型的研究多为慢升温速率(20℃/min以内)下的转变过程,对迅速升、降温条件下多晶型变化规律及结晶特征变化规律尚未见报道。闪速差示扫描量热方法(Flash DSC,简称FDSC)是一种具有极快的升、降温速率,高灵敏度,宽温度范围的测温量热新技术,微机电系统技术的芯片传感器是Flash DSC仪的“心脏”,该芯片传感器有16对热电偶,由涂有铝箔涂层的氮化硅和二氧化硅制成,从而实现其高灵敏与极速响应性。因此,本研究采用闪速差示扫描量热方法(Flash DSC)[11-13]考察了极快速升降温条件下AN的固-固、液-固等相变特征,获得了其变化的规律,旨在为材料晶型控制方法的研究及多晶型转变材料的应用提供参考。
1 试 验
1.1 样品与仪器
AN,白色颗粒,纯度≥99.99%,西安近代化学研究所; 硅油,德国Blue star 公司。
Flash DSC1闪速差示扫描量热仪,梅特勒公司;MultiSTAR芯片传感器,梅特勒公司;EZ5电子显微镜,莱卡公司,放大倍数可达2000; Huber TC100制冷系统,吹扫气及流速为50mL/min的高纯氮气。
1.2 样品制备
用镊子夹取小粒干燥的AN颗粒于玻载片表面,利用仪器自带切刀的平面进行碾研,尺寸约10~30μm。
打开电子显微镜,将事先进行过修正试验的一个芯片传感器置于闪速量热仪内,调节电子显微镜焦距;利用仪器自带防静电单毛笔沾取极少量硅油于芯片试样端中心点;擦拭单毛笔后,沾取玻载片上碾研过的试样,显微镜下将试样置于硅油中心点,并保证与芯片传感器有良好的接触,锁紧装置,盖好隔温隔热炉盖。
1.3 试验条件
FDSC升温试验的升温速率分别为100、500、1000、5000K/s(以不同的速率进行升温,降温采用-100K/s相同的速率进行)。
FDSC降温试验的降温速率分别为-10、-50、-100、-500、-1000、-1500、-2000、-3000、-3500K/s(以100K/s相同的速率进行升温,分别进行不同的速率降温循环试验)。
试验温度范围为-95~220℃。
2 结果与讨论
2.1 快反应速率下AN的晶型转变、熔融与结晶特征
AN有Ⅴ、Ⅳ、Ⅲ、Ⅱ、Ⅰ型5种晶型,在升温加热或降温冷却条件下有从Ⅴ→Ⅰ型或Ⅰ→Ⅴ型间的多晶型转变过程[7],为考察在闪速升降温速率条件下的相变特征,分别进行了以100、500、1000、5000K/s不同速率的升温试验,该过程均以-100K/s速率线性降温,并进行2次循环试验,得到温度─热流的FDSC曲线,见图1。其中,数字1和2分别表示第1次和第2次循环试验。
从图1可知,AN在未经热循环前的升温FDSC曲线上均呈现有5步吸热过程,从低温至高温段分属其从Ⅴ→Ⅳ型、Ⅳ→Ⅲ型、Ⅲ→Ⅱ型、Ⅱ→Ⅰ型5种晶型间的转晶吸热峰和一个熔融吸热峰,对比图1(a)、(b)、(c)、(d)中的曲线,发现随着升温速率的逐渐增快,各个过程的吸热峰峰形逐渐变宽,当速率增至5000K/s时,吸热峰形变得平坦。为考察快速升降温条件下这些相变特征的可逆性,记录了以-100K/s降温过程的FDSC曲线,发现4种试验条件下降温过程均有4步放热,从高温至低温方向分属其液-固转变的结晶峰、固-固转变的Ⅰ→Ⅱ型、Ⅱ→Ⅲ型和Ⅲ→Ⅳ型的可逆转晶峰,但4种试验条件下Ⅳ→Ⅴ型的可逆转变则微弱,导致检测不到。在随后的循环升降温试验中也未检测到Ⅴ→Ⅳ型(或Ⅳ→Ⅴ型)的吸(放)热峰,试验条件下AN各个相变均存在“过冷”现象。
对图1(a)~(d)中各个试验条件下的FDSC进行数据处理,获得各个过程相应的相变温度特征值分别见表1(升温试验)和表2(降温试验),各个过程的过冷度见表3。
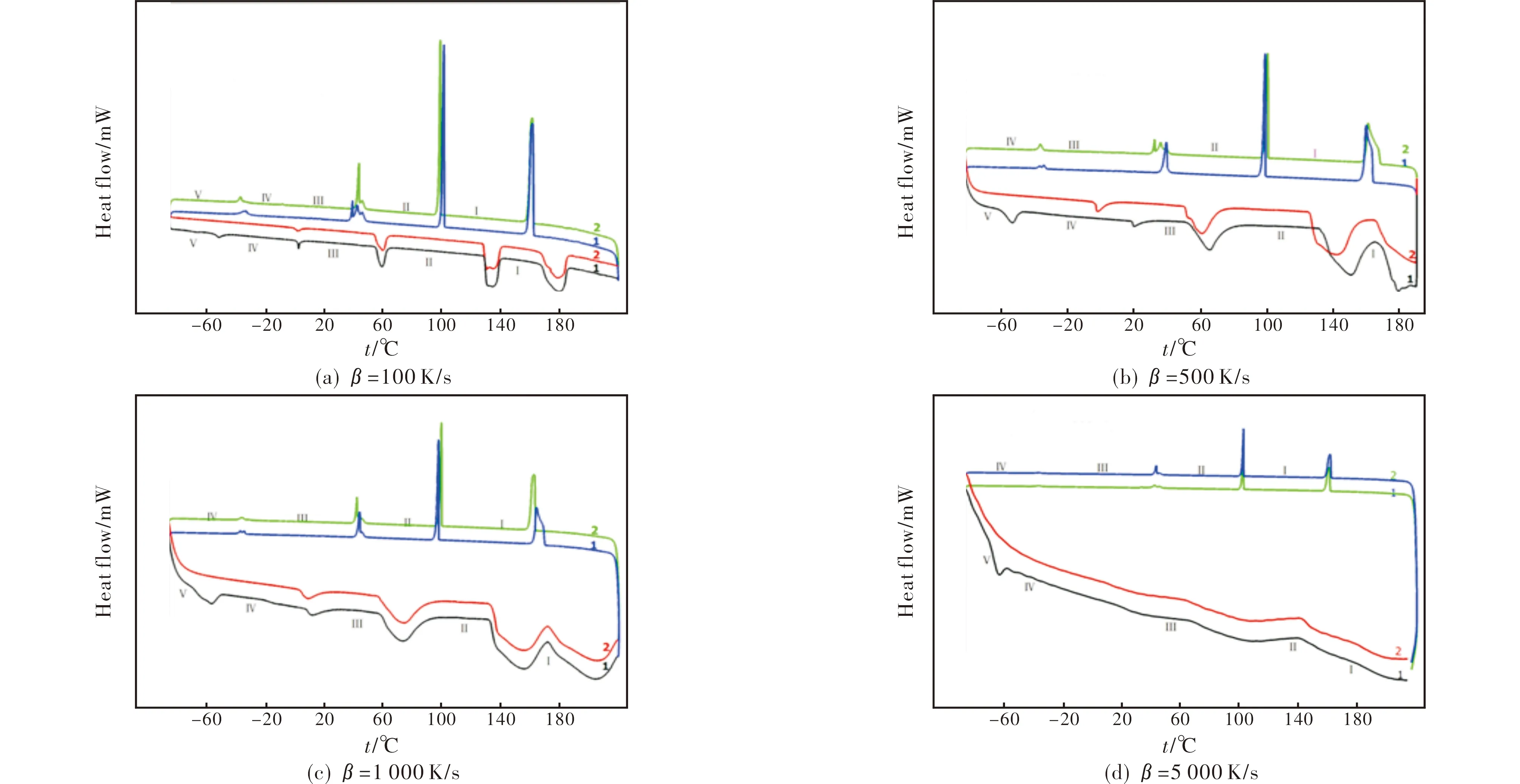
图1 不同升温速率下2次循环试验AN相变的FDSC曲线Fig.1 FDSC curves of AN phase transition under different heating rates two cycle tests
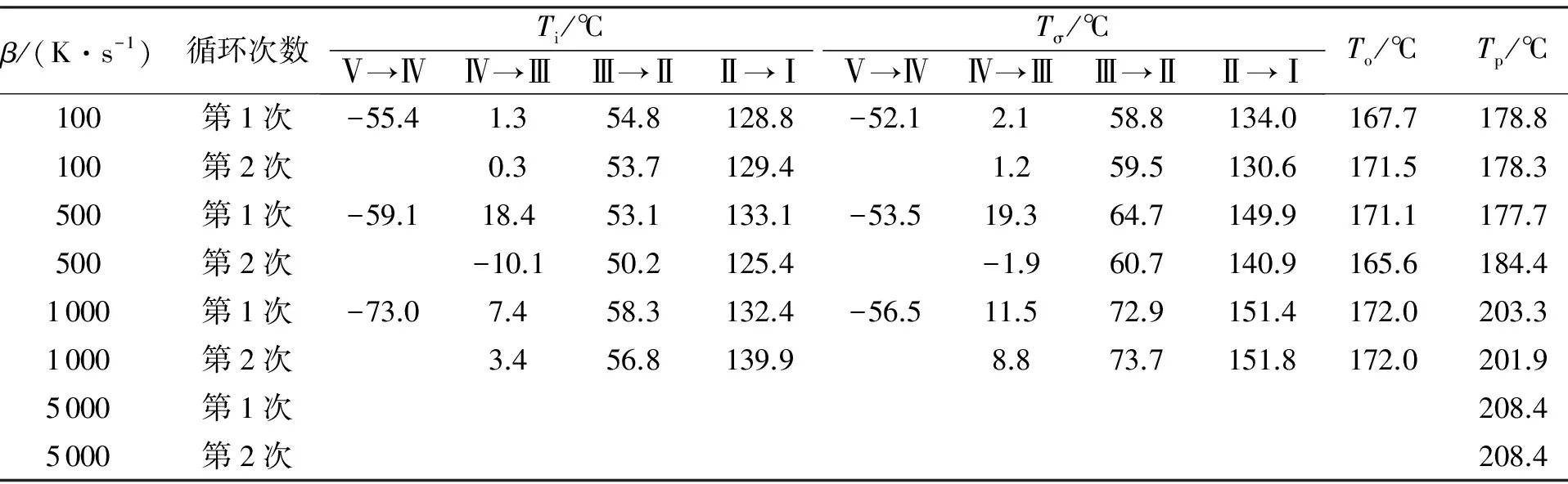
β/(K·s-1)循环次数Ti/℃Ⅴ→ⅣⅣ→ⅢⅢ→ⅡⅡ→ⅠTσ/℃Ⅴ→ⅣⅣ→ⅢⅢ→ⅡⅡ→ⅠTo/℃Tp/℃100第1次-55.41.354.8128.8-52.12.158.8134.0167.7178.8100第2次0.353.7129.41.259.5130.6171.5178.3500第1次-59.118.453.1133.1-53.519.364.7149.9171.1177.7500第2次-10.150.2125.4-1.960.7140.9165.6184.41000第1次-73.07.458.3132.4-56.511.572.9151.4172.0203.31000第2次3.456.8139.98.873.7151.8172.0201.95000第1次208.45000第2次208.4
注:Ti和Tσ分别为转晶起始温度和峰温;To和Tp分别为熔融起始温度和峰温。
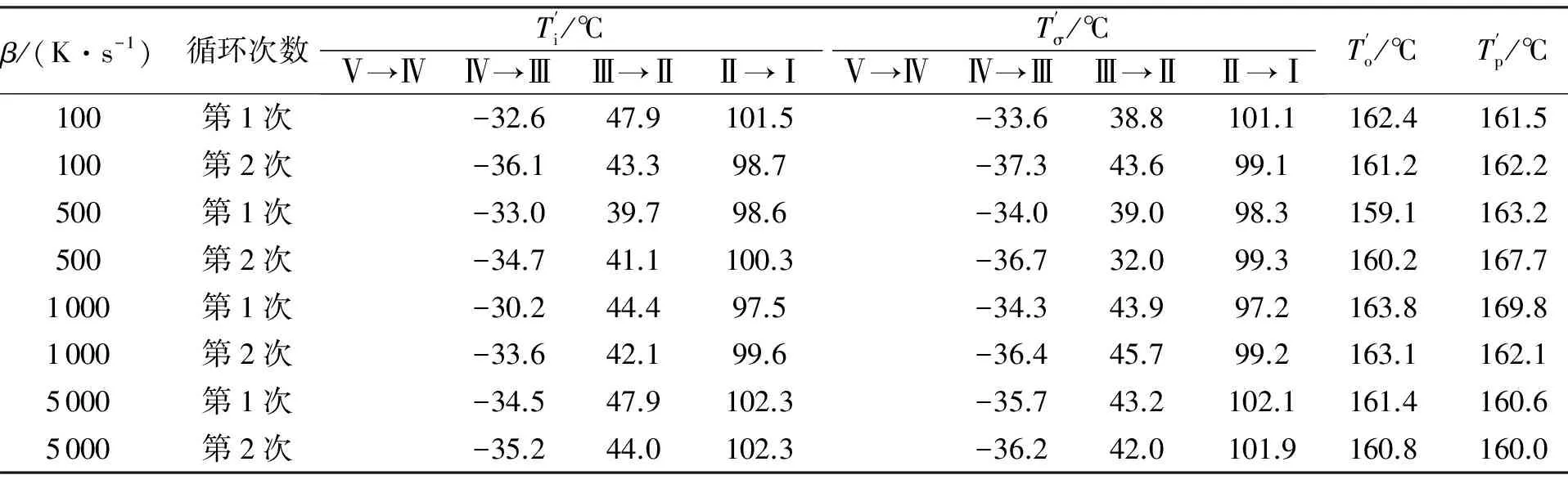
表2 热循环试验中AN降温可逆相变特征温度

由表1可以看出,除Ⅴ→Ⅳ型转晶的峰温随速率增加向低温方向漂移外,其余相变过程的峰温随速率增加均向高温方向移动,该变化规律为快反应速率下AN相变的一个显著特征。该变化趋势在二次升温过程中同样存在,数据重复性较好(除Ⅳ→Ⅲ型)。相变起始温度也有类似的变化特征,但受峰形变化的影响,该数据稳定性不及峰温好。
由表2可以看出,相同降温速率下、经历不同速率的升温对AN可逆相变的峰温、起始温度影响并不明显,两次循环结果一致。但循环降温对Ⅲ→Ⅳ型转变的特征温度有一定规律性,略微向低温漂移。对比表1与表2各级相变峰的峰温值,认为AN相变存在明显的过冷现象,以峰温值计算AN相变的过冷度见表3。
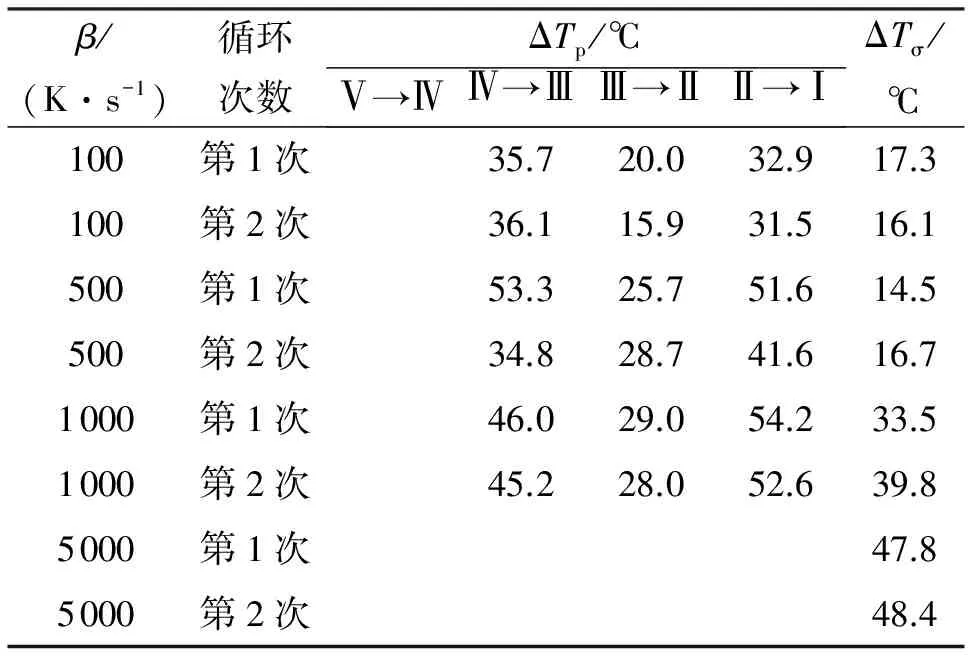
表3 AN相变的过冷度
注:ΔTσ为以峰温计的晶型转变过程过冷度;ΔTp为以峰温计的结晶过程过冷度。
从表3可知,不同升温速率下AN各级相变的过冷度值均较大,且随着升温速率加快,过冷度值呈现增加的趋势。
2.2 较大过冷度下AN的相变规律
AN相变存在显著的过冷现象,因此,采用Flash DSC进一步对这种较大过冷度下的相变规律进行研究。以100K/s升温,分别以-1、-10、-50、-100、-500、-1000、-1500、-2000、-3000、-3500K/s进行降温的循环试验,获得的温度─热流FDSC曲线见图2。
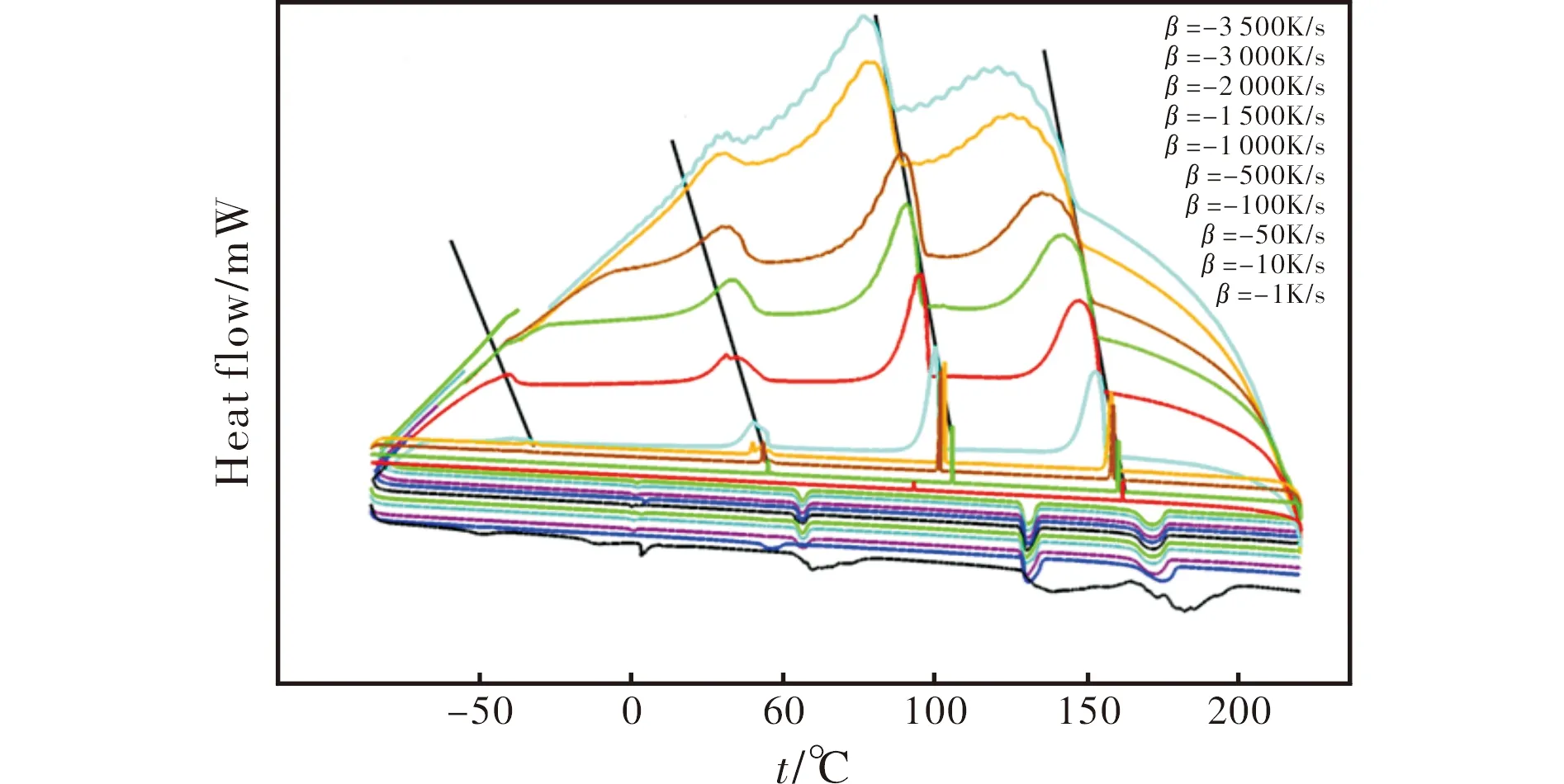
图2 不同降温速率下AN的FDSC曲线Fig.2 FDSC curves of AN under different cooling rate conditions
从图2可知,降温速率对结晶过程及Ⅰ→Ⅱ型晶型转变过程有显著影响,随降温速率加快,峰温向低温方向漂移,漂移幅度结晶峰大于Ⅰ→Ⅱ型晶型转变峰,致使在更快速降温时两峰紧紧相连,过冷结晶并未完全时Ⅰ→Ⅱ型晶型转变已开始,在该温度段内系统为一个Ⅰ型与Ⅱ型AN的固液相混合态。随降温速率加快,AN的Ⅱ→Ⅲ型和Ⅲ→Ⅳ型转变的峰温均向低温方向漂移,各相变之间的“温程”越来越近。在-3000和-3500K/s降温时未见Ⅲ→Ⅳ型晶型转变峰,由此推测,受降温速率影响,AN各个温区的相变存在一定的边界条件,依据Flash DSC的快速升降温方法,可以寻找到该边界条件。
分别对图2各个温区的相变峰进行积分,获得各个过程相变转化率随温度变化的规律曲线见图3,图3(a)、(b)、(c)分别对应的是过冷的结晶、Ⅰ→Ⅱ型和Ⅱ→Ⅲ型晶型转变。图4是各个过程的峰温与速率关系。
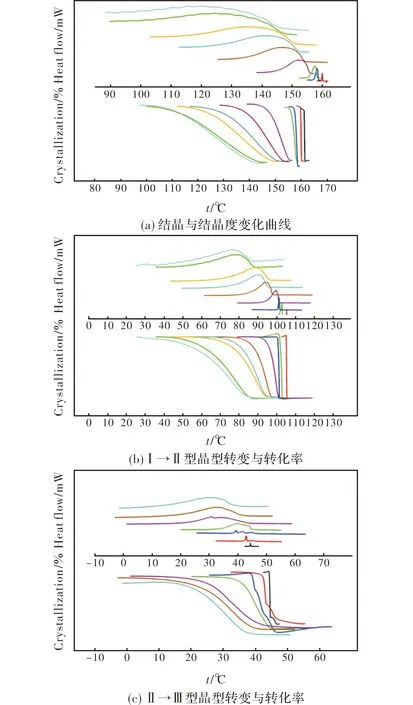
图3 不同降温速率时AN的相变转化率曲线Fig.3 Phase transition percentage curves of AN at different cooling rate
从图4显示的趋势,采用速率范围(-10~-500K/s和-1000~-3500K/s)分段法,依据经典的Kissinger模型动力学方程对AN相变动力学进行计算,参数见表4。
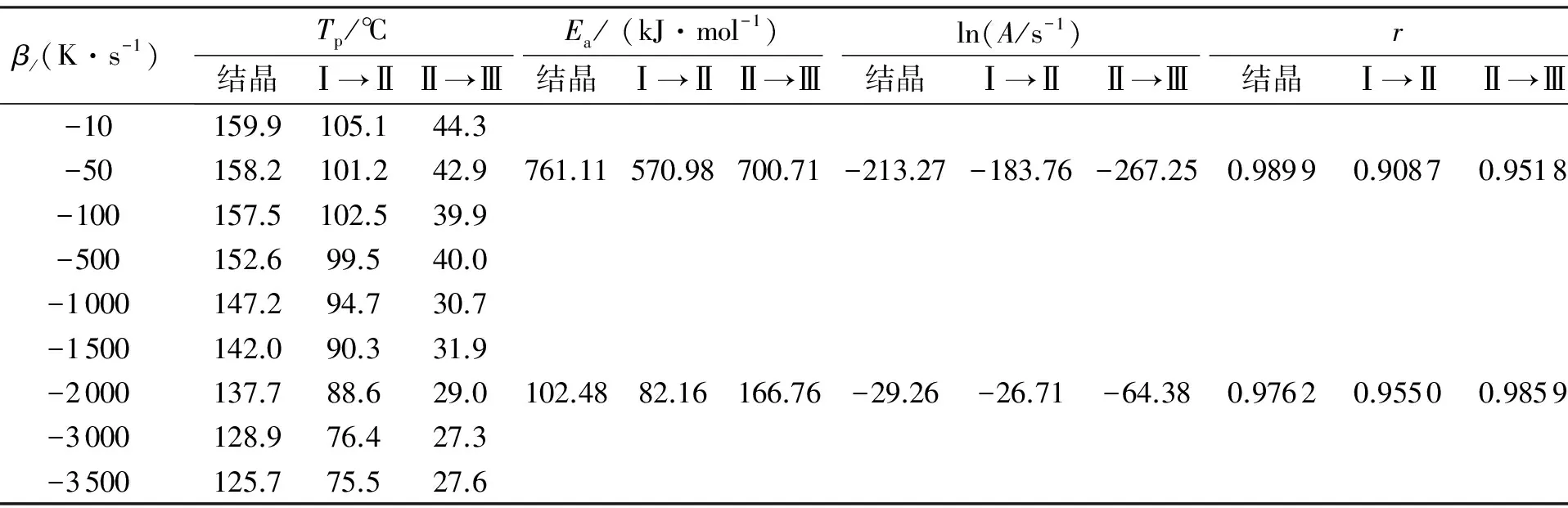
表4 过冷条件下AN的相变动力学参数
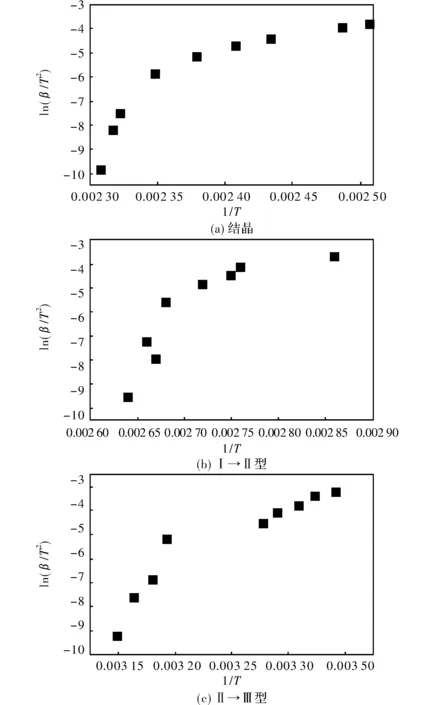
图4 过冷条件下AN的相变峰温与速率关系Fig.4 Relationship of phase transition peak temperature with rate of AN under the supercooled conditions
表4表明,过冷条件下AN相变动力学参数在不同的降温速率范围相差较大,各相变在-10~-500K/s速率范围内活化能值显著大于-1000~-3500K/s速率范围的活化能值,说明通过调节降温速率可以更“活化”AN可逆相变,动力学参数的计算也可佐证用Flash DSC的温度特征值寻找相变的边界条件,为相变的条件控制提供方法手段。
3 结 论
(1)升降温速率对AN炸药的物理相变特征影响显著,随着升温速率的加快,AN的Ⅴ→Ⅳ型、Ⅳ→Ⅲ型晶形转变的吸热峰逐渐减弱或消失,对应的可逆转变放热峰有一致的特征。热循环会影响相变特征温度,但与速率的影响相比,强度较小。
(2)在快速降温条件下,AN的各个物理相变过程均有较显著的过冷现象,随降温速率加快过冷度值增大;受速率条件的调控,AN各个温区相变的变化特征不同,过冷使得AN不同温区的系统相态发生改变。
(3)采用模型动力学方程对较大过冷度下AN炸药相变动力学进行计算应以不同速率范围分区进行,采用Kissinger法获得AN不同速率范围内的活化能值和指前因子明显不同。
(4)依据快速升降温速率的变化和不同速率范围分区动力学计算的方法,可以获得AN各个相变发生的边界条件,对AN各个相变过程进行控制。
[1] Enoksson E. Mechanical instability of ammonium nitrate duo to phase transition [C]∥Chemical Problems Connected with the Stability of Explosives, Sixth Symposium. Sweden:[s.n.],1982: 487-512.
[2] Engel W. Thermoanalytical investigation of stored ammonium nitrate doped with diammine copper-(Ⅱ) [J]. Propellants, Explosives, Pyrotechnics, 1985,10(3):84-86.[3] 熊言涛,刘祖亮.用改性直链烷烃改善硝酸铵的吸湿性[J].火炸药学报,2013,36(4):50-52.
XIONG Yan-tao, LIU Zu-liang. Improvement of the hygroscopicity of AN by modified paraffin[J]. Chinese Journal of Explosives & Propellants(Huozhayao Xuebao), 2013, 36(4): 50-52.
[4] 任晓雪.国外工业炸药的研究与发展[J].火炸药学报,2011,34(5):50-52.
REN Xiao-xue. Study and development of foreign commercial explosives[J]. Chinese Journal of Explosives & Propellants(Huozhayao Xuebao), 2011, 34(5): 50-53.
[5] 张杰,杨荣杰,刘云飞,等.聚乙烯醇缩丁醛包覆硝酸铵的性能研究[J].火炸药学报,2001,24(1):41-43.
ZHANG Jie, YANG Rong-jie, LIU Yu-fei, et al. Study on properties of the coated AN with poly-vinyl Butyral[J]. Chinese Journal of Explosives & Propellants(Huozhayao Xuebao), 2001, 24(1): 41-43.
[6] Brown R N, McLaren A C. On the mechanism of the thermal transformations in solid ammonium nitrate [J]. Proc R So. London, Ser A,1962, 266: 329-343.
[7] Cady H H. The ammonium nitrate-potassium nitrate system [J]. Propellants, Explosives, Pyrotechnics, 1981(6): 45-54.
[8] Hall P G. Thermal decomposition and phase transition in solid nitramines[J]. Journal of the Chemical Society, Faraday Transactions, 1971, 67(Pt2): 556-562.
[9] Liu Z R, Zhang M N. The influence of crystal perfection on the thermal decomposition of explosives[J]. Acta Ordnance Sinica, 1979(1): 50-55.
[10] Liu Z R. Thermal Analyses for Energetic Materials[M]. Beijing: National Defence Industry Press, 2008: 384-386.
[11] Zhuravlev E, Schick C. Fast scanning power compensated differential scanning nano-calorimeter. 1. The device[J]. Thermochimica Acta, 2010(505): 1-13.
[12] Pijpers M F J, Mathot V B F, Goderis B, et al.High speed calorimetry for the analysia of kinetics of vitrification, crystallization and melting of macromolecule[J]. Macromllecules, 2002(35): 3601-3613.
[13] Efremov M Y, Olson E A, Zhang M, et al. Ultrasensitive, fast, thin-film differential scanning calorimeter[J]. Review of Scientific Instruments, 2004,75(1): 179-191.
Investigation on Phase Transformation Characteristics and Regulars of Ammonium Nitrate(AN) Using Flash DSC
REN Xiao-ning, ZHAO Feng-qi, GAO Hong-xu, XUAN Chun-lei, LI Na
(Science and Technology on Combustion and Explosion Laboratory, Xi′an Modern Chemistry Research Institute, Xi′an 710065,China)
The crystal transformation and crystallization characteristics of ammonium nitrate(AN)were studied using Flash DSC method. The characteristic regulars corresponding to the transformation process were obtained, and the phase transformation kinetic parameters were calculated based on Kissinger′s equation. The results show that with the increase of heating rate from 100K/s to 5000K/s, the shape of each phase transformation peak of AN gradually widens. The starting temperature of the crystal transformation of Ⅴ→Ⅳ is significantly shifted to low temperature, and the starting temperature of the crystal transformation of Ⅳ→Ⅲ、Ⅲ→Ⅱ、Ⅱ→Ⅰis slightly shifted to high temperature. In cooling rate test from -10K/s to -3500K/s, there were obviously super-cooled phenomenon in the reversible phase transitions of AN, the peak temperature of the crystallization of AN, Ⅰ→Ⅱ,Ⅱ→Ⅲ,Ⅲ→Ⅳ are shifted to low temperature. The activation energiesEaof the crystallization and crystal transformation of Ⅰ→Ⅱ、Ⅱ→Ⅲ under two kinds of cooling rate range -10~-500K/s and -1000~-3500K/s are 761.11, 570.98, 700.71kJ/mol and 102.48, 82.16, 166.76kJ/mol, respectively. The pre-exponential factors ln (A/s-1) are -213.27、-183.76、-267.25 and-29.26、-26.71、-64.38,respectively.
ammonium nitrate; AN; Flash DSC; phase transition rule; crystal transformation; crystallization;thermal analysis
10.14077/j.issn.1007-7812.2016.05.010
2016-08-19;
2016-09-21
国家自然科学基金(No.21173163;No.21473131)
任晓宁(1981-),女,副研究员,从事含能材料热化学热分析研究。E-mail:xueyexy@163.com
TJ55;O642
A
1007-7812(2016)05-0064-05
