含密胺基团新型酰胺类凝胶因子的合成、性能及Hansen溶度参数对凝胶行为的预估
2016-11-23杨新国沈启立
王 潇,杨新国,沈启立
(湖南大学材料科学与工程学院,湖南省喷射沉积技术及应用重点实验室,长沙410082)
含密胺基团新型酰胺类凝胶因子的合成、性能及Hansen溶度参数对凝胶行为的预估
王 潇,杨新国,沈启立
(湖南大学材料科学与工程学院,湖南省喷射沉积技术及应用重点实验室,长沙410082)
设计合成了一种含有密胺基团的新型酰胺类凝胶因子AMOG,其在多种常用有机溶剂中均能形成凝胶,且在甲苯和二甲苯中形成凝胶的临界凝胶浓度(CGC)约为1 mmol/L.采用“试管倒转法”确定了凝胶的溶剂⁃凝胶转变温度(Tgel),利用SEM表征了凝胶的微观结构,发现AMOG具有明显的溶剂效应.运用溶剂的Hansen溶度参数探索溶剂对凝胶行为的作用机制,发现溶剂的氢键作用参数(δh)对凝胶的微观结构和凝胶性质有显著影响:AMOG在1.0 MPa1/2<δh<4.1 MPa1/2的溶剂中形成透明凝胶,在4.1 MPa1/2<δh<8.0 MPa1/2的溶剂中为不透明凝胶,在δh>8.0 MPa1/2的溶剂中为沉淀或溶液状态.进一步将溶剂的Hansen溶度参数以三维坐标(δd,δp和δh)表示,发现能使AMOG形成凝胶的溶剂主要集中在Hansen空间的特定区域内.实验结果表明,凝胶体系的溶液⁃凝胶转变温度主要受色散参数δd与极性参数δp的影响,氢键参数δh对其有微调的作用.
有机凝胶;酰胺;密胺;Hansen溶度参数;溶剂效应
近年来,小分子有机凝胶因子(LMOGs)因其在生物材料[1,2]、药物输送[3]、气体吸附[4]、自愈合材料[5]、模板合成[6]及传感器[7]等领域的应用潜力而受到广泛关注.这类凝胶的形成是一个自组装过程[8,9],其主要驱动力是凝胶因子分子之间以及凝胶因子与溶剂之间的非共价键作用,如氢键作用、π⁃π相互作用、偶极⁃偶极作用以及范德华力等[10~15].迄今,已有大量LMOG被发现,但其中许多LMOG的发现都是偶然的[16,17],因此,有关新凝胶因子的设计、合成及其凝胶机制的研究仍然是研究的热点问题.
探索溶剂对凝胶行为的作用机制可以更好地理解和预测凝胶因子的凝胶行为.研究者试图通过引入各种溶度参数来直观地表现溶剂与凝胶因子之间的作用机制,这些溶度参数包括溶剂的介电常数(ε)[18]、Hildebrand溶度参数(δ)[19]、Flory⁃Huggins参数(χ)[20]、Kamlet⁃Taft参数(π∗,α,β)[21]以及Hansen溶度参数(δd,δp,δh)[22]等.其中,Hansen溶度参数以原子的色散力(δd)、分子的偶极作用(δp)和分子间的氢键作用(δh)作为3个分量[23],更精确地表现了各种不同作用对溶度参数的贡献.目前Hansen溶度参数已成为理解与预测凝胶因子凝胶行为的有效方法[24~27].如Shen等[28]将2种溶剂按一定比例混合,构造出一系列具有不同Hansen溶度参数的混合溶剂,采用这些溶剂研究了1,3∶2,4⁃二(3,4⁃二甲基苯亚甲基)山梨糖醇(DMDBS)的凝胶行为,并认为该方法可以预测山梨糖醇同系物在混合溶剂中的凝胶行为.Curcio等[29]对一种含有氨基酸基团的LMOG的研究表明,溶剂Hansen溶度参数中的分子间氢键作用(δh)是凝胶形成的关键因素,当溶剂的δh值在0.4~2.9 MPa1/2范围内时才能形成凝胶.
本文设计合成了一种含有密胺基团的酰胺类凝胶因子AMOG,考察了AMOG在不同溶剂中形成凝胶的能力及其凝胶的微观结构,并引入Hansen溶度参数探索了溶剂对凝胶行为的影响.
1 实验部分
1.1 试剂与仪器
1⁃羟基苯并三唑(HOBt,纯度99%),1⁃(3⁃二甲氨基丙基)⁃3⁃乙基碳二亚胺盐酸盐(EDC,纯度98.5%)及二异丙基乙胺(DIPEA,纯度99%)等均购自阿拉丁试剂有限公司;三聚氯氰(纯度99%)购自Alfa Aesar公司;其它试剂无特别说明均为分析纯试剂,所有试剂均直接使用;2,4⁃二(十二氨基)⁃6⁃氯⁃1,3,5⁃三嗪(M2)由本实验室合成[30].INOVA⁃400型核磁共振波谱仪(四甲基硅烷为内标,美国Varian公司);Nicolet⁃460型红外光谱仪(KBr压片,美国Nicolet公司);HITACHI⁃S4800型场发射扫描电子显微镜(日本日立公司);SWG⁃X4型显微熔点测定仪(上海精密仪器有限公司).
1.2 实验过程
AMOG的合成过程见Scheme 1.
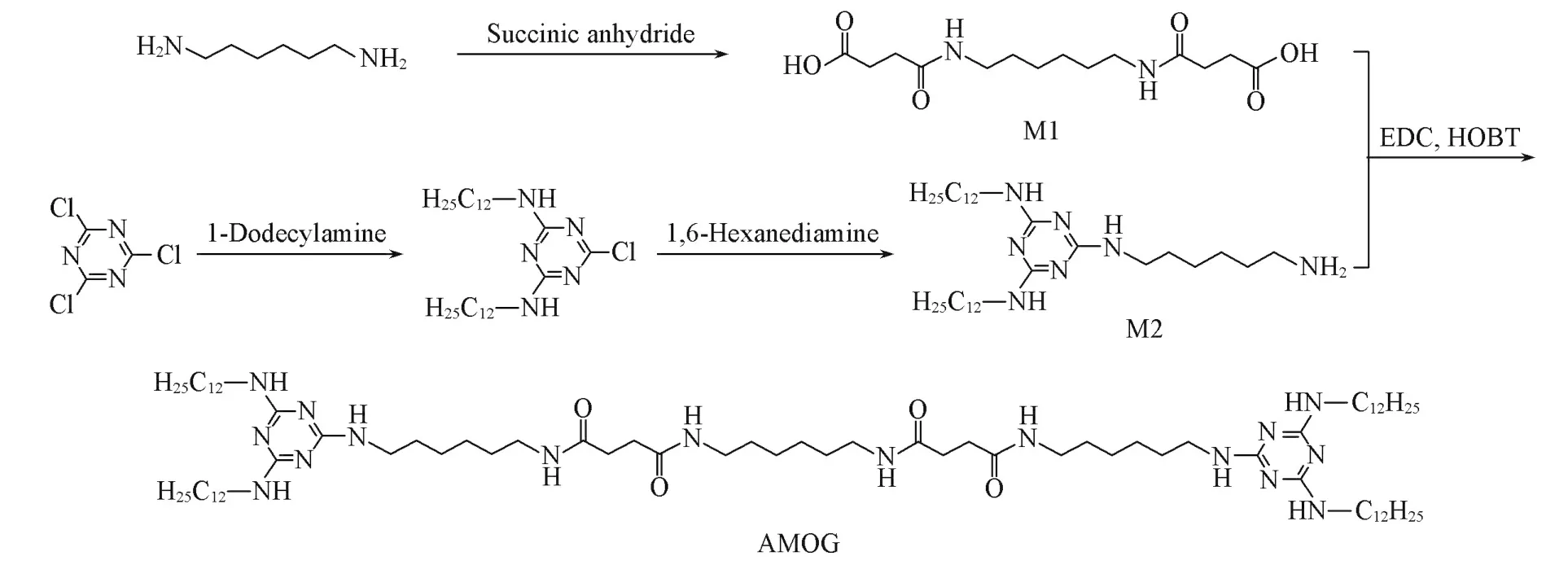
Scheme 1 Synthesis of gelator AMOG
1.2.1 M1的合成 取4.00 g(0.04mol)丁二酸酐溶解于30mL冰醋酸中,滴加2.78mL(0.02mol)己二胺,于30℃搅拌反应2 h.冷却,过滤,用丙酮洗涤2次,得到白色产物M1,产率82.30%,m.p. 188~189℃.1H NMR(DMSO⁃d6),δ:12.04(s,2H),7.78~7.81(t,J=4 Hz,2H),2.98~3.03(m,4H),2.39~2.44(m,4H),2.27~2.30(m,4H),1.33~1.39(m,4H),1.22~1.28(m,4H).IR(KBr),ν~/cm-1:3309.73(νN—H),3057.86(νOH),2938.45(νCH3),2858.77(ν—CH2—),1694.38(),1537.22(δN—H).
1.2.2 AMOG的合成 将0.079 g(0.25 mmol)M1,0.337 g(0.6 mmol)M2和0.007 g(0.05 mmol)HOBt溶于20 mL无水THF中,超声振荡5 min使各组分混合均匀.加入0.106 g(0.55 mmol)EDC,于70℃回流反应48 h.待反应液冷却后立即抽滤,将滤液倒入大量水中,静置24 h,过滤得到微黄色固体.以三氯甲烷/甲醇(体积比25∶1)作淋洗剂,采用硅胶柱分离得白色固体AMOG 0.176 g,产率50.14%,m.p.181~183℃.1H NMR(CDCl3),δ:6.392~6.582(s,4H),4.709~5.267(s,6H),3.185 ~3.342(s,12H),3.044~3.172(m,8H),2.421~2.535(s,8H),1.344~1.509(m,20H),1.109~1.327(m,84H),0.751~0.879(t,J=8 Hz,12H).13C NMR(CDCl3),δ:172.51,172.42,166.09,40.70,39.48,31.91,31.74,29.88,29.64,29.35,27.00,26.58,22.67,14.09.IR(KBr),/cm-1:3300.56(νN—H),2919.26(νCH3),2850.29(ν—CH2—),1539.81(δN—H).
1.2.3 凝胶实验 称取一定量的凝胶因子,加入不同的溶剂,加热使凝胶因子完全溶解于溶剂中,室温下放置冷却.当体系在倒置情况下能够支撑住自身的重量而不落下时即可认定为凝胶形成.溶液⁃凝胶转变温度(Tgel)的测定采用“试管倒转法”[16],即随着测定温度的升高倒转试管,以试管底部的凝胶开始发生流动时的温度为溶液⁃凝胶转变温度.临界凝胶浓度(CGC)的测定从1 mmol/L浓度的凝胶因子开始,以每次1mmol/L的增加量加入,然后加热溶解并冷却至室温,通过“试管倒转法”判断凝胶是否形成.能够形成凝胶的最小凝胶因子浓度即为该种溶液的临界凝胶浓度.所有待测样品在测试前均
在室温下放置约12 h.
2 结果与讨论
2.1 凝胶行为
表1数据表明,AMOG在非极性的甲基环己烷、甲苯、二甲苯和苯乙烯等溶剂中可形成透明凝胶;在弱极性的二氯甲烷、乙酸丁酯、丙酮、乙酸乙酯和四氢呋喃中可形成不透明凝胶;在强极性的DMF和甲醇中形成沉淀.这表明AMOG形成凝胶的能力与溶剂的种类有很大关系,呈现出明显的溶剂效应.

Table 1 Gelation behavior of AMOG in various solvents
图1示出了AMOG在甲基环己烷、甲苯、苯乙烯、二甲苯、乙酸丁酯和甲基丙烯酸丁酯6种溶剂中的Tgel与其浓度的关系.可见,在测试的大多数溶剂中所形成凝胶的溶液⁃凝胶转变温度(Tgel)均随着AMOG浓度的提高而上升;并且随着AMOG浓度的提高,大多数测试样品的Tgel存在先快速上升,后缓慢增加,最后出现一个温度“平台”(当凝胶因子浓度大于5 mmol/L时甲基环己烷中出现了部分沉淀).AMOG在所测溶剂中的Tgel大致呈现出甲基丙烯酸丁酯>乙酸丁酯>二甲苯>甲苯>苯乙烯的规律.
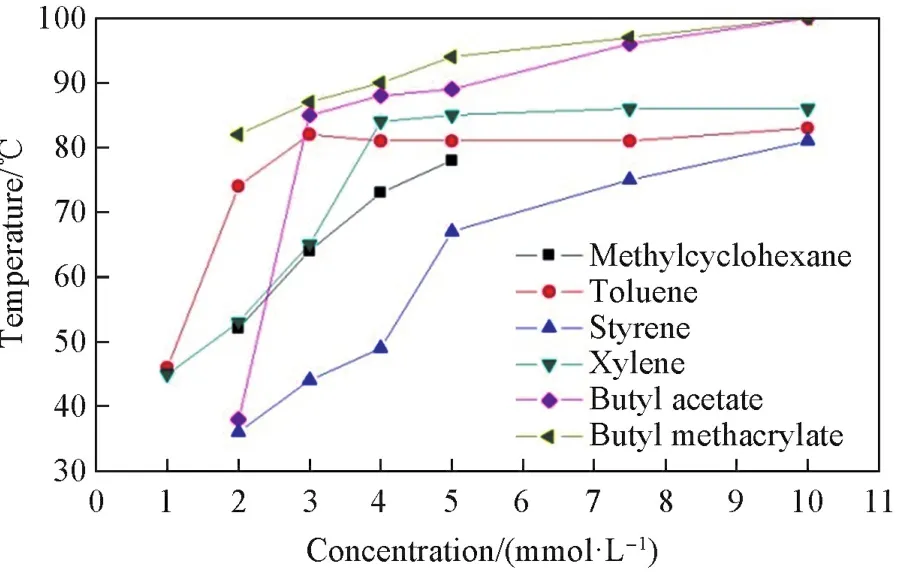
Fig.1 Effect of the solvent environment on the Tgelof gelator AMOG
2.2 凝胶的微观形貌结构
图2为凝胶因子AMOG在4种溶剂中所形成凝胶的SEM照片.可见,在甲苯[图2(A)]与二甲苯[图2(B)]等溶剂中AMOG形成透明凝胶,凝胶由细长的凝胶纤维相互缠绕而成,凝胶纤维之间的缠结比较紧密;而在乙酸乙酯[图2(C)]与乙酸丁酯[图2(D)]等溶剂中AMOG形成不透明凝胶,凝胶纤维的直径更大,且纤维之间的缠结有所减弱.这些结果表明,不同溶剂对凝胶的微观结构具有明显影响,而这种微观结构上的差异导致凝胶在宏观上表现出透明或者不透明状态.

Fig.2 SEM images of gel formed by gelator AMOG in toluene(A),xylene(B),ethyl acetate(C)and butyl acetate(D)
2.3 凝胶的形成与溶剂Hansen溶度参数的关系
为了探索凝胶的形成与溶剂溶度参数之间的关系,将Hansen溶度参数引入凝胶体系中,以期帮助理解与预测凝胶行为.
溶度参数δ可以表示为单位体积内内聚能的平方根[31],即

式中:内聚能E主要有3个来源,分别是由分散作用带来的能量Ed,由极性作用带来的能量Ep和由氢键作用带来的能量Eh.因此,可将总的内聚能E表述为3个来源的分量之和[23],即

于是有

将式(4)中δd,δp和δh3个参数称为Hansen溶度参数.
为了揭示Hansen溶度参数对凝胶行为的影响,实验采用了若干种不同类型的溶剂,这些溶剂的Hansen溶度参数值均来自文献[23],并列于表2中.
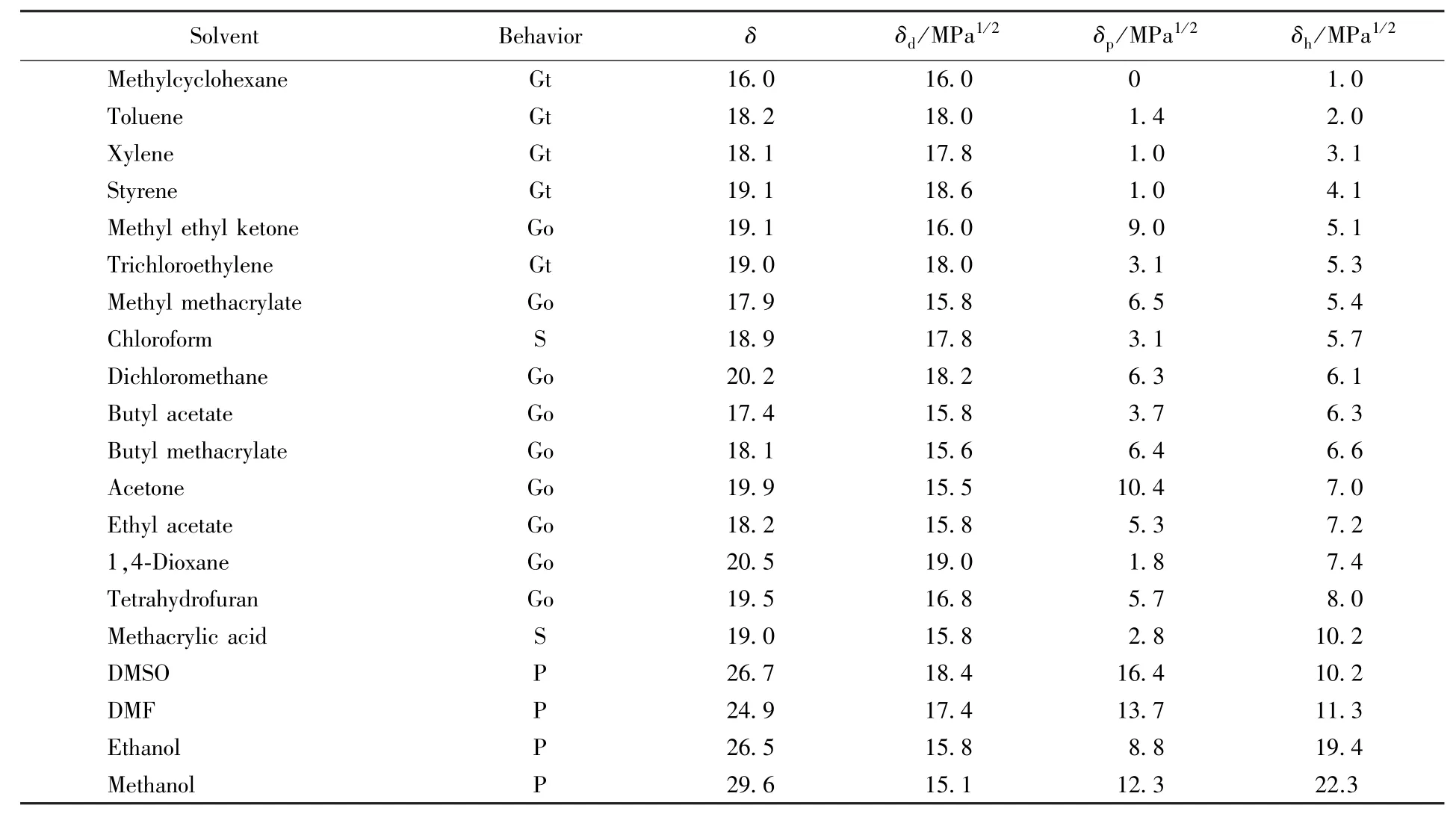
Table 2 Gelation behavior of gelator AMOG in various solvents and Hansen solubility parameters obtained from literature[23]∗
由表2可见,在1.0 MPa1/2<δh<4.1MPa1/2的溶剂中,AMOG倾向于形成透明凝胶;在4.1MPa1/2<δh<8.0 MPa1/2的溶剂中,AMOG倾向于形成不透明凝胶;在δh>8.0 MPa1/2的溶剂中,AMOG倾向于不形成凝胶,而是形成稳定的溶液或者沉淀.
经过计算可知,单个AMOG分子完全伸展开时的长度约为7.6 nm,而图2(A)中的凝胶纤维直径约为10 nm,可以认为此时AMOG分子是沿着凝胶纤维方向排列生长的;图2(D)中的凝胶纤维直径约为50 nm,可以认为此时AMOG分子除了沿纤维方向排列以外,还存在着垂直于纤维方向的排列.当1.0 MPa1/2<δh<4.1 MPa1/2时,由于溶剂与AMOG之间的氢键作用较小,导致凝胶因子两端的三嗪基团上的长烷基链因疏水作用较弱而较为舒展.三嗪基团被“包埋”在内部,难以产生氢键相互作用.此时产生氢键作用的主要基团是酰胺基团,因此大部分AMOG是沿着凝胶纤维方向排列的,形成的凝胶纤维直径较小.当4.1 MPa1/2<δh<8.0 MPa1/2时,溶剂与AMOG之间的氢键作用增大,同时分子两端的烷基链因疏水作用较强而聚集,从而使三嗪基团“暴露”出来,导致酰胺基团和三嗪基团之间可以形成氢键,存在沿纤维方向的排列和垂直于纤维方向的组装,此时形成的凝胶纤维直径较大.当δh>8.0 MPa1/2时,AMOG中的长烷基链的疏水作用进一步增强,AMOG之间的氢键作用进一步减弱,
难以形成相互缠结的三维网状结构,导致稳定溶液或沉淀的形成.
在所测试的溶剂中,大多数非极性或低极性溶剂的Hansen溶度参数均具有同样的特点,即溶剂的δp值和δh值都较小.δp值较小意味着该溶剂是非极性或低极性溶剂,δh值较小意味着溶剂与凝胶因子之间形成氢键的能力较弱,因此有利于透明凝胶的形成.δh对凝胶的微观形貌结构的影响比δp更大.一种情况是二氧六环(δp=1.8 MPa1/2,δh=7.4 MPa1/2),其δp值较小,与甲苯、二甲苯等低极性溶剂类似,然而由于其本身分子结构较容易形成氢键,δh值较大,因而导致了在二氧六环中形成的是不透明凝胶.由此可见,δh值对凝胶微观形貌的影响较大.另外一种情况是三氯乙烯(δp=3.1 MPa1/2,δh=5.3 MPa1/2)和甲基丙烯酸甲酯(δp=6.5 MPa1/2,δh=5.4 MPa1/2),这2种溶剂的δh值相似,但是AMOG在三氯乙烯中形成的是透明凝胶,而在甲基丙烯酸甲酯中形成的是不透明凝胶.
由于甲基丙烯酸甲酯的δp值较大,导致AMOG与溶剂之间产生了较强的疏水作用,AMOG分子两端的长烷基链处于蜷曲或聚集状态,从而使三嗪基团之间也可以形成氢键,从而形成较粗的凝胶纤维.因此,氢键作用(δh)和极性作用(δp)对凝胶纤维的微观形貌均有一定的影响,其中氢键作用(δh)的影响更大.
为了更好地理解Hansen溶度参数的3个变量与凝胶行为之间的关系,以δd,δp和δh为三维坐标构造Hansen空间,则每一种物质都可以在Hansen空间中以1个点表示.Hansen空间中两点间的“距离”的定义是:
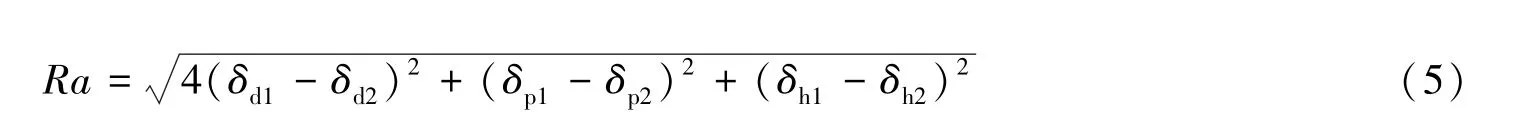
在Hansen溶度参数的应用中,通常可以通过Ra值的大小来判断物质在溶剂中的溶解性[23],如,能溶解在某种溶剂中的物质的Hansen溶度参数往往均集中在Hansen空间的某一特定“溶度球”区域内.而将Hansen溶度参数引入凝胶体系中,则可以通过构造“凝胶球”并根据Ra值的大小来预测凝胶因子在不同溶剂中的凝胶行为[32].
在Ra的表达式中,δd项前的参数“4”为经验参数,如果以2δd-δp-δh为三维坐标进行绘图,则两点之间几何意义上的距离就与其Ra相同,可以使计算出的“凝胶球”区域保持球形[23,33].
一个理想的“凝胶球”区域需要包含尽可能多的能够形成凝胶的溶剂在内,同时将尽可能多的不能形成凝胶的溶剂排除在外.按Gharagheizi等[34]报道的方法,经过计算发现,大多数可以形成凝胶的溶剂都集中分布在以2δd=32.4 MPa1/2,δp=4.1 MPa1/2,δh=3.9 MPa1/2为球心,Ra=5.8 MPa1/2为半径的球形区域内.
如图3所示,能够形成凝胶的溶剂以绿色标出,形成溶液的溶剂以黄色标出,不能溶解或者析出沉淀的溶剂以红色标出.可见,除了丙酮(2δd=31.0 MPa1/2,δp=10.4 MPa1/2,δh=7.0 MPa1/2)和二氧六环(2δd=38.0 MPa1/2,δp=1.8 MPa1/2,δh=7.4 MPa1/2)以外,所有能形成凝胶的溶剂均包含在图3左下角的橙色“凝胶球”内.除了三氯甲烷(2δd=35.6 MPa1/2,δp=3.1 MPa1/2,δh=5.7 MPa1/2)以外,所有不能形成凝胶的溶剂均位于“凝胶球”外.
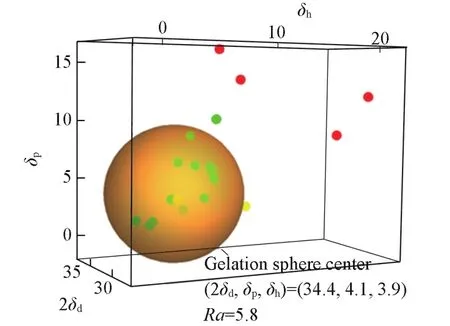
Fig.3 Gelation behavior for gelator AMOG in various solvents p lotted in 3D Hansen space
2.4 凝胶热行为与Hansen溶度参数的关系
为了更清楚地表示凝胶的Tgel与Hansen溶度参数中各个分量的关系,选取10种常用溶剂并在5 mmol/L的AMOG浓度下测量其Tgel,结果如表3所示.将Tgel与Hansen溶度参数的各个分量作为坐标轴绘得图4.
由图4可见,所测溶剂中凝胶的Tgel与Hansen溶度参数的各个单独的参数并无明显的关联性,表明Tgel不是由某一个参数单独决定的,而可能是多个参数共同作用的结果.
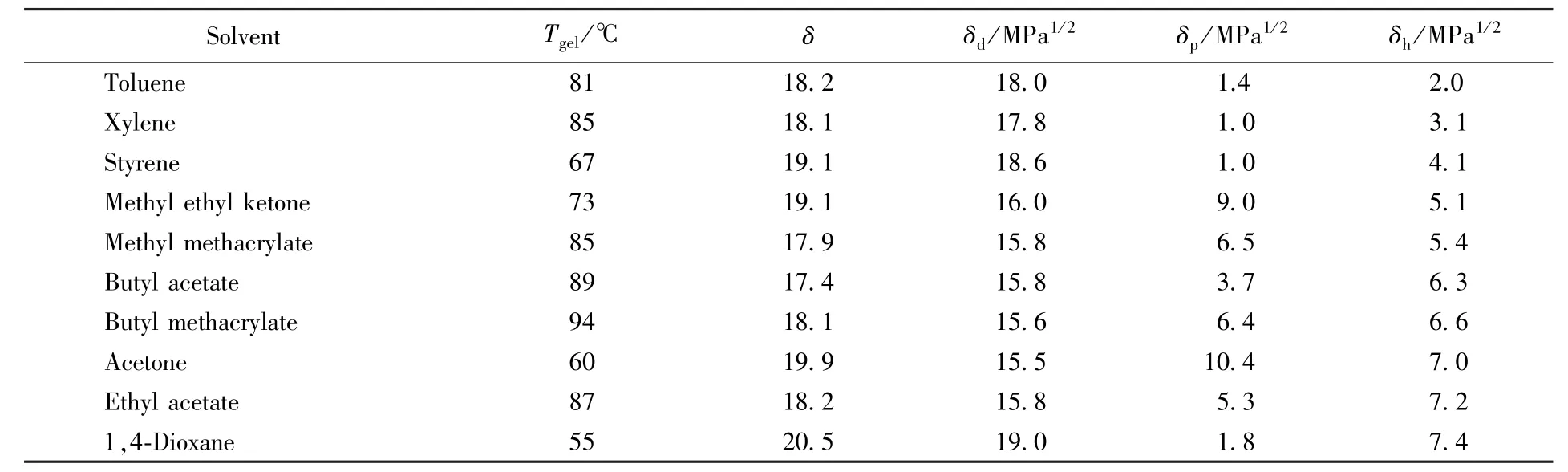
Tab le 3 Tgelof gels formed in ten different solvents and Hansen solubility param eters of these solvents
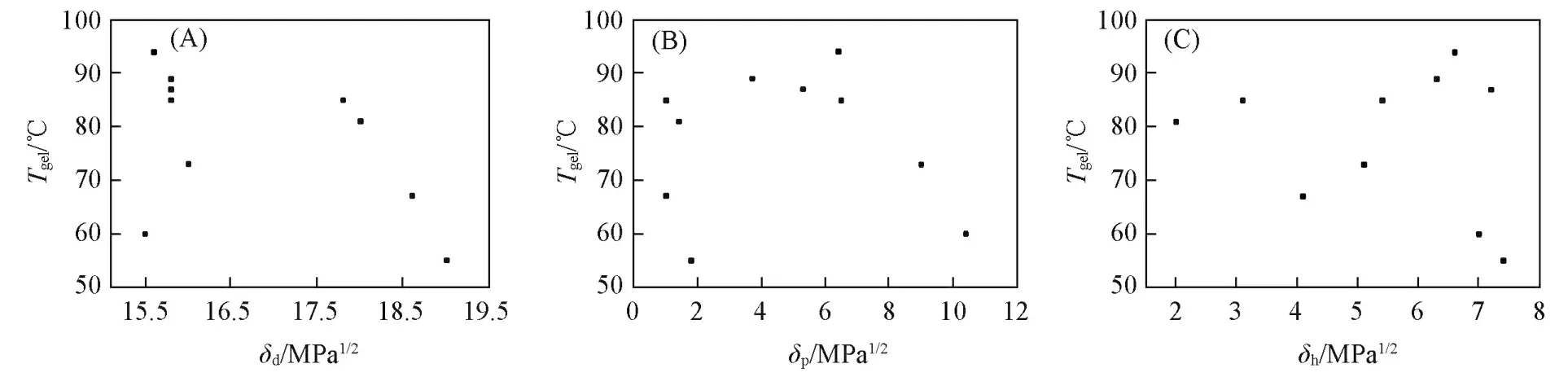
Fig.4 Effects of individual Hansen solubility parametersδd(A),δp(B)andδh(C)on Tgel
通过构造含有2种参数分量的新溶度参数,可以考察这2种分量对Tgel的影响.因此将Hansen溶度参数中的δd,δp及δh进行组合,构造了几个新的溶度参数δdp,δdh和δph:

式中:δ0是包含了3个Hansen溶度参数分量的参数.
以新构造的3个溶度参数及δ0和Tgel作为坐标轴绘图得到图5.
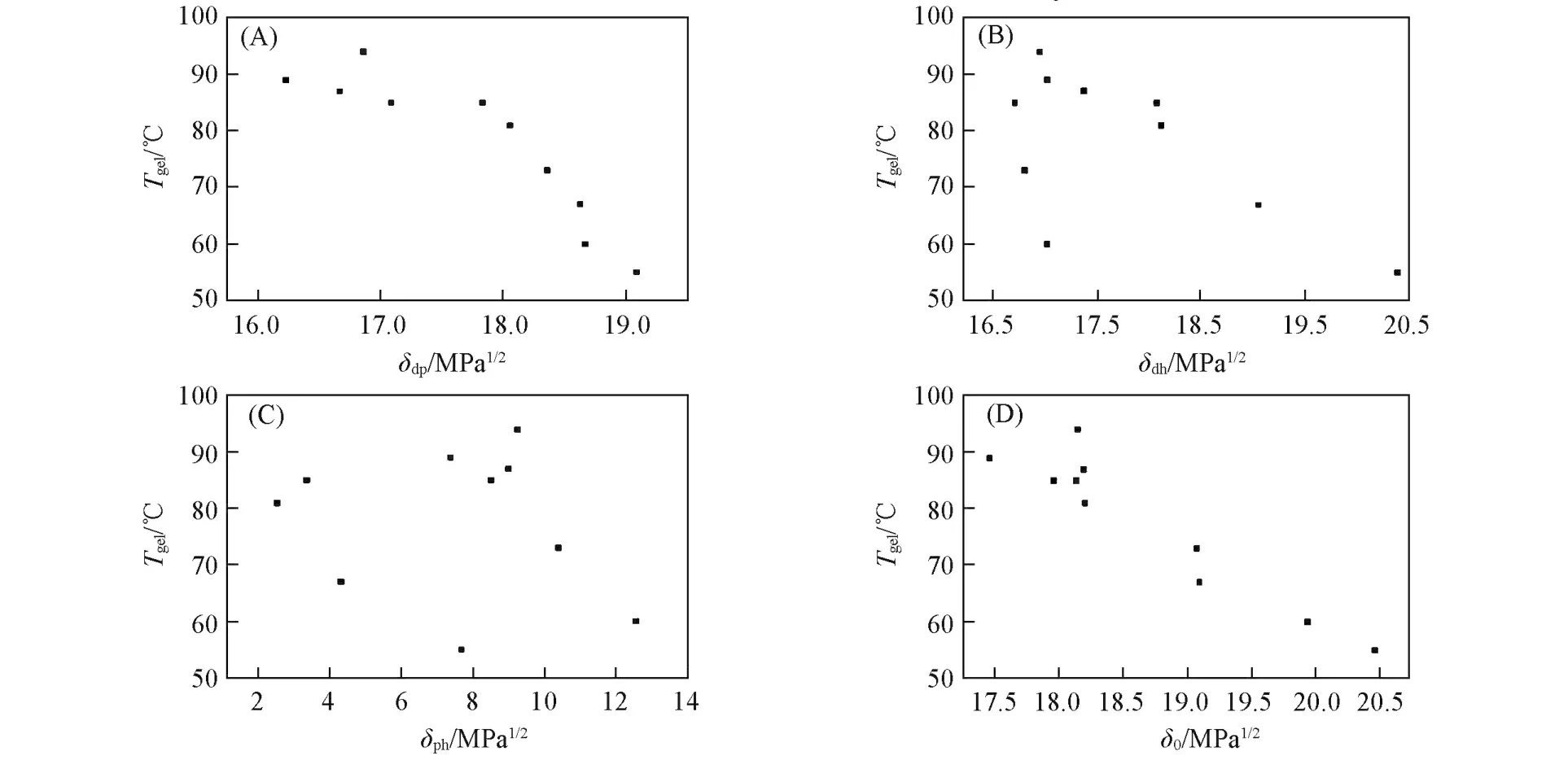
Fig.5 Effects of constructed solubility parametersδdp(A),δdh(B),δph(C)andδ0(D)on Tgel
由图5可见,凝胶的Tgel与新构造的溶度参数δdp及Hansen溶度参数δ0均呈现良好的线性关系[图5(A)和(D)].对图5(A)和(D)中的散点进行线性拟合,得到δdp和δ0相关系数R2分别为0.78和
0.89.因此,Hansen溶度参数δ0与Tgel有较佳的线性相关关系,溶度参数δdp与Tgel的线性相关关系次之.而在图5(B)和(C)中,并不能观察到明显的线性相关.因此,对于所讨论的凝胶体系来说,Tgel在很大程度上受到溶剂的色散作用(δd)与极性作用(δp)的共同影响,而氢键作用(δh)对Tgel的影响相对较弱.
3 结 论
设计合成了一种含有酰胺基团与密胺基团的凝胶因子AMOG,其在常用有机溶剂中有较强的凝胶形成能力,所形成凝胶的溶液⁃凝胶转变温度与凝胶微观结构表现出明显的溶剂效应.在低极性的溶剂中AMOG形成凝胶纤维直径较小的透明凝胶;在较高极性的溶剂中AMOG形成纤维直径较大的不透明凝胶.利用Hansen溶度参数对不同溶剂中的凝胶行为进行研究表明,在1.0 MPa1/2<δh<4.1 MPa1/2的溶剂中,凝胶因子倾向于形成透明凝胶;在4.1 MPa1/2<δh<8.0 MPa1/2的溶剂中,凝胶因子倾向于形成不透明凝胶;在δh>8.0 MPa1/2的溶剂中,凝胶因子倾向形成稳定的溶液或者沉淀.大多数可以形成凝胶的溶剂均集中分布在以2δd=32.4 MPa1/2,δp=4.1 MPa1/2,δh=3.9 MPa1/2为球心,Ra=5.8 MPa1/2为半径的球形区域内.凝胶的溶液⁃凝胶转变温度(Tgel)与色散参数δd和极性参数δp有关,且两者的组合参数δdp越大,凝胶的Tgel越小.本文结果有助于更好地理解溶剂在凝胶形成过程中的作用,也为进一步利用Hansen溶度参数预测凝胶因子的凝胶行为提供了可靠依据.
[1] Stupp S.I.,Nano Lett.,2010,10(12),4783—4786
[2] ShinjiM.,Satoshi Y.,Shiori U.,Harunobu K.,Masato I.,Koji I.,Yuko I.,Kazuhito V.T.,Hiroyuki A.,Shinzaburo I.,Hiroyuki N.,Itaru H.,Chem.Eur.J.,2008,14(13),3977—3986
[3] Shigeki K.,Kazunori S.,Seiji S.,Itaru H.,J.Am.Chem.Soc.,2002,124(37),10954—10955
[4] Chen S.R.,Xue M.,Pan Y.,Xu D.,Qiu S.L.,Chem.J.Chinese Universities,2015,36(5),815—820(陈思如,薛铭,潘莹,徐丹,裘式纶.高等学校化学学报,2015,36(5),815—820)
[5] Yu X.D.,Chen L.M.,Zhang M.M.,Yi T.,Chem.Soc.Rev.,2014,43(15),5346—5371
[6] Grace T.,Mohit S.,Jibao H.,John V.T.,Mcpherson G.L.,Langmuir,2005,21(20),9322—9326
[7] Jong J.J.D.D.,Lucas L.N.,Kellogg R.M.,Esch J.H.V.,Feringa B.L.,Science,2004,304(15),278—281
[8] Supratim B.,Rajat K.D.,Uday M.,J.Mater.Chem.,2009,19(37),6649—6687
[9] Abdallah D.J.,Weiss R.G.,Adv.Mater.,2000,12(17),1237—1247
[10] Zhang H.L.,Yan N.,Wu S.W.,Cai X.Q.,Liu K.Q.,Fang Y.,Chem.J.Chinese Universities,2011,32(7),1573—1580(张荷兰,晏妮,武思文,蔡秀琴,刘凯强,房喻.高等学校化学学报,2011,32(7),1573—1580)
[11] Sangeetha N.M.,Uday M.,Chem.Soc.Rev.,2005,34(10),821—836
[12] Aparicio F.,García F.,Sánchez L.,Chem.Eur.J.,2013,19(9),3239—3248
[13] Yan C.,Xiao Y.L.,DaiH.,Cheng X.H.,Chem.J.Chinese Universities,2016,37(3),475—479(严超,肖玉龙,戴衡,程晓红.高等学校化学学报,2016,37(3),475—479)
[14] George M.,Weiss R.G.,Accounts Chem.Res.,2006,37(45),489—497
[15] Fan D.L.,Zhai Y.,Zhang Y.,Tu W.,Huang Y.D.,Chem.J.Chinese Universities,2014,35(11),2447—2454(樊冬丽,翟岩,张妍,涂伟,黄耀东.高等学校化学学报,2014,35(11),2447—2454)
[16] Parthasarathi D.,Chem.Soc.Rev.,2008,37(12),2699—2715
[17] Esch J.H.V.,Langmuir,2009,25(15),8392—8394
[18] BielejewskiM.,Lapiński A.,Luboradzki R.,Tritt⁃Goc J.,Langmuir,2009,25(14),8274—8279
[19] And G.Z.,Dordick J.S.,Chem.Mater.,2006,18(25),5988—5995
[20] Tong C.,Fan K.,Niu L.,Li J.,Guan X.,Tao N.,Soft Matter,2014,10(5),767—772
[21] Hirst A.R.,Smith D.K.,Langmuir,2004,20(25),10851—10857
[22] Yan N.,Xu Z.Y.,Diehn K.K.,Raghavan S.R.,Fang Y.,Weiss R.G.,Langmuir,2012,29(2),793—805
[23] Hansen C.M.,Hansen Solubility Parameters:a User's Handbook.CRC Press,Boca Raton,2007
[24] Matthieu R.,Laurent B.,Chem.Commun.,2011,47(29),8271—8273
[25] Bonnet J.,Suissa G.,Raynal M.,Bouteiller L.,Soft Matter,2014,10(18),3154—3160
[26] Yan N.,Xu Z.Y.,Diehn K.K.,Raghavan S.R.,Fang Y.,Weiss R.G.,J.Am.Chem.Soc.,2013,135(24),8989—8999
[27] Gao J.,Wu S.,Rogers M.A.,J.Mater.Chem.,2012,22(25),12651—12658
[28] Shen H.,Niu L.,Fan K.,Li J.,Guan X.,Song J.,Langmuir,2014,30(30),9176—9182
[29] Curcio P.,Allix F.,Pickaert G.,Chemistry,2011,17(48),13603—13612
[30] Yuan H.,Synthesize and Self⁃assembly of Dendritic Functional Polymers Based on Perylene Bisimide/Triazine,Hunan University,Chang⁃sha,2009(袁欢.基于苝酰亚胺/三嗪的树枝状功能聚合物的合成与自组装,长沙:湖南大学,2009)
[31] Hansen C.M.,Prog.Org.Coat.,2004,51(1),77—84
[32] Zhao C.X.,Wang H.T.,LiM.,Acta Physico⁃Chimica Sinica,2014,30(12),2197—2209(赵呈孝,王海涛,李敏.物理化学学报,2014,30(12),2197—2209)
[33] Diehn K.K.,Oh H.,Hashemipour R.,Weiss R.G.,Raghavan S.R.,Soft Matter,2014,10(15),1308—1311
[34] Gharagheizi F.,J.Appl.Polym.Sci.,2007,103(1),31—36
Synthesis and Gel Properties of a Novel Am ide Gelator with Melamine Moieties and Rationalizing Gelation Behavior by Hansen Solubility Parameters†
WANG Xiao,YANG Xinguo∗,SHEN Qili
(College ofMaterials Science&Engineering,Hunan Province Key Laboratory for Spray Deposition Technology&Application,Hunan University,Changsha 410082,China)
A novel amide gelator with melamine moieties(AMOG)was designed and synthesized.Gelator AMOG is capable of forming gel in various common organic solvents and the critical gelation concentration (CGC)of the gels formed in toluene and xylene are as low as 1mmol/L.Tube inversion method is adopted to define the sol⁃gel transition temperature(Tgel)and the scanning electron microscope(SEM)is used to investi⁃gatemicro⁃morphology of gels.The results of these tests exhibit obvious solvent effect on gelation behavior of AMOG.Further investigation for gelation behavior based on Hansen solubility parameters(HSPs)of solvents reveals that hydrogen bonding parameter(δh)has significant influence on themicro⁃morphology and properties of gels.1.0 MPa1/2<δh<4.1 MPa1/2for organic solvents is the favorable domain for transparent gels formation,opaque gels occur in the range of 4.1 MPa1/2<δh<8.0 MPa1/2and solution/precipitation remain ifδhis larger than 8.0 MPa1/2.HSPs values for tested solvents are plotted as a point in Hansen space,which is constructed withδd,δpandδhas its three⁃dimensional coordinates.Most of the solvents that could form gels cluster in a certain region in above Hansen space.Sol⁃gel transition temperature is related to parameterδdandδp.
Organogel;Amide;Melamine;Hansen solubility parameter;Solvent effect
O648.17
A
10.7503/cjcu20160268
(Ed.:V,Z,K)
†Supported by the National Natural Science Foundation of China(Nos.50573019,51273061)and the Natural Science Foundation of Hunan Province,China(No.2016JJ2027).
2016⁃04⁃22.
日期:2016⁃10⁃19.
国家自然科学基金(批准号:50573019,51273061)和湖南省自然科学基金(批准号:2016JJ2027)资助.
联系人简介:杨新国,男,博士,副教授,主要从事有机/高分子功能材料的制备与应用研究.E⁃mail:xgyang@hnu.edu.cn
