阻断孕鼠子宫动脉后宫内窘迫胎鼠海马组织内谷氨酸浓度的变化
2016-11-22任杰戴晓怡李利彪吴凡郭春燕
任杰 戴晓怡 李利彪 吴凡 郭春燕
1.内蒙古医科大学附属医院心外科,内蒙古呼和浩特010050;2.内蒙古医科大学附属医院妇产科,
内蒙古呼和浩特010050;3.内蒙古医科大学附属医院麻醉科,内蒙古呼和浩特010050
阻断孕鼠子宫动脉后宫内窘迫胎鼠海马组织内谷氨酸浓度的变化
任杰1戴晓怡2李利彪3吴凡3郭春燕3
1.内蒙古医科大学附属医院心外科,内蒙古呼和浩特010050;2.内蒙古医科大学附属医院妇产科,
内蒙古呼和浩特010050;3.内蒙古医科大学附属医院麻醉科,内蒙古呼和浩特010050
目的观察阻断孕鼠子宫动脉后宫内窘迫胎鼠海马组织内谷氨酸(Glu)浓度的变化。方法随机将72只SD孕鼠采用3伊3析因设计方法[阻断子宫动脉的程度(3水平院轻度阻断、中度阻断、完全阻断)和阻断时间(3水平院5、10、15min)],分为9组(n=8),建立宫内窘迫的大鼠模型。全部胎儿宫内窘迫制模结束后,剖宫取出胎鼠,留取海马,采用高效液相色谱法检测受试胎鼠海马组织中Glu含量。结果阻断孕鼠子宫动脉后宫内窘迫可以诱发胎鼠海马组织Glu浓度升高,轻度阻断(5、10、15 min)分别为(50.20依7.67)、(54.67依7.52)、(65.40依7.61)滋mol/gprot,中度阻断(5、10、15 min)分别为(69.17依12.08)、(90.53依18.95)、(121.84依22.62)滋mol/gprot,完全阻断(5、10、15min)分别为(137.81依29.78)、(170.93依18.77)、(184.39依20.86)滋mol/gprot;在相同阻断时间下,随阻断子宫动脉的程度加大,可增加受试胎鼠海马组织内Glu浓度(F=46.699、110.803、84.633,P<0.01);在相同阻断程度下,随阻断时间增加,Glu在胎鼠海马组织内的浓度亦增加(F=8.448、16.562、8.240,P<0.01);且阻断时间和阻断程度对Glu的影响呈相互增加效果(F=3.088,P<0.05)。结论阻断子宫动脉后宫内窘迫可以诱发胎鼠海马组织内Glu浓度明显升高,而且海马组织中Glu浓度随阻断子宫动脉的程度和阻断时间而增加。
谷氨酸;胎儿宫内窘迫;高效液相色谱法;海马
胎儿宫内窘迫主要是由宫内胎儿的血供绝对或相对下降引起的,造成胎儿出生后学习和记忆等脑功能下降,但其具体的发病机制不明,可能与中枢神经谷氨酸(Glu)信息传递系统出现功能异常有一定关系。研究者的首要疑问是,胎儿宫内窘迫后的缺血缺氧强应激诱发的神经组织内Glu浓度升高是否可以通过制作动物模型、以动物实验来得到实际验证钥不同程度和时间阻断子宫动脉会对胎鼠海马组织中的Glu含量是否有不同的影响钥为此设计本实验,研究不同程度和时间阻断子宫动脉的宫内窘迫模型的制作和其诱发的缺血缺氧强应激对胎鼠海马组织内Glu含量的影响。
1 材料与方法
1.1 实验动物
选择无特定病源体级(SPF)SD大鼠,鼠龄24周,体重为275~300 g,雌雄各80只,由内蒙古医科大学动物实验部提供(动物合格批准文号院内医动-第013号)。雌雄大鼠合笼饲养之后,研究者需要每天使用棉签擦拭雌鼠阴道,进行阴道精液涂片检测,若为阳性则将该日记录为雌鼠受孕的第1天,并且换用高营养的饲料进行喂养。此后,实验人员应每日观察该雌鼠的腹部是否有膨隆的怀孕表现,如果连续10 d均无子宫膨隆现象,则可以认定为该雌鼠受孕过程失败。本实验实施方案经内蒙古医科大学伦理审查委员会和内蒙古医科大学附属医院伦理审查委员会审查批准,并且全部操作均按照动物实验相关经典指南严格执行。所有实验都严格遵循标准的动物实验原则,即随机、对照、双盲的实验原则。
1.2 方法
1.2.1 实验动物分组
选取72只受孕18 d大鼠作为试验对象,采用3伊3析因设计院阻断子宫动脉的程度(3水平院轻微阻断、中度阻断、完全阻断)和阻断时间(3水平院5、10、15min),随机分为9组(n=8)。
1.2.2 大鼠子宫动脉夹闭模型的制作及取材
选择符合实验要求的SD大鼠雌、雄合笼饲养受孕。受孕18 d时按照参考文献[1]制作大鼠子宫动脉夹闭模型(宫内窘迫大鼠模型),方法为院充分暴露大鼠子宫动脉后,用硅酮血管阻断带紧绕动脉,实验开始时以一把血管钳夹血管阻断带交汇处为轻微阻断;两把血管钳并列夹为中度阻断;完全阻断动脉血流为完全阻断。子宫动脉夹闭模型制模结束后,剖宫取出胎鼠,麻醉下断头取脑、分离获取胎鼠海马,组织进行称重后,加甲醇-水配制的离心液1mL,在低温下匀浆处理,继而取出一部分的匀浆液置于4益,以12 000 r/min的条件,进行15 min离心处理,最后取出上清液,再经滤膜过滤处理之后,将其放置在-80益冰箱之内保存,待测Glu具体含量。
1.2.3 高效液相色谱法(HPLC)检测Gl u在胎鼠海马中的含量[2]
1.2.3.1 检测样品处理好的胎鼠右侧海马匀浆上清液。
1.2.3.2 试剂Glu标准品(Sigma公司、L-Glutamic acid ReagentPlusR,批号2013000312),邻苯二甲醛(上海碧云天生物有限公司,批号201200431),茁-巯基乙醇(Gibco公司,2-Mercaptoethanol-1000X,批号20140000545),色谱级甲醇(上海碧云天生物有限公司,批号201200652)。
1.2.3.3 仪器及色谱条件低温高速离心机(Centrifuge 5810R,HPLC色谱系统(Shimadzu/岛津,型号LC-10AD VP),包括600泵、荧光2475检测器、Empower色谱工作站;18-ODS色谱柱,柱温35益;流动相A院0.1 mol/L醋酸钾,流动相B院甲醇;进行二元梯度洗脱,梯度洗脱程序院(T,B%)(0,45%)(1,65%)(6,75%)(20,45%)。T指时间(min),B%指B流动相所占比例。流动相经0.45滋m微孔滤膜过滤,超声脱气。流速1.0 mL/min、激发波长250 nm,发射波长410 nm,以Glu的峰面积定量。
1.2.3.4 衍生化试剂的配制将20mg OPA溶于500滋L色谱级的甲醇中,进行超声溶解,再加入茁-巯基乙醇500滋L,加入9 mL pH 10.0的硼酸缓冲液,避光密封后置于0~4益冰箱保存。
1.2.3.5 氨基酸标准液的配制Glu标准品配成100滋mol/L的标准溶液,检测之前进行稀释。
1.2.3.6 衍生及分析取100滋L标准液或者组织样品液和Eppendorf 3810型微量离心管(简称EP管),加入100滋L衍生化试剂反应2min后进样20滋L。
1.2.3.7 Glu标准曲线的建立配制浓度分别为0.15、0.30、0.735、1.47、2.94、3.675、5.88mg/L的Glu标准溶液,衍生化处理后测定。应用外标法进行定量分析,以其峰面积(Y)对其浓度(X)进行直线回归,得到线性方程。
1.2.3.8 海马组织内Glu含量的测定对海马组织的匀浆上清液进行解冻,置入玻璃匀浆器,加冰冻的甲酸(1 mol/L,2 mL),冰浴下手动充分匀浆。将匀浆液于4益7000 r/min离心30 min。取上清液置-20益保存。每1毫升匀浆上清液加0.75 mL 4%的碳酸氢钠溶液混匀,4益3000 r/min离心5 min,取上清液过0.45滋m滤膜,分装。取分装液24滋L,在进样瓶中加衍生试剂12滋L,四硼酸钠缓冲液(pH 9.18)960滋L,混匀,20益下静置3 min后再依次进样,继而梯度洗脱,测定海马组织的Glu含量。
1.3 统计学方法
采用SPSS 20.0统计学软件进行数据分析,计量资料数据用均数依标准差(x±s)表示,首先对各组样本行方差齐性的检验,若经过检验证明方差齐,则采用析因设计方差分析,分析各因素的交互效应和主效应;各因素的单独效应采用单因素方差分析。以P< 0.05为差异有统计学意义。
2 结果
随阻断子宫动脉的程度加大,相同阻断时间的胎鼠海马组织内Glu浓度逐渐增加(F=46.699、110.803、84.633,P<0.01);随阻断时间增加,相同阻断程度的受试胎鼠海马组织内Glu浓度亦逐渐增加(F=8.448、16.562、8.240,P<0.01);阻断时间和阻断程度对胎鼠海马组织Glu的影响呈相互增加效果(F= 3.088,P<0.05)。见表1。
表1 不同时间和程度阻断子宫动脉后胎鼠海马组织Glu含量(滋mol/gprot,,n=8)
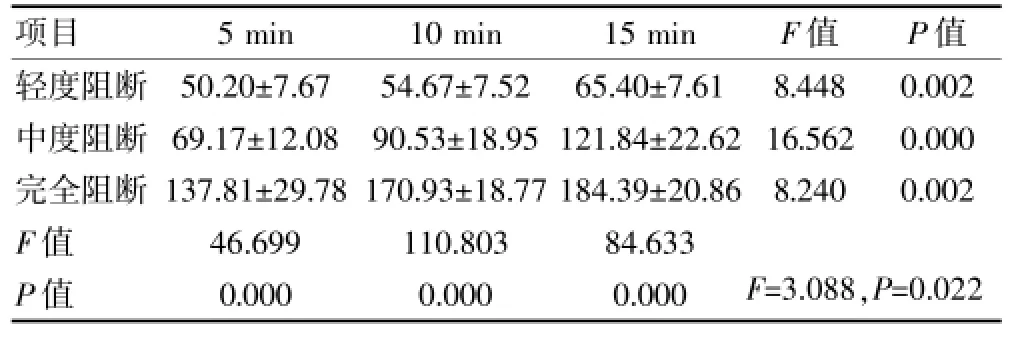
表1 不同时间和程度阻断子宫动脉后胎鼠海马组织Glu含量(滋mol/gprot,,n=8)
项目5 min 10 min 15 min F值P值轻度阻断中度阻断完全阻断F值P值50.20依7.67 69.17依12.08 137.81依29.78 46.699 0.000 54.67依7.52 90.53依18.95 170.93依18.77 110.803 0.000 65.40依7.61 121.84依22.62 184.39依20.86 84.633 0.000 8.448 16.562 8.240 0.002 0.000 0.002 F=3.088,P=0.022
3 讨论
本研究选用SD大鼠,通过雌性和雄性大鼠合笼,以促使雌鼠受孕。通过不同程度阻断受孕鼠的子宫动脉造成胎盘循环障碍诱发胎鼠宫内窘迫,达到所需时间后以制作胎儿宫内窘迫的大鼠模型,来测定胎鼠海马组织中Glu的含量。Glu在人脑中的含量为8.4滋mol/g,哺乳动物中枢神经系统中突触的神经递质大约40%为Glu[3-5],是最重要的兴奋性神经递质。Glu作为神经递质,其对神经细胞的作用具双向性[6-8]院一是正常含量的Glu递质激动Glu受体以激动神经细胞N-甲基-D-天冬氨酸(N-methyl-d-aspartic acid,NMDA)受体是保持神经细胞传递正常信息、保持信息传导通路畅通所必须的;二是如果脑内过度大量释放Glu,会过度激动膜电位依赖式Glu受体,会引起Cl-、Na+、H2O和Ca2+大量内流,导致神经细胞内Ca2+超载,通过磷酸肌醇环路的激活破坏神经细胞的超微结构,最终神经细胞溶解、凋亡或坏死,造成机体学习记忆等脑功能障碍。基于Glu及NMDA受体的相关研究表明,强应激能够使Glu在受试动物脑内海马组织中的表达水平明显增加,过高表达的Glu使得NMDA受体过度激活,引起Cl-、Na+、H2O和Ca2+大量内流,导致神经细胞内Ca2+超载等兴奋性神经细胞毒性反应[9-11],其可以导致神经细胞损伤[12-16],造成学习记忆等脑功能障碍[17-20]。
宫内窘迫诱发的缺血缺氧强应激导致Glu介导的神经细胞兴奋性毒性反应[13]。本实验发现,宫内窘迫诱发的缺血缺氧强应激后胎鼠海马组织内Glu浓度明显上升,结果提示宫内窘迫可诱发Glu信息传递系统的异常兴奋,可能会给胎鼠带来Glu过度表达和过度激活相关的Glu受体,造成神经细胞的兴奋性毒性,使宫内窘迫后胎鼠的脑内神经细胞受损,即宫内窘迫造成的胎鼠缺血缺氧的强刺激可激活Glu介导的神经传递系统的过度兴奋。本研究还发现宫内窘迫诱发缺血缺氧强应激后引起Glu浓度在胎鼠脑内海马组织中的升高,具有量效性的特点和时效性的特点。实验结果提示,阻断孕鼠子宫动脉的时间越长和程度越重,Glu在胎鼠脑内海马组织内中的表达越高,可以推断宫内窘迫的时间和宫内窘迫的程度对胎鼠神经系统的损害呈正相关。这为临床治疗和预防宫内窘迫后胎儿学习记忆障碍提供了新的指导方向,即应充分改善子宫动脉的供血,可减轻胎儿宫内窘迫诱发的缺血缺氧强应激后的胎儿机体神经细胞损伤。
[1]张华,卢敏,漆洪波,等.2脱氧葡萄糖诱导葡萄糖调节蛋白78表达上调对宫内窘迫胎鼠脑神经元的保护作用[J].中华妇产科杂志,2008,43(5):356-360.
[2]Singh M,Kamal YT,Khan MA,et al.Matrix Solid-Phase Dispersion Extraction and Quantification of Alpinetin in Amomum Seed using Validated HPLC and HPTLC Meth-ods[J].Indian JPharm Sci,2015,77(1):49-54.
[3]Wilkie IC,Fassini D,Cullor伽E,et al.Mechanical Proper-ties of the Compass Depressors of the Sea-Urchin Para-centrotus lividus(Echinodermata,Echinoidea)and the Ef-fects of Enzymes,Neurotransmitters and Synthetic Ten-silin-Like Protein[J].PLoSOne,2015,10(3):e0120339.
[4]BurketJA,Benson AD,Green TL,etal.EffectsofVU0410120,a novel GlyT1 inhibitor,on measures of sociability,cog-nition and stereotypic behaviors in a mouse model of autism[J].Progress in Neuro-Psychopharmacology and Biological Psychiatry,2015,61院10-17.
[5]Ferreira NR,Lourenco CL,Barbosa RM,et al.Coupling of ascorbate and nitric oxide dynamics in vivo in the rat hip-pocampus upon glutamatergic neuronal stimulation院a nov-el functional interplay[J].Brain Res Bull,2015,114(22):13-19.
[6]Chong W,Kim SN,Han SK,et al.Low Non-NMDA Re-ceptor Current Density as Possible Protection Mechanism from Neurotoxicity of Circulating Glutamate on Subfornical Organ Neuronsin Rats[J].Korean JPhysiolPharmacol,2015,19(2):177-181.
[7]S覥omka M,Kuszczyk M,覵azarewicz JW,et al.NMDA re-ceptor antagonists MK-801 and memantine induce toler-ance to oxygen and glucose deprivation in primary cul-tures of rat cerebellar granule cells[J].Acta Neurobiol Exp(Wars),2014,74(4):396-404.
[8]Cunha MP,Pazini FL,Ludka FK,et al.The modulation of NMDA receptors and L-arginine/nitric oxide pathway is implicated in the anti-immobility effect of creatine in the tail suspension test[J].Amino Acids,2015,47(4):795-811.
[9]Gasperini L,Meneghetti E,Pastore B,et al.Prion Protein and Copper Cooperatively Protect Neurons by Modulating NMDAReceptor Through S-nitrosylation[J].Antioxid Redox Signal,2015,22(9):772-784.
[10]Richter M,Nickel C,Apel L,et al.SK channel activation modulatesmitochondrial respiration and attenuates neu-ronal HT-22 cell damage induced by H2O2[J].Neu-rochem Int,2015,81院63-75.
[11]Z伲grean AM,Spataru A,Ceang伲M,et al.The single ver-sus combinatorial effects of MK-801,DNQX,Nifedipine and AP-3 on primary cultures of cerebellar granule cells in an oxygen-glucose deprivationmodel[J].Rom JMor-phol Embryol,2015,55(3):811-816.
[12]Bell JD1,Thomas TC,Lass E,et al.Platelet-mediated changes to neuronal glutamate receptor expression at sites of microthrombosis following experimental sub-arachnoidhemorrhage[J].JNeurosurg,2014,121(6):1424-1431.
[13]Rangel-L佼pez E,Col侏n-Gonz佗lez AL,Paz-Loyola AL,et al.Cannabinoid receptor agonists reduce the short-term mitochondrial dysfunction and oxidative stress linked to excitotoxicity in the rat brain[J].Neuroscience,2015,29(285):97-106.
[14]Black SA,Stys PK,Zamponi GW,et al.Cellular prion protein and NMDA receptor modulation院protecting a-gainst excitotoxicity[J].Front Cell Dev Biol,2015(2):41-45.
[15]Paniz LG,Calcagnotto ME,Pandolfo P,et al.Neuropro-tective effects of guanosine administration on behavioral,brain activity,neurochemical and redox parameters in a ratmodel of chronic hepatic encephalopathy[J].Metab Brain Dis,2015,29(3):645-654.
[16]TabuchiM,Lone SR,Liu S,et al.Sleep interacts with a茁tomodulate intrinsic neuronal excitability[J].Curr Biol,2015,25(6):702-712.
[17]Da Silva-Alves KS,Ferreira-da-Silva FW,Coelho-de-Souza AN,et al.Essential Oil of Croton zehntneriand Its Main Constituent Anethole Block Excitability of Rat Pe-ripheral Nerve[J].Planta Med,2015,81(4):292-297.
[18]Zhang H,Dougherty PM.Enhanced excitability of prima-ry sensory neurons and altered gene expression of neu-ronal ion channels in dorsal root ganglion in paclitaxelinduced peripheral neuropathy[J].Anesthesiology,2014,120(6):1463-1475.
[19]Choi IY,Lim JH,Kim C,et al.4-hydroxy-2(E)-None-nal facilitates NMDA-Induced Neurotoxicity via Trig-gering Mitochondrial Permeability Transition Pore Open-ing and Mitochondrial Calcium Overload[J].Exp Neuro-biol,2013,22(3):200-207.
[20]Lozano D,Gonzales-Portillo GS,Acosta S,et al.Neuroin-flammatory responses to traumatic brain injury院etiology,clinical consequences,and therapeutic opportunities[J]. Neuropsychiatr Dis Treat,2015,11(22):97-106.
Change of glutam ate in the hippocam pus of neonatal rats after fetal intrauterine distress by blocking uterine blood supp ly
REN Jie1DAIXiaoyi2LILibiao3WU Fan3GUOChunyan3
1.Department of Cardiovascular Surgery,Affiliated Hospital of Inner Mongolia Medical University,Inner Mongolia Au-tonomous Region,Huhhot 010050,China;2.Department of Gynaecology and Obstetrics,Affiliated Hospital of Inner Mongolia Medical University,Inner Mongolia Autonomous Region,Huhhot 010050,China;3.Department of Anesthe-siology,Affiliated Hospital of Inner Mongolia Medical University,Inner Mongolia Autonomous Region,Huhhot 010050,China
Objective To observe the changes of glutamate in the hippocampus of neonatal rats after fetal intrauterine distress by blocking uterine blood supply.M ethods 72 pregnant ratswere random ly divided into 9 experimental groups (n=8,in each group).As the analysis of variance of factorial design set up two intervention factorswhich were the de-gree of blocking uterine blood supply(three levels:mild blocked,moderate blocked,completely blocked)and the dura-tion of blocking uterine blood supply(three levels:5,10,15 min).After the fetal intrauterine distressmodel estab-lished,cut open the uterus to remove the fetal rats.The hippocampuses of fetal rats were removed,and the content of glutamate of fetal hippocampuses were detected by high performance liquid chromatography.Resu lts Fetal intrauterine distress can significantly up-regulated the content of glutamate,which of themild blocked(5,10,15min)was(50.20依7.67),(54.67依7.52),(65.40依7.61)滋mol/gprot respectively;moderate blocked(5,10,15min)was(69.17依12.08),(90.53依18.95),(121.84依22.62)滋mol/gprot respectively;completely blocked(5,10,15 min)was(137.81依29.78),(170.93依18.77),(184.39依20.86)滋mol/gprot respectively.The changeswere correlated with the degree and duration of blocking uterine blood supply of the fetal intrauterine distress(F=46.699,110.803,84.633,P<0.01;F=84.633,16.562,8.240, P<0.01),and both influenced present additive effect(F=3.088,P<0.05).Conclusion This results indicate that the content of glutamate are up-regulated by fetal intrauterine distress in the hippocampus of fetal rats,and its increased with the duration and degree of blocking uterine blood supply.
Glutamate;Fetal intrauterine distress; High performance liquid chromatography;Hippocam-pus
R364.4
A
1673-7210(2016)07(a)-0022-04
院2016-04-01本文编辑院程铭)
内蒙古医科大学科技百万工程项目(YKD2015KJBW022)。
李利彪(1975.11-),男,内蒙古和林格尔人,医学博士,副主任医师;研究方向院麻醉与认知功能障碍。
