钙调神经磷酸酶基因多态性对环孢素A药效的影响Δ
2016-11-18海英民陈丁丁葛卫红朱怀军南京大学医学院附属鼓楼医院药学部南京0008中国药科大学基础医学与临床药学院南京0008
姚 婧,海英民,陈丁丁,葛卫红,朱怀军#(.南京大学医学院附属鼓楼医院药学部,南京 0008;.中国药科大学基础医学与临床药学院,南京 0008)
钙调神经磷酸酶基因多态性对环孢素A药效的影响Δ
姚婧1,2*,海英民2,陈丁丁2,葛卫红1,朱怀军1#(1.南京大学医学院附属鼓楼医院药学部,南京210008;2.中国药科大学基础医学与临床药学院,南京210008)
目的:研究钙调神经磷酸酶基因多态性对环孢素A(CsA)药效的影响。方法:收集服用CsA患者的血样,采用酶放大免疫法检测CsA谷浓度,以限制性片段长度多态性-聚合酶链反应(RFLP-PCR)方法检测PPP3CA和PPP3CB的基因型,以T细胞核因子(NFAT)下游基因白细胞介素(IL)2、γ干扰素(IFN-γ)和粒-巨噬细胞集落刺激因子(GM-CSF)的表达作为CsA间接药效指标,并采用实时定量PCR(RT-qPCR)法检测其表达,利用相关性分析和多因素回归等方法研究基因多态性与CsA药效的关系。结果:共收集CsA血液样本100份,CsA药效相关的NFAT下游基因GM-CSF的表达与CsA谷浓度无显著性相关(rGM-CSF=-0.04,P=0.238),IL-2和IFN-γ的表达与CsA谷浓度存在显著性负相关(rIL-2=-0.384 3,P<0.001;rIFN-γ=-0.335 4,P<0.001)。以IL-2和IFN-γ mRNA表达均数作为间接药效指标,发现PPP3CB rs3763679位点基因多态性对CsA药效有显著性影响(P<0.05),而未发现PPP3CA rs3804358对药效有明显影响(P>0.05)。分层分析结果显示,肾移植和免疫病患者中PPP3CB rs3763679基因变异(TC+TT)的患者药效优于野生型(CC)(P<0.05)。将药效以浓度标化后,多因素回归分析显示CsA浓度标化后的药效与患者性别、PPP3CB rs3763679、乳酸脱氢酶和肌酐呈显著性负相关,与PPP3CA rs3804358、白细胞计数、尿素氮和三酰甘油等呈显著性正相关。结论:PPP3CB rs3763679基因多态性对CsA药效有影响,在肾移植和免疫性疾病患者中,PPP3CB rs3763679TT+TC者药效优于CC者;同时,性别、PPP3CArs3804358、白细胞计数、乳酸脱氢酶、肌酐、尿素氮和三酰甘油等多种因素皆可不同程度影响标化后CsA药效,在给予CsA时也需同时考虑多方面的因素。
钙调神经磷酸酶;环孢素A;个体化给药;基因多态性
环孢素A(Cyclosporin A,CsA)是一种由11个氨基酸组成的天然亲脂性环状多肽,于1978年首次试用于心脏和肝脏移植,可大大提高移植患者的存活率,是临床常用的强效免疫抑制剂之一[1]。目前,CsA被广泛应用于各种器官和组织移植,同时还被用于治疗一些自身免疫性疾病、类风湿性疾病和血液系统疾病。
CsA作为钙调神经蛋白抑制剂的代表药物,其作用机制在于可选择性阻滞T细胞介导的免疫反应。CsA进入体内后与亲环蛋白A结合,抑制钙调神经磷酸酶(Calcineurin,CaN)的活性,从而抑制活化的T细胞核因子(Nuclear factor of activated T cells,NFAT)的去磷酸化,使其无法进入细胞核内,从而阻滞白细胞介素(Interleukin,IL)2、γ干扰素(Interferon,IFN-γ)和粒-巨噬细胞集落刺激因子(Granulocyte macrophage-colonystimulating factor,GM-CSF)等促炎症细胞因子基因的转录,最终导致T细胞的活化和增殖被抑制[2-3]。
由于CsA药动学参数个体差异很大,治疗窗窄,不良反应多且严重,故临床常采用CsA谷浓度来监测其药效,指导药物剂量的调整,以提高药物治疗的有效性和安全性[4]。但这种方式有其自身的局限性,血药浓度的改变与药效改变并非完全相关,存在很大的个体化差异[5-6]。因此,为完善个体化给药方法,提高用药安全性和有效性,深入探究CsA药效的影响因素显得十分重要和迫切。
从CsA的作用通路可以看出,CaN是CsA作用通路的重要环节。CaN是由催化亚基和调节亚基组成的异性二聚体,其编码基因为PPP3CA、PPP3CB、PPP3CC、PPP3R1和PPP3R2[7]。He ZH等[8]对CaN编码基因的55个多态性位点进行了研究,发现其中PPP3CArs3804358和PPP3CB rs3763679两个位点具有功能性作用,能直接影响CaN的表达。笔者推测,CaN编码基因的这两个功能性位点可能与CsA药效的差异存在相关性。
近年来,相关研究表明IL-2、IFN-γ和GM-CSF等NFAT下游基因的表达与CaN抑制剂的药效显著相关,可作为该药的药效指标[2,9-10]。基于此,本试验以NFAT下游基因IL-2、IFN-γ和GM-CSF的表达作为CsA的药效指标,研究PPP3CA rs3804358和PPP3CB rs3763679的基因多态性与CsA药效的关系,在分子水平探索CsA反应个体差异的可能机制,以期提高CsA的治疗效果,降低药品不良反应发生的风险,从而优化CsA个体化给药方案。
1 材料与方法
1.1材料
1.1.1仪器AB2720型聚合酶链式反应(PCR)仪、Rotor-Gene 3000型定量PCR仪(澳大利亚Corbett Research公司);VIVA-E型药物浓度分析仪(德国Siemems公司);Sub-Cell型水平电泳槽(美国Bio-Rad公司);GelX520型凝胶成像分析系统(中国Bioshine公司)。
1.1.2试剂DNA提取试剂盒(美国Promega公司,批号:0000074196);PCR扩增试剂盒[宝生物工程(大连)有限公司,批号:K9507MA];引物[宝生物工程(大连)有限公司,批号:AK2405];内切酶RsaⅠ(北京NEB有限公司,批号:0491212);内切酶DdeI(北京NEB有限公司,批号:1431306);逆转录试剂PrimeScriptTMRT Master Mix试剂盒[宝生物工程(大连)有限公司,批号:AK2402];qPCR扩增试剂SYBR®Premix Ex TaqTM试剂盒[宝生物工程(大连)有限公司,批号:K9507MA];1640培养基(上海立菲生物技术有限公司,批号:8113274);Trizol(上海立菲生物技术有限公司,批号:28218);血药浓度试剂盒(德国Siemems公司,批号:100711)。
1.2方法
1.2.1研究对象收集2013年7月-2014年6月服用CsA并于南京大学医学院附属鼓楼医院(以下简称“我院”)监测血药浓度的患者血样,诊断不限,性别不限。排除标准:骨髓移植患者、48 h内输血的患者、CsA同一剂量服用未满3 d即进行血药浓度监测的患者、当日送检血样超过抽血时间4 h的患者。经患者知情同意后,收集其血样(外周静脉血,肝素抗凝)约3~5 ml用于后续研究;同时,收集患者基本资料和临床检测数据。
1.2.2血样处理获取患者送检血样后,4 h内处理。取1 ml血样提取DNA后用于PPP3CA和PPP3CB基因型检测;另取1 ml血样用佛波酯(100 ng/ml)和离子霉素(5 μg/ml)37℃刺激3 h后,使用ACK红细胞裂解液裂解红细胞,使用Trizol法提取外周血单个核细胞(Peripheral blood lymphocytes,PBMC)总RNA,检测纯度和浓度后,逆转录为互补DNA(cDNA),于-20℃储存;另取100 μl血样用于CsA全血谷浓度检测。用于基因型检测的血样冻存于-20℃,RNA提取立即进行,血药浓度检测于当日进行。
1.2.3CsA血药谷浓度检测采用酶放大免疫(EMIT)法检测CsA谷浓度,使用VIVA-E型药物浓度分析仪,按照血药浓度试剂盒说明书操作。取受试者全血100 μl,加入前处理液300 μl,涡旋40 s,以转速14 000 r/min、离心半径13.5 cm离心10 min,取上清液检测。
1.2.4基因型检测采用限制性段长度多态性-聚合酶链反应(RFLP-PCR)法。取1 ml血样提取DNA后,进行PCR扩增反应,PPP3CA rs3804358和PPP3CB rs3763679及其引物序列见表1。PCR产物置-20℃保存,并使用电泳分析检测PCR扩增产物,扩增产物应均有1条清晰条带且阴性对照无条带。PPP3CA rs3804358扩增产物为296 bp,PPP3CB rs3763679扩增产物为370 bp。使用DdeⅠ和RsaⅠ限制性内切酶酶切,酶切产物用琼脂糖凝胶电泳分析,并以此作基因分型。凝胶电泳基同型分析结果见表2。

表1 基因及其引物序列Tab 1 Gene and primer sequence

表2 凝胶电泳基因型分析结果Tab 2 Results of gel electrophoresis genotype analysis
1.2.5CsA药效相关基因表达的检测取20μl cDNA,采用实时定量PCR(RT-qPCR)法测定IL-2、IFN-γ和GM-CSF等NFAT下游基因的表达。条件为:95℃预变性30 s,40个循环包含95℃变性5 s和60℃退火30 s,最后进行溶解曲线分析。扩增后根据扩增曲线获取Cp(Crossing point,指PCR过程中,其反应液荧光信号增至超过其本底荧光所需要的循环数)值。以β-actin为内参。所用引物见表1。
1.3统计学方法
2 结果
2.1患者基本资料
纳入本研究的患者100例,其中男性60例,女性40例;年龄(41.24±14.9)岁;诊断包括血液疾病46例,肾移植35例,免疫性疾病15例,其他疾病4例;CsA平均谷浓度为(142.51±72.9)ng/ml,中位数为116.9 ng/ml,四分位间距为42.5~325.4 ng/ml。患者基本资料见表3。
表3 患者基本资料(±s)Tab 3 The basic information of patients(±s)

表3 患者基本资料(±s)Tab 3 The basic information of patients(±s)
44.0±34.9 39.2±19.7 220.3±90.5 16.6±1.1 74.5±2.1 43.8±4.0 5.0±1.1 4.9±3.8 7.5±48.1 1.88±0.63项目n性别(男/女),例年龄,岁CsA谷浓度,ng/ml血常规白细胞计数,×109L-1淋巴细胞计数,×109L-1实验室检查指标丙氨酸转氨酶,U/L天冬氨酸转氨酶,U/L乳酸脱氢酶,U/L总胆红素,μmol/L总蛋白,g/L白蛋白,g/L葡萄糖,mmol/L尿素氮,mmol/L肌酐,μmol/L三酰甘油,mmol/L血液疾病46 27/19 35.0±14.6 180.9±80.3肾移植35 27/8 44.5±11.5 99.4±31.6免疫性疾病15 3/12 44.2±14.0 131.89±59.00其他4 3/1 61.5±14.4 116.7±71.2 3.28±2.10 1.26±0.95 7.33±2.29 1.80±0.70 7.36±3.60 1.80±0.90 5.7±1.91 1.73±0.50 35.86±29.40 23.7±14.7 225.2±88.6 15.7±8.1 65.9±7.2 40.3±5.0 5.4±1.0 6.5±3.0 68.0±34.8 2.08±1.35 41.8±71.1 24.2±15.1 198.5±52.8 17.1±7.7 69.1±6.4 44.3±3.8 5.0±0.5 7.2±2.4 99.8±32.8 1.56±0.80 77.7±129.0 37.5±45.5 224.5±113.6 12.9±7.5 64.4±7.0 39.6±5.5 5.2±1.5 6.5±2.6 56.5±35.4 2.15±0.52
2.2CaN基因型
根据酶切产物进行基因分型。两个基因在本研究方法条件下扩增,所得PCR产物经2%琼脂糖凝胶电泳分析,并与DNA Marker对照后,得PPP3CA和PPP3CB基因的分型结果,详见表4。
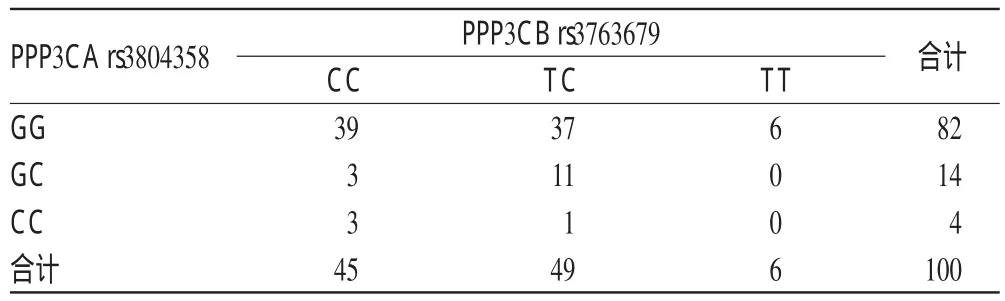
表4 PPP3CA和PPP3CB基因的分型结果Tab 4 Genotyping of PPP3CA and PPP3CB
2.3CsA药效相关基因表达与血药浓度的相关性
本研究主要检测了CsA药效相关的NFAT下游基因mRNA的表达,包括IL-2、IFN-γ和GM-CSF。每批次qPCR均带校正样本,用以校正批次之间的误差,所有批次结果最终以qBASE 1.0.1处理,得IL-2 mRNA相对表达量为(-6.26± 4.2),IFN-γ的相对表达量为(-2.6±3.3),GM-CSF相对表达量为(-6.81±3.54)。NFAT下游基因mRNA相对表达量与CsA谷浓度的关系散点图见图1。
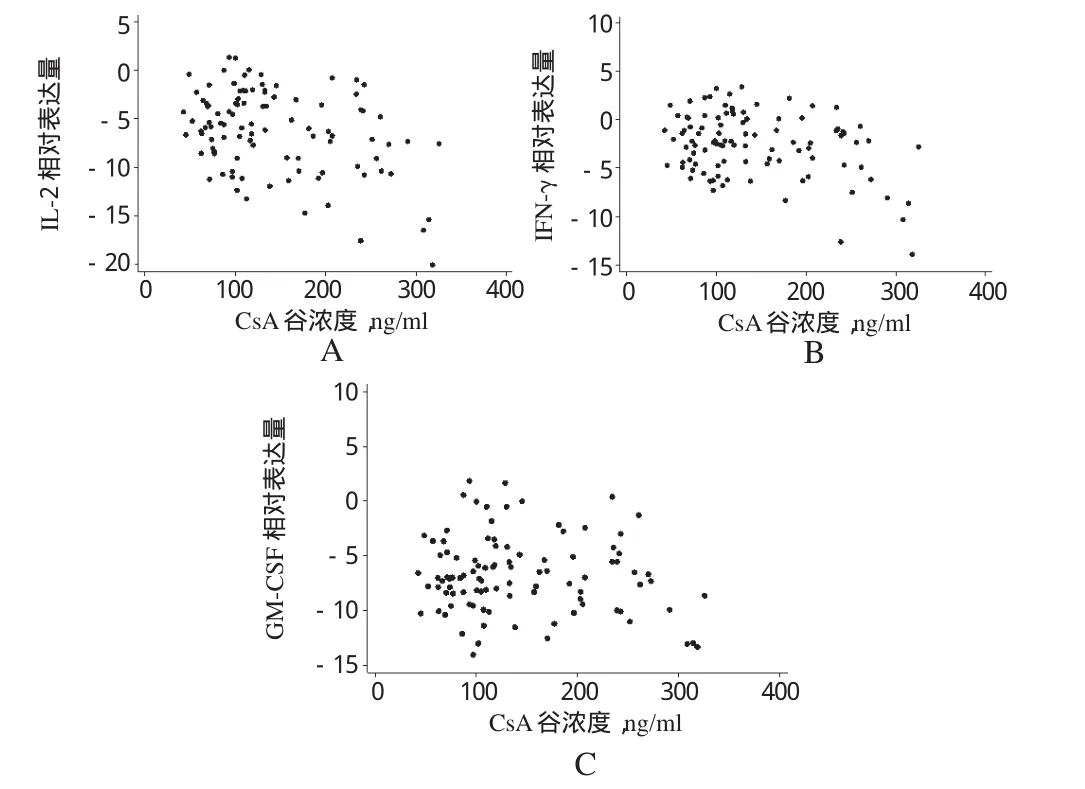
图1 NFAT下游基因mRNA相对表达量与CsA谷浓度的关系散点图A.IL-2;B.IFN-γ;C.GM-CSFFig 1 The scatter plot of relative mRNA expression of NFAT-regulated genes with trough concentration of CsAA.IL-2;B.IFN-γ;C.GM-CSF
分别以IL-2、IFN-γ和GM-CSF 3种基因表达为因变量,CsA谷浓度为自变量,进行单因素相关分析。结果发现,IL-2和IFN-γ的表达与CsA谷浓度存在显著性负相关(rIL-2=-0.384 3,P<0.001;rIFN-γ=-0.335 4,P<0.001),而GM-CSF表达与CsA谷浓度无线性相关(rGM-CSF=-0.04,P=0.238)。可见,CsA谷浓度与药效的相关性存在个体差异。
2.4CaN基因多态性与CsA药效的关系
为评估影响CsA药效的基因型,以IL-2和IFN-γ两个基因mRNA的相对表达均数作为间接药效指标,定义CsA药效E(%)=(mRNA相对表达均数最大值-mRNA相对表达均数)/ mRNA相对表达均数极差×100%。
使用Skewness/Kurtosis tests检验E符合正态分布,故采用t检验比较PPP3CA rs3804358和PPP3CB rs3763679两个位点基因型对药效的影响,由于PPP3CA rs3804358 CC及PPP3CB rs3763679 TT基因型例数较少,合并至杂合子分析,结果如图2、图3所示。

图2 CaN基因多态性与CsA药效的关系箱图A.PPP3CArs3804358基因型;B.PPP3CB rs3763679基因型Fig 2 Boxplots of the relationship between CaN mononucleotide gene polymorphism and the efficacy of CsAA.PPP3CArs3804358genotype;B.PPP3CB rs3763679genotype
从图2可以看出,PPP3CA rs3804358位点基因多态性对CsA的药效无影响(P>0.05),而PPP3CB rs3763679位点的基因多态性对CsA药效有显著性的影响(P<0.05),突变型(TC+ TT)患者服用CsA药效优于野生型(CC)患者。以患者疾病类型进行分层分析,如图3所示,PPP3CB rs3763679位点的基因多态性对血液疾病患者无显著影响(P>0.05),而在肾移植和免疫性疾病患者中有显著性影响,突变型(TC+TT型)皆优于野生型(CC型)患者(P<0.05)。

图3 PPP3CB rs3763679位点基因多态性对不同疾病CsA药效的影响A.血液疾病;B.肾移植;C.免疫性疾病Fig 3 The effect of PPP3CB rs3763679 gene polymorphism on CsA efficacy in different diseasesA.hematology;B.renal transplant;C.immunopathy
2.5CsA浓度标化后药效的相关影响因素的多因素分析
为更好地衡量CsA的药效,将“2.4”项下计算的药效以谷浓度进行标化(E/C),分析CsA浓度标化后药效的影响因素。采用多因素回归分析,以E/C为因变量,患者的年龄、性别(男:0,女:1)、基因型(野生型:1,突变型:2)、白细胞计数、淋巴细胞计数、转氨酶、总蛋白、白蛋白、尿素氮、肌酐和三酰甘油等作为自变量,通过逐步法筛选影响药效指标的因素。结果显示,上述因素皆可以不同程度影响浓度标化后的CsA药效,结果见表5。由表5可见,CsA浓度标化后药效与患者性别、PPP3CB rs3763679突变型(TC+TT)、乳酸脱氢酶和肌酐呈显著性负相关,与PPP3CA rs3804358突变型(GC+CC)、白细胞计数、尿素氮和三酰甘油呈显著性正相关。

表5 CsA浓度标化后药效的影响因素Tab 5 Influential factors of CsA efficacy after normalized by CsA trough concentration
3 讨论
本研究以CsA药效通路中的CaN为研究对象,以NFAT下游基因的表达作为药效指标,分析CaN编码基因PPP3CA和PPP3CB的多态性对CsA药效的影响,从而为CsA临床应用的效果和安全性提供理论依据和指导作用。
本研究共收集CsA血样100份,患者诊断包含血液疾病、肾移植和免疫性疾病等。在数据处理中发现,虽然IL-2、IFN-γ与CsA谷浓度存在显著相关,但个体之间的表达存在差异,可能是不同个体药效基因的差异所导致,CsA的药效很容易受机体各种因素的影响[11-12]。从比较的结果看,未发现PPP3CA rs3804358多态性对CsA药效的影响,笔者考虑这可能是由于该位点突变率较低的缘故。而肾移植和免疫性疾病PPP3CB rs3763679 TT+TC基因型患者CsA药效高于CC基因型患者,提示此类患者PPP3CB rs3763679基因型为CC时,需考虑更高的CsA剂量。
为探寻CsA药效的其他影响因素,笔者使用谷浓度将药效进行标化,从而排除浓度对药效的影响,并使用多因素回归模型进行分析。结果发现,除了PPP3CB rs3763679多态性对药效有显著影响(P<0.05),患者的性别也会对CsA的标化后药效产生影响(P<0.05)。有研究发现男女激素分泌、药物代谢等各方面差异皆可对CaN抑制剂的治疗结果产生差异[13-14]。Tornatore KM等[15]研究发现。由于CsA清除率和ABCB1基因表达的不同,男性和女性患者使用CsA后会有不同的转运速率和胞内浓度。动物实验显示,雌性动物需要较高的CsA剂量来抑制肾移植后排斥反应的发生[16]。还有可能在CsA药效通路中,存在着尚未发现的男女性基因上的差异等其他原因,有待于进一步研究。
多因素回归结果表明,除了CaN基因多态性和性别可影响CsA浓度标化后的药效外,患者白细胞计数、乳酸脱氢酶、尿素氮、肌酐和三酰甘油等各种因素都会对CsA浓度标化后的药效产生影响。这提示,CsA的药效会受到多种因素的影响,在给予患者CsA时也需综合考虑多方面的指标。
除此之外,个体间仍然存在很多未知的、可影响药效的个体因素。本研究尚存在样本量小、未考量患者服药后临床表现等不足之处。在后续研究阶段,有待扩大样本量的进一步考察。
[1]Robertsen I,Falck P,Andreassen AK,et al.Endomyocardial,intralymphocyte,and whole blood concentrations of ciclosporin A in heart transplant recipients[J]. Transplant Res,2013,2(1):5.
[2]Steinebrunner N,Sandig C,Sommerer C,et al.Pharmacodynamic monitoring of nuclear factor of activated T cell-regulated gene expression in liver allograft recipients on immunosuppressive therapy with calcineurin inhibitors in the course of time and correlation with acute rejection episodes:a prospective study[J].Ann Transplant,2014,19(1):32.
[3]Sommerer C,Meuer S,Zeier M,et al.Calcineurin inhibitors and NFAT-regulated gene expression[J].Clin Chim Acta,2012,413(17/18):1379.
[4]Barnard JB,Thekkudan J,Richardson S,et al.Cyclosporine profiling with c2and c0monitoring improves outcomes after heart transplantation[J].J Heart Lung Transplant,2006,25(5):564.
[5]Sommerer C,Giese T,Meuer S,et al.Pharmacodynamic monitoring of calcineurin inhibitor therapy:is there a clinical benefit?[J].Nephrol Dial Transplant,2009,24(1):21.
[6]Zhu HJ,Ge WH.Future of the pharmacogenomics of calcineurin inhibitors in renal transplant patients[J].Pharmacogenomics,2011,12(11):1505.
[7]He ZH,Hu Y,Li YC,et al.Polymorphisms in the calcineurin genes are associated with the training responsiveness of cardiac phenotypes in Chinese young adults[J].Eur J Appl Physiol,2010,110(4):761.
[8]He ZH,Hu Y,Li YC,et al.Are calcineurin genes associated with athletic status?A function,replication study[J]. Med Sci Sports Exerc,2011,43(8):1433.
[9]Billing H,Giese T,Sommerer C,et al.Pharmacodynamic monitoring of cyclosporine A by NFAT-regulated gene expression and the relationship with infectious complica-tions in pediatric renal transplant recipients[J].Pediatric Transplant,2010,14(7):844.
[10]Sommerer C,Giese T,Schmidt J,et al.Ciclosporin A tapering monitored by NFAT-regulated gene expression:a new concept of individual immunosuppression[J].Transplantation,2008,85(1):15.
[11]Zhu HJ,Yuan SH,Fang Y,et al.The effect of CYP3A5 polymorphism on dose-adjusted cyclosporine concentration in renal transplant recipients:a meta-analysis[J]. Pharmacogenomics J,2011,11(3):237.
[12]Forsythe P,Paterson S.Ciclosporin 10 years on:indications and efficacy[J].Vet Rec,2014,174(2):S13.
[13]Velickovic-Radovanovic R,Mikov M,Catic-Djordjevic A,et al.Gender-dependent predictable pharmacokinetic method for tacrolimus exposure monitoring in kidney transplant patients[J].Eur J Drug Metab Pharmacokinet,2015,40(1):95.
[14]Cvetkovic TP,Stefanovic NZ,Velickovic-Radovanovic RM,et al.Gender differences in oxidative and nitrosative stress parameters in kidney transplant patients on tacrolimus-based immunosuppression[J].Int Urol Nephrol,2014,46(6):1217.
[15]Tornatore KM,Brazeau D,Dole K,et al.Sex differences in cyclosporine pharmacokinetics and ABCB1 gene expression in mononuclear blood cells in African American and Caucasian renal transplant recipients[J].J Clin Pharmacol,2013,53(10):1039.
[16]Muller V,Szabo AJ,Erdely A,et al.Sex differences in response to cyclosporine immunosuppression in experimental kidney transplantation[J].Clin Exp Pharmacol Physiol,2008,35(5/6):574.
(编辑:李劲)
Influence of Calcineurin Gene Polymorphisms on the Efficacy of Cyclosporine A
YAO Jing1,2,HAI Yingmin2,CHEN Dingding2,GE Weihong1,ZHU Huaijun1(1.Dept.of Pharmacy,the Affiliated Drum Tower Hospital of Nanjing University Medical School,Nanjing 210008,China;2.School of Basic Medicine and Clinical Pharmacy,China Pharmaceutical University,Nanjing 210008,China)
OBJECTIVE:To study the influence of calcineurin gene polymorphism on the efficacy of cyclosporine A(CsA). METHODS:The blood samples of patients treated with CsA were collected.The trough blood concentration of CsA was detected by EMIT.The genotype of PPP3CA and PPP3CB was assayed by RFLP-PCR method.The expression of NFAT-regulated gene IL-2,IFN-γ and GM-CSF were measured by RT-qPCR,which were used to define the index of indirect efficacy of CsA.The relationship of gene polymorphism with CsA efficacy was study by relationship analysis and multiple factor regression method,etc.RESULTS:A total of 100 blood samples were collected.There was no significant correlation between the expression of CsA efficacy-related NFAT-regulated gene GM-CSF and trough concentration of CsA(rGM-CSF=-0.04,P=0.238);the expression of IL-2 and IFN-γ were negatively correlated with trough concentration of CsA significantly(rIL-2=-0.384 3,P<0.001;rIFN-γ=-0.335 4,P<0.001).Using the average value of mRNA expression of IL-2 and IFN-γ as indirect efficacy index,the polymorphism of PPP3CB rs3763679 site significantly influenced the efficacy of CsA(P<0.05),but PPP3CA rs3804358 had no any effect on it(P>0.05).Stratified analysis showed that among patients with immune disease underwent renal transplantation,efficacy of patients with PPP3CB rs3763679 genovariation(TC+ TT)were better than those with wild-type gene(CC)(P<0.05).After the efficacy was normalized by CsA trough concentration,multivariate analysis showed that normalized efficacy of CsA was negatively correlated with gender,PPP3CB rs3763679,lactate dehydrogenase and creatinine significantly,but positively correlated with PPP3CA rs3804358,leucocyte count,usea nitrogen,glycerin trilaurate,etc.CONCLUSIONS:PPP3CB rs3763679 gene polymorphism influence the efficacy of CsA;among patients with immune disease underwent renal transplantation,efficacy of patients with PPP3CB rs3763679 TT+TC is better than that of CC type.At the same time,gender,PPP3CA rs3804358,leucocyte count,usea nitrogen,glycerin trilaurate and other factors all can influence the normalized efficacy of CsA to different extent.Multiple factors should be considered when using CsA.
Calcineurin;CyclosporinA;Individual administration;Gene polymorphism
R969.1;R979.5
A
1001-0408(2016)29-4033-05
10.6039/j.issn.1001-0408.2016.29.01
南京市科技发展指导性计划药学项目(No.2013 YX001);江苏省“六大人才高峰”资助项目(No.2011-WS-009)
*硕士研究生。研究方向:临床药学。电话:025-83105670。E-mail:yyaojing@yeah.net
主管药师。研究方向:临床药学。电话:025-83105670。E-mail:sesisi@163.com。
(2015-11-13
2015-12-05)
