西门子BNⅡ全自动蛋白分析仪性能验证报告
2016-11-15于淼琛
于淼琛,朱 鸿,王 凤
(大连医科大学附属第一医院检验科,辽宁大连116011)
西门子BNⅡ全自动蛋白分析仪性能验证报告
于淼琛,朱 鸿,王 凤
(大连医科大学附属第一医院检验科,辽宁大连116011)
目的对西门子BNⅡ全自动蛋白分析仪主要分析性能进行验证。方法根据实验室认可准则和美国CLIA'88性能验证文件,对西门子BNⅡ全自动蛋白分析仪上开展的8个常规项目进行精密度、正确度、临床可报告范围和生物参考区间验证。结果西门子BNⅡ全自动蛋白分析仪精密度、正确度、线性范围、临床可报告范围和生物参考区间验证等均符合要求。结论西门子BNⅡ全自动蛋白分析仪检测性能完全满足预期的临床应用要求。
CLIA'88;性能验证;BNⅡ全自动蛋白分析仪
ISO15189 CNAS-CL02:2012《医学实验室质量和能力认可准则》[1]中对免疫领域的要求中,检验方法和程序的分析性能验证内容至少应包括正确度、精密度和可报告范围。根据认可要求,本实验对使用的西门子BNⅡ全自动蛋白分析仪进行精密度、正确度、临床可报告范围和参考范围验证[1,2]。
1 材料与方法
1.1 标本来源标本来源于大连医科大学附属第一医院住院、门、急诊、体检合格的健康人标本,且无溶血、乳糜。
1.2 仪器与试剂西门子BNⅡ全自动蛋白分析仪(简称BNⅡ)及原装配套试剂、校准品、质控品。
1.3 方法
1.3.1 精密度验证选取二个水平的质控血浆,连续检测5d,每天测定四次,得到20个数据连续重复测定20次,计算批内精密度,计算批间精密度,批内精密度≤1/4允许总误差(TEa),批间精密度≤1/3允许总误差(TEa)。
1.3.2 正确度验证目前常用的正确度验证方法为统计实验室参加室间质评活动的成绩,比较回报靶值和实验室检测结果,计算偏差及偏倚,绝对值后统计平均值,平均偏倚≤1/2允许总误差(TEa)。
1.3.3 临床可报告范围选择低浓度(L)和高浓度(H)患者标本各1份,浓度覆盖仪器说明。H和L按等比关系配制形成系列浓度血清(如:5L,4L+1H,3L+2H,2L+3H,1L+4H,5H)。每个实验样品在检测系统上重复测定2次,记录结果。将实测值与预期值作比较。样品应含有的待测物的预期值为(X),所有样品重复测定的均值为实测值(Y),将所有结果点在X-Y坐标图上,计算回归方程:Y=aX+b[3]。要求:a值在1±0.05范围内,相关系数r≥0.975或r2≥0.95。
1.3.4 生物参考区间验证参考CLSI C28-A2文件,选择20份体检合格的健康人标本(男、女各10例),在检测系统上进行测定,对结果进行统计并对参考区间进行验证,若20份标本的检测结果均在使用的参考区间内或仅有1个标本超出,则验证通过。若又有2个以上观察值超过验证参考区间,应重新检查分析程序,考虑两个样本总体生物学特征上可能存在差异,需要实验室自行建立参考区间。
2 结果
2.1 精密度验证IgG、IgA、IgM、C3、C4、ASO、RF、CRP的检测批内精密度和批间精密度结果均合格,见表1。
2.2 正确度验证本次实验采用2015年本实验室参加国家卫计委组织的正确度验证计划,成绩合格,可利用卫计委全国室间质评的靶值与本科室的实测值进行比较,计算该项目在医学决定水平时与靶值的相对偏倚,以<1/2EQA对应浓度水平允许误差为评价标准,见表2。
2.3 临床可报告范围IgG136.5~4585mg/dl、I-gA27.7~811mg/dl、IgM18.1~652.5mg/dl、C3230~3179.5mg/L、C459.6~1752.5mg/L、ASO51.6~1587.5 IU/ml、RF12.5~645IU/ml、CRP3.4~200.5mg/L。8项回归方程a值均在1±0.05范围内,相关系数r≥0.975,见表3。
2.4 生物参考区间验证IgG700~1600mg/dl、IgA70~400mg/dl、IgM40~230mg/dl、C900~1800mg/L、C100~400mg/L、ASO<200IU/ml、RF<20IU/ml、CRP<8mg/ L。生物参考区间验证均合格,见表4。
3 讨论
为确保临床实验室检验结果的准确可靠,本文依据CL1A'88[4]、EP15-A2[5]、EP9-A2[6]、EP6-A2[7]等对BNⅡ全自动蛋白分析仪进行精密度、正确度、可报告范围、参考区间进行验证。ISO15189 CNAS-CL02:2012《医学实验室质量和能力认可准则》中规定,对开展某一新的检测项目,更换检测系统或仪器或改变检测试剂盒产商时,实验室需对其相关方法学分析性能予以验证,对产商提供的评价资料中的主要性能予以确认,每年并定期对仪器进行性能验证。

表1 精密度验证结果
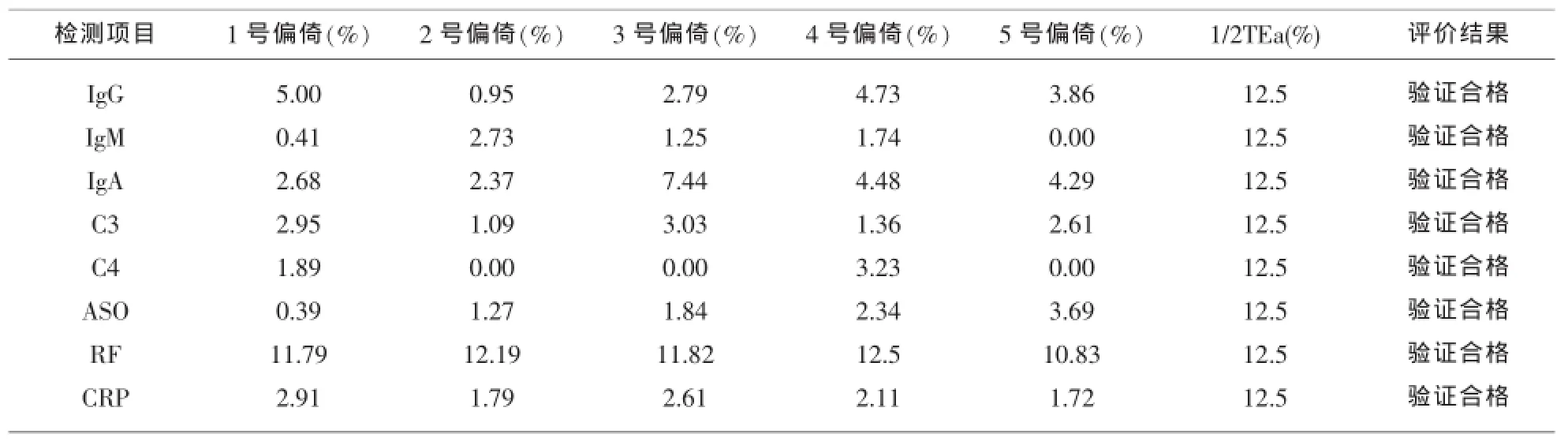
表2 正确度验证结果

表3 线性范围证结果

表4 生物参考区间验证
检测系统的良好分析性能是保证检验结果准确性的前提,而检测系统或方法的性能验证,是评价检测系统能否用于常规工作的前提[8,9]。精密度即多次重复检测结果的一致性,包括批内和批间精密度[10]。8项免疫指标两个水平质控批内精密度<1/4Tea,批间精密度<1/3Tea,表明本仪器检测结果重复性良好[11]。正确度验证偏倚均小于1/ 2Tea,表明该仪器检测结果准确。线性范围是一种能力,在一定测量区间,可提供测量结果与样本中测量物的量值直接成比例,在此范围内,报告结果显示标本中确实含有被检测物的含量线性范围验证[12]。8项回归方程a值均在1±0.05范围内,相关系数r≥0.975,表明本仪器线性范围良好[13]。生物参考区间验证均合格,厂商或提供参考区间的实验室报告的95%参考区间可以接受,表明可以引用此参考范围。
本次BNⅡ全自动蛋白分析仪精密度验证使用了EP15方案,它比EP5精密度方案、EP9A正确度方案相对简单、易于实验室操作且能够满足统计学意义[14]。综上所述,BNⅡ全自动蛋白分析仪是一部具有良好精密度、准确度、可报告范围宽的检测系统[15],每年定期对该体系进行性能验证,保证检测结果可靠、准确。
[1]中国合格评定国家认可委员会.CNAS-C02医学实验室质量和能力认可准则.(ISO15189:02)[S].北京:中国标准出版社,2012.
[2]医学实验室质量和能力的专用要求:GB/T 22576 2008[S].2008.
[3]NCCLS.EP6-P-2002 Evalution of the linearity of quantitative analytical methods[S].2002.
[4]Federal Register.CL1A'88 Rules and regulation[S].1992:57-40.
[5]Clinical and Laboratory Standards Institute.EP15-A2.Evaluation of precision performance of quantitative measurement methods[S]. Wayne,PA,USA:CLSI,2000.
[6]National Committee for Clinieal Laboratory Standards.EP9-A2 Method Comparison and BiasEstimation Using patient Samples[S]. Wayne,PA:NCCLS,2002.
[7]Clinical and Laboratory Standards Institute.Evaluation of the lin-earity of quantitative measurement procedures:CLSI EP6-A2[S]. 2003.
[8]吴宗勇,贾德强,李佳,等.自动生化分析仪的能力验证[J].临床和实验医学杂志,2011,10(7):524-525.
[9]ISO 15189.医学实验室质量和能力认可准则[S].2007.
[10]徐江霞,龚淑琪,万振华,等.新型乙肝定量PCR试剂检测性能验证[J].实验与检验医学,2016,34(2):149-151.
[11]王治国.临床检验质量控制技术[M].第2版.北京:人民卫生出版,2010:41-46.
[12]李婷婷,宁芬,陆雅春,等.日立7600全自动生化分析仪检测系统性能验证[J].安徽医学,2013,34(11):1679-1682.
[13]寿爽,徐胜,吕洁,等.迈瑞BC-6900全自动血细胞分析仪血液模式的性能验证和评价[J].实验与检验医学,2015,33(3):310-316.
[14]韩静,胡梅,杨桂花,等.BNⅡ特种蛋白仪测定IgG、IgA和IgM性能评价[J].国际检验医学杂志,2013,34(10):1292-1294.
[15]陈丽娟,罗俐莺,魏权,等.尿液有形成分全自动分析仪(UF-1000i)性能评价[J].实验与检验医学,2015,33(4):435-475.
Performance verification of Siemens BNⅡautomatic protein analyzer
YU Miaochen,ZHU Hong,WANG Feng.
Clinical Labo-ratory,the First Affiliated Hospital of Dalian Medical University,Dalian Liaoning 116011,China.
Objective To verify the performance of Siemens BNⅡautomatic protein analyzer.Methods According to laboratory accreditation criteria and performance verification documents of American CLIA'88,the precision,accuracy,clinical reportable range and biological reference interval were verified for the tests of 8 conventional biochemical indicators performed on Siemens BNⅡautomatic protein analyzer.Results The precision,accuracy,liner range,clinical reportable range and biological reference interval were all acceptable.Conclusion Siemens BNⅡautomatic protein analyzer could fully meet the requirements in clinical application.
CLIA'88;performance verification BNⅡautomatic protein analyzer
R446.62
A
1674-1129(2016)05-0595-03
10.3969/j.issn.1674-1129.2016.05.018
2016-06-02;
2016-08-25)
于淼琛,女,1982年12月出生,学位硕士,主管技师。主要从事临床免疫学检测的研究。E-mail:ymc7788999@163.com
王凤,女,1981年9月出生,学位硕士,主管技师。主要从事临床血液学检测的研究。E-mail:wangfeng5006@163.com
