含磷活性炭作为双电层电容器电极材料的电化学性能
2016-11-08王永芳左宋林
王永芳 左宋林
(南京林业大学化学工程学院,江苏省生物质绿色燃料与化学品重点实验室,南京 210037)
含磷活性炭作为双电层电容器电极材料的电化学性能
王永芳左宋林*
(南京林业大学化学工程学院,江苏省生物质绿色燃料与化学品重点实验室,南京 210037)
采用磷酸活化和磷酸改性制备了不同种类的含磷活性炭,采用元素分析、X射线光电子能谱(XPS)和氮气吸附等手段分析了活性炭的元素含量、表面化学性质和孔隙结构,采用恒电流充放电、循环伏安和交流阻抗分别考察了活性炭在KOH和H2SO4电解质溶液中作为超级电容器电极材料的电化学性能,采用自由截距多元线性回归拟合统计分析研究了活性炭电极比电容量的影响因素,应用三电极体系分析了磷元素对活性炭电化学性能的影响机理。研究结果表明,活性炭掺杂的磷引入了赝电容,提高了活性炭电极的比电容量,磷元素含量为5.88%(w)的活性炭的比电容量在0.1 A∙g-1下达到185 F∙g-1。统计分析结果显示,活性炭的中孔有利于电解质离子向微孔内的扩散。在6 mol∙L-1KOH电解质溶液中,孔径在1.10-1.61 nm、2.12-2.43 nm及3.94-4.37 nm范围内是电解质离子在活性炭孔隙内部形成双电层的主要场所;在1 mol∙L-1H2SO4电解质溶液中,孔径在0.67-0.72 nm范围内有利于双电层电容的形成。
活性炭;含磷基团;孔隙结构;赝电容;超级电容器
doi:10.3866/PKU.WHXB201511041
1 引言
超级电容器作为一种新型的电能储存设备,其性能介于电池与传统静电电容器之间,具有比电池更大的功率密度和比传统静电电容器更高的能量密度,被广泛应用于电动汽车及通讯装置中1。活性炭作为超级电容器电极材料,具有比表面积大、导电性能优良、抗化学腐蚀性能好、廉价易得、易于实现工业化生产等优点,是目前超级电容器电极材料的研究热点。
研究影响活性炭电极电容器性能的相关报道很多,但这些研究报道多数是采用氢氧化钾活化法或水蒸气活化法制备的活性炭2-4,这些活性炭的表面官能团含量较低,且通过同一种活化方法制备的活性炭其电极阻抗差异很小,因此仅研究了活性炭的比表面积及孔径分布或孔径大小对活性炭电极的比电容量的影响。由于通过不同活化方法或不同原料制备的活性炭,其物理性质及表面化学性质存在明显差异,这些差异对活性炭作为超级电容器电极材料都有很大的影响,比如活性炭电极的电化学阻抗会存在明显的区别3。
活性炭的表面化学性质取决于其表面的杂原子(氮、磷、硫、硼等)。其中,含氮、硫、硼官能团对活性炭电极电容性能的影响已有不少研究报道5-7。而有关含磷官能团对活性炭电极电容性能的影响报道甚少8-11。Puziy等9首次报道了磷酸法活性炭的比电容量在1 A∙g-1的电流密度下达到220 F∙g-1,明显高于商业微孔活性炭Norit(140 F∙g-1),但其所研究的活性炭的孔径分布范围较窄,微孔所占比例较大,因此未能体现出活性炭孔径分布对其比电容量的影响。而后,该小组在400-1000°C范围内通过磷酸活化法制备含磷活性炭研究其电容器性10。其所制备的活性炭的孔径分布范围基本一致,结果仅表明了不同电位窗下的拟合方差结果,并未对影响活性炭电极的比电容量因素进行具体分析。另外,以往含磷活性炭作为超级电容器电极材料是在1 mol∙L-1H2SO4电解质溶液中研究其电化学性能8-11,在KOH碱性条件下未有过相关报道。
为研究活性炭表面含磷基团对活性炭电极电化学性能的影响,本文采用商业磷酸法活性炭的高温热处理、木质纤维原料的高温磷酸活化与椰壳活性炭(水蒸气活化)的磷酸高温改性三种方法制备含磷活性炭,并分别在6 mol∙L-1KOH和1 mol∙L-1H2SO4电解质溶液中,研究了活性炭表面化学性质、孔隙结构及电阻对其电化学性能的影响。
2 实验部分
2.1活性炭的制备
商业磷酸法活性炭由福建元力活性炭股份有限公司提供;商业椰壳基活性炭由南京林昌炭业科技有限公司提供;其它化学试剂均为分析纯,购于南京化学试剂有限公司。
称取干燥后的420-2000 μm的杉木屑10.0 g,按照磷酸与木屑的浸渍比为1.75混合浸渍磷酸溶液和木屑,然后在通氮气条件下在管式炉中进行活化,活化温度分别为600、700、800和900°C,在最终温度下活化2 h,冷却至室温后取出,并用去离子水洗至近中性,经干燥、研磨制得活性炭样品。所制备的活性炭命名为ACP-X,其中X代表活化温度。
在氮气保护下,将商业磷酸法活性炭(ACP)加热至800°C热处理2 h,然后冷却取出,所得到的样品命名为HACP-800。
取10.0 g商业椰壳基活性炭(CS)与20%(w)的磷酸溶液50 mL混合,室温下磁力搅拌2 h,在120°C下干燥5 h后放置于卧式管式炉中,然后通人氮气保护在800°C下热处理2 h,冷却后用去离子水洗至近中性,干燥制得,所得到的样品命名为CS-800。
2.2活性炭孔隙结构和表面化学性质的分析
活性炭的C、H、N、S和O含量采用VARIO EL cube元素分析仪(德国Elementar公司)进行分析,P含量采用电感耦合等离子体发射光谱仪(ICPAES,OPTIMA-7000,美国PE公司)进行分析。X射线光电子能谱(XPS)分析采用英国岛津/克雷托斯(Kratos)公司生产的AXIS UItra DLD X射线光电子能谱仪,使用Al靶Kα为X射线源。
采用型号为Autosorb-iQ2(美国Quantachrome公司)的吸附仪测定活性炭的氮气吸附等温线。测试前,活性炭样品在250°C下脱气12 h。根据氮气吸附等温线,采用Brunauer-Emmet Teller (BET)方程计算活性炭的比表面积(SBET),由相对压力为0.99处的氮气吸附量计算总孔容(Vtot),采用Dubinin-Radushkevic方程计算微孔孔容(Vmic),中孔孔容(Vmes)由总孔容减去微孔孔容得到,孔径分布通过quenched solid density functional theory (QSDFT)方程计算12,并通过QSDFT方程计算一定孔径范围内的比表面积。
2.3双电层电容器的组装与性能研究
称取一定量活性炭样品粉末,用乙醇润湿后,根据活性炭、乙炔黑和聚四氟乙烯乳液按质量比例8:1:1均匀混合,将粘稠状的浆料压成厚度为((200±50)μm)的薄片,截取直径为1.1 cm的圆形电极片,在5 MPa压力下,压到相同直径的泡沫镍集流体上,制成电极片,120°C烘干至恒重,将压制后的电极片和聚丙烯薄膜(日本NKK公司,MPF30AC100)加入6 mol∙L-1KOH电解质溶液后抽真空4 h,然后组装成双电层电容器。为了对比,以1 mol∙L-1H2SO4为电解质溶液,采用同样方法,制备了双电层电容器。采用美国Arbin公司生产的高精度电池单体测试系统(BT-G-5V-5A-4)对电容器进行恒电流充放电测试,并根据恒电流充放电曲线计算电极材料的比电容量5,如式(1)所示。
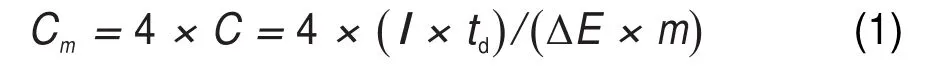
式中,Cm为单个电极的质量比电容量,F∙g-1;C为电化学电容器的质量比电容量,F∙g-1;I为放电电流,A;td为放电时间,s;ΔE为电势窗,V;m为电容器双电极中活性成分活性炭的质量,g。
使用电化学工作站(Thales 20426,德国ZHAHER公司),用循环伏安、交流阻抗等电化学方法研究双电层电容器的充放电稳定性和可逆性。由循环伏安曲线,可以根据式(2)计算炭材料的比电容13。
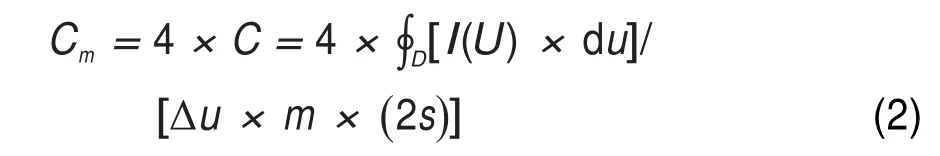
式中,由循环伏安曲线计算积分面积,u为电势,Δu为电势差,D为封闭的曲线积分,s为扫描速率。
交流阻抗测量的频率范围为10 mHz-200 kHz,施加的交流信号振幅为5 mV。
2.4三电极体系的测试
采用2.3节中的方法制备电极片,选取两片质量相近的电极片,其中一片作为工作电极,另一片作为对电极,Ag/AgCl(饱和KCl,美国Pine公司)为参比电极11,以6mol∙L-1KOH和1mol∙L-1H2SO4为电解质溶液,采用循环伏安法以5mV∙s-1的扫描速率分别在-1.0-0V(vsAg/AgCl)和-0.1-0.9V(vsAg/AgCl)下测试三电极体系的循环伏安曲线。
2.5统计回归分析
为了研究影响比电容量的关键因素,本文通过使用自由截距多元线性回归拟合法进行统计分析9,10。其公式为:
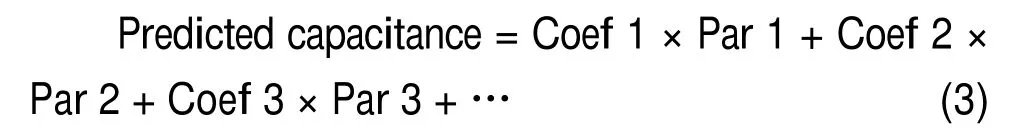
式中,Coef和Par分别代表系数和参变量。原则上通过结合不同参变量拟合(单参变量拟合、两个参变量拟合、三个参变量拟合等)进行分析,计算出相关性最好的统计模型。
3 结果与讨论
3.1磷酸法活性炭的孔隙结构和元素含量
活性炭的元素含量(w)分析结果见表1。从表1可看出,当活化温度在600-800°C范围内,磷酸活化所制备的活性炭的磷元素含量在700-800°C时达到最大值,为5.8%(与其它文献的研究结果一致14-17)。这是由于在活化过程中,活化剂磷酸及其衍生物多聚磷酸在700°C下开始大量热分解并产生了P2O5,这可以由实验现象得到验证,即在该活化条件下反应管壁上沉积了大量的磷化合物。分解产物在高温下通过氧化活性炭类石墨微晶边缘的碳原子,形成了大量的表面含磷官能团。当活化温度升高到900°C后,由于含磷官能团的分解导致活性炭的磷含量减少。这些变化也导致了当活化温度升高到900°C后,所制备的磷酸法活性炭的碳元素含量的升高及氧元素含量的降低。在800°C下磷酸改性椰壳活性炭,引入的磷元素含量达到3.86%,同时导致碳元素含量由93.94%显著降低至80.27%,氧元素含量由5.00%显著升高至16.86%,其原因与磷酸活化过程相同。HACP-800样品的磷含量较低是由于热处理之前的磷酸法活性炭是在500°C左右的活化温度下制得的。在该温度下活化剂磷酸及其衍生物多聚磷酸还未分解,在回收磷酸过程中能被洗出,导致活性炭中的磷含量较低。
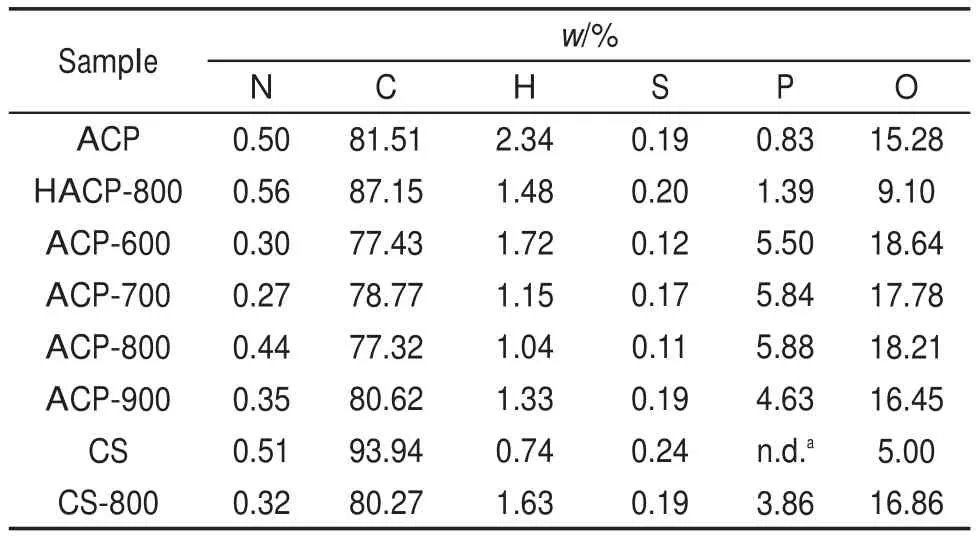
表1 活性炭的元素含量Table 1 Element contents of the activated carbons
活性炭的氮气吸附-脱附等温线以及由此计算得到的各种孔隙结构参数见图1和表2。从图1和表2可以看出,所有的活性炭都具有发达的孔隙结构,其比表面积达到1200 m2∙g-1以上。根据国际纯粹与应用化学联合会(IUPAC)18分类法,活性炭CS及其磷酸改性的CS-800活性炭样的吸附等温线属于I型等温线,它们是以微孔为主的活性炭,比表面积相对最高,微孔容积最大,中孔容积较小(表2)。其余四种活性炭都含有较发达的中孔,其中孔孔容所占比例都大于40%,其中ACP-700、ACP-800和ACP-900的吸附-脱附等温线具有明显的滞回归圈。HACP-800的中孔最发达,滞回归圈最明显。
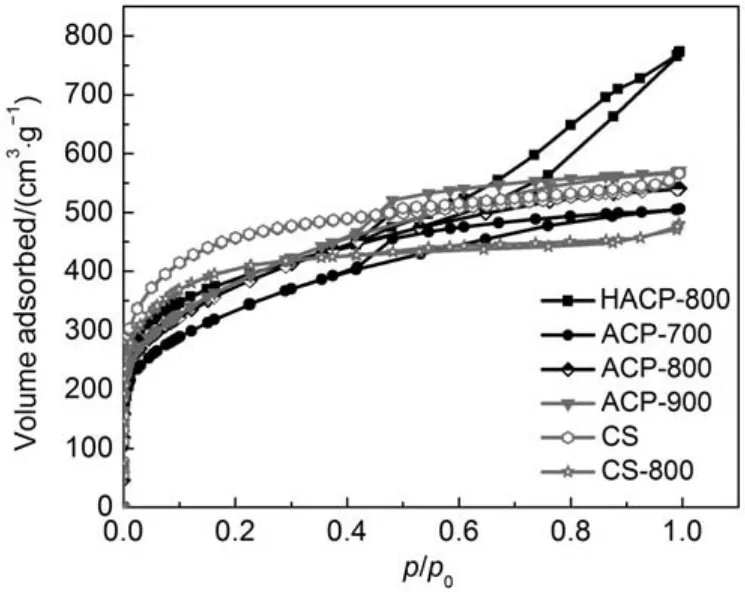
图1 活性炭的氮气吸附-脱附等温线Fig.1 Nitrogen adsorption-desorption isotherms of the activated carbons
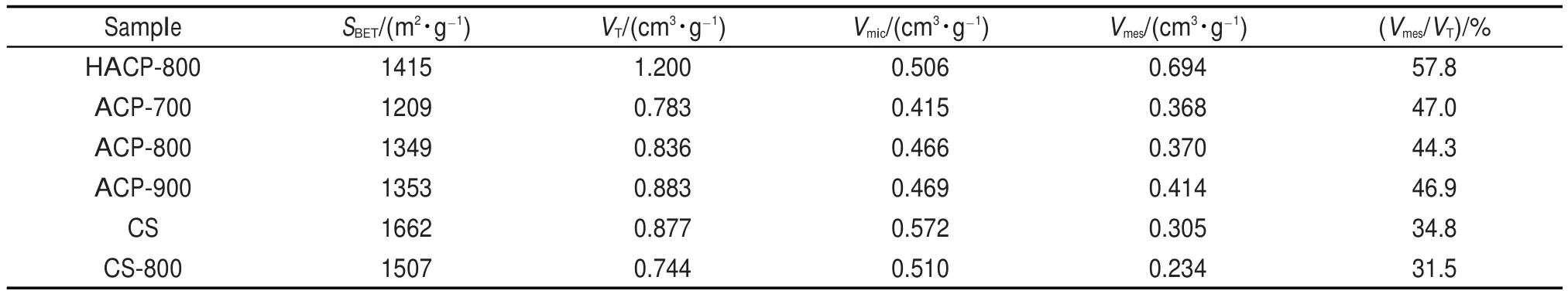
表2 活性炭的孔隙结构参数Table 2 Parameters of pore structure of the activated carbons
活性炭的孔径分布是影响双电层电容器性能的主要因素之一。已有研究证明,中孔是电解质离子向微孔内扩散的运输通道,合适孔径的微孔是形成电容器双电层的主要场所19。从活性炭的孔径分布曲线(图2)可以看出,活性炭HACP-800具有较宽的孔径分布,微孔孔径主要集中在0.56和1.00 nm左右,中孔孔径主要集中在2-30 nm之间。活性炭ACP-700、ACP-800、ACP-900及CS-800的孔径分布范围相对较窄,活性炭ACP-700、ACP-800及ACP-900的微孔孔径主要集中在0.6及0.9 nm左右,中孔孔径主要集中在2.5-4.7 nm范围内,且在4.7 nm处分布最为集中。活性炭CS及CS-800的微孔孔径主要集中在0.6-1.2 nm范围内,且在0.6 nm处分布最为集中,少量中孔的孔宽主要集中在2.3-3.1 nm处。经过磷酸改性的活性炭CS-800相对于活性炭CS,其微孔在0.6及0.8 nm处的比例明显增大,而在1.2 nm及2.3-3.1 nm处的孔容比例均降低,说明经过磷酸改性引入的含磷基团占据了活性炭原有的部分孔隙。
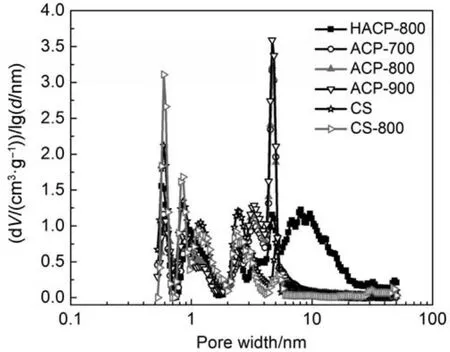
图2 用QSDFT方法计算活性炭的孔径分布图Fig.2 Pore size distributions of the activated carbons calculated by quenched solid density functional theory(QSDFT)method
3.2含磷活性炭的表面化学性质
图3是XPS对活性炭ACP-800表面的O 1s和P 2p的分析谱图,表3列出了XPS谱图的拟合分析结果以及由此计算得到的氧和磷元素含量(A/%)。由XPS(表3)和ICP-AES(表1)两种方法分析得到的活性炭的磷元素含量变化一致。在活性炭表面的氧原子存在五种结合能(表4),它们分别是峰位于(531.1±0.2)eV的醌型氧(C=O)及磷酸盐结构中的P=O20,(532.5±0.3)eV的C―O―C和C―O―P结构中的单键氧21,(533.8±0.2)eV的P―O―P结构22,(534.9±0.2)eV的化学吸附的氧(羧基)或水23,以及(537.0±0.5)eV的羟基基团21。
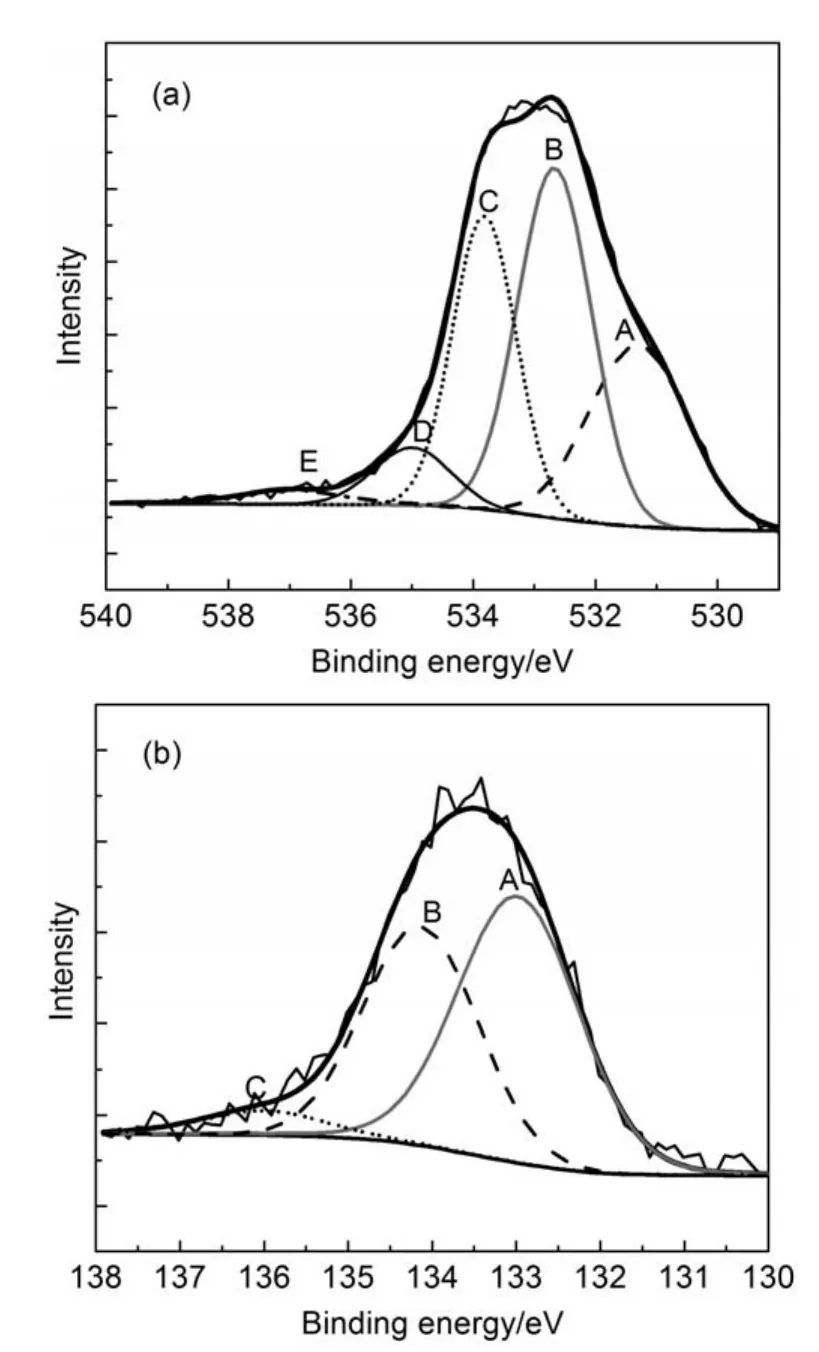
图3ACP-800的(a)O 1s和(b)P2p XPS图谱Fig.3 (a)O 1s and(b)P2p XPS spectra ofACP-800
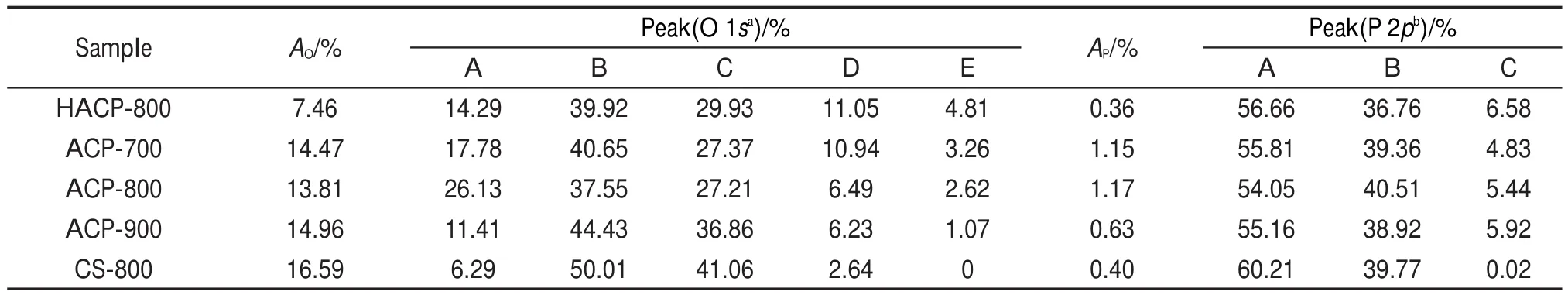
表3 由P2p和O 1s XPS峰得到的含磷活性炭的磷元素和氧官能团含量分布Table 3 Distributions of phosphorus and oxygen functional groups of phosphorus-containing activated carbons obtained from the P2p and O 1s XPS peaks
P 2p分峰拟合结果显示了磷存在三种不同的结合能(表4),位置分别在132.8、134.0和136.0 eV,它们分别对应焦磷酸盐20,21、偏磷酸盐21,24和五氧化二磷22三种结构(分子结构11见图4)。值得注意的是,膦酸盐(C―P―O)的结合能与焦磷酸盐的结合能在同一位置25,因此,无法明确计算出C―O―P和C―P―O的含量。但以往的原子核磁共振(31PNMR)研究表明,磷酸法活性炭中少量的磷是以C―P―O的形式存在8,21。表3显示,活性炭ACP-800具有最高含量的C=O和P=O,结合P 2p拟合结果可知,活性炭ACP-800具有较高含量的焦磷酸盐。活性炭CS-800的磷酸改性引入了较高的氧含量,且双键氧(C=O和P=O)含量较少。另外,活性炭CS-800具有最少的五氧化二磷含量,相应的其化学吸附的氧或水含量最少。
3.3含磷活性炭在KOH和H2SO4电解质溶液中的电化学性能
3.3.1恒电流充放电和循环伏安性能
为了研究孔隙结构及磷元素含量对活性炭电化学性质的影响,本文采用恒电流充放电、循环伏安及交流阻抗考察了活性炭在6 mol∙L-1KOH电解质溶液中的电化学性能。为了对比活性炭在酸、碱性电解质溶液中的电化学性能,以1 mol∙L-1H2SO4为电解质溶液,采用恒电流充放电和循环伏安测试活性炭电极的电化学行为。由于活性炭ACP及ACP-600的导电性较差,研究其电化学行为意义不大。
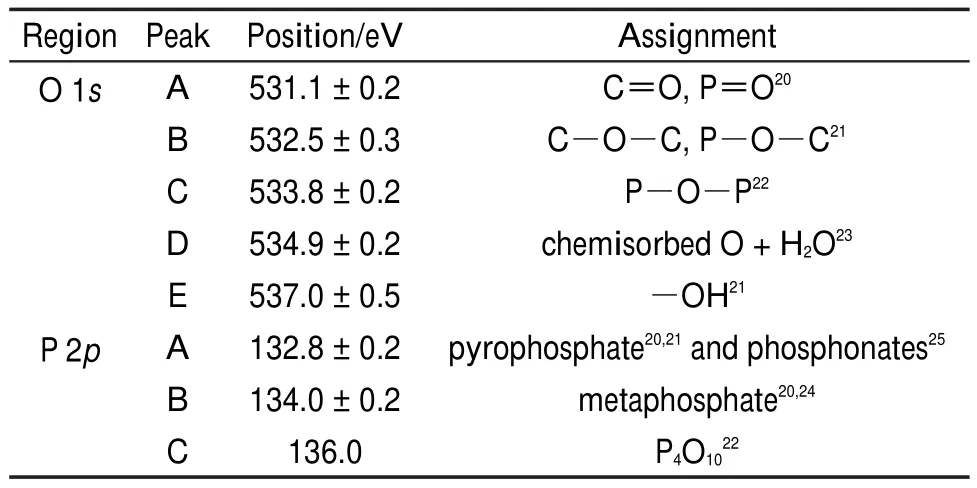
表4 O 1s和P2p XPS图谱对应的结合能位置和官能团形式Table 4 Types of functional groups and their binding energy based on the O 1s and P2p XPS peaks
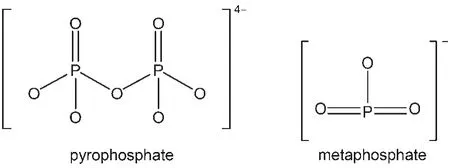
图4 焦磷酸盐和偏磷酸盐的化学结构11Fig.4 Chemical structures of pyrophosphate and metaphosphate11
在6 mol∙L-1KOH电解质溶液中,活性炭在0.1 A∙g-1和10 A∙g-1电流密度下的恒电流充放电曲线如图5所示,由此计算得到的活性炭单电极的比电容量结果列于表5。从图5中可以看出,所研究的活性炭电极的恒电流充放电曲线都呈现比较对称的等腰三角形,表明这些活性炭电极具有良好的电容特性,充放电效率高。比较图5(a,b)可以看出,较高的电流密度导致活性炭电极在放电瞬间出现较明显的电压降,这是由于电解质离子扩散滞后所引起。在这些活性炭中,中孔比例较高的HACP-800在放电瞬间出现的电压降明显低于其它活性炭(图5(b)),显然是由于中孔促进了电解质离子在孔隙内扩散的缘故。因此,较低电流密度下活性炭的充放电时间明显要长。
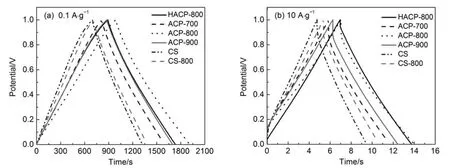
图5 活性炭在6 mol∙L-1KOH电解质溶液中测试的不同电流密度下的恒电流充放电曲线Fig.5 Galvanostatic charge-discharge curves of the activated carbons recorded at different current densities measured in 6 mol∙L-1KOH electrolyte
在4种中孔较发达的活性炭HACP-800、ACP-700、ACP-800和ACP-900中,尽管ACP-800的比表面积和比孔容积都明显小于HACP-800,但其比电容量最高,在0.1 A∙g-1的电流密度下其比电容量达到185 F∙g-1;ACP-900的比表面积和比孔容积与ACP-800非常接近,中孔孔容较高,但其比电容量却较低。这些含磷活性炭的不同表面化学性质无疑是产生这些差异的主要原因。含磷量最高的样品ACP-800有最高的比电容量,表明含磷官能团明显提高了活性炭电极的比电容量。同样,微孔活性炭CS经磷酸改性后,尽管比表面积和比孔容积都降低,但其比电容量反而有所增加。
在6 mol∙L-1KOH电解质溶液中,活性炭在5和100 mV∙s-1下的循环伏安曲线见图6,由此计算得到的活性炭单电极比电容量结果见表6,其规律与恒电流充放电曲线计算得到的活性炭单电极比电容量一致。它们进一步支持了含磷表面基团提高了活性炭电极的比电容量这一结论。从图6可以看出,所研究的活性炭电极在较低扫描速率5 mV∙s-1下的循环伏安曲线均具有典型电容器的类似四边形电势窗口,在较高扫描速率100 mV∙s-1下的,活性炭HACP-800的对称性优于其它活性炭,这主要是由于在较高扫描速率下,微孔的存在限制了电解质离子扩散到活性炭孔隙内,增加了活性炭电极的欧姆阻抗26。活性炭HACP-800的微孔比例较低,因而其在较高扫描速率下的循环伏安曲线仍具有很好的对称性。
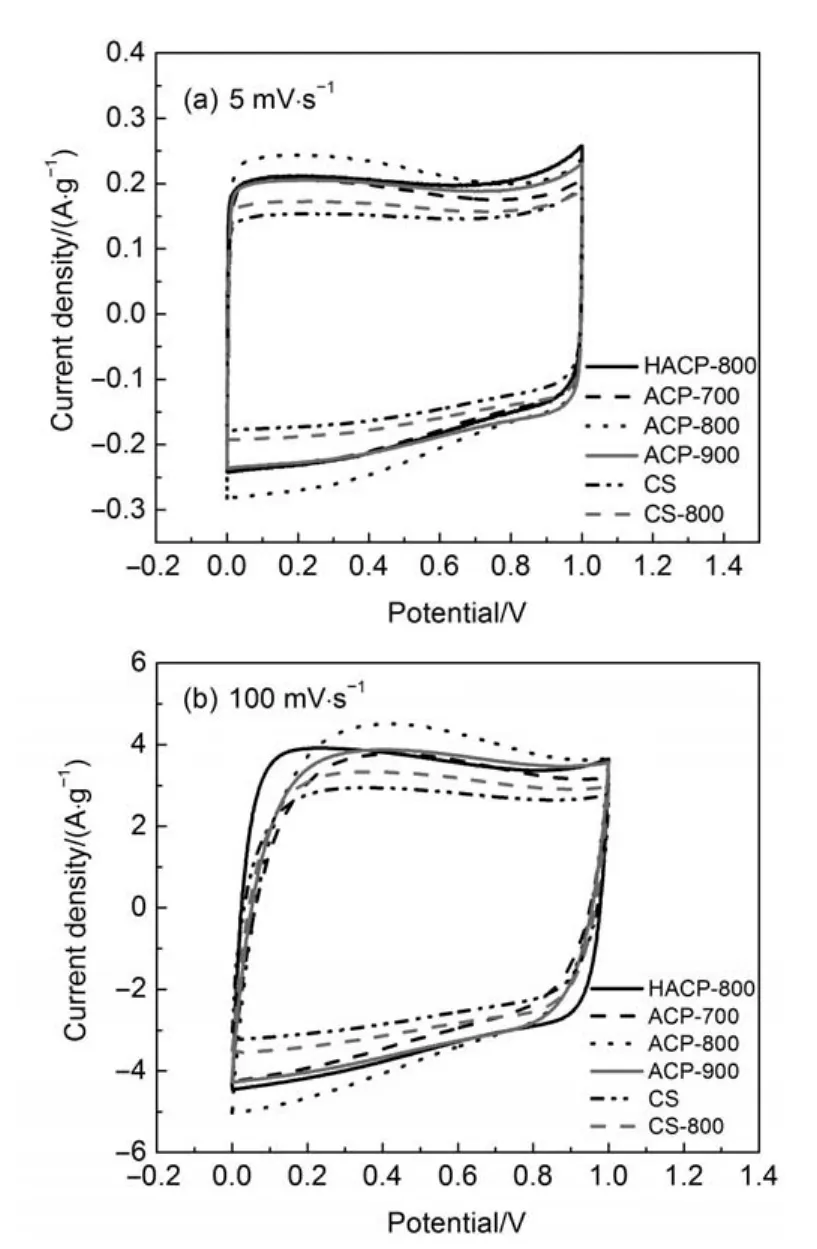
图6 活性炭在6 mol∙L-1KOH电解质溶液中测试的不同扫描速率下的循环伏安曲线Fig.6 Cyclic voltammogram curves of the activated carbons recorded at different scan rates measured in 6 mol∙L-1KOH electrolyte
在1 mol∙L-1H2SO4电解质溶液中,活性炭电极在0.1 A∙g-1电流密度下的恒电流充放电曲线和5 mV∙s-1扫描速率下的循环伏安曲线见图7,充放电曲线所计算得到的活性炭单电极比电容量见表5。从图7可以看出,所研究的活性炭电极的恒电流充放电曲线都呈现比较对称的等腰三角形,且它们的循环伏安曲线均具有典型电容器的类似四边形电势窗口,表明活性炭电极在1 mol∙L-1H2SO4电解质溶液中具有良好的电容特性,充放电效率高。从表5可看出在1 mol∙L-1H2SO4和6 mol∙L-1KOH电解质溶液中活性炭电极的比电容量变化规律一致。
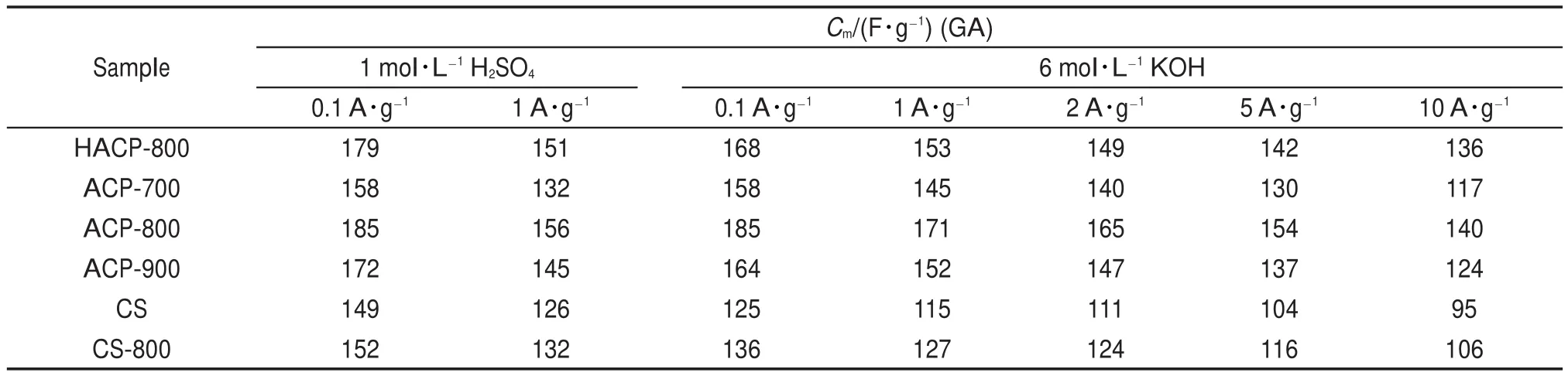
表5 活性炭在1 mol∙L-1H2SO4和6 mol∙L-1KOH电解质溶液中测试的不同电流密度下的单电极比电容量Table 5 Specific capacitance of the activated carbons at different current densities measured in 1 mol∙L-1H2SO4and 6 mol∙L-1KOH electrolytes
3.3.2阻抗分析
图8(a,b)分别是活性炭电极在6 mol∙L-1KOH电解质溶液中的Nyquist交流阻抗谱图及其等效电路图。从谱图可以看出,含磷活性炭的Nyquist谱图中在高频区显示出一个半圆弧,紧随着在中频区表现为一段45°的Warburg阻抗区。在高频区,实部Zʹ轴上的截距为电容器内电阻(Ri),包括电解液电阻、电极材料内阻以及电极材料与泡沫镍集流体间的接触电阻27。从表7可知,各活性炭电极的Ri均小于530mΩ,说明测试的电容器样品具有很好的导电性。随着频率的降低,Nyquist谱图中出现了半圆弧,这是由于电极与电解液界面间的电荷转移阻抗所引起的27,且半圆的直径越大表明法拉第准电容越高28。因此,活性炭CS未出现半圆弧,主要是由于该活性炭碳元素含量高,达到93.94%(w),其氧元素含量仅为5.00%(w),说明该活性炭电极的电容主要是双电层电容,其法拉第准电容所占比例很小。在中频区表现为一段45°的Warburg阻抗区代表电解质离子在活性炭孔隙中的扩散电阻(Rw),其大小与电极材料的孔径分布有关。从图8可以看出,活性炭HACP-800在阻抗图谱中表现出最短的45°斜线,其Rw值仅为146 mΩ,进一步说明了活性炭HACP-800的孔径分布范围很宽,中孔的存在起到了通道的作用,有利于电解质离子扩散到微孔内。在低频区除活性炭CS外,其余各含磷活性炭电极均表现为近似垂直的直线,表明含磷活性炭电极具有良好的电容特性。
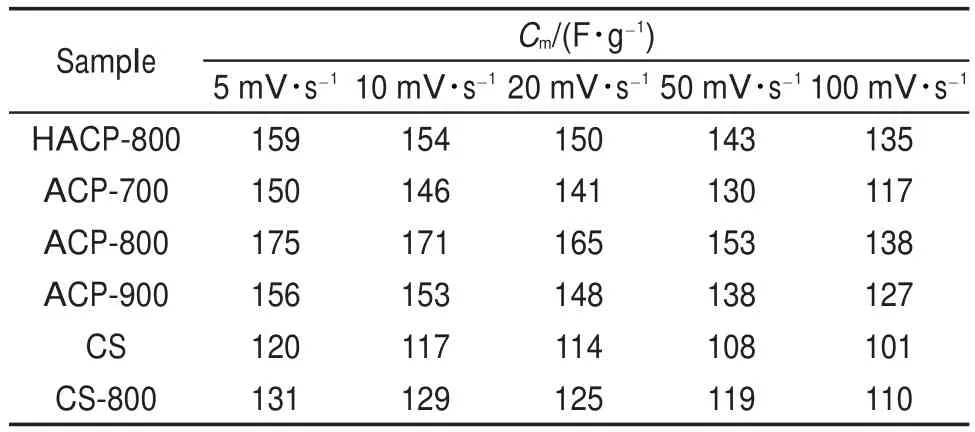
表6 用循环伏安法测试活性炭在6 mol∙L-1KOH电解质溶液中不同扫描速率下的单电极比电容量Table 6 Specific capacitance of the activated carbons at different scan rates measured in 6 mol∙L-1KOH electrolyte by cyclic voltammograms method
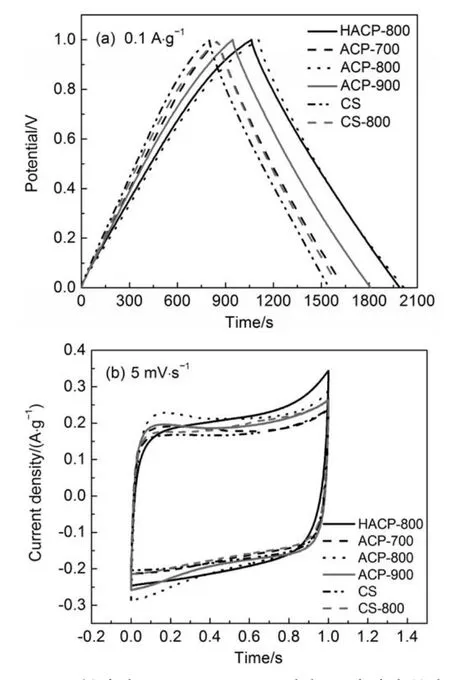
图7 活性炭在1 mol∙L-1H2SO4电解质溶液中的在0.1A∙g-1电流密度时的恒电流充放电曲线(a)和5 mV∙s-1速率时的循环伏安曲线(b)Fig.7 Galvanostatic charge-discharge curves recorded at the current density of 0.1A∙g-1(a)and cyclic voltammograms recorded at the scan rate of 5 mV∙s-1(b)for the activated carbons measured in 1 mol∙L-1H2SO4electrolyte
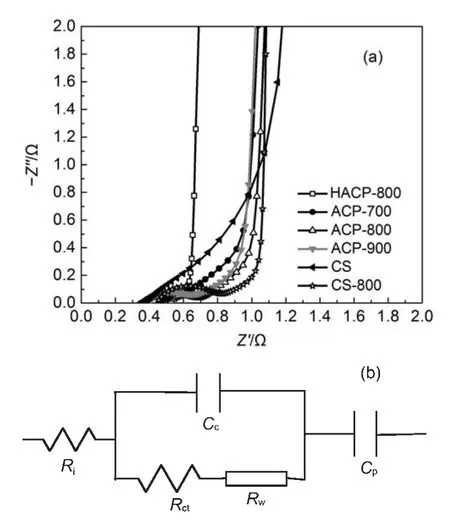
图8 (a)活性炭在6 mol∙L-1KOH电解质溶液中测试的Nyquist交流阻抗谱和(b)等效电路图Fig.8 (a)Nyquist impedance spectra of the activated carbons measured in 6 mol∙L-1KOH electrolyte and (b)equivalent circuit modeling
3.4活性炭表面含磷基团对电化学性能的影响机理
为了研究活性炭表面含磷基团对电化学性能的影响机理,应用三电极体系测试活性炭电极的循环伏安曲线11,29。图9分别是在6 mol∙L-1KOH和1 mol∙L-1H2SO4电解质溶液中,以5 mV∙s-1的扫描速率测试的活性炭电极的循环伏安曲线。
从图9(a)可以看出,在6 mol∙L-1KOH电解质溶液中,在-0.3至-1.0 V(vs Ag/AgCl)之间,随着电势的降低,活性炭电极的响应电流增加,这主要是由于活性炭的表面基团与电解质离子发生反应产生了赝电容,类似的循环伏安曲线以往也有很多相关的研究报道6,27,30,31,且随着电势的降低,活性炭ACP-800的响应电流增加最明显,说明活性炭ACP-800的表面基团引入的赝电容最高。结合XPS分析结果(表4)可知,相对于其它活性炭,活性炭ACP-800表面磷原子含量最高,氧原子含量较低,说明活性炭ACP-800表面含磷基团与电解质离子发生反应产生了赝电容。因此可推测,在6 mol∙L-1KOH电解质溶液中,活性炭的表面含磷基团可与电解质离子发生反应产生赝电容从而提高活性炭电极的比电容量,但其具体反应机理有待进一步研究。
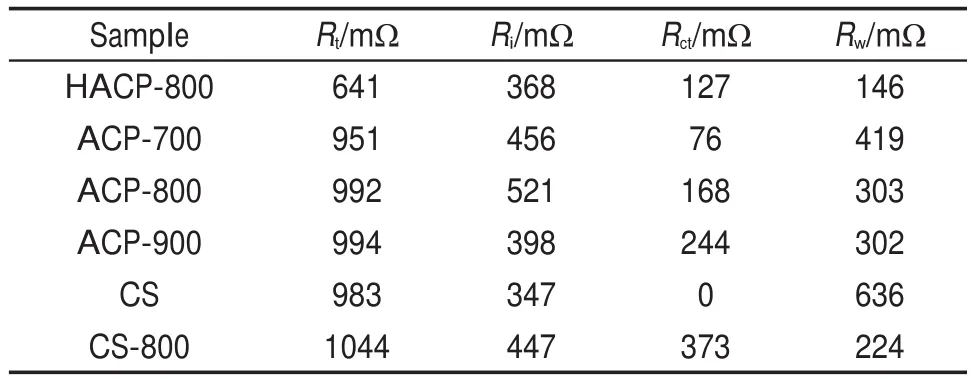
表7 6 mol∙L-1KOH电解质中活性炭的总电阻Rt、Ri、荷转移电阻Rct和RwTable 7 Overall resistance Rt,Ri,Rct,and Rwmeasured in 6 mol∙L-1KOH electrolyte
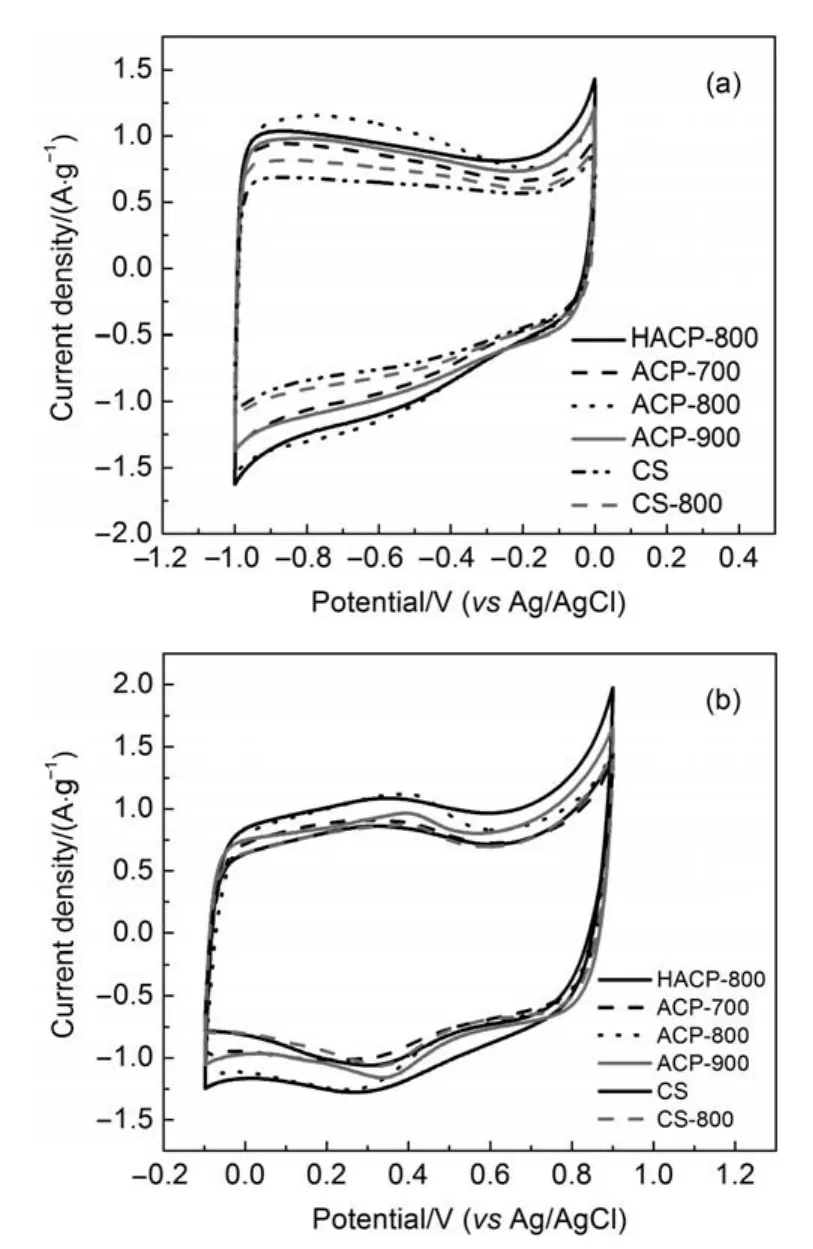
图9 扫描速率为5 mV∙s-1时测得活性炭在不同电解质溶液中三电极体系的循环伏安曲线Fig.9 Cyclic voltammograms of the activated carbons at a scan rate of 5 mV∙s-1measured in a three-electrode cell with different electrolytes
从图9(b)可以看出,在1mol∙L-1H2SO4电解质溶液中,循环伏安曲线在0.2-0.4V(vsAg/AgCl)范围内存在氧化还原峰,且活性炭ACP-800的氧化还原峰最明显,同样可推测,活性炭的表面含磷基团可与H2SO4电解质中的阳离子或阴离子发生反应产生赝电容,以往也有相关报道将其归因于活性炭中的焦磷酸盐与H+发生氧化还原反应产生了赝电容8,11。
3.5磷酸法活性炭电化学性能的综合分析
已有大量研究表明2-5,9,10,13,活性炭的孔隙结构、表面化学结构和微观结构不同程度地影响活性炭电极的比电容量。为了更加准确表述活性炭结构与其电化学性能之间的关系,已有研究者开始尝试采用各种数学方法定量探讨它们之间的关系。Shi32用一个简单的模型描述了孔隙结构对比电容量的影响,如式(4)所示。

其中,Cmes和Cmic分别代表单位中孔比表面积和单位微孔比表面积的比电容量;Smes和Smic分别为中孔比表面积和微孔比表面积。Zhi等33采用逐步回归法拟合了磷酸法活性炭电极的比电容量与孔隙结构的关系,结果表明活性炭电极的比电容量与微孔孔容存在线性关系,但其测定系数R2仅为74.6%,线性关系较差。Puziy等9首次采用自由截距多元线性回归分析法拟合分析得到了活性炭中磷元素含量和比表面积两个因素与其比电容量的关系方程;最近,该课题组采用同样的方法拟合分析了不同电位窗下,活性炭的磷含量、孔径分布和电阻等因素与比电容量的关系(但没有给出具体方程)10,其拟合方程的测定系数R2都大于0.9。这些结果表明含磷活性炭的比电容量的影响因素包括活性炭的孔隙结构、表面化学性质以及电阻。
3.5.1KOH电解质
为了更加深入分析含磷活性炭的比电容量的影响因素,本文采用自由截距多元线性回归拟合分析方法,以活性炭的磷含量、孔隙结构和电阻为参变量,分别拟合分析了含磷活性炭在不同电流密度下采用充放电测试得到的比电容量和在不同扫描速率下采用伏安法所测试得到的比电容量与这些参变量的定量关系。
图10采用线性回归拟合得到某一孔径范围所对应的比表面积(根据QSDFT计算)与在6 mol∙L-1KOH电解质溶液中测定的比电容量(0.1A∙g-1)之间的相关系数,选取其中相关系数大于0.8的孔径范围所对应的比表面积(表8)作为多元线性回归拟合分析中孔隙结构对活性炭电极比电容量的影响因素9。因此,影响活性炭电极比电容量的多元线性回归拟合的参变量包括w(P)、孔径从范围为0.57-0.59nm、1.10-1.61nm、2.12-2.43nm及3.94-4.37 nm分别所对应的比表面积S0.57-0.59nm、S1.10-1.61nm、S2.12-2.43nm、S3.94-4.37nm(表8)以及总电阻Rt(表7),拟合出测定系数R2达到0.95的统计模型(表9)。
从表9可以看出,统计模型中A值相对很大,说明磷元素含量的影响较显著,活性炭所具有的表面含磷官能团明显提高了活性炭电极的比电容量。正如在吸附过程中一样,不同尺寸大小的孔隙所起作用不同;同样,在形成双电层过程中,不同尺寸大小的孔隙所起的作用也不同。通常来说,孔径较大的中孔可能主要是起着电解质扩散通道的作用,微孔则主要是形成双电层的主要场所。由本文多元线性回归拟合得到的方程可看出,在孔径由范围1.10-1.61 nm、2.12-2.43 nm及3.94-4.37 nm内的孔隙对比电容量都有显著的贡献。Puziy等9也拟合分析得到活性炭在孔径范围0.5-0.6 nm、0.77-0.84 nm、1.34-1.55 nm、6.5-8.2 nm中对活性炭的比电容量都有显著贡献。Gryglewicz等2的研究报道指出中孔的孔径小于5 nm也可形成双电层电容。因此可推测,活性炭的中孔有利于电解质离子向微孔内的扩散,在1.10-1.61 nm、2.12-2.43 nm及3.94-4.37 nm之间的孔径则是电解质离子在活性炭孔隙内部形成双电层的主要场所。本文所研究的几种含磷活性炭是由不同原料及不同活化过程所制备的,活性炭电极的电化学阻抗存在明显差异,这主要是由于活性炭的微孔比例,孔隙形状3及导电性的区别,因此活性炭电极的总电阻Rt也是影响活性炭电极比电容量的关键因素之一。
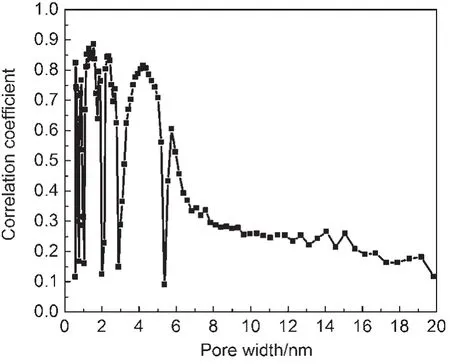
图10 在6 mol∙L-1KOH电解质溶液中测定的0.1A∙g-1电流密度下的比电容量与不同孔径范围所对应的比表面积之间的相关系数Fig.10 Correlation coefficient between the special surface area corresponding to the given pore width and the experimental capacitance at the current density of 0.1A∙g-1measured in 6 mol∙L-1KOH electrolyte
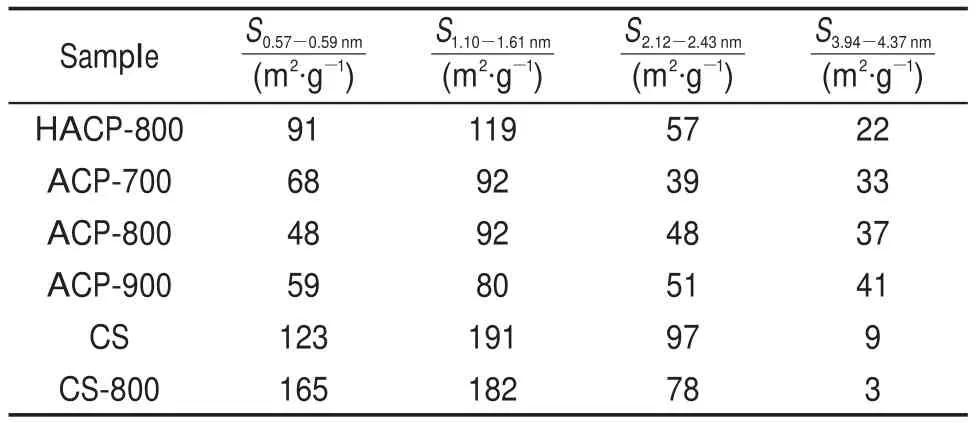
表8 由氮气吸附等温线应用QSDFT方法计算不同孔径范围内的比表面积(S)Table 8 Special surface areas(S)corresponding to pores in the given width range calculated from N2adsorption isotherms using QSDFT method
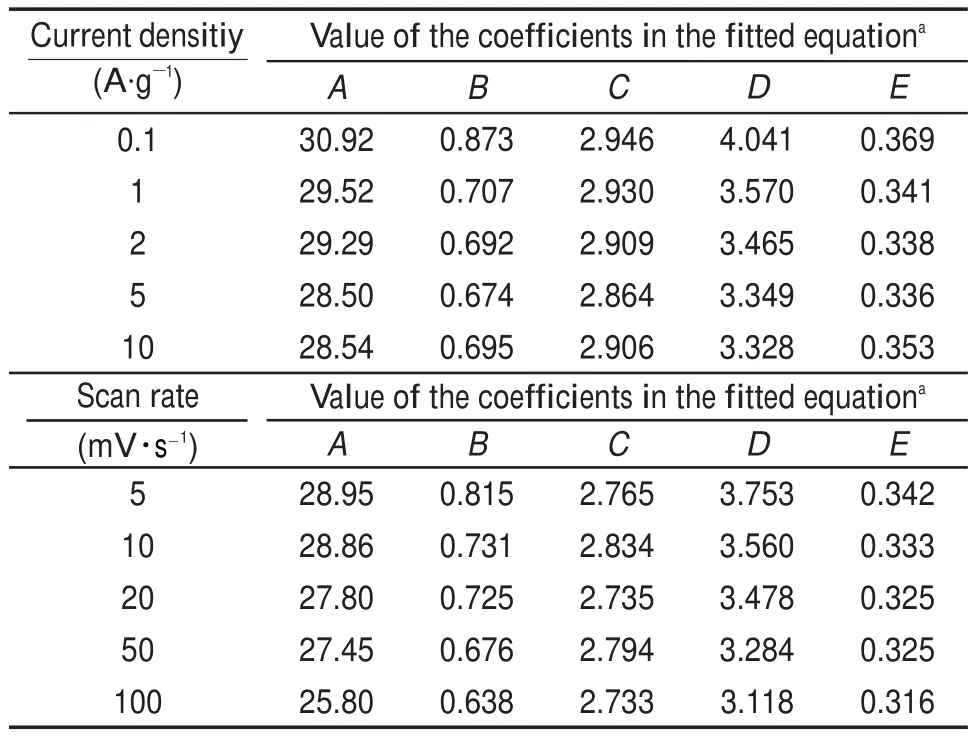
表9 不同电流密度和扫描速率下的多元线性回归模型Table 9 Multiple linear regression model at different current densities and scan rates
图11是采用线性回归拟合得到的由统计模型预测的比电容量(PC)与实验测定的比电容量之间的线性关系。从图11可以看出,不管是哪种活化方法制备的含磷活性炭,在不同电流密度或扫描速率下,由统计模型预测的比电容量与实验测定的比电容量之间都表现出很好的线性关系,说明影响活性炭电极比电容量的因素包括磷元素含量,孔径范围为1.10-1.61 nm、2.12-2.43 nm及3.94-4.37 nm之间所对应的比表面积以及总电阻。由于随着电流密度或扫描速率的增大,活性炭电极的比电容量会降低,且不同活性炭的中孔比例及表面化学性质存在差异,其比电容量的降低幅度也不同。因此,许多研究报道一般是在较小的电流密度或扫描速率下研究影响活性炭电极比电容量的影响因素2,3,9。本文在不同的电流密度及扫描速率下研究由统计模型预测的比电容量与实验测定的比电容量之间的线性关系,其测定系数R2均达到0.95以上,高于以往的研究结果3,9,10,33,说明通过这些参变量拟合的线性相关程度很高,参变量完整。
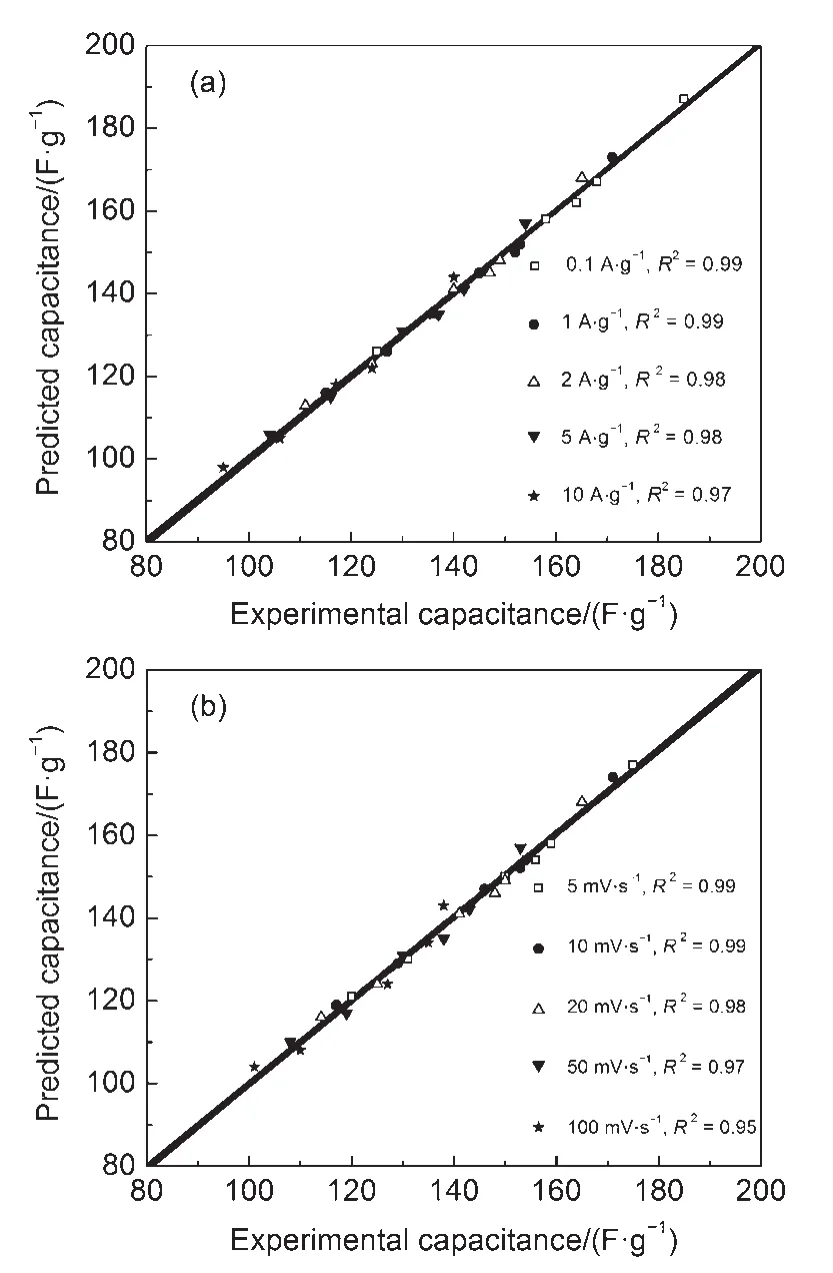
图11 在6 mol∙L-1KOH电解质溶液中测定的活性炭比电容量与预测的比电容量之间的线性关系Fig.11 Linear relation between predicted capacitance vs experimental capacitance of the activated carbons measured in 6 mol∙L-1KOH electrolyte
3.5.2H2SO4电解质
同样地,采用自由截距多元线性回归拟合分析方法,以活性炭的磷含量、孔隙结构(表10)为参变量,拟合分析了含磷活性炭在0.1 A∙g-1下得到的比电容量与这些参变量的定量关系。通过结合不同参数拟合进行方差分析,计算出相关性最好的统计模型如下:

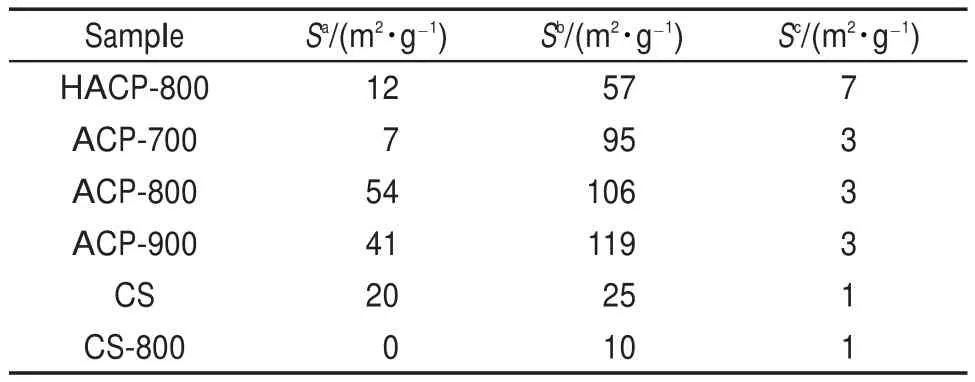
表10 由氮气吸附等温线应用QSDFT方法计算不同孔径范围内的比表面积(S)Table 10 Special surface areas(S)corresponding to pores in the given width range calculated from N2adsorption isotherms using QSDFT method
从式(5)可以看出,统计模型中磷含量的系数相对很大,说明磷元素含量的影响较显著。在孔径范围0.67-0.72 nm及5.75-5.95 nm内的孔隙对比电容量都有显著的贡献。其中,孔径范围0.67-0.72 nm最有利于形成双电层电容,孔径在5.75-5.95 nm范围内有利于电解质离子向微孔内扩散. Puziy等9在1 mol∙L-1H2SO4溶液中测试磷酸法活性炭电极的比电容量,通过拟合发现活性炭孔径在0.65-0.83 nm范围内最有利于形成双电层电容。
图12是采用线性回归拟合得到的由统计模型预测的比电容量与实验测定的比电容量之间的线性关系,其测定系数R2达到0.81,说明活性炭电极的比电容量与磷元素含量、孔径范围为0.67-0.72 nm及5.75-5.95 nm之间所对应的比表面积存在较好的线性关系。
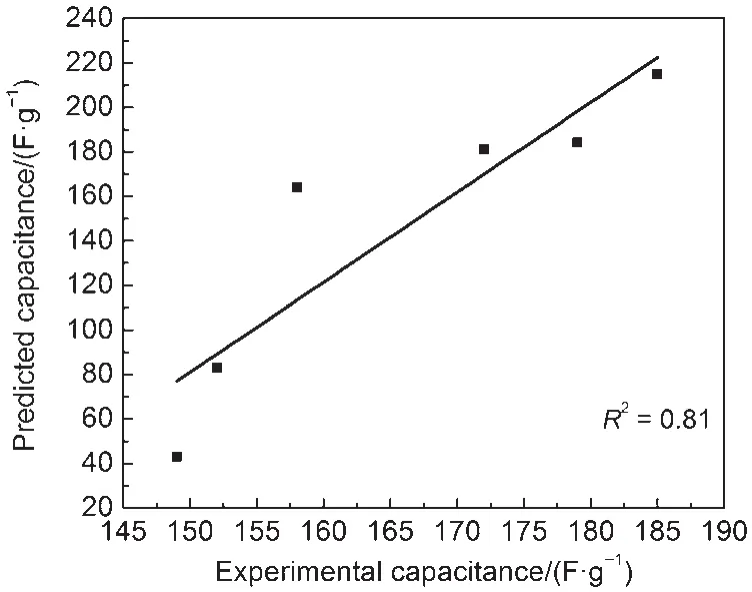
图12 在1 mol∙L-1H2SO4电解质溶液中测定的活性炭比电容量与预测的比电容量之间的线性关系Fig.12 Linear relation between predicted capacitance vs experimental capacitance of the activated carbons measured in 1 mol∙L-1H2SO4electrolyte
与在KOH电解质溶液中拟合出的统计模型相比,在H2SO4电解质溶液中仅拟合出孔径在0.67-0.72 nm范围内有利于双电层电容的形成。但以KOH和H2SO4为电解质溶液,通过拟合得到的统计模型可看出,在无机电解质溶液中,微孔最有利于双电层电容的形成。另外,不管在KOH或H2SO4电解质溶液中,磷含量对活性炭电极的比电容量都有较大的影响。
4 结论
以6 mol∙L-1KOH和1 mol∙L-1H2SO4作为电解质溶液,研究了含磷活性炭的电化学性能,结果表明,活性炭掺杂的磷可引入赝电容提高活性炭电极的比电容量,磷元素含量为5.88%(w)的活性炭的比电容量在0.1 A∙g-1下达到185 F∙g-1。根据统计分析结果表明:活性炭的中孔有利于电解质离子向微孔内的扩散,在6 mol∙L-1KOH电解质溶液中,孔径在1.10-1.61 nm、2.12-2.43 nm及3.94-4.37 nm范围内是电解质离子在活性炭孔隙内部形成双电层的主要场所;在1 mol∙L-1H2SO4电解质溶液中,孔径在0.67-0.72 nm范围内有利于双电层电容的形成。
References
(1)Wu,Y.B.;Bi,J.;Wei,B.B.Acta Phys.-Chim.Sin.2015,31(2), 315.[吴艳波,毕军,魏斌斌.物理化学学报,2015,31(2), 315.]doi:10.1016/j.electacta.2004.07.045
(2)Gryglewicz,G.;Machnikowski,J.;Lorenc-Grabowska,E.;Lota, G.;Frackowiak,E.Electrochim.Acta 2005,50(5),1197. doi:10.1016/j.electacta.2004.07.045
(3)Chmiola,J.;Yushin,G.;Dash,R.;Gogotsi,Y.J.Power Sources 2006,158(1),765.doi:10.1016/j.jpowsour.2005.09.008
(4)Raymundo-Piñero,E.;Kierzek,K.;Machnikowski,J.;Béguin, F.Carbon 2006,44(12),2498.doi:10.1016/j. carbon.2006.05.022
(5)Seredych,M.;Hulicova-Jurcakova,D.;Lu,G.Q.;Bandosz,T.J. Carbon 2008,46(11),475.doi:10.1016/j.carbon.2008.06.027
(6)Li,Z.H.;Li,S.J.;Zhou,J.;Zhu,T.T.;Shen,H.L.;Zhuo,S.P. Acta Phys.-Chim.Sin.2015,31(4),676.[李朝辉,李仕蛟,周晋,朱婷婷,沈红龙,禚淑萍.物理化学学报,2015,31(4), 676.]doi:10.3866/PKU.WHXB201501281
(7)Zhou,Y.;Wang,D.L.;Xiao,N.;Hou,Y.C.;Qiu,J.S.Acta Phys.-Chim.Sin.2014,30(6),1127.[周颖,王道龙,肖南,侯雨辰,邱介山.物理化学学报,2014,30(6),1127.]doi: 10.3866/PKU.WHXB201404013
(8)Hulicova-Jurcakova,D.;Seredych,M.;Lu,G.Q.;Kodiweera, N.K.A.C.;Stallworth,P.E.;Greenbaum,S.;Bandosz,T.J. Carbon 2009,47(6),1576.doi:10.1016/j.carbon.2009.02.006
(9)Hulicova-Jurcakova,D.;Puziy,A.M.;Poddubnaya,O.I.; Suárez-García,F.;Tascón,J.M.D.;Lu,G.Q.J.Am.Chem. Soc.2009,131(14),5026.doi:10.1021/ja809265m
(10)Huang,C.C.;Puziy,A.M.;Sun,T.;Poddubnaya,O.I.;Suárez-García,F.;Tascón,J.M.D.;Hulicova-Jurcakova,D. Electrochim.Acta 2014,137,219.
(11)Huang,C.C.;Sun,T.;Hulicova-Jurcakova,D.ChemSusChem 2013,6(12),2330.doi:10.1002/cssc.201300457
(12)Neimark,A.V.;Lin,Z.;Ravikovitch,P.I.;Thommes,M. Carbon 2009,47(7),1617.doi:10.1016/j.carbon.2009.01.050
(13)Guo,H.L.;Gao,Q.M.J.Power Sources 2009,186(2),551. doi:10.1016/j.jpowsour.2008.10.024
(14)Puziy,A.M.;Poddubnaya,O.I.;Martínez-Alonso,A.; Suárez-García,F.;Tascón,J.M.D.Carbon 2002,40(9),1493. doi:10.1016/S0008-6223(01)00317-7
(15)Puziy,A.M.;Poddubnaya,O.I.;Martínez-Alonso,A.; Suárez-García,F.;Tascón,J.M.D.Carbon 2005,43(14),2857. doi:10.1016/j.carbon.2005.06.014
(16)Puziy,A.M.;Poddubnaya,O.I.;Martínez-Alonso,A.; Castro-Muñiz,A.;Suárez-García,F.;Tascón,J.M.D.Carbon 2007,45(10),1941.doi:10.1016/j.carbon.2007.06.014
(17)Puziy,A.M.;Poddubnaya,O.I.;Sobiesiak,M.;Gawdzik,B. Adsorption 2013,19,717.doi:10.1007/s10450-013-9497-4
(18)Sing,K.S.W.;Everett,D.H.;Haul,R.A.W.;Moscou,L.; Pierotti,R.A.;Rouquérol,J.;Siemieniewska,T.Pure Appl. Chem.1985,57(4),603.
(19)Frackowiak,E.;Béguin,F.Carbon 2001,39(6),937.doi: 10.1016/S0008-6223(00)00183-4
(20)Kannan,A.G.;Choudhury,N.R.;Dutta,N.K.Polymer 2007, 48(24),7078.doi:10.1016/j.polymer.2007.09.050
(21)Puziy,A.M.;Poddubnaya,O.I.;Socha,R.P.;Gurgul,J.; Wisniewski,M.Carbon 2008,46(15),2113.doi:10.1016/j. carbon.2008.09.010
(22)Shih,P.Y.;Yung,S.W.;Chin,T.S.J.Non-Cryst.Solids 1999, 244(2-3),211.doi:10.1016/S0022-3093(99)00011-3
(23)Biniak,S.;Szymański,G.;Siedlewski,J.;Światkowski,A. Carbon 1997,35(12),1799.doi:10.1016/S0008-6223(97) 00096-1
(24)Barbaux,Y.;Dekiouk,M.;Maguer,D.L.;Gengembre,L.; Huchette,D.;Grimblot,J.Appl.Catal.A 1992,90(1),51. doi:10.1016/0926-860X(92)80247-A
(25)Van der Plas,T.Texture and Chemistry of Carbon Surface.In Physical and Chemical Aspects of Adsorbents and Catalysts; Linsen,B.G.Ed.;Academic Press:London,1970;Chapter 9.
(26)Fuertes,A.B.;Pico,F.;Rojo,J.M.J.Power Sources 2004,133 (2),329.doi:10.1016/j.jpowsour.2004.02.013
(27)Zhao,X.;Zhang,Q.;Chen,C.M.;Zhang,B.;Reiche,S.;Wang, A.;Zhang,T.;Schlöl,R.;Su,D.S.Nano Energy 2012,1(4), 624.doi:10.1016/j.nanoen.2012.04.003
(28)Gu,W.;Sevilla,M.;Magasinski,A.;Fuertes,A.B.;Yushin,G. Energy Environ.Sci.2013,6(8),2465.doi:10.1039/c3ee41182f
(29)Zapata-Benabihe,Z.;Moreno-Castilla,C.;Carrasco-Marín,F. Langmuir 2014,30(6),1716.doi:10.1021/la404667y
(30)Hulicova,D.;Kodama,M.;Hatori,H.Chem.Mater.2006,18 (9),2318.doi:10.1021/cm060146i
(31)Konno,H.;Ito,T.;Ushiro,M.;Fushimi,K.;Azumi,K.J.Power Sources 2010,195(6),1739.doi:10.1016/j. jpowsour.2009.09.072
(32)Shi,H.Electrochim.Acta 1996,41(10),1633.doi:10.1016/ 0013-4686(95)00416-5
(33)Zhi,M.;Yang,F.;Meng,F.;Li,M.;Manivannan,A.;Wu,N. ACS Sustainable Chem.Eng.2014,2(7),1592.doi:10.1021/ sc500336h
Electrochemical Properties of Phosphorus-Containing Activated Carbon Electrodes on Electrical Double-Layer Capacitors
WANG Yong-FangZUO Song-Lin*
(Jiangsu Key Laboratory of Biomass-based Green Fuels and Chemicals,College of Chemical Engineering, Nanjing Forestry University,Nanjing 210037,P.R.China)
Different kinds of phosphorus-containing activated carbons were prepared by phosphoric acid activation of lignocellulosic precursor and modification with H3PO4.Elemental analysis,X-ray photoelectron spectroscopy(XPS),and nitrogen adsorption were employed to analyze the elemental content,surface chemistry,and pore structures of the activated carbons.The electrochemical properties of the carbon materials were characterized for their application as supercapacitors in KOH and H2SO4electrolytes using galvanostaticcharge/discharge,cyclicvoltammetry,andelectrochemicalimpedancespectroscopic analyses.A statistical analysis by an intercept-free multiple linear regression method was employed to investigate the factors that influence the specific capacitance of activated carbon electrodes.In addition,a three-electrode cell setup was used to analyze the cause of the phosphorus contribution on capacitance. The results show that phosphorus increases the specific capacitance of activated carbons by the introduction of pseudo-capacitance;the activated carbon with phosphorus content of 5.88%(w)exhibits a specific capacitance of 185 F∙g-1at 0.1 A∙g-1.The statistical analysis showed that mesopores facilitate an access of electrolyte ions to the surface of micropores.The pores in the width ranges of 1.10-1.61 nm, 2.12-2.43 nm and 3.94-4.37 nm benefit the formation of the electric double layer in 6 mol∙L-1KOHelectrolyte;the pores with sizes of 0.67-0.72 nm have a positive effect in 1 mol∙L-1H2SO4electrolyte.
Activated carbon;Phosphorus functional group;Pore structure;Pseudo-capacitance; Supercapacitor
June 30,2015;Revised:November 3,2015;Published on Web:November 4,2015.
O646
*Corresponding author.Email:zslnl@hotmail.com;Tel:+86-25-85428840.
The project was supported by the National Natural Science Foundation of China(31270621)and State ForestryAdministration 948 Importation Project,China(2012-4-08).
国家自然科学基金(31270621)和国家林业局948引进项目(2012-4-08)资助
©Editorial office ofActa Physico-Chimica Sinica
