羟考酮缓释片联合吗啡片滴定方案治疗中、重度癌痛的临床研究
2016-11-06庞华春傅健曾令洋云浮市新兴县人民医院肿瘤科广东云浮527400
庞华春,傅健,曾令洋(云浮市新兴县人民医院肿瘤科,广东云浮527400)
·论著·
羟考酮缓释片联合吗啡片滴定方案治疗中、重度癌痛的临床研究
庞华春,傅健,曾令洋
(云浮市新兴县人民医院肿瘤科,广东云浮527400)
目的观察中、重度癌痛患者应用羟考酮缓释片与吗啡片联合滴定治疗的效果。方法选取2012年3月至2015年12月期间在我院肿瘤科住院治疗的中、重度癌痛患者126例,采用单盲数字随机表法分为三组,每组各42例。A组采用羟考酮缓释片滴定治疗,B组采用吗啡片滴定治疗,C组应用羟考酮缓释片与吗啡片联合滴定治疗,比较三组患者用药24 h后的临床治疗效果和不良反应。结果A组、B组和C组患者的止痛有效率分别为88.10% (37/42)、92.86%(39/42)和97.62%(41/42),三组比较差异无统计学意义(P>0.05);滴定剂量比较,C组的滴定剂量为(55.24±2.18)mg/d,较A组的(60.23±2.41)mg/d和B组的(66.23±4.56)mg/d降低,差异均有统计学意义(P<0.05);治疗后A、B、C三组的疼痛数字评价量表(NRS)评分分别为(2.07±1.15)分、(2.11±1.19)分、(1.92±1.02)分,较治疗前显著降低,差异均有显著统计学意义(P<0.01);治疗后A、B、C三组的Karnofsky(卡氏,KPS)评分分别为(69.89±9.34)分、(68.12±8.79)分、(80.23±7.89)分,较治疗前明显升高,差异有统计学意义(P<0.05);C组的便秘发生率为11.90% (5/42),低于A组的23.81%(10/42)和B组的57.14%(24/42),差异有统计学意义(P<0.05)。结论羟考酮缓释片与吗啡片联合滴定治疗中、重度癌痛具有良好的安全性与有效性,联合应用可起到疗效协同作用,减少用药剂量及副反应,改善患者的生活质量。
癌痛;羟考酮缓释片;吗啡片;临床疗效
癌痛是一种常见的恶性肿瘤并发症,在晚期恶性肿瘤患者中,60%~80%的患者遭受癌痛的折磨,缓解癌痛不仅是临床治疗的关键,也是癌症患者的基本权利[1]。滴定治疗是指根据患者的疼痛反应,采用逐渐递增剂量的方式进行治疗,遵循剂量个体化原则,可避免因用量过度所致副反应或用量不足所致镇痛效果不理想[2]。本研究在中、重度癌痛患者的滴定治疗中应用阿片类受体激动剂吗啡片联合其控释缓释剂羟考酮缓释片联合治疗,获得了显著疗效,现报道如下:
1 资料与方法
1.1 一般资料收集我院肿瘤科于2012年3月至2015年12月收治入院的中、重度癌痛患者126例,采用单盲数字随机表法分为三组,每组各42例。A组患者中男性24例,女性18例;年龄22~78岁,平均(51.23±2.24)岁;肿瘤临床分期:Ⅱ期14例,Ⅲ期20例,Ⅳ期8例;原发肿瘤:肺癌12例,乳腺癌8例,直结肠癌8例,肝癌5例,其他9例。B组患者中,男性26例,女性16例;年龄25~80岁,平均(52.01±2.57)岁;肿瘤临床分期:Ⅱ期11例,Ⅲ期22例,Ⅳ期9例;原发肿瘤:肺癌14例,乳腺癌9例,直结肠癌8例,肝癌5例,其他6例。C组患者中男性27例,女性15例;年龄25~72岁,平均(50.31±2.79)岁;肿瘤临床分期:Ⅱ期10例,Ⅲ期22例,Ⅳ期10例;原发肿瘤:肺癌15例,乳腺癌10例,直结肠癌7例,肝癌6例,其他4例。三组患者的一般情况比较差异均无统计学意义(P>0.05),具有可比性。
1.2 病例选择
1.2.1 纳入标准经临床病理证实为中、晚期恶性肿瘤,疼痛数字评价量表(NRS)评分均≥4分,预计生存期≥3个月,无既往阿片类止痛药用药史,能够配合临床治疗与评估。
1.2.2 排除标准合并严重心、脑、肝、肺、肾功能障碍者,合并慢性呼吸功能不全以及消化道梗阻者,严重颅内高压、肿瘤脑转移以及中枢性呼吸抑制风险者,妊娠期与哺乳期妇女,对本研究用药过敏者。
1.3 方法A组应用羟考酮缓释片滴定治疗,B组应用吗啡片滴定治疗,C组应用羟考酮缓释片联合吗啡片滴定治疗,滴定方案如下:
1.3.1 羟考酮滴定方法予以羟考酮缓释片口服,初始剂量为10mg/次,每12 h用药1次。首次服药1 h后评估,如NRS<4分则继续观察,如NRS仍≥4分,则按照25%~50%的剂量递增,每次用药后1 h评估1次并调整用药剂量,直至NRS<4分,达到最佳维持剂量进行维持治疗。
1.3.2 吗啡滴定方法予以吗啡片口服,初始剂量为5~15mg/次,每12 h用药1次,滴定方法同A组。
1.3.3 联合滴定方法先予以羟考酮缓释片10mg口服,每12 h服药1次。首次服药1 h后进行NRS评价及不良反应观察。如NRS降低至<4分则继续观察,24 h内予以5mg吗啡片口服;如NRS为4~6分,则予以吗啡10mg口服;如NRS≥7分,则予以15mg吗啡口服。服药1 h后再次评估,如NRS<4分则观察2~4 h,如NRS无变化或仍≥7分,吗啡按50%剂量增加,观察1 h后再次评估,如此循环直至确定最佳维持剂量,12 h后予以羟考酮缓释片10mg口服。
1.4 观察指标三组患者均在用药24 h后,统计阿片类药物的滴定剂量(最佳维持剂量),吗啡片换算成等效羟考酮缓释片,换算原则为10mg的羟考酮缓释片对应等效的20mg即效吗啡片。评价治疗前后患者的NRS评分、不良反应,并参照Karnofsky(KPS)评分法评价生活质量,得分越高则生活质量越好。
1.5 疗效标准完全缓解(CR):患者完全无痛;部分缓解(PR):患者的疼痛度较治疗前显著降低,恢复正常生活及作息;轻度缓解(MR):疼痛度较治疗前略有缓解,但疼痛感仍较为明显,影响睡眠及日常生活;无效(NR):疼痛无减轻甚至加重。计算总有效率= (CR+PR)/42×100%。
1.6 统计学方法应用SPSS18.0统计学软件包进行数据分析,计量资料以均数±标准差(±s)表示,组间两两比较采用t检验,多组间比较采用方差分析,计数资料以率(%)表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 三组患者的滴定剂量比较C组的滴定剂量平均为(55.24±2.18)mg/d,较A组的(60.23±2.41)mg/d明显降低,差异有统计学意义(t=9.9514,P<0.05),较B组的(66.23±4.56)mg/d明显降低,差异有统计学意义(t=14.0916,P<0.05)。
2.2 三组患者治疗前后的NRS评分比较治疗24 h后三组NRS评分较治疗前显著降低(P<0.01),且治疗后三组间比较差异无统计学意义(P>0.05),但C组仍较A、B组有降低的趋势,见表1。
表1 三组患者治疗前后NRS评分比较(±s,分)

表1 三组患者治疗前后NRS评分比较(±s,分)
组别A组B组C组F值P值例数42 42 42治疗前7.89±2.41 7.71±2.56 7.94±2.69 0.824 0.687治疗后2.07±1.15 2.11±1.19 1.92±1.02 0.943 0.645 t值14.1249 12.8556 13.5611 P值0.000 0.000 0.000
2.3 三组患者的镇痛疗效比较C组的镇痛总有效率略高于A组和B组,但三组间比较差异无统计学意义(χ2=1.869,P>0.05),见表2。
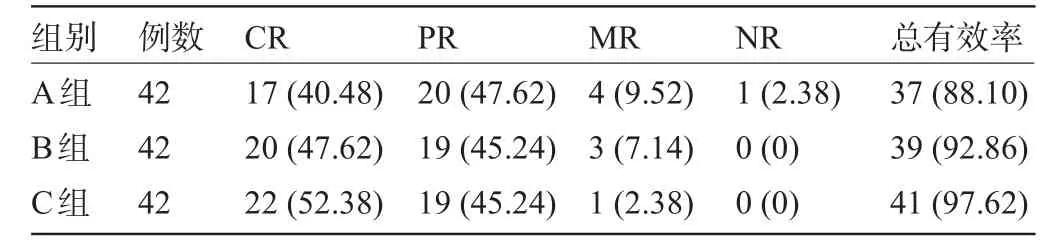
表2 三组患者镇痛疗效比较[例(%)]
2.4 三组患者治疗后的生活质量比较三组治疗后的KPS评分均显著高于治疗前(P<0.05),治疗后C组显著高于A组及B组(P<0.05),而A组与B组治疗后比较差异无统计学意义(P>0.05),见表3。
表3 三组患者治疗后KPS评分比较±s,分)

表3 三组患者治疗后KPS评分比较±s,分)
注:治疗后C组与A组和B组比较,a P<0.05。
组别A组B组C组F值P值例数42 42 42治疗前43.89±7.02 44.45±7.46 45.67±6.78 0.893 0.524治疗后69.89±9.34 68.12±8.79 80.23±7.89a 4.945 0.000 t值14.4435 13.3056 21.5299 P值0.000 0.000 0.000
2.5 三组患者的不良反应比较A、C组的便秘发生率低于B组,且C组低于A组,三组间比较差异有统计学意义(P<0.05),其余不良反应率三组比较差异均无统计学意义(P>0.05),见表4。

表4 三组患者的不良反应比较[例(%)]
3 讨论
阿片类受体激动剂是目前临床干预治疗癌痛的一线治疗药物,癌痛有效缓解率可达85%~90%[3]。由于患者对于阿片类药物所具有敏感度存在个体化差异,临床难以衡量用药剂量标准。滴定治疗通过动态评估药物镇痛效果并适时调整用药剂量,最终确定最佳维持剂量,可避免用量过度或用量不足等问题。在癌痛滴定治疗中,用药第1天具有关键性意义,在首个24 h内实现快速止痛效果并确定维持剂量维持镇痛,能够迅速控制患者的疼痛症状,改善患者的生活质量,有利于增强患者对医务人员的信任感及后续治疗信心[4]。
2011年,速效类阿片制剂被我国卫生部推荐为癌痛滴定治疗的首选药物。即效吗啡片的起效迅速且达峰时间较短,是临床治疗癌痛的标准药物,但吗啡滴定治疗由于体内代谢快速且药效持续时间较短,治疗期间需要反复多次给药,滴定治疗疗程较长,临床护理工作量大,副反应较多,患者的耐受性及依从性较低[5]。羟考酮缓释片是一种阿片类受体激动剂的控释缓释剂,具有释放-吸收双相作用,释放相药物占比约为38%,控释相药物占比约为62%,释放相能够在用药后快速(1 h左右)释放药物量达到峰值而起到快速止痛效果,而控释相则能够在12 h内缓慢、平稳释放而持续镇痛,以确保12 h内镇痛持续有效[6]。文献报道显示,在应用羟考酮缓释片后1 h内,有91.7%~93.1%的癌痛患者可获得疼痛控制[3]。但控释相的存在可导致羟考酮在体内的代谢时间延长,在滴定治疗过程中由于用药剂量提升可能出现体内药物蓄积,增加不良反应发生风险。羟考酮缓释片无封顶效应,故对爆发性疼痛患者可联用羟考酮缓释片与即效吗啡片,以弥补羟考酮缓释片的即时释放剂量不足、镇痛效果不理想等问题[7]。临床研究表明,以羟考酮缓释片作为背景用药联合即效吗啡片滴定治疗,不仅能够快速控制疼痛,还可缩短滴定治疗时间与滴定周期,减少医护工作量,提高患者的治疗依从性[8]。李静等[9]研究表明,将吗啡片与羟考酮缓释片联合滴定治疗中重度癌痛能够有效降低药物用量、改善患者的生活质量,并增强患者的疼痛与伴随症状管理能力。本研究中,C组以羟考酮缓释片作为癌痛滴定治疗的背景药物,在滴定治疗过程中予以羟考酮缓释片作为持续缓释成分,同时加用即效吗啡片进行滴定治疗,能够快速、持续地控制疼痛,缩短达到维持剂量的时间。结果显示,A、B、C组的镇痛总有效率及治疗后NRS评分无明显差异,但与A、B组比较,C组的滴定剂量显著降低,而KPS评分显著提高,认为联合滴定方案能够更好地改善患者的身心健康状态,与文献报道一致[9-11]。同时,C组在便秘发生率方面较B组显著降低,除嗜睡乏力发生率略有增加外,其余不良反应均表现出降低的趋势,C组的用药安全性更好。
综上所述,对中、重度癌痛患者应用羟考酮缓释片及吗啡片联合滴定治疗能够快速有效的控制疼痛,减少滴定剂量及滴定次数,减少不良反应并改善患者的生活质量,值得临床推广应用。
[1]王忠波.癌痛的评估和药物治疗[J].海南医学,2010,21(3)∶76-77.
[2]易基群,王秀文,梁继珍,等.羟考酮缓释片对老年癌痛患者滴定治疗的可行性及疗效[J].中国老年学杂志,2014,34(24)∶7082-7083.
[3]吴海霞,陈燕平,沈齐,等.羟考酮缓释片联合吗啡片在癌痛滴定治疗中的应用[J].肿瘤药学,2015,5(2)∶112-115.
[4]宋延海.盐酸羟考酮缓释片与硫酸吗啡缓释片对重度癌痛的疗效观察[J].中国实用医药,2015,10(11)∶150-151.
[5]程凯,蔡红,魏阳,等.盐酸羟考酮缓释片与盐酸吗啡缓释片治疗中度癌痛回顾性分析[J].中国药师,2014,17(7)∶1170-1172.
[6]于文军,刘杰.盐酸羟考酮缓释片与硫酸吗啡缓释片治疗重度癌痛疗效与不良反应比较分析[J].青岛医药卫生,2011,43(3)∶193-195.
[7]Samolsky Dekel BG,TomasiM,VasarriA,etal.Opioid titration w ith sustained⁃release oxycodone and immediate-release morphine for moderate/severe cancer pain∶a pilotassessmentof the CoDem protocol[J].JOpioid Manag,2014,10(1)∶29-38.
[8]原凌燕,柳珂,王湛,等.羟考酮控释片作为止痛背景用药在中重度癌痛滴定中的临床观察[J].临床肿瘤学杂志,2015,20(8)∶722-725.
[9]李静,庄雪梅,杨宗凡,等.奥施康定联合罗通定治疗老年晚期癌痛患者中重度疼痛的临床研究[J].现代肿瘤医学,2014,22(9)∶2191-2194.
[10]吴国武,曾娟紫,黄喜文,等.羟考酮缓释片联合吗啡片在中重度癌痛滴定治疗中的应用[J].中国肿瘤临床与康复,2014,21(5)∶599-601.
[11]黄琰菁,陈俊民,王海霞.盐酸羟考酮控释片治疗肝动脉化疗栓塞术后疼痛的疗效观察[J].海南医学,2013,24(17)∶2535-2537.
Clinical study of oxycodone sustained-release tablets combined w ith morphine titration regimen in treatment of patientsw ithmoderateand severe cancer pain.
PANGHua-chun,FU Jian,CENGLing-yang.DepartmentofOncology, thePeople'sHospitalof Xinxing County,Yunfu 527400,Guangdong,CHINA
Objective To observe the effectof oxycodone sustained-release tablets combined w ithmorphine titration regimen on patientsw ithmoderate and severe cancer pain.Methods A total of 126 patientsw ithmoderate and severe cancer pain,who admitted to Departmentof Oncology of our hospital from March 2012 to December 2015,were selected and divided into three groups(n=42)according to the digital random tablemethod,w ith 42 cases in each group. Group A,group B and group C were respectively treated with oxycodone sustained-release tablets,morphia titration therapy,and oxycodone sustained-release tablets and morphine titration.A fter 24h treatment,the clinical therapeutic effect of and adverse reactionswere compared.Results The analgesic efficiency rate of group A,group B and group C were respectively 88.10%(37/42),92.86%(39/42)and 97.62%(41/42),and the difference between the threegroupswasnotstatistically significant(P>0.05);the titration dose of group C[(55.24±2.18)mg/d]was significantly lower than thatof group A [(60.23±2.41)mg/d]and group B[(66.23±4.56)mg/d](P<0.05);the Numerical Rating Scale(NRS)scoresof digital pain evaluation in three groups after treatment[(2.07±1.15),(2.11±1.19),(1.92±1.02),respectively]were significantly lower than those before treatment(P<0.01);the Karnofsky Performance Status Scale(KPS)in three groups after treatment [(69.89±9.34),(68.12±8.79),(80.23±7.89)]were significantly higher than those before treatment(P<0.05);the incidence of constipation in group C[11.90%(5/42)]was significantly lower than that in group A[23.81%(10/42)and group B [57.90%(24/42)],P<0.05.Conclusion Oxycodone sustained-release tablets combined w ithmorphine titration regimen on patientsw ithmoderate and severe cancer pain has good safety and effectiveness.The jointapplication has the synergistic effect,which can reduce the dosageand sideeffectsof drug usage,and improve thequality of lifeof patients.
Cancerpain;Oxycodone sustained-release tablets;Morphine tablets;Clinicalcurativeeffect
R730.53
A
1003—6350(2016)16—2621—03
2016-01-26)
doi∶10.3969/j.issn.1003-6350.2016.16.014
庞华春。E-mail:puachun@126.com
