STAR Evolution检测纤维蛋白原的方法学性能评价
2016-11-04朱克清
朱克清
(安徽省宿州市医学检验中心 234000)
·临床研究·
STAR Evolution检测纤维蛋白原的方法学性能评价
朱克清
(安徽省宿州市医学检验中心234000)
目的评估STAR Evolution全自动血凝分析仪检测全血纤维蛋白原(FIB)浓度的临床性能。方法参照相关标准检测FIB的准确度、精密度、交叉污染率、线性范围及参考区间。结果水平1、水平2批内精密度(CV)分别为1.9%和3.17%;批间精密度(CV)分别为3.27%和2.89%;5 份室间质控品检测结果与靶值偏倚为 1.18%~4.30%;线性范围为1.95~9.81,r>0.975;SE%<8%,线性范围与厂家说明相近;FIB验证的参考区间为2.502~2.904g/L,比率R(%)=96.7%;交叉污染率为0.11%。结论STAGOEvolution全自动血凝分析仪检测FIB 的方法学性能良好,检验结果可靠、准确,可满足临床需要。
STAR Evolution;性能评价;纤维蛋白原
检测纤维蛋白原(FIB)含量是凝血试验筛检的最常用项目之一,STAR Evolution全自动凝血分析仪,是集免疫比浊法、凝固法及发色底物法等检测方法融于一体的全自动凝血分析系统[1]。临床诊断许多疾病的出凝血机制异常、抗凝、止血和溶栓药物的应用,都离不开凝血功能的检测[2]。依据医学实验室质量和能力认可准则(ISO15189文件)及美国病理家协会(CAP)实验室质量的要求,为保证仪器检测系统的有效性和完整性。现对该仪器检测FIB进行系统性评价,包括准确度、精密度、变异系数(CV)、携带交叉污染率、线性范围及参考区间等相关指标,验证结果是否准确可靠,能否满足临床需要。
1 资料与方法
1.1一般资料2015年10月1日至12月31日宿州市医学检验中心的就诊患者,采集抗凝血(3.8%枸橼酸钠抗凝剂,抗凝剂与血量1∶9 混合)标本,3 000 r/min离心10 min;当红细胞压积(HCT)<20%时,抗凝剂和血液比例按照公式调整:抗凝剂用量(L)=0.001 85(L)×(100-HCT)。全血标本混匀后采用STAR Evolutio 全自动凝血分析仪进行检测。
1.2仪器与试剂法国STAR Evolution全自动血凝分析仪,试剂盒由北京利德曼生物工程有限公司提供(批号015263K)。
1.3检测方法STAR Evolutio全自动凝血分析仪质控在控后,进行标本检测。
1.4评价方法
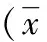
1.4.2准确度以参加2015年10月安徽省临床检验中心组织的室间质评(EQA)活动进行评价,对5份凝血室间质控品进行检测,靶值标准以临检中心回报的FIB靶值,相对偏倚计算采用本实验室上报结果与靶值比较,验证本实验室检测结果是否在质控允许范围之内。
1.4.3线性范围参照CLSI EP6-A文件[4],选取1份接近预期下限(L)和1份接近预期上限(H)血浆浓度,并按照5L、4L+1H、3L+2H、2L+3H、1L+4H、5H配制混合血浆,组成一系列评价标本,每个标本重复检测3次后计算其均值,并将实测值与理论值进行比较,计算SE%;以理论值为X轴,实测值为Y轴,回归方程Y=aX+b;线性范围判定标准是相关系数(r)>0.975或R2>0.95。
1.4.4携带交叉污染率取高值标本和低值标本1份,分别检测3次,获得 H1、H2、H3 和 L1、L2、L3,携带交叉污染率为(L1-L3)/(H3-L3)×100%,携带污染率小于或等于3%。
1.4.5参考范围参照CLSI C28-A2文件[5],选取60例体检标本(男、女各30例),同批分别检测各项目,计算均值、SD及结果落在正常参考范围的例数与总标本例数的比例,即R值,R>0.900则验证结果适用。
1.5统计学处理运用Excel2003统计软件进行数据分析。
2 结 果
2.1精密度验证结果批内、批间CV<8%,检测结果均小于厂家提供的标准,提示该仪器具有较高的批内和批间精密度。见表1。
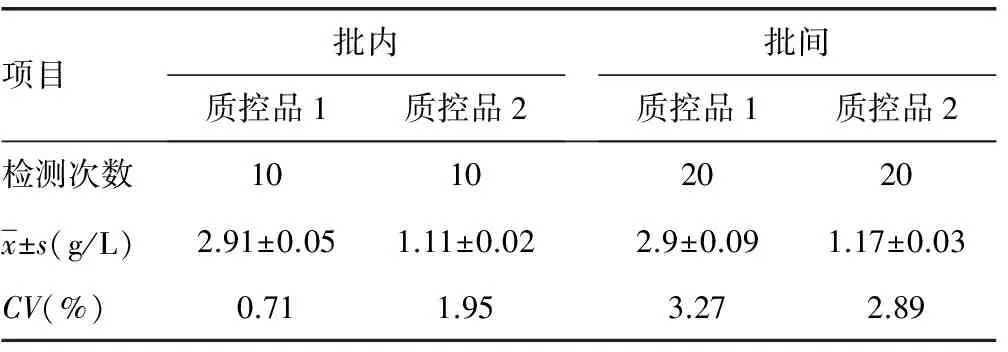
表1 FIB批内、批间检测不精密度检测结果
2.2准确度评价结果安徽省临床检验中心回馈的FIB室间质评结果显示,5份FIB室间质控品的检测结果与靶值偏倚为1.18%~4.30%,结果均为“符合”。采用厂家提供的正常及病理值质控血浆FIB,每个项目分别检测3次,均值分别为2.87、1.12 g/L,结果均在厂家提供的质控范围之内。见表2。
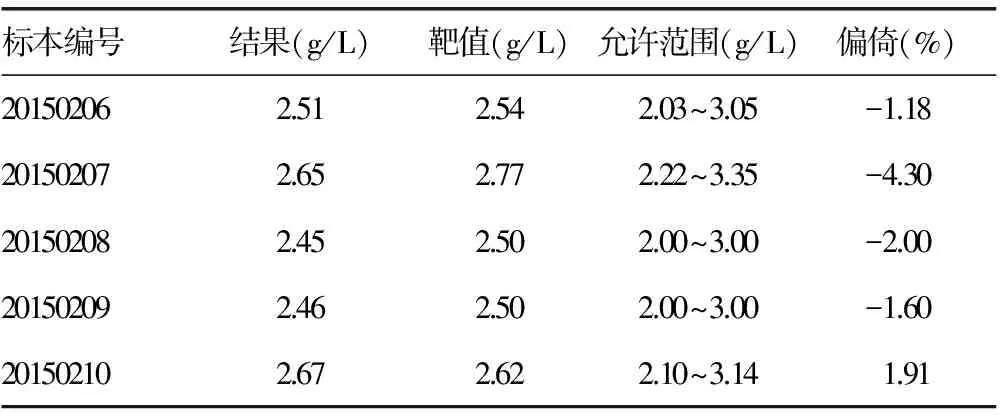
表2 FIB准确度评价结果
2.3线性范围评价结果以理论值为X轴,实测值为Y轴进行比较,结果偏差均在±8%之间,回归方程Y=1.029 8X+0.040 8,r=0.997 0,r2≥0.975,斜率a为0.97~1.03,线性范围为1.95~9.81 g/L。见表3和图1。
2.4交叉污染率评价结果3次连续检测的低浓度标本结果分别是L1为1.68 g/L,L2 为 1.7g/L,L3为1.67 g/L,3次连续检测的高浓度标本结果分别是H1为9.84 g/L,H2 为 9.86 g/L,H3为9.85 g/L,交叉污染率为 0.11%。
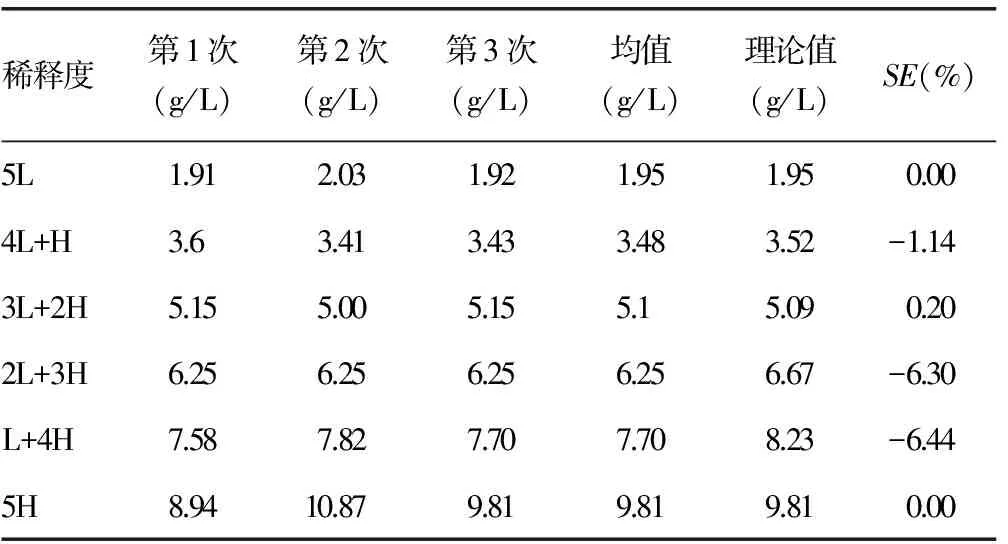
表3 FIB的线性范围评价结果
注:a=1.029 8;r=0.997 0。
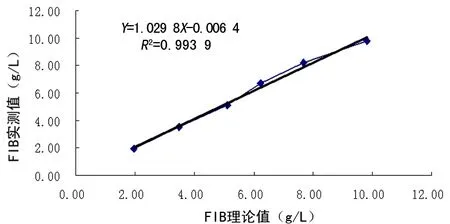
图1 STAR Evolutio检测FIB的实测值与理论值相关线性关系
2.5参考区间范围20例健康体检者FIB检测结果,χ2=3.33,S=0.41 g/L,比率R(%)=92.0%,95%CI为(2.30~3.82)g/L,其结果在厂家推荐的参考区间(2.0~4.0)g/L范围内。
3 讨 论
FIB是血栓性疾病的一个独立危险因子,也是反映血液高凝状态的指标之一,在诊断和评估糖尿病具有非常重要的临床价值[6]。由于各地区各实验室之间存在差异,应定期对检测仪器进行性能评价,保证检验质量的可靠性,也是开展实验室认可的重要措施。STAR Evolution全自动凝血分析仪可实现自动标本加样、自动稀释样品、自动搅拌试剂、重复测定、定标、控温、感应试剂和样品液面的自动化[7]。
本实验室通过检测FIB,对该仪器的性能进行评价,结果显示,STAR Evolution检测FIB批内精密度水平1、2的CV分别为1.95%和0.17%,批间精密度浓度的CV分别为3.27%和2.89%,均小于说明书要求的8%,提示STAR Evolution检测FIB精密度良好。EQA是由外部独立实验机构收集和反馈各实验室上报结果,是评价实验室检测结果准确性的重要依据[8]。本实验室检测的5份质控品FIB结果与靶值偏倚介于1.18%~4.30%,评价结果均为“符合”,通过室间质量评价,说明STAR Evolution有较高的准确度。本组系列稀释血浆标本结果表明,该仪器检测FIB的线性范围为(1.95~9.8)g/L,r=0.997 0,证实线性较好,实际工作中遇到高于检测范围的标本,仪器可自动对标本稀释倍数增加,获得较宽的检测范围,满足临床需求[9]。交叉污染率评价验证结果表明,交叉污染率仅为0.11%,结果准确可靠。随机抽取60例健康体检者,获得95%CI为(2.502~2.904)g/L,与说明书提供的参考区间基本一致。由于生活方式、习惯、饮食和仪器、方法、试剂、检测条件等各种原因,应当建立本实验室的参考区间,这将是下一步工作;同时也要重视检验前质量控制。
综上所述,STAR Evolution检测FIB具有良好的方法学性能,可为临床提供可靠、准确的检验结果,很好地满足临床需要。
[1]何洁静,李林海,全静雯,等.STA-R Evolution全自动凝血分析仪常见故障处理和维护保养[J].中国误诊学杂志,2009,9(31):7637-7638.
[2]陆红兵,孙文旦,王妍,等.STA-Compact型全自动血凝仪的性能评价[J].血栓与止血学,2005,11(4):174-175.
[3]NCCLS.EP5-A2 Evaluation of precision performance of quantitative measurement methods[S].Approved guideline-second edition,PA:NCCLS,2004.
[4]NCCLS.EP6-A Evaluation of the Linearity of quantitative measurement procedures[S].Statistecal approved guideline,PA:NCCLS,2003.
[5]NCCLS.C28-A2 How to define and determine reference intervals in the clinical laboratory[S].Approved guideline second edition,PA:NCCLS,2000.
[6]杨春生,梁金山,刘艳梅,等.缓冲液在全自动血凝仪内摆放位置对纤维蛋白原测定的影响[J].国际检验医学杂志,2013,34(8):1055.
[7]何艳,洪流.STA-R全自动血凝仪应用性能评价[J].河北医学,2011,17(2):263-266.
[8]陆明洋,邓海峰,李敏,等.肿瘤标志物室间质评结果的评价[J].标记免疫分析与临床,2011,18(2):135-136.
[9]许小英,于海涛,周存敏,等.某型号全自动血凝分析仪的性能评价[J].国际检验医学杂志,2012,33(11):1361-1362.
10.3969/j.issn.1673-4130.2016.19.051
A
1673-4130(2016)19-2771-03
2016-03-18
2016-05-23)
