维持性血液透析患者血管钙化相关因素研究
2016-11-01陈忠辉
陈忠辉,何 静
·临床医学·
维持性血液透析患者血管钙化相关因素研究
陈忠辉,何静
目的:观察维持性血液透析(MHD)患者的血管钙化情况,并分析相关检查结果,探讨影响MHD患者血管钙化的可能因素。方法:选取行MHD且透析时间>3个月的患者102例,行腹部侧位平片观察腹主动脉钙化情况,提示腹主动脉钙化为钙化组,未发现腹主动脉钙化为非钙化组。心脏及颈部血管彩超检查观察2组心脏瓣膜钙化及颈动脉内膜中层厚度(IMT),根据Kauppila法进行血管钙化评分,同时计算心血管钙化指数。并抽血检查血全段甲状旁腺激素、超敏C反应蛋白(hs-CRP)、血常规、肝肾功能、血糖、血脂、血钙、血磷、碱性磷酸酶等生化指标。结果:钙化组年龄、透析龄、血磷、是否糖尿病肾病、hs-CRP、IMT与非钙化组差异均有统计学意义(P<0.05~P<0.01)。相关性分析研究发现年龄、透析龄、hs-CRP、血磷和IMT与血管钙化评分均呈正相关关系(P<0.05~P<0.01)。logistic回归发现患者的年龄、透析龄、是否糖尿病和hs-CRP均是患者发生血管钙化的独立危险因素(P<0.01)。结论:MHD患者血管钙化现象较为常见,伴发糖尿病、高龄、长透析龄及微炎症状态可能是MHD患者血管钙化的独立危险因素。
血液透析;血管钙化;心血管钙化指数;糖尿病
近年来随着维持性血液透析(MHD)患者数量的增多,年龄和透析龄的增加,一系列严重的并发症逐渐在部分患者身上出现。血管钙化是MHD患者常见的并发症之一,目前病因并不十分清楚。但可以肯定的是血管钙化极大增加MHD患者心血管事件发生率,而心血管疾病又是MHD患者最常见的死亡原因。MHD患者导致血管钙化的因素较多,如钙磷沉积增加、甲状旁腺功能亢进、口服钙片、微炎症状态等。本研究分析透析时间>3个月患者的血管钙化情况,探讨影响MHD患者血管钙化的相关因素,为临床早期防治MHD患者血管钙化提供参考。现作报道。
1 资料与方法
1.1研究对象选取长期在我院血液净化中心行MHD的患者102例,其中男56例,女46例;年龄23~82岁;原发病:慢性肾小球肾炎58例,高血压病20例,糖尿病肾病15例,多囊肾2例,高尿酸性肾病3例,梗阻性肾病3例,间质性肾炎1例。所有患者透析时间均>3个月,且排除合并恶性肿瘤、骨髓瘤、淀粉样变、严重感染、严重营养不良的患者。透析方式为每周3次,每次透析时间为4 h,透析液钙浓度均为1.5%,血流量200~270 mL/min,透析液流量500 mL/min。透析器:威高F14型。所有患者均签署知情同意书。
1.2研究方法
1.2.1实验室检查所有患者均在透析前空腹抽取静脉血,检测常规项目包括血常规、血白蛋白、血糖、低密度脂蛋白(LDL-C)、三酰甘油(TG)、血钙、血磷、碱性磷酸酶(ALP)、超敏C反应蛋白(hs-CRP)、全段甲状旁腺激素(iPTH)等。透析次日测量患者腹围、体质量、血压等,记录患者年龄、透析龄、吸烟史等。根据血钙及血白蛋白计算校正钙,校正血钙值(mmol/L)=血清总钙测定值(mmol/L)+(40-血清白蛋白测定值)×0.025(mmol/L)。采用sysmex xe-2100型血常规仪,Olympus AU5400型生化检测仪。iPTH检测外送合肥金域医学检验所。
1.2.2影像学检查用彩色多普勒超声检查患者的颈动脉内膜中层厚度(IMT),心脏彩超判断患者心脏瓣膜钙化情况,所有扫描均由专人采用同一台超声仪完成。并行腹部侧位平片检查观察患者腹主动脉钙化情况。
1.3血管钙化评分方法根据腹主动脉的是否钙化分为钙化组和非钙化组。钙化组患者根据Kauppila法进行血管钙化评分(AACs评分),记录心脏瓣膜钙化情况,发现瓣环钙化>1 mm的强回声为心脏瓣膜钙化,同时计算心血管钙化指数(CCI)。CCI的计分方法为患者的年龄为60~69岁计1分,
≥70岁计2分;透析龄每2年计1分;主动脉和二尖瓣钙化各3分和1分;AACs 1~6分计2分,AACs≥7分计4分,所得总分为CCI[1]。
1.4统计学方法采用t(或t′)检验、χ2检验、直线相关和等级相关及logistic回归分析。
2 结果
2.1患者血管钙化情况本研究共纳入102名MHD患者,通过腹部侧位平片发现血管钙化共40例(见图1),钙化率为39.21%。钙化组患者中AACs评分≥8分占50%。CCI指数0~1分45例,2~4分27例,5分3例,6~8分19例,≥9分8例。
2.2钙化组和非钙化组患者一般资料比较2组患者年龄、透析龄、血磷、IMT、hs-CRP和是否糖尿病肾病间差异均有统计学意义(P<0.05~P<0.01)。而2组患者性别、是否吸烟、基础代谢率、腹围、平均动脉压、血糖、TG、LDL-C、血白蛋白、ALP、校正血钙和iPTH间差异均无统计学意义(P>0.05)(见表1)。
2.3MHD患者血管钙化因素相关分析相关性分析发现患者年龄、透析龄、hs-CRP、血磷和IMT与AACs评分均呈正相关关系(P<0.05~P<0.01),IMT与CCI指数呈显著正相关关系(r=0.745 7)(表2)

表1 血管钙化组与非钙化组患者一般资料比较
*示χ2值;△示t′值
表2MHD患者部分血管钙化因素与AACs评分的相关分析(n=102)
2.4MHD患者血管钙化相关因素的logistic回归分析logistic回归分析发现患者的年龄、透析龄、糖尿病肾病和hs-CRP均是患者发生血管钙化的独立危险因素(P<0.01),而诸多因素中hs-CRP的OR值最高(3.30)(见表3)。
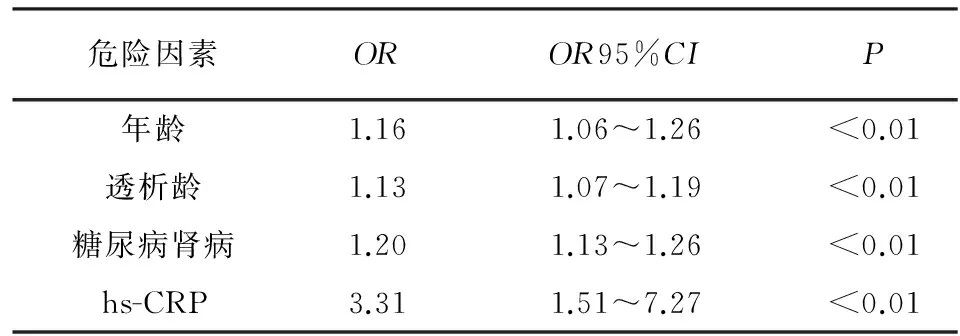
表3 影响AACs的危险因素的logistic回归分析
3 讨论
血管钙化是终末期肾脏病患者常见的并发症之一[2],是终末期肾脏病患者心血管疾病发生及死亡的重要危险因素,是预测患者发生心血管疾病的重要指标[3]。早期发现和治疗MHD患者血管钙化情况对减少其心血管疾病发生及发展有重要的临床意义。利用钙化积分计算动脉年龄能更好地预测心血管事件的发生[4],目前国际上主要有螺旋或电子束CT获取冠状动脉钙化评分(CACs)、AACs等方法。而CACs是评估血管钙化的金标准,但CACs费用较高,因此推荐用AACs和心脏瓣膜钙化联合计算CCI来判断心血管钙化情况。且已有研究[5]提出腹主动脉钙化和冠状动脉、胸主动脉钙化发生率相似,是MHD心血管死亡事件的独立预测因子。本研究就是通过检测患者腹部平片及心脏彩超来计算MHD患者的CACs。文献[6-7]报道血液透析患者血管钙化率为58.0%~79.8%,本组患者血管钙化率为39.2%,较文献报道低,分析原因可能为患者血液透析龄较短及选取的原发病为糖尿病的占比较少有关。
慢性肾衰竭患者导致血管钙化原因较多,DISTHABANCHONG[8]认为在慢性肾衰竭时过饱和的血钙、磷潴留,长透析龄是导致血管钙化的重要因素。本研究结果显示,钙化组与非钙化组患者年龄、透析龄、血磷、IMT、hs-CRP和是否糖尿病肾病间差异均有统计学意义(P<0.05~P<0.01),充分说明诸多因素在血管钙化形成中的重要作用,与相关报道[9]一致。相关分析发现年龄、透析龄、hs-CRP、血磷和IMT与AACs评分均呈正相关关系(P<0.05~P<0.01)。
尿毒症患者普遍存在钙磷代谢异常。新近的研究发现,在慢性肾脏病患者中,高血磷是尿毒症患者血管钙化的独立危险因素,高磷、钙磷乘积增加能诱导血管平滑肌细胞向成骨样细胞转化,从而促进血管钙化[10]。血钙磷的代谢紊乱是异位钙化的必要条件。本组研究显示钙化组与非钙化组血磷差异有统计学意义(P<0.01),与相关报道一致,充分说明了血磷在维持性血液透析患者中血管钙化形成中的起重要作用。但是患者血磷不是血管钙化的独立危险因素,分析原因可能为钙化组患者血磷平均值较非钙化组差异并不大,在与年龄、透析龄、hs-CRP的比较中明显较小,血磷对血管钙化的影响被弱化。且本研究发现高的iPTH并不是血管钙化的独立危险因子,其原因可能为我院尿毒症患者在长期口服骨化三醇后未及时监测血iPTH,导致部分血iPTH过度抑制,甚至出现甲状旁腺功能减退。
SHROFF等[11]研究显示,慢性肾脏病患者可通过诱导血管平滑肌细胞凋亡而加速患者血管的钙化。提示随着患者年龄的增加,血管平滑肌细胞的衰老、凋亡可加速患者血管钙化。本研究也发现年龄及透析龄是MHD患者血管钙化的重要因素。但在logistic回归中发现年龄及透析龄OR值并不比糖尿病肾病及hs-CRP的OR值高,与国内外部分报道[1-14]透析龄及年龄是MHD患者血管钙化强烈的危险因素不相符,分析原因可能我们选取的研究对象透析龄及年龄均较报道的短有关。MHD患者中往往存在微炎症状态,究其原因与感染等因素有关,而hs-CRP是反映患者体内微炎症状态的很好指标。LIU等[12]对其具体机制研究发现炎症可通过干扰低密度脂蛋白受体通路而加速终末期肾脏病患者的血管钙化,类似于炎症在动脉粥样硬化中的作用机制。本研究检测MHD患者hs-CRP,结果显示hs-CRP是血管钙化的独立危险因素,且OR值较高。与相关报道[13-14]一致。充分说明了炎症在MHD患者血管钙化形成中的重要作用。
冠状动脉和心脏瓣膜钙化患者中糖尿病患者明显增加,且一半心血管死亡患者存在糖尿病[15]。研究[16-17]发现O位N-乙酰葡糖胺糖基化及晚期糖化终产物在调节糖尿病血管钙化中起到重要作用。本实验同样验证了糖尿病是MHD患者血管钙化的独立危险因素。而糖尿病本身容易导致钙磷代谢紊乱、微炎症状态,这也是糖尿病患者容易导致血管钙化的病因之一。本研究将患者的IMT与CCI指数及AACs评分作一相关性分析,发现我院MHD患者IMT与CCI指数及AACs评分均呈显著正相关关系(P<0.01)。KRASNIAK等[14]在2007年检测了73 例维持血透患者的IMT及CACS,发现二者有显著的相关性,本实验得出了类似结论。我们认为颈动脉和冠状动脉硬化间存在着密切的关系,因颈动脉位置表浅,和冠状动脉具有相同的解剖结构特点和动脉粥样硬化机制,因此在预测心血管发病方面较大优势。
[1]贾玉凤,徐斌,龚德华,等.维持性血液透析患者心血管钙化的发生率及分布特点[J].肾脏病与透析肾移植杂志,2014,5(23):401.
[2]YEH HT,HUANG IJ,CHEN CM,etal.Regression of vascular calcification following an acute episode of calciphylaxis:a case report[J].J Med Case Rep,2014,8(1):52.
[3]LIABEUF S,OKAZAKI H,DESIARDINS L,etal.Vascular calcification in chronic kidney disease:are biomarkers useful for probing the pathobiology and the health risks of this process in the clinical scenario[J].Nephrol Dial Transplant,2014,29(7):1275.
[4]LIBEMAN M,PESARO AE,CARMO LS,etal.Vascular calcification:pathophysiology and clinical implications[J].Einstein (Sao Paulo),2013,11(3):376.
[5]RAGGI P,BELLASI A,FERRAMOSCA E,etal.Association of Pulse wave velocity with vaular and valvular caldfication in hemodiaIysis patients[J].Kidney Int,2007,71(8):802.
[6]PENCAK P,CZERWIENSKA B,FICEK R,etal.Calcification of coronary arteries and abdominal aorta in relation to traditional and novel risk factors of atherosclerosis in hemodialysis patients[J].BMC Nephrol,2013,14(1):10.
[7]ABDELMALEK JA,STARK P,WALTHER CP,etal.Associations between coronary calcification on chest radiographs and mortality in hemodialysis patients[J].Am J Kidney Dis,2012,60(6):990.
[8]DISTHABANCHONG S.Vascular calcification in chronic kidney disease:Pathogenesis and clinical implication[J].World J Nephrol,2012,1(2):43.
[9]MCCARTY MF,DINICOLANTONIO JJ.The molecular biology and pathophysiology of vascular calcification[J].Postgrad Med,2014,126(2):54.
[10]CROUTHAMEL MH,LAU WL,LEAF EM,etal.Sodium-dependent phosphate cotransporters and phosphate-induced calcification of vascular smooth muscle cells:redundant roles for PiT-1 and PiT-2[J].Arterioscler Thromb Vasc Biol,2013,33(11):2625.
[11]SHROFF RC,MCNAIR R,SKEPPER JN,etal.Chronic mineral dysregulation promotes vascular smooth muscle cell adaptation and extracellular matrix calcification[J].J Am Soc Nephrol,2010,21(1):103.
[12]LIU J,MA KL,GAO M,etal.Inflammation disrupts the LDL receptor pathway and accelerates the progression of vascular calcification in ESRD patients[J].PLoS One,2012,7(10):e47217.
[13]KIU WEBER CI,DUCHATEAU-NGUYEN G,Solier C,etal.Cardiovascular risk markers associated with arterial calcification in patients with chronic kidney disease Stages 3 and 4[J].Clin Kidney J,2014,7(2):167.
[14]KRASNIAK A,DROZDZ M,PASOWICZ M,etal.Factors involved in vascular calcification and atherosclerosis in maintenance haemodialysis patients[J].Nephrol Dial Transplant,2007,22(2):515.
[15]AVOGARO A,RATTAZZI M,FADINI GP,etal.Ectopic calcification in diabetic vascular disease[J].Expert Opin Ther Targets,2014,18(5):595.
[16]HEATH JM,SUN Y,YUAN K,BRADLEY WE,etal.Activation of AKT by O-linked N-acetylglucosamine induces vascular calcification in diabetes mellitus[J].Circ Res,2014,114(7):1094.
[17]BRODEUR MR,BOUVET C,BOUCHARD S,etal.Reduction of advanced-glycation end products levels and inhibition of RAGE signaling decreases rat vascular calcification induced by diabetes[J].PLoS One,2014,9(1):e85922.
(本文编辑刘梦楠)
Analysis of the related factors of the angiosteosis in patients with maintenance hemodialysis
CHEN Zhong-hui,HE Jing
(DepartmentofNephrology,ThePeople′sHospitalofXuancheng,XuanchengAnhui242000,China)
Objective:To observe the vascular calcification,analyze the related examination results,and explore its possible influencing factor in patients with maintenance hemodialysis(MHD).Methods:One hundred and two MHD patients with time more than 3 months were selected,and divided into the calcification group and non-calcification group according to the abdominal aorta calcification diagnosed by lateral plain film of abdomen.The cardiac valve calcification and carotid artery intima-media thickness(IMT) in two groups were observed by the heart and neck vascular ultrasound examination.The abdominal aorta calcification score(AACs) was analyzed according to the Kauppila,and the cardiovascular calcification index was calculated in two groups.The biochemical indicators of serum intact parathyroid hormone,high sensitive C reactive protein(hs-CRP),blood routine test,liver and renal function,and blood glucose,lipid,calcium,phosphorus and alkaline phosphatase alkaline phosphatase between two groups were compared.Results:There were significant differences in the age,age of dialysis,blood phosphorus,diabetic nephropathy,hs-CRP and IMT between two groups(P<0.05 toP<0.01).The correlation analysis showed that the age,age of dialysis,blood phosphorus,hs-CRP and IMT of patients were positively correlated with AACs scores(P<0.05 toP<0.01).Logistic regression showed that the age,age of dialysis,diabetes and hs-CRP of patients were the independent risk factor of vascular calcification(P<0.01).Conclusions:The vascular calcification is more common in MHD patients,and the risk factors of vascular calcification in patients with MHD may be associated with diabetes,aging,long duration of dialysis and microinflammatory.
hemodialysis;vascular calcification;cardiovascular calcification index;diabetes
2015-03-15
单位] 安徽省宣城市人民医院 肾内科,242000
[作者简介] 陈忠辉(1980-),男,硕士,主治医师.
1000-2200(2016)09-1207-04
R 458.5
ADOI:10.13898/j.cnki.issn.1000-2200.2016.09.028
