六味地黄口服液薄层色谱鉴别研究*
2016-10-29刘金坤白殊同高洪燕喻晓雯
刘金坤,王 琴,白殊同,高洪燕,喻晓雯,吴 斌
(重庆市中医院,重庆400021)
六味地黄口服液薄层色谱鉴别研究*
刘金坤,王琴,白殊同,高洪燕,喻晓雯,吴斌
(重庆市中医院,重庆400021)
目的建立鉴别六味地黄口服液中中药材的薄层色谱(TLC)法。方法采用TLC法对六味地黄口服液中牡丹皮、山茱萸、泽泻、茯苓、山药5味中药进行定性鉴别。结果薄层色谱分离度好,鉴别斑点清晰,特征斑点专属性强,阴性对照品溶液无干扰。结论该法结果准确、可靠、重复性好,可用于六味地黄口服液的质量控制。
六味地黄口服液;薄层色谱法;牡丹皮;山茱萸;泽泻;茯苓;山药
六味地黄方具有滋补肾阴之功效,用于治疗头晕耳鸣、腰膝酸软、遗精盗汗等。其传统的剂型为大蜜丸,随着制药技术的发展,逐渐出现了水丸、水蜜丸、浓缩丸、片剂、胶囊剂、滴丸、口服液等不同的剂型[1-2]。六味地黄口服液是六味地黄丸的改进剂型,由熟地、山茱萸、牡丹皮、泽泻、山药及茯苓6味中药组方,具有口感好、服用方便、起效迅速、吸收快、生物利用度高等优点。目前,口服液质量标准采用薄层扫描法测定山茱萸中熊果酸的含量,以吸收系数法测定牡丹皮中丹皮酚的含量[3]。2010年版、2015年版《中国药典(一部)》均无六味地黄口服液的薄层鉴别[4]。笔者采用薄层色谱(TLC)法鉴定其中的牡丹皮、山茱萸、泽泻、茯苓、山药5味中药材,作为检测该制剂的指标,以期为改进该制剂的质量标准提供参考。
1 仪器与试药
1.1仪器
BT25S型电子天平(德国赛多利斯集团公司); Q-250DB型超声波清洗器(昆山市超声波仪器有限公司);HH-S11-2型恒温水浴锅(上海跃进医疗器械厂),薄层层析硅胶G板、GF254板(青岛海洋化工集团公司,10 cm×20 cm);UV-1型三用紫外分析仪(上海顾村电光仪器厂);ThermoPico17离心机(美国Thermo Fisher Scientific公司);TGL-16G型高速离心机(上海医用分析仪器厂);Thermo ScientificTMBarnsteadTMPacificTMTIIⅡ级纯水仪(美国Thermo Fisher Scientific公司)。
1.2试药
牡丹皮对照药材(批号为121490-201102)、山茱萸对照药材(批号为121495-200702)、泽泻对照药材(批号为121081-201406)、茯苓对照药材(批号为121117-201308)、山药对照药材(批号为121137-201305),均由中国食品药品检定研究院提供;六味地黄口服液(安徽黄山市天目药业有限公司,批号为141201,150501,150801,规格为每瓶10 mL);甲醇、乙酸乙酯、正己烷、氯仿、石油醚、甲苯、甲酸甲酯、甲酸(分析纯,重庆西南化学试剂有限公司),水为超纯水。
2 方法与结果
2.1牡丹皮
取样品(批号为150801)10 mL,50℃烘干,残渣加甲醇1 mL溶解,作为供试品溶液。另取牡丹皮对照药材1 g,加甲醇20 mL,超声提取30 min,离心5 min (8 000 r/min),滤过,上清液浓缩为1 mL,作为对照药材溶液。按六味地黄口服液处方制备缺牡丹皮阴性样品,同法制成阴性对照品溶液。吸取上述3种溶液各2 μL,分别点于同一硅胶G254薄层板上,以氯仿-醋酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以2%香草醛硫酸乙醇溶液,紫外灯(254 nm)检测。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰,见图1A。
2.2山茱萸
取样品(批号为150801)10 mL,50℃烘干,残渣加甲醇1 mL溶解,作为供试品溶液。取山茱萸对照药材粉末0.5 g,加醋酸乙酯10 mL,超声处理15 min,离心5 min (8 000 r/min),滤过,滤液蒸干,残渣加甲醇1 mL溶解,作为对照药材溶液。按六味地黄口服液处方制备缺山茱萸阴性样品,同法制成阴性对照品溶液。吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以甲苯-醋酸乙酯-冰醋酸(12∶4∶0.5)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品溶液色谱中,与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰,见图1B。
2.3泽泻
取样品(批号为150801)10 mL,50℃烘干,残渣加甲醇1 mL溶解,作为供试品溶液。取泽泻对照药材粉末0.5 g,加甲醇10 mL,超声处理15 min,离心5 min (8 000 r/min),滤过,滤液蒸干,残渣加甲醇1 mL溶解,作为对照药材溶液。按六味地黄口服液处方制备缺泽泻阴性样品,同法制成阴性对照品溶液。吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以环己烷-醋酸乙酯-丙酮(4∶2∶1)为展开剂,展开,取出,晾干,喷以2%香草醛硫酸溶液-乙醇(4∶1)溶液,在105℃加热至斑点显色清晰。供试品溶液色谱中,与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰,见图1C。
2.4山药
取样品(批号为150801)10 mL,50℃烘干,残渣加甲醇1 mL溶解,作为供试品溶液。取山药对照药材粉末1 g,加甲醇20 mL,加热回流1 h,离心5 min (8 000 r/min),滤过,滤液蒸干,残渣加入甲醇1 mL溶解,作为对照药材溶液。按六味地黄口服液处方制备缺山药阴性样品,同法制成阴性对照品溶液。吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品溶液色谱中,与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液无干扰,见图1D。
2.5茯苓
取样品(批号为150801)10 mL,50℃烘干,残渣加甲醇1 mL溶解,作为供试品溶液。取茯苓对照药材粉末2 g,加乙醚20 mL,超声处理30 min,离心5 min (8 000 r/min),滤过,滤液蒸干,残渣加甲醇1 mL溶解,作为对照药材溶液。按六味地黄口服液处方制备缺泽泻阴性样品,同法制成阴性对照品溶液。吸取上述3种溶液各2 μL,分别点于同一硅胶G254薄层板上,以氯仿-醋酸乙酯-甲酸(10∶1∶0.2)为展开剂,展开,取出,晾干,紫外灯(254 nm)检测。供试品溶液色谱中,与对照药材溶液色谱相应位置上,显相同颜色的斑点,阴性对照品溶液无干扰,见图1E。
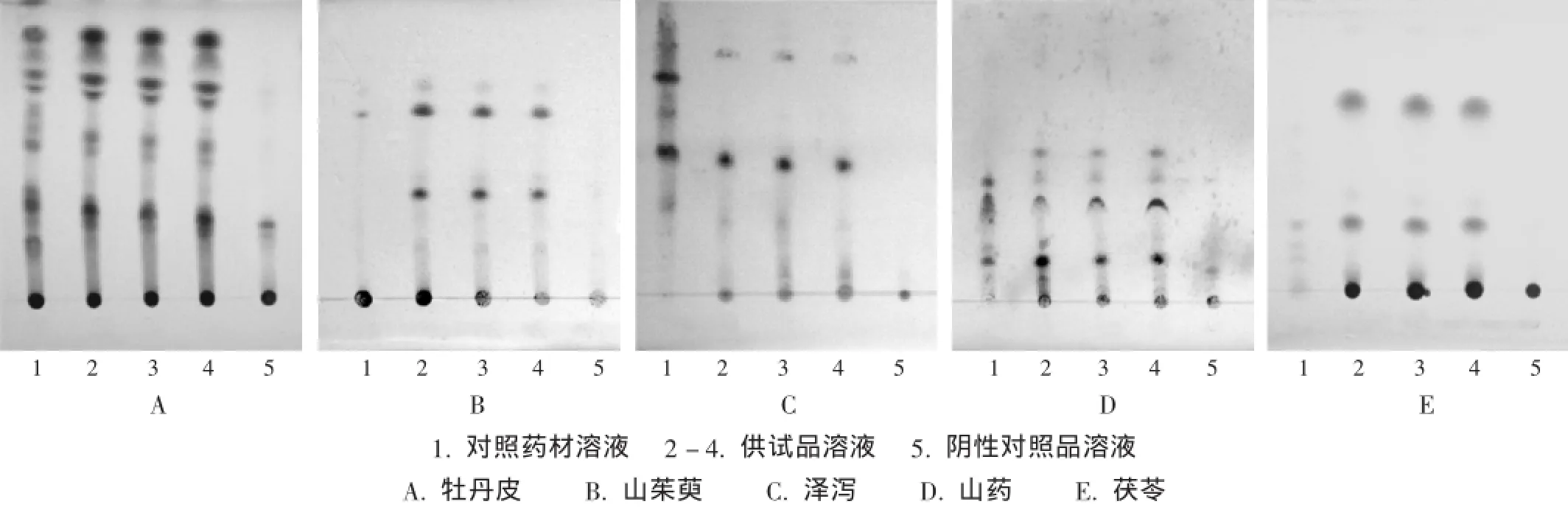
图1 薄层色谱图
3 讨论
2015年版《中国药典(一部)》记载了六味地黄丸、浓缩丸、软胶囊、颗粒剂的薄层色谱鉴别方法,部分方法提取、鉴别比较烦琐,未见口服液的鉴别方法。因此,笔者对六味地黄口服液剂型进行薄层色谱鉴别,并对药典的方法进行了改进。本试验直接采用醋酸乙酯超声提取,按照熊果酸的检测方法,采用甲苯-醋酸乙酯-冰醋酸(12∶4∶0.5)为展开剂,色谱斑点唯一,适用于鉴别[5-6]。
鉴别牡丹皮药材时,按照2015年版《中国药典(一部)》检测方法,以环己烷-醋酸乙酯-冰醋酸(4∶1∶0.1)为展开剂,以2%香草醛硫酸乙醇溶液为显色剂,但色谱斑点较少,同时斑点分离效果并不理想。因此,改用氯仿-醋酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,可以得到多个斑点[7-8]。
鉴别茯苓药材时,以1∶1的乙醚-石油醚(60~90℃)为展开剂展开,晾干,喷以磷钼酸试液,105℃下加热显色,结果斑点拖尾较严重,且阴性对照品溶液有干扰,故未采用此方法。后采用10%硫酸乙醇溶液作为显色试剂,可检测出色谱斑点。但紫外检测法既可减少硫酸试剂的使用,又可灵敏地检测色谱斑点[9-10]。
鉴别泽泻药材时,曾尝试乙醚-食盐水、氯仿-盐酸-水混合液的方法制备供试品溶液,结果显色斑点较少,故改为甲醇处理,同时展开剂改为环己烷-醋酸乙酯-丙酮(4∶2∶1),获得较理想的斑点[11-12]。
鉴别山药药材时,2015年版《中国药典(一部)》以二氯甲烷为提取试剂,对环境污染较大,改进后采用甲醇提取。同时,对其中展开剂加以改良,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂。试验中曾以10%磷钼酸乙醇溶液、茚三酮、10%硫酸乙醇显色剂,经比较,以10%硫酸乙醇显色效果最佳[13-14]。
[1]李全斌.六味地黄方研究进展[J].辽宁中医药大学学报,2013,15(1):217-219.
[2]郭泉,胡容峰,高松,等.六味地黄制剂的研究现状与中药制剂质量标准的构建[J].现代中药研究与实践,2014,28(4):78-81.
[3]韩燕全,洪燕,黄正明,等.六味地黄口服液的质量标准提高研究[J].中国实验方剂学杂志,2009,15(11):9-11.
[4]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:7-9.
[5]谭梅.六味地黄散薄层色谱鉴别方法的改进[J].中国兽药杂志,2005,39(6):27-28.
[6]张先林,杨大凯,刘志辉,等.降压益肾颗粒质量标准研究[J].中国中医药信息杂志,2008,15(11):45-47.
[7]谢培山,周嘉琳,王永山.中药配方颗粒薄层色谱彩色图集[M].南京:江苏科学技术出版社,2004:75.
[8]张永玲.妇炎清颗粒的薄层色谱鉴别[J].中国药业,2007,16(19):25.
[9]胥秀英,易中宏,郑一敏,等.茯苓药材质量标准研究[J].中药材,2008,31(4):597-599.
[10]王玉鹏,黄顺旺,陈师农,等.白柏颗粒质量标准初步研究[J].中国药业,2016,25(2):72-74.
[11]巩丽萍,王少云,侯准,等.中药泽泻质量控制方法的研究[J].中药新药与临床药理,2006,17(2):125-127.
[12]马莹.六味地黄胶囊中3种药材的薄层色谱鉴别[J].中国药业,2010,19(20):31-32.
[13]郑颖,蓝闽波,张宁.健胃消食片中山楂及山药的薄层色谱鉴别[J].时珍国医国药,2006,17(8):1 512-1 513.
[14]戴军.肤美康胶囊的质量控制研究[J].中国药业,2014,23(15):43-45.
Identification of Liuwei Dihuang Oral Liquid by TLC
Liu Jinkun,Wang Qin,Bai Shutong,Gao Hongyan,Yu Xiaowen,Wu Bin
(Chongqing Traditional Chinese Medicine Hospital,Chongqing,China400021)
ObjectiveTo explore the thin layer chromatography(TLC)method for identification of the Chinese herbal components in Liuwei Dihuang Oral Liquid.MethodsThe method for determination of Paeonia suffruticosa,Cornus officinalis,Alisma,Fuling,and Chinese Yam in Liuwei Dihuang Oral Liquid was established utilizing TLC method.ResultsThe TLC spots were fairly clear and the characteristic spots corresponded well while the negative control revealed no interference.ConclusionTLC is proved to be convenient,accurate and stable for identifying the five herbs,which can be served as the quality control of Liuwei Dihuang Oral Liquid.
Liuwei Dihuang Oral Liquid;TLC;Paeonia suffruticosa;Cornus officinalis;Alisma;Fuling;Chinese Yam
R284.1;R286.0
A
1006-4931(2016)13-0068-03
刘金坤(1985-),男,执业中药师,研究方向为中药药理作用机制,(电话)023-67633702(电子信箱)liujinkun007@163.com;吴斌,博士研究生,主任中医师,主要从事风湿病与老年病的基础与临床研究工作,本文通讯作者,(电子信箱)wuubinn@126.com。
2016-02-20;
2016-03-02)
*重庆市科委科技专项,项目编号:cstc2015jbky330025011;重庆市卫生局中医药科技重点项目,项目编号:2012-1-6。
