灵芝孢子多糖含量不同方法测定的比较※
2016-10-26罗爱勤
罗爱勤 陈 亮 李 菁
(广州白云山汉方现代药业有限公司/中药提取分离过程现代化国家工程研究中心,广州510240)
灵芝孢子多糖含量不同方法测定的比较※
罗爱勤陈亮李菁
(广州白云山汉方现代药业有限公司/中药提取分离过程现代化国家工程研究中心,广州510240)
目的比较3种不同方法测定灵芝孢子中多糖的含量。方法采用2015版《中国药典》一部灵芝药材项下收载的多糖含量测定方法,《保健食品功效成分检测方法》(白鸿主编)中粗多糖的苯酚-硫酸分光光度测定法和葡聚糖的分光光度测定法测定灵芝孢子中多糖含量。结果10批灵芝孢子中,药典蒽酮硫酸法测得的多糖百分含量均值为2.05%;苯酚-硫酸法测得的多糖百分含量均值为2.72%;葡聚糖分光光度法测得的多糖百分含量均值为1.09%。结论3种不同测定方法测定灵芝孢子的多糖含量存在较大的差异。
灵芝孢子;多糖;含量测定
灵芝是多孔菌科灵芝属的一种药用真菌,在我国具有悠长的药用历史[1],灵芝孢子是灵芝在生长成熟期从菌盖弹射出来的极其细小的卵状生殖孢子,灵芝孢子含有丰富的多糖、三萜、脂肪酸以及多种氨基酸及微量元素,在调节免疫、抑制肿瘤、调节血脂、降低血糖方面有明显作用[2-6]。近年来,灵芝孢子相关保健食品等产品发展迅速,市场上含灵芝孢子的产品繁多,但是,各类灵芝孢子产品的多糖含量却参差不齐。目前,《中国药典》(2015版)一部仅收录了灵芝标准,规定灵芝的多糖含量测定法[7],但灵芝孢子未载入药典,尚未有灵芝孢子多糖含量测定法的国家标准。市售的灵芝孢子相关产品的多糖含量测定法,主要是企业根据中国药典或《保健食品功效成分检测方法》制定的企业标准,不同方法测得多糖含量的差异较大。本文采用三种测定法分别对十批灵芝孢子进行多糖含量测定,比较不同方法的差异[8,9],为标准化灵芝孢子多糖含测的必要性提供了依据。
1 仪器与试药
1.1仪器BS210S型电子天平(德国Sartorius)、SHIMADZU UV-2550(岛津杭州)、HHS型电热恒温油浴锅(上海博迅实业有限公司医疗设备厂)、W201B恒温水浴锅(上海申顺生物科技有限公司)、LXJ-IIB低速大容量多管离心机(上海棱谱仪器仪表有限公司)
1.2试药灵芝孢子(广州白云山汉方现代药业有限公司);D-无水葡萄糖对照品(批号:110833-201205,中国食品药品检定研究院);相对分子质量5×105的葡聚糖对照品(Sigama公司);铜试剂溶液(广州白云山汉方现代药业有限公司);乙醇、蒽酮、苯酚、硫酸、氢氧化钠等均为分析纯;水为纯化水。
2 方法与结果
2.1药典法测定灵芝孢子中多糖含量
2.1.1对照品溶液的制备取无水葡萄糖对照品适量,精密称定,加水制成每1 mL含0.114 mg的溶液,即得。
2.1.2标准曲线的制备精密量取对照品溶液0.2、0.4、0.6、0.8、1.0、1.2、1.6、2.0 mL,分别置10mL具塞试管中,各加水至2.0 mL,迅速精密加入硫酸蒽酮溶液(精密称取蒽酮0.1 g,加硫酸100 mL使溶解,摇匀)6 mL,立即摇匀,放置15 min后,立即置冰浴中冷却15分钟,取出,以相应的试剂为空白,照紫外-可见分光光度法(通则0401),在625 nm波长处测定吸光度,以吸光度为纵坐标,质量为横坐标,绘制标准曲线,见表1、图1。

表1 葡萄糖标准曲线
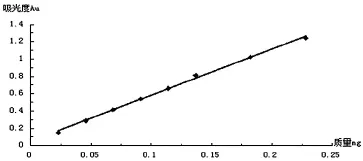
图1 葡萄糖标准曲线
2.1.3供试品溶液的制备取灵芝孢子,破壁,精密称取破壁孢子粉2 g,置圆底烧瓶中,加水60 mL,静置1 h,加热回流4 h,趁热滤过,用少量热水洗涤滤器和滤渣,将滤渣及滤纸置烧瓶中,加水60 mL,加热回流3 h,趁热滤过,合并滤液,置水浴上蒸干,残渣用水2.5 mL溶解,边搅拌边缓慢滴加乙醇37.5 mL,摇匀,在4℃放置12 h,离心,弃去上清液,沉淀物用热水溶解并转移至50 mL量瓶中,放冷,加水至刻度,摇匀,取溶液适量,离心,精密量取上清液2 mL置25 mL量瓶中,加水至刻度,摇匀,即得。
2.1.4样品测定精密量取供试品溶液2 mL,置10 mL具塞试管中,照标准曲线制备项下的方法,自“迅速精密加入硫酸蒽酮溶液6 mL”起,同法操作,测定吸光度,从标准曲线上读出供试品溶液中无水葡萄糖的含量,计算,即得。计算公式:多糖含量=(A样品-0.05)÷5.3238× 312.5÷M样品÷1000×100%;其中,A样品是样品的吸光度值(Au),M样品为样品的称样量(g)。结果见表2。
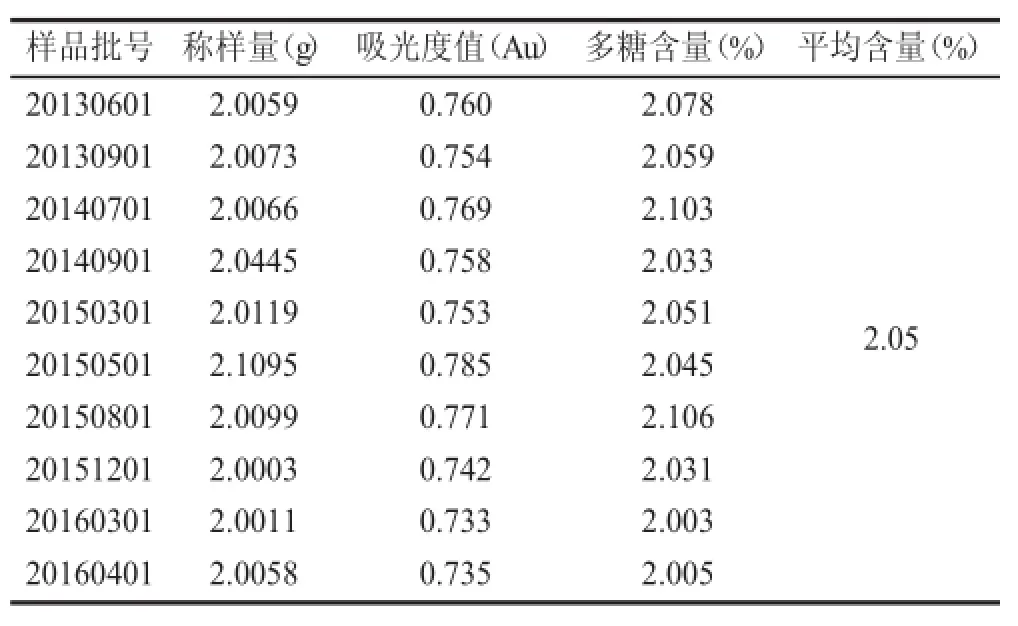
表2 灵芝孢子粉的多糖含量测定结果
从表2结果可知,药典蒽酮硫酸法测得10批灵芝孢子的多糖含量均值为2.05%。
2.2苯酚硫酸分光光度法测定灵芝孢子中多糖的含量[10](1)对照品溶液的制备取无水葡萄糖适量,精密称定,加水制成每1 mL含0.03648 mg的溶液,即得。
(2)标准曲线的制备精密量取对照品溶液0.0、1.0、1.5、2.0、2.5、3.0、3.5、4.0分别置于25 mL比色管中,补加水至2.0 mL,加入5%苯酚溶液1.0 mL,摇匀,迅速加入硫酸10 mL,摇匀,置沸水浴中加热2分钟,取出,冷却至室温,用分光光度计在485 nm波长处以试剂空白为参比,1 cm比色皿测定吸光度值。以葡萄糖质量为横坐标,吸光度值为纵坐标,绘制标准曲线,见表3和图2。

表3 葡萄糖标准曲线
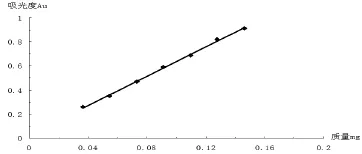
图2 葡萄糖标准曲线
(3)供试品溶液的制备。取灵芝孢子,破壁,精密称取破壁孢子粉1.2 g,置100 mL锥形瓶中,加水约80 mL,于沸水浴中加热1 h,冷却至室温,滤过。滤液置100 mL量瓶中,加水稀释至刻度,摇匀,准确吸取稀释液2.0 mL,加入无水乙醇8.0 mL,混匀,于4℃冰箱静置4 h以上,以4000 r/min离心5 min,弃去上清液,残渣用80%(V/V)乙醇溶液数毫升洗涤,离心弃去上清液,反复操作3次。残渣用水溶解并定容10 mL,摇匀,即得。
(4)样品测定。精密量取供试品溶液2 mL,置25 mL比色管中,照标准曲线制备项下的方法,自“加入5%苯酚溶液1.0 mL”起,同法操作,测定吸光度,从标准曲线上读出供试品溶液中无水葡萄糖的含量,计算,即得。计算公式:
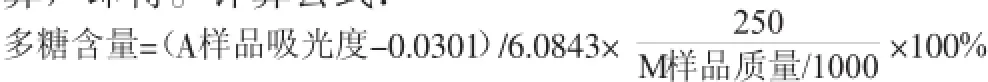
其中,A样品是样品的吸光度值(Au),M样品为样品的称样量(g)。结果见表4。
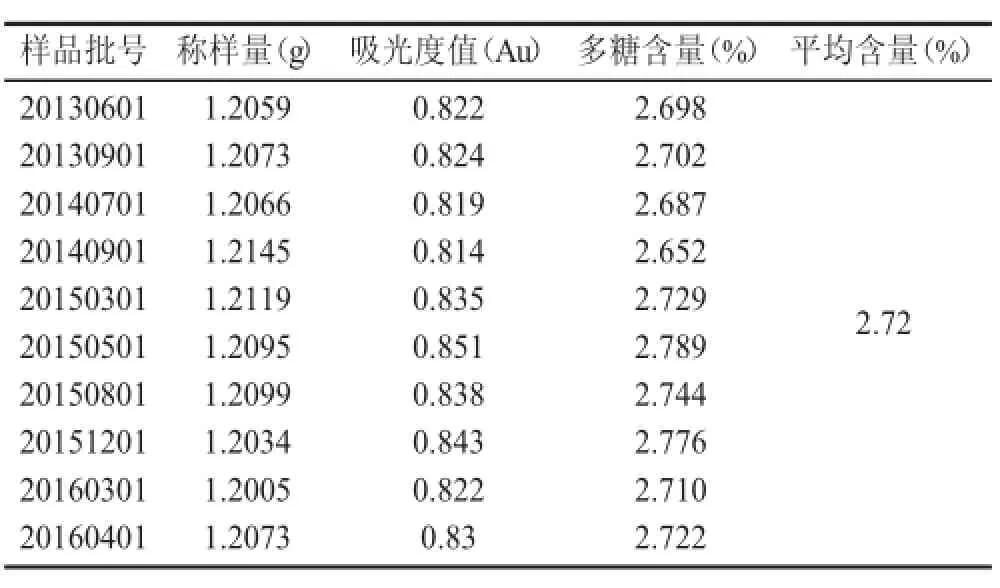
表4 灵芝孢子粉中多糖的含量
从表4结果可知,苯酚硫酸法测得10批灵芝孢子的多糖含量均值为2.72%。
2.3葡聚糖分光光度法测定灵芝孢子中多糖的含量[10](1)葡聚糖标准储备液配制准确称取相对分子量5×105已干燥至恒重的葡聚糖标准品0.10225 g,加水溶解,并定容至10 mL,混匀,置冰箱中保存。此溶液1 mL含10.225 mg葡聚糖。
(2)葡聚糖标准使用液配制吸取葡聚糖标准储备液1.0 mL,置于100 mL容量瓶中,加水至刻度,混匀,置冰箱中保存。此溶液1 mL含葡聚糖0.10225 mg。
(3)标准曲线制备。准确吸取葡聚糖标准使用液0、0.20、0.40、0.80、1.20、1.60、2.00 ml,分别置25 ml比色管中,准确补水至2.0ml,加入50 g/L苯酚溶液1.0 mL,快速摇匀,快速加入浓硫酸10.0 ml,快速摇匀,置沸水浴中煮2 min,冷却后用分光光度计在485 nm波长处以试剂空白溶液为参比,1 cm比色皿测定吸光度值,以葡聚糖量(mg)为横坐标,吸光度值(Au)为纵坐标,绘制标准曲线,见表5和图3。
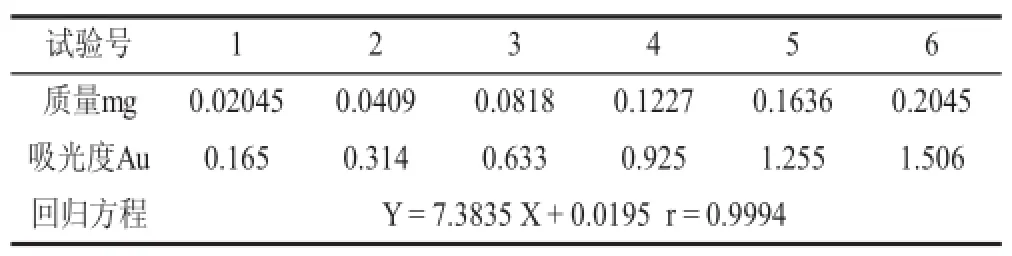
表5 葡聚糖标准曲线
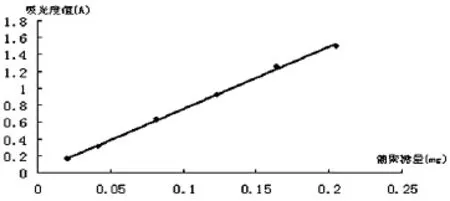
图3 葡聚糖标准曲线
(4)供试品溶液的制备。取灵芝孢子,破壁,精密称取破壁孢子粉18 g,加水100 mL,于沸水浴上加热2 h,取出,放冷,滤过,滤液置100 mL量瓶中,加水稀释至100 mL,摇匀,准确吸取稀释液2.0 mL置离心管中,加入无水乙醇8.0 mL,混匀5 min后,以3000 r/min离心5 min,弃去上清液,残渣用80%(V/V)乙醇溶液数毫升洗涤,离心后弃去清液,反复操作3~4次,残渣用水溶解并定容至5.0 mL,摇匀,准确吸取定容后溶液2.0 mL置离心管中,加入100 g/L氢氧化钠溶液2.0 mL、铜试剂溶液2.0 mL,沸水浴中煮沸2 min,冷却,以3000 r/min离心5 min,弃去上清液,残渣用洗涤液洗涤,离心后弃去上清液,反复操作3次,残渣用10%(体积分数)硫酸溶液2.0 mL溶解并转移至25 mL量瓶中,加水稀释至刻度,摇匀,即得。
(5)样品测定。精密吸取供试品溶液2.0mL置25mL比色管中,照标准曲线制备项下的方法,自“加入50g/L苯酚溶液1.0mL”起,同法操作,测定吸光度,从标准曲线上读出供试品溶液中葡聚糖的含量,计算,即得。计算公式:
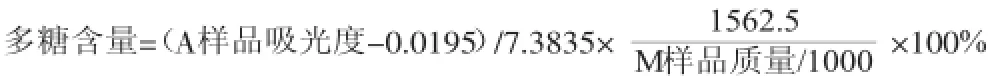
其中,A样品是样品的吸光度值(Au),M样品为样品的称样量(g)。结果见表6。
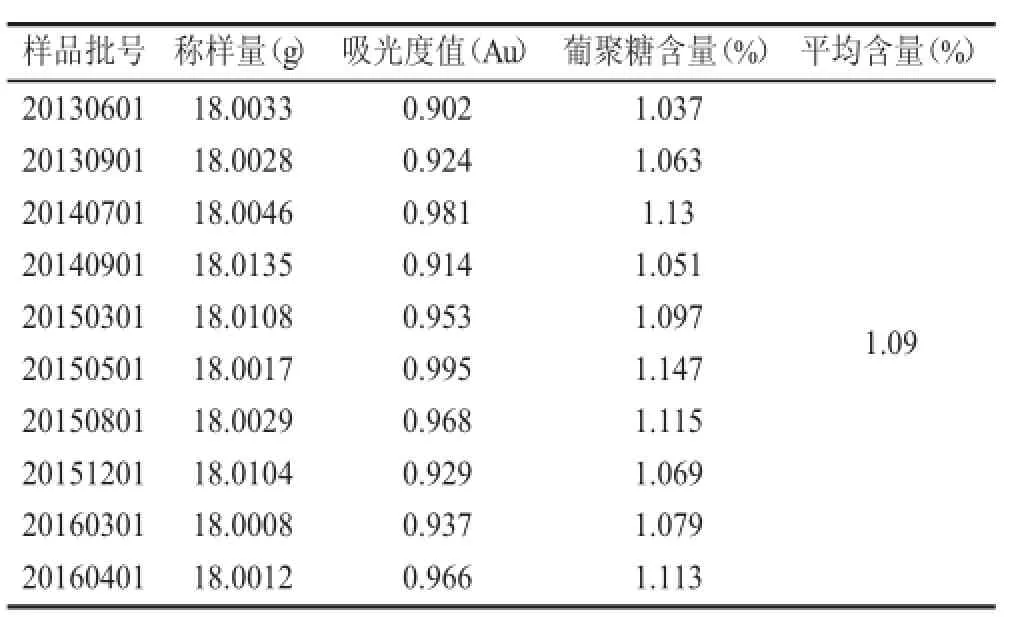
表6 灵芝孢子粉中多糖含量测定
从表6结果可知,葡聚糖分光光度法测得10批灵芝孢子的多糖含量均值为1.09%。
3 讨论
本文采用蒽酮硫酸法、苯酚硫酸法和葡聚糖分光光度法测定十批灵芝孢子的多糖含量,发现不同测定方法测得的结果相差很大。广药牌破壁灵芝孢子粉胶囊是在不添加任何辅料下,把破壁灵芝孢子粉加乙醇湿法制粒、干燥和填充所得的胶囊,其标示的粗多糖含量大于0.6%,而保健食品数据库中其他已有保健食品批文的同类产品均标示多糖含量较高,但这些产品的多糖测定方法未有公开。广药牌破壁灵芝孢子粉胶囊的多糖含量是采用葡聚糖分光光度法测定,所测得的是相对分子量较大的多糖,因此粗多糖的含量较低,但是笔者研究发现采用蒽酮硫酸法和苯酚硫酸法测定广药牌破壁灵芝孢子粉胶囊的多糖含量均大于2.0%。因此,笔者认为为了让消费者能选择到真正质量更好的灵芝孢子系列产品,在规定多糖含量时,应该标准化多糖含量的测定方法。
[1]郭春沅.灵芝的药理研究综述[J].中国食用菌,1998,17(3):34-35.
[2]邓海林,吴佩颖,王建新.灵芝的研究进展[J].时珍国医国药,2005,16(2):141-143.
[3]李抒诗,于丽薇.灵芝中的化学成分及其药物作用和保健价值[J].中国医药指南,2009,7(4):108-109.
[4]唐柳,张志军,魏雪生,等.灵芝孢子粉药理作用研究进展[J].天津农业科学,2011,17(3):25-28.
[5]王卫霄,吕艳茹,姚苗苗,等.灵芝孢子粉抗肿瘤活性的研究进展[J].河北医药,2015,37(1):105-107.
[6]周素娟,张晓娜.食用菌保健功能及保健食品应用与开发[J].中国食用菌,2015,34(1):4-6.
[7]国家药典委员会.中华人民共和国药典[S].一部.北京:中国医药科技出版社,2015:188-189.
[8]陈永刚,刘晓涵,区计明,等.不同测定方法测定淫羊藿中总黄酮含量的比较[J].食品科技,2009,34(5):291-294.
[9]王香祖,吴建平,韩学平,等.苜蓿芽多糖含量不同测定方法的比较研究[J].甘肃科技,2006,22(1):174-175.
[10]白鸿.保健食品功效成分检测方法[M].北京:中国中医药出版社,2011(5):73-76,82-85.
Comparison of Different Methods for Determination of Polysaccharide in Ganoderma Lucidum Spore
LUO Aiqin,CHEN Liang,LI Jing
(Guangzhou Hanfang Pharmaceutical Co.,Ltd./National Engineer Research Center for the Modernization of Extraction and Separation of TCM,Guangzhou 510240,China)
Objective To compare three different methods for the determinationof polysaccharides in Ganoderma lucidum spore. Methods Determination methods in the 2015 edition of"China Pharmacopeia"and"Phenol-sulfuric acid spectrophotometric method for the determination of crude polysaccharide"and"Spectrophotometric Determination of dextran"of"Health food efficacy component detection method(Bai Hong)"were applied to assay Ganoderma lucidum spore polysaccharide content.Results The experiment results showed that the average percent contents of polysaccharide with determine methods of"China Pharmacopeia"," Phenol-sulfuric acid spectrophotometric method for the determination of crudepolysaccharide"and"Spectrophotometric Determination of dextran"were 2.05%,2.72%and 1.09%,respectively,in the 10 batchs of Ganoderma lucidum spore.Conclusion There is a big difference among three different methods for the determination of Ganoderma lucidum spore polysaccharide content.
Ganoderma lucidum spore;polysaccharide;determination
10.3969/j.issn.1672-2779.2016.19.058
1672-2779(2016)-19-0132-03
:李海燕本文校对:蒋兆健
2016-06-14)
广州市科技惠民专项对口科技帮扶专题(No:2014Y2-00539)
