N-甲基-D-天冬氨酸受体拮抗剂在精神分裂症治疗中作用的Meta分析
2016-10-22李倩张红星寇延娜董召张海三司亚静吕路线
李倩,张红星,寇延娜,董召,张海三,司亚静,吕路线
(1.新乡医学院第二附属医院精神科,河南新乡453002;2.新乡医学院心理学系,河南新乡453003)
N-甲基-D-天冬氨酸受体拮抗剂在精神分裂症治疗中作用的Meta分析
李倩1,张红星2,寇延娜1,董召1,张海三1,司亚静1,吕路线1
(1.新乡医学院第二附属医院精神科,河南新乡453002;2.新乡医学院心理学系,河南新乡453003)
目的探讨N-甲基-D-天冬氨酸受体拮抗剂在精神分裂症治疗中的作用。方法在PubMed、万方、维普、CNKI中检索发表于2016年2月之前的应用NMDA受体拮抗剂治疗精神分裂症的随机对照研究。由2位研究者独立评价纳入研究的质量、提取数据,统计分析采用R evMan5.2.7软件进行。结果纳入7个研究,共370例患者,其中N-甲基-D-天冬氨酸受体拮抗剂组187例,对照组183例。Meta分析结果显示,N-甲基-D-天冬氨酸受体拮抗剂与对照组在精神分裂症阴性症状量表得分(SMD=-0.71,95%CI:-1.25,-0.16,P=0.01)、精神分裂症症状量表总分(SMD=-0.65,95%CI:-1.19,-0.11,P=0.02)方面存在显著性差异,但是其对于精神分裂症的阳性症状量表得分(SMD=0.00,95%CI:-0.20,0.21,P=0.96),一般精神病理得分(SMD= 0.18,95%CI:-0.30,0.67,P=0.46)与对照组差异无统计学意义。结论相比于对照组,N-甲基-D-天冬氨酸受体拮抗剂对精神分裂症的阴性症状有治疗作用,但是其对于精神分裂症的阳性症状和一般精神病理症状无明显的改善。对于此课题还需要更多更科学、更可靠的临床实验去证实和研究。
N-甲基-D-天冬氨酸受体;精神分裂症;Meta分析
精神分裂症是一种十分复杂、临床表现异质性、病因病理机制未明的重性精神障碍。不同的患者可表现为阳性症状、阴性症状、认知障碍、情感障碍等不同症状[1]。其中,精神分裂症患者的认知损害越来越受到重视。认知损害包括记忆力、注意力、执行功能、处理速度和语言等方面认知领域的异常,导致患者认知功能残疾,给患者及其家庭和社会都带来很大的经济负担。
目前关于精神分裂症的发病机制存在着较多争议,神经递质是其中研究热点之一,而谷氨酸系统与精神分裂症发病机制的相关性得到了广泛关注。研究者发现,精神分裂症患者体内谷氨酸含量与正常人相比较少;谷氨酸系统的功能障碍可以导致中脑边缘的多巴胺能活性增强,并降低中脑皮层的活动[2-3];在中枢神经系统中,谷氨酸是一种作用于离子型受体和代谢型受体的兴奋性氨基酸神经递质[4],N-甲基-D-天冬氨酸受体(N-Methyl-D-aspartic receptor,NMDA)则属于离子型受体,而临床上最常用的NMDA受体拮抗剂包括金刚烷胺、美金刚等;对NMDA受体拮抗剂如金刚烷胺的一些研究发现,其可以改善精神分裂症的阴性症状和认知障碍[5-6],国内外同样有报道指出抗精神病药物联合美金刚治疗精神分裂症,可显著缓解患者的阴性症状[7]。近年来,已经出现针对于谷氨酸能药物对精神分裂症患者各种治疗效果的文献及综述[8],同时,目前临床常用抗精神病药物如第1代和第2代抗精神病药因较好的疗效和耐受性已广泛用于治疗精神分裂症,但其不良反应如体重增加和糖脂代谢障碍等也受到关注。而有研究[9]报道,金刚烷胺可以减轻奥氮平导致的体重增加。但是关于NMDA受体拮抗剂专门针对精神分裂症的作用仍然缺乏更全面的综述。鉴于此,笔者按照Cochrane系统评价的方法,全面检索相关文献,通过Meta-分析的方法来评价NMDA受体拮抗剂在精神分裂症治疗中的作用,进而为精神分裂症新一代的药物开发提供依据。
1 资料与方法
1.1检索策略
按照Cochrane Handbook 5.1.0自由词结合主题词作为检索策略,以“schizophrenia,Memantine,A-mantadine,NMDA receptor antagonists”检索PubMed;以“精神分裂症,金刚烷胺,美金刚以及NMDA受体拮抗剂”检索中国知识基础设施工程(CNKI)、维普、万方数据库。检索时间范围从各数据库建库时间到2016年2月。
1.2纳入标准
1.2.1研究类型公开发表的随机对照试验。语言为中英文。
1.2.2研究对象通过《疾病和有关健康问题的国际统计分类》第10次修订本《美国精神障碍诊断统计手册第4版》以及《中国精神障碍分类与诊断标准第3版》等标准诊断为精神分裂症的患者。
1.2.3干预措施观察组采用NMDA受体拮抗剂,而不管其是否额外施加其他的抗精神药物;对照组采用安慰剂。精神分裂症的阴性症状以及阳性症状等采用标准量表进行评价。
1.2.4测量指标精神分裂症症状量表总分;阳性症状量表分;阴性症状量表分;一般精神病理症状量表分等。
1.3排除标准
排除非随机对照试验,排除未报告相关感兴趣指标的研究,以及数据严重缺乏的研究;排除干预周期少于2周的试验。
1.4资料提取与质量评价
由2位研究员分别独立对文献标题和摘要进行阅读,对于符合纳入条件的,阅读全文并提取数据和所采用的具体方法,纳入完所有相关文献后,两个研究员对自己所纳入的文献信息进行交叉核对。对于不一致数据请其他研究员进行讨论,并决定纳入与否。本研究应用Cochrane评价手册对纳入的研究质量进行评价。
1.5统计学方法
采用RevMan 5.2.7软件对纳入的数据进行Meta分析,计量资料用均数±标准差(±s)表示。计数资料应用相对危险度进行计算,各效应量的置信区间(Confidenceinterval,CI)均为95%。对于一些异质性因素采用亚组分析,并应用I2值来检验各研究之间异质性。对于I2值,如果其数值在50%以下则认为异质性较低;50%~75%范围内则表明有中等程度的异质性;而在75%则以上则说明各研究之间有着较高的异质性[10]。在异质性较低的情况下,采用固定效应模型统计分析,反之,则采用随机效应模型分析[11],P<0.05为差异有统计学意义。
2 结果
2.1文献检索结果
对各个数据库进行初检,总计有102篇相关文献,通过阅读文献的标题和摘要,并进行最终的全文阅读,排除重复,排除评论、综述,排除非随机对照及干预周期少于2周的试验,只筛查到7篇相关文献。其中5篇为英文文献,2篇为中文文献。见表1。
2.2纳入研究的一般情况
7个研究从2005~2014年不等,共370例患者,其中NMDA受体拮抗剂组187例,对照组183例。7个研究均统计分析组间的基线情况,且给出基线之间的P值,表明干预组和对照组之间的基线差异无统计学意义。见表1。

表1 纳入研究的一般情况
2.3质量评价
本研究纳入的7篇文献中,有5篇在4分以上,整体质量较好。SILVER[12],LEE[13]和纪家武等[14]详细描述了采用的随机分组方法,而其余4个研究[16-19]均描述为随机分配,但是未描述具体的实施方法。所有的研究均施用双盲法。见表2。

表2 纳入研究的质量评价
2.4结局指标
2.4.1NMDA受体拮抗剂对精神分裂症症状量表总分的影响有7个研究报道谷氨酸受体拮抗剂对精神分裂症症状量表总分的影响。共371例患者,其中应用谷氨酸受体拮抗剂为188例,对照组为183例,各研究之间差异有统计学意义(P=0.000,I2=82%),故采用随机效应模型分析。结果显示,干预组与对照组对精神分裂症症状量表总分影响方面差异有统计学意义[标准化均数差(SMD)=-0.65,95%CI:-1.19, -0.11,P=0.02],干预组即服用谷氨酸受体拮抗剂组对精神分裂症症状量表总分的影响方面与对照组有差异。见图2。
2.4.2NMDA受体拮抗剂对精神分裂症阳性症状量表得分的影响有7个研究报道谷氨酸受体拮抗剂和对照组对精神分裂症阳性症状的治疗情况。共370例患者,其中应用谷氨酸受体拮抗剂组为187例,对照组为183例,各研究之间差异有统计学意义(P=0.24,I2=24%),故采用固定效应模型分析。结果显示,干预组与对照组在治疗精神分裂症的阳性症状方面差异无统计学意义(SMD=0.00,95%CI:-0.20,0.21,P=0.96),干预组即服用谷氨酸受体拮抗剂组在治疗精神分裂症阳性症状方面与对照组无明显差异。见图3。

图1 检索流程图

图2 NMDA受体拮抗剂对精神分裂症症状量表总分的影响
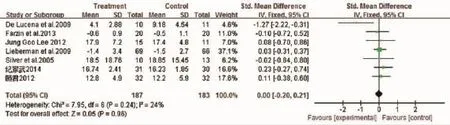
图3 NMDA受体拮抗剂对精神分裂症阳性症状量表得分的影响
2.4.3NMDA受体拮抗剂对精神分裂症阴性症状量表得分的影响有7个研究报道了两组的治疗情况。共370例患者,其中应用谷氨酸受体拮抗剂组为187例,对照组为183例,各研究之间差异有统计学意义(P=0.000,I2=81%),故采用随机效应模型分析。结果显示,与对照组比较,干预组与对照组在治疗精神分裂症阴性症状方面差异有统计学意义(SMD= -0.71,95%CI:-1.25,-0.16,P=0.010),干预组即服用谷氨酸受体拮抗剂组在治疗精神分裂症阴性症状方面与对照组存在差异。见图4。

图4 NMDA受体拮抗剂对精神分裂症阴性症状量表得分的影响
2.4.4NMDA受体拮抗剂对精神分裂症一般精神病理量表得分的影响有4个研究报道了两组的治疗情况。共191例患者,其中应用谷氨酸受体拮抗剂组为98例,对照组为93例,各研究之间差异有统计学意义(P=0.040,I2=63%),故采用随机效应模型分析。结果显示,与对照组相比,干预组与对照组在治疗精神分裂症一般病理症状方面差异无统计学意义(SMD=0.18,95%CI:-0.30,0.67,P=0.460),干预组即服用谷氨酸受体拮抗剂组在治疗精神分裂症一般精神病理症状方面与对照组没有明显差异。见图5。
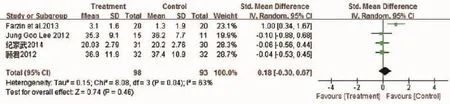
图5 NMDA受体拮抗剂对精神分裂症一般精神病理量表得分的影响
3 讨论
Meta分析是对具备特定条件的、同课题的诸多研究结果进行综合的一类统计学方法,其基于循证医学,纳入大样本量,与传统描述性综述相比可以对证据进行更为客观的评价。而本研究经过数据的纳入、排除以及汇总,笔者发现与安慰剂比较,NMDA受体拮抗剂对精神分裂症的阴性症状的有治疗或增效作用,但是其对于精神分裂症的阳性症状、一般精神病理症状和认知障碍暂没发现治疗或增效作用。
最新的研究显示,脑部功能紊乱导致的疾病与NMDA受体有一定的关系,因此现在有不少文献集中于研究NMDA受体拮抗剂与精神分裂症的关系[15]。NMDA受体在兴奋毒过程中起着很重要的作用,原因是过量的谷氨酸释放会使NMDA受体被过度激活,使细胞内钙离子聚集,导致神经元死亡。另外,纹状体丘脑NMDA通路功能低下时,会使得经丘脑的感觉冲动增强增多,从而增强皮质的单胺递质活性。前额皮质的5-HT增强会进一步激动5-HT2A受体,进而抑制DA的释放,导致前额皮质D1受体功能下降,引起精神分裂症的阴性症状。因此这可能是NMDA受体拮抗剂对精神分裂症的阴性症状有治疗或增效作用的原因。而有研究显示NMDA受体拮抗剂可以增加多巴胺能,当增加中脑边缘通路多巴胺能时,会恶化阳性症状,当增加中脑皮质通路多巴胺能时,可以改善阴性症状,这也可以解释其对精神分裂症阳性症状为什么无改善作用。
从本文的结果可以看出,NMDA受体拮抗剂对精神分裂症的阴性症状有一定的治疗作用,但是其疗效仍须加强,通过提高拮抗剂对不同亚单位的选择性可以大大增强药效,降低其副作用。因此,在未来以NMDA受体不同亚单位作为靶点的拮抗剂是以后精神分裂症药品研发的重点方向和目标。
通过筛查文献发现,近年来将NMDA受体拮抗剂应用于精神分裂症治疗中的相关文献甚少,而分析发现其对精神分裂症的阴性症状及对症状量表总分的影响是已知的。因此以NMDA受体不同亚单位作为靶点的拮抗剂作为治疗靶点可能是精神分裂症治疗中的一个新途径。相较于目前的第一代和第二代抗精神病药物,其很可能为人们带来一种更好的治疗选择。
[1]TANDON R,KESHAVAN M S,NASRALLAH H A.Schizophrenia,"just the facts"what we know in 2008.2.Epidemiology and etiology[J].Schizophr Res,2008,102(1/2/3):1-18.
[2]王绍礼,翁永振.氯氮平治疗精神分裂症的机制与谷氨酸假说[J].医药导报,2002,21(10):638-639.
[3]ZARATE C,MACHADO-VIEIRA R,HENTER I,et al.Glutamatergic modulators:the future of treating mood disorders[J]. Harv Rev Psychiatry,2010,18(5):293-303.
[4]GOFF D C,COYLE J T.The emerging role of glutamate in the pathophysiology and treatment of schizophrenia[J].American Journal of Psychiatry,2001,158(9):1367-1377.
[5]GAMA C S,LUCENA D D,CRU C,et al.Improvement of schizophrenia negative and positive symptoms with amantadine as add-on therapy to antipsychotics:a case series[J].Rev Bras Psiquiatr,2010,32(2):193-194.
[6]CARPENTER S S,HATCHETT A D,FULLER M A.Catatonic schizophrenia and the use of memantine[J].Ann Pharmacother, 2006,40(2):344-346.
[7]喻东山,唐艳.金刚烷胺强化治疗精神分裂症阴性症状1例[J].临床荟萃,2006,21(6):432.
[8]NISWENDER C M,CONN P J.Metabotropic glutamate receptors: physiology,pharmacology,and disease[J].Annu Rev Pharmacol Toxicol,2010,50(2):295-322.
[9]DAS C,MENDEZ G,JAGASIA S,et al.Second-generation antipsychotic use in schizophrenia and associated weight gain:a critical review and meta-analysis of behavioral and pharmacologic treatments[J].Ann Clin Psychiatry,2012,24(3):225-239.
[10]HIGGINS J P,THOMPSON S G,DEEKS J J,et al.Measuring inconsistency in meta-analyses[J].BMJ,2003,327(7414):557-560.
[11]ARMITAGE P,BERRY G,MATTHEWS J NS.Analysing means and proportions.statistical methods in medical research[J].Blackwell Science Ltd,2008,1(1):83-146.
[12]SILVER H,GOODMAN C,ISAKOV V,et al.A double-blind, cross-over comparison of the effects of amantadine or placebo on visuomotor and cognitive function in medicated schizophrenia patients[J].International Clinical Psychopharmacology,2005,20(6): 319-326.
[13]LEE J G,LEE S W,LEE B J,et al.Adjunctive memantine therapy for cognitive impairment in chronic schizophrenia:a placebo-controlled pilot study[J].Psychiatry Investigation,2012, 9(2):166-173.
[14]纪家武,蒋昕,陈华云,等.奥氮平联合金刚烷胺治疗精神分裂症首次发病患者的随机双盲对照研究[J].临床精神医学杂志, 2014,24(1):1-3.
[15]REZAEI F,MOHAMMDA-KARIMI M,SEDDIGHI S,et al. Memantine add-onto rispeidone fortreatmentofnegative symptoms in patients with stable schizzophrenia;randomized, double-blind,placebo-controlled study[J].Journal of Clinical Psychopharmacology,2013,33(3):336-342.
[16]LEIBERMAN J A,PAPADAKIS K,CSERNANSKKY J,et al.A randomized,placebo-controlled study of memantine as adjunctive treatment in patients with schizophrenia[J].Neuropsychopharmacology,2008,34(5):1322-1329.
[17]DE LUCHNA D,FERNANDES B S,BERK M,et al.Improvement ofnegativeandpositivesymptomsintreatment-refractory schizpphrenia:a double-boind,rannomized,placebo-controlled trail with menantine as add-on trerapy colzapine[J].The Journal of Clinical Psychiraty,2009,70(10):1416-1423.
[18]顾君,吴越,汤莉.氯氮平联合美金刚治疗精神分裂症阴性症状对照研究[J].临床精神医学杂志,2012,12(4):261-263.
[19]KEMP J A,MCKERNAN R M.NMDA receptor pathways as drug targets[J].Nature Neuroscience,2002,5(1):1039-1042.
(张西倩编辑)
Meta-analysis of N-methyl-D-aspartic receptor antagonists for treatment of schizophrenia
Qian Li1,Hong-xing Zhang2,Yan-na Kou1,Zhao Dong1,Hai-san Zhang1,Ya-jing Si1,Lu-xian Lyu1
(1.Department of Psychiatry,the Second Affiliated Hospital of Xinxiang Medical University,Xinxiang,Henan 453002,China;2.Department of Psychology,Xinxiang Medical University,Xinxiang,Henan 453003,China)
Objective To evaluate the clinical effect of N-methyl-D-aspartic receptor antagonists(NMDA-RA)in the treatment of schizophrenia.Methods Randomized controlled studies about the effect of NMDA receptor antagonists on schizophrenia published before February 2016 were retrieved in PubMed,Wanfang,VIP and CNKI databases.Methodological quality assessment and data collection were performed by two individual reviewers.A meta-analysis was performed by RevMan 5.2.7 software.Results In accordance with inclusive and exclusive criteria,7 randomized controlled trials(RCTs)were included.There were totally 370 patients,including 187 patients in the NMDA-RA intervention groups and 183 in the control groups.The meta analysis results showed that there were significant differences in the negative syndrome score(SMD=-0.71;95%CI:-1.25,-0.16;P=0.01)and the total symptom score(SMD=-0.65;95%CI:-1.19,-0.11;P=0.02)of the Positive and Negative Syndrome Scale(PANSS)for schizophrenia between the NMDA-RA intervention groups and the control groups,but there was no significant difference in the positive symptom score of PANSS(SMD=0.00;95%CI:-0.20,0.21;P=0.96)or score of the Brief Psychiatric Rating Scale(BPRS)(SMD=0.18;95%CI:-0.30,0.67;P=0.46)between them. Conclusions N-methyl-D-aspartic receptor antagonists have certain therapeutic effects on the negative symptoms of schizophrenia,but can not obviously alleviate the positive symptoms and general symptoms of schizophrenia.So this study still needs to be confirmed by more scientific,more reliable clinical trials.
N-methyl-D-aspartic receptor antagonist;schizophrenia;Meta-analysis
R 749.3
B
10.3969/j.issn.1005-8982.2016.18.021
1005-8982(2016)18-0104-06
2015-12-18
张红星,E-mail:zhx166666@163.com;Tel:13849362593
