葵花籽壳对溶液中铀酰离子的吸附
2016-10-20王长福刘峙嵘薛桂荣周利民
王长福,刘峙嵘,薛桂荣,赖 毅,王 云,周利民
东华理工大学化学生物与材料科学学院,江西南昌 330013
葵花籽壳对溶液中铀酰离子的吸附
王长福,刘峙嵘*,薛桂荣,赖 毅,王 云,周利民
东华理工大学化学生物与材料科学学院,江西南昌 330013
选取农业副产物葵花籽壳作为吸附剂,研究其对溶液中铀酰离子的吸附性能。用元素分析、扫描电镜、红外光谱分析等方法对吸附铀前后的葵花籽壳进行分析和表征,通过静态实验分别研究了时间、温度、p H值、铀酰离子初始浓度、葵花籽壳用量等因素对吸附效果的影响。结果表明:吸附的适宜p H为5.0~6.0,35℃下,当铀溶液初始质量浓度为50 mg/L,溶液p H=5.0,葵花籽壳质量浓度为1.00g/L时,饱和吸附量可达29.2 mg/g。
葵花籽壳;铀;吸附
农林作物的收获和加工过程中所产生的废弃物资和垃圾称为农林废弃物,如玉米、花生、高梁、棉花、豆类等的秸秆,植物的枝叶和藤蔓,木材加工的废料,以及食品加工过程中产生的残渣,如饼粕、酒糟、蔗渣、甜菜渣、食品工业下脚料等[1]。近年来,农林废弃物等已逐渐开始被用做吸附剂来修复污染水体。农林废弃物主要由蛋白质以及纤维、半纤维、木质素等成分组成,对重金属离子有良好的吸附效果。稻草[2-4]、橘子皮[5-7]、香蕉皮[8]、米糠[9]、玉米芯[10-13]、锯屑[14-15]、树皮[16]、树叶[17]、椰壳纤维[18]、甘蔗渣[19]、水生植物[20]等植物材料常被用来做为吸附剂。叶林顺等[21-23]的研究表明,改性稻草对废水中的Cu2+有很好的吸附效果并且吸附过程的自发趋势很强。Montanher等[24]研究了米糠对Cd2+、Cu2+、Pb2+、Zn2+等重金属离子的吸附性能,发现米糠对重金属离子的吸附也是自发进行的,并且符合Freundlich等温吸附模型。张庆芳等[25]对改性玉米芯吸附污染水中Cr6+的研究表明,最佳实验条件下去除率可高达98.2%。徐涛等[26]用改性处理后的花生壳活性炭吸附废水中的Pb2+,利用傅里叶红外光谱(FT-IR)、X射线光电子能谱分析(XPS)等方法探讨了其吸附机理,发现吸附过程中发挥主要作用的基团为羧基、羰基和磷氧基,并且改性处理大大提高了这些基团的吸附能力。葵花籽壳作为向日葵的副产品,每年约有70万吨,但多数未能得到合理的处置和有效地利用,只有很少一部分用作家畜饲料,大部分被就地焚烧或者被弃于野外任其自然腐烂降解,既污染环境又造成资源的极大浪费。如果将这一资源充分利用到放射性含铀废水的处理,则可以变废为宝,实现资源再利用。葵花籽壳来源广、成本低,并且目前国内外在葵花籽壳吸附铀方面的研究较少,所以本工作拟选取价格低廉的葵花籽壳作为吸附剂,研究其对溶液中铀酰离子的吸附性能,通过静态实验分别研究时间、温度、p H值、铀酰离子初始质量浓度、葵花籽壳用量等因素对吸附效果的影响,并对其吸附动力学、热力学进行研究。
1 实验部分
1.1 试剂及仪器
2,4-二硝基苯酚、乙酸钠、无水乙醇,分析纯,国药集团化学股份有限公司;氯乙酸,分析纯,西陇化工股份有限公司;盐酸、偶氮胂Ⅲ、氢氧化钠,分析纯,天津市永大化学试剂有限公司;八氧化三铀,分析纯,核工业北京化工冶金研究院。
721E型可见分光光度计,天津冠泽科技有限公司;AL204电子分析天平,精度为0.000 1g,北京赛多利斯仪器系统有限公司;SHA-B水浴恒温振荡器,国华电器有限公司;S-30 p H计,仪电科学仪器股份有限公司;H1650台式高速离心机,湘仪实验室仪器开发有限公司;Gx-07A多功能粉碎机,上海高翔食品机械厂;Nicoletis5傅里叶红外变换光谱仪,美国Thermo Fisher Scientific公司;Carlo-Erba 1106元素分析仪,意大利Milan公司;S4800扫描电子显微镜,日本HITACHI公司。
1.2 葵花籽壳的制备
将从市场购买的未经炒制的葵花籽人工剥壳。称取一定量的葵花籽壳,用蒸馏水浸泡24 h,然后用大量蒸馏水充分洗涤,洗涤多次,直至洗涤后的蒸馏水接近无色,然后放在鼓风干燥箱中进行干燥,105℃干燥24 h,再将其粉碎,过80目筛,保存备用。
1.3 铀溶液的配制及U(Ⅵ)的测定
铀溶液的配制:准确称取1.179 2g经预处理过的基准八氧化三铀于150 m L烧杯中,加入5 m L王水,盖上表面皿,在电热板上加热溶解,并蒸至近干(湿盐状),取下稍微冷却,加入10 m L浓盐酸,再次加热至盐类溶解,用去离子水冲洗表面皿,将溶液转入体积为100 m L的容量瓶中,用去离子水定容至刻度,摇匀。所配铀溶液质量浓度为10g/L。
U(Ⅵ)的测定:在25 m L容量瓶中加入一定量的待测液,然后依次加入两滴2,4-二硝基苯酚溶液、两滴3mol/L的盐酸、2 m L缓冲溶液(0.5mol/L乙酸钠溶液和0.5mol/L氯乙酸溶液,按3:7的体积比混合后,摇匀,调节p H至2.5)和2 m L偶氮胂Ⅲ溶液,每加入一种试剂都充分摇匀。用蒸馏水定容至刻度,先充分摇匀,然后静置25min。用分光光度计于650nm波长处,以空白试剂做参比,测定溶液的吸光度。
1.4 静态吸附实验
取50 m L一定初始浓度的铀酰离子溶液加入到100 m L的具塞锥形瓶中,分别改变葵花籽壳对铀酰离子的吸附实验条件:溶液p H值、反应温度、振荡时间、铀酰离子初始质量浓度、葵花籽壳投加量等因素对葵花籽壳吸附铀的影响,所有实验均在恒温水浴振荡器中进行。设置离心机的转速为10 000 r/min,时间设为5min,对反应完成后的体系进行离心分离,分离后用分光光度法测定上层清液中铀酰离子的浓度。
葵花籽壳对铀的去除率Y及t时刻的吸附量qt(mg/g)计算如式(1)、(2)。
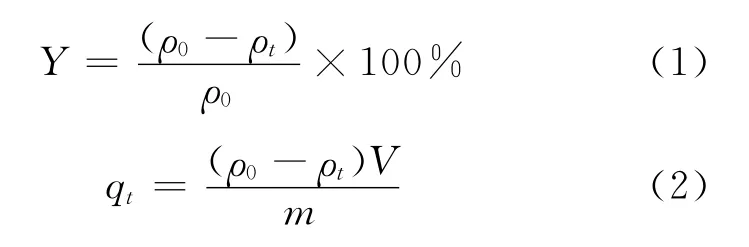
式中:Y为去除率,%;qt为葵花籽壳t时刻对铀的吸附量,mg/g;ρ0为铀的初始质量浓度,mg/L;ρt为吸附t时刻时溶液中铀的质量浓度,mg/L;V为溶液体积,L;m为吸附剂质量,g。
2 结果与讨论
2.1 材料表征
2.1.1 元素分析 以C、H、N模式分析待测样品的元素含量,C、H、N的质量分数分别为47.25%、5.75%、1.90%。葵花籽壳的主要组成中H和N的含量较小,主要为C。
2.1.2 能谱分析 利用扫描电子显微镜辅助设备X射线能量色散仪(EDAX)分别对葵花籽壳吸附铀前后的表层进行区域扫描,探测其表层各元素的含量组成情况,分析样品的元素含量特征。首先对待测样品进行扫描,随后用X射线能量色散仪在所选取的微区域进行X射线能量色散扫描,结果示于图1并列入表1。如图1和表1可知:葵花籽壳主要包含C和O两种元素,理论上还应含有N元素,但可能由于含量少、扫描区域小,所以未能在扫描结果中体现出来;元素含量变化与元素分析结果基本一致。吸附铀酰离子前后葵花籽壳中U元素的质量分数由0增加到24.21%,原子百分比由0增加到2.94%,说明葵花籽壳对发生了吸附作用,更加证实了葵花籽壳对的吸附作用。

图1 葵花籽壳吸附铀前(a)、后(b)的元素X射线能量色散图Fig.1 EDAX spectrums of chemical elements on sunflower seed shells before(a)and after(b)adsorption for
表1 葵花籽壳吸附铀前后的元素X射线能量色散扫描结果Table 1 Results of EDAX about chemical elements on sunflower seed shells before and after adsorption for
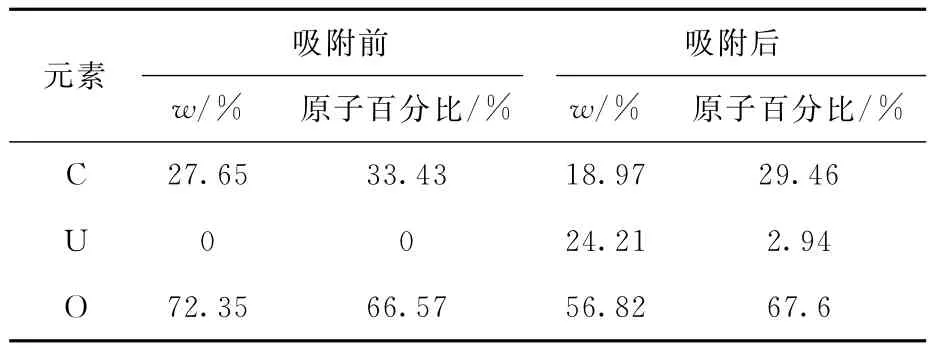
表1 葵花籽壳吸附铀前后的元素X射线能量色散扫描结果Table 1 Results of EDAX about chemical elements on sunflower seed shells before and after adsorption for
元素吸附前吸附后w/%原子百分比/%w/%原子百分比/% C 27.65 33.43 18.97 29.46 U 0 0 24.21 2.94 O 72.35 66.57 56.82 67.6
2.1.3 扫描电镜(SEM) 分别对葵花籽壳以及吸附铀后的葵花籽壳进行扫描电镜分析,结果示于图2。由图2可知,葵花籽壳表面具有良好的多孔结构,分布连续而又均匀,孔道规则类似蜂窝状,有利于吸附;吸附铀后,葵花籽壳表面孔隙度降低,整体看起来变得比较平整,可能由于吸附在葵花籽壳表面,使得葵花籽壳的表面发生了变化。
2.1.4 红外光谱(FT-IR) 葵花籽壳吸附铀前后的红外光谱曲线示于图3。由图3可知,葵花籽壳吸附铀酰离子后,其红外光谱图与吸附前相比虽然在特征峰的数量上没有太大变化,但是主要特征峰的位置均出现了一定程度的偏移,这表明葵花籽壳吸附铀后,其自身结构发生了改变。吸附铀后,O—H的伸缩振动峰的峰形没有明显变化,但是波数变成了3 394 cm-1,即向低波数移动了7 cm-1;CC键的最大吸收峰波数没有变化;醇羟基的面内弯曲振动吸收峰向高波数移动9 cm-1;1 016 cm-1处由C—O健的伸缩振动引起的特征吸收峰向高波数移动至1 030 cm-1处;642 cm-1处纤维素的羟基面外弯曲振动吸收峰向高波数移动至646 cm-1。引起谱峰位移的原因可能是,葵花籽壳吸附后,原来结合到活性吸附位点上的H+其中一部分被取代,使得葵花籽壳表面的化学组成发生了变化,从而导致O—H、C—O及醇羟基峰发生变化。

图2 葵花籽壳吸附铀前(a)、后(b)的SEM图Fig.2 Microcosmic configuration of sunflower seed shells before(a)and after(b)adsorption for
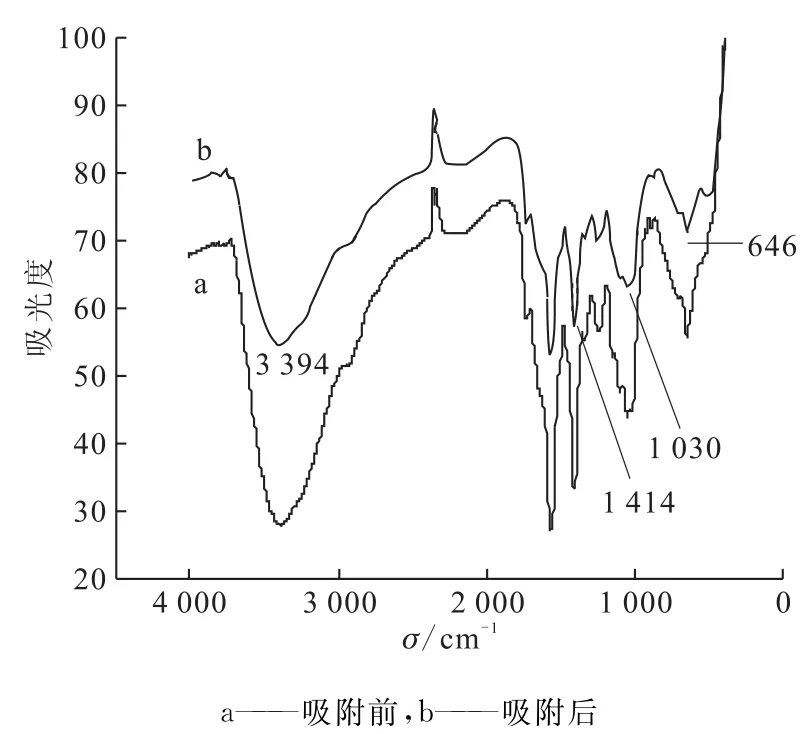
图3 吸附前后葵花籽壳的红外光谱图Fig.3 IR spectra of sunflower seed shells before adsorption and after adsorption
2.2 p H值对葵花籽壳吸附铀的影响
分别向6个100 m L的具塞锥形瓶中各加入50 m L初始质量浓度为50 mg/L的铀溶液,6个锥形瓶中铀溶液的p H值分别为2.0、3.0、4.0、5.0、6.0和7.0,然后各加入0.20g葵花籽壳,35℃下,在水浴恒温振荡器中振荡90min,反应完成后测定铀酰离子的浓度,并分析初始溶液p H对葵花籽壳吸附铀效果的影响,结果示于图4。由图4可知,p H值对葵花籽壳吸附U(Ⅵ)的效果有较大影响。在p H为5.0~6.0时,葵花籽壳对U(Ⅵ)的去除效果最好,去除率及吸附量最大,分别为80%和19.5 mg/g;当p H<5.0时,去除率和吸附量均随p H的减小而减小;p H为6.0~7.0时,随着p H的增大,去除率和吸附量也逐渐减小,并且后一种情况下减小的更快。在p H=2.0时,去除率和吸附量最小,分别只有2.26%和0.56 mg/g。
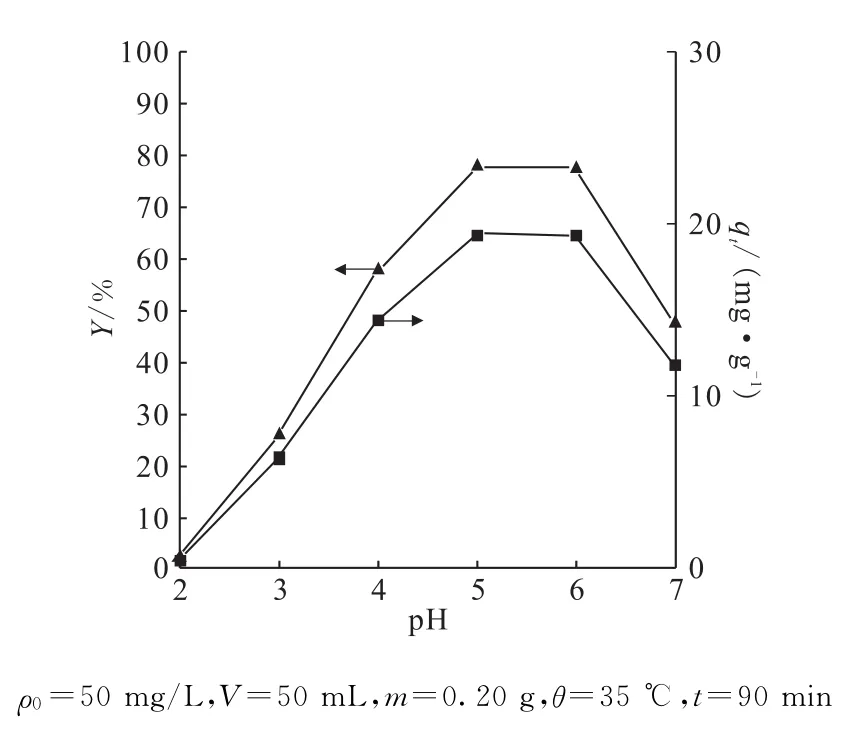
图4 p H值对葵花籽壳吸附U(Ⅵ)的影响Fig.4 Effect of p H on sunflower seed shells adsorption of U(Ⅵ)
p H对溶液中铀的存在形态影响较大,从而影响葵花籽壳对铀的吸附。当吸附反应在强酸性溶液环境中进行时,溶液中高浓度的H+会与溶液中的竞争吸附剂上的活性吸附位点,葵花籽壳表面的活性位点有很大一部分会被H+占据,随后便会产生斥力作用,受斥力作用的影响,溶液中的铀酰离子便很难向活性位点靠近,从而难以有机会与活性位点结合,这使得葵花籽壳对铀的吸附量较低。当溶液p H>5.0,随着溶液中OH-的浓度增加,溶液中的OH-与形成[UO2OH]+、[(UO2)3(OH)4]2+、[(UO2)3(OH)5]+、[(UO2)2(OH)2]2+、[(UO2)2OH]3+、[(UO2)3OH]5+、[(UO2)4OH]7+、[UO2(OH)4]2-、[(UO2)3(OH)7]-等离子,使得葵花籽壳对铀酰离子的吸附量减小;另一方面溶液中的CO2-3与结合形成了[UO2CO3]0、[UO2(CO3)2]2-、[UO2(CO3)3]4-、[(UO2)3(CO3)6]6-等离子[27]也使得葵花籽壳对的吸附量降低。
2.3 温度对葵花籽壳吸附铀的影响
分别向5个100 m L的具塞锥形瓶中各加入50 m L初始质量浓度为50 mg/L、p H=5.0的铀溶液,然后各加入0.10g葵花籽壳,在不同温度下,在水浴恒温振荡器中振荡吸附90min,反应完成后测定铀酰离子的浓度,并分析温度对葵花籽壳吸附铀效果的影响,结果示于图5。由图5可知,葵花籽壳对铀的去除率和吸附量受温度的影响较小。当20℃时,葵花籽壳对溶液中铀酰离子的去除率为76.4%,吸附量为19.1 mg/g;当60℃时,葵花籽壳对溶液中铀酰离子的去除率为78.3%,吸附量为19.6 mg/g。由此可以知道,反应温度从20℃升高到60℃,葵花籽壳对铀酰离子的去除率仅提高了1.92%,吸附量也只增多了0.480 mg/g。在20~60℃下,升高反应温度只能很小程度地提高葵花籽壳对铀酰离子的去除率和吸附量。葵花籽壳吸附水溶液中U(Ⅵ)的过程中吸附和脱附并存,随着温度的升高,吸附的速率和脱附的速率同时增大,而两者的增大量相差不大时就会出现图5中的这种情况,即温度升高后吸附量并没有显著的增大。为了操作方便,吸附实验在35℃下进行。

图5 温度对葵花籽壳吸附U(Ⅵ)的影响Fig.5 Effect of temperature on sunflower seed shells adsorption of U(Ⅵ)
2.4 吸附剂的投加量对葵花籽壳吸附铀的影响
分别向6个100 m L的具塞锥形瓶中各加入50 m L初始质量浓度为50 mg/L、p H=5.0的铀溶液,改变葵花籽壳用量,35℃下,在水浴恒温振荡器中振荡90min,反应完成后测定铀酰离子的浓度,并分析吸附剂用量对葵花籽壳吸附铀效果的影响,结果示于图6。葵花籽壳质量浓度由1.00g/L增加到2.00g/L时,铀的去除率由58.4%增加到78.0%。吸附量的变化与去除率刚好相反,吸附量从29.2 mg/g下降到6.82 mg/g。主要因为铀溶液浓度一定时,吸附剂用量增加,活性吸附位点的数目就会增加,对铀的去除率增大;由于溶液中铀酰离子的数量固定,吸附剂用量多了,单位质量吸附剂吸附铀的量减少,从而引起吸附量减小。

图6 葵花籽壳投加量对吸附U(Ⅵ)的影响Fig.6 Effect of sunflower seed shells dose on adsorption of U(Ⅵ)
2.5 吸附时间对葵花籽壳吸附铀的影响
分别向9个100 m L的具塞锥形瓶中各加入50 m L初始质量浓度为50 mg/L、p H=5.0的铀溶液,然后各加入0.10g葵花籽壳,35℃下,在水浴恒温振荡器中振荡吸附一定时间,反应完成后测定铀酰离子的浓度,并分析反应时间对葵花籽壳吸附铀效果的影响,结果示于图7。由图7可知,在吸附反应进行30min后,葵花籽壳对铀酰离子的去除率已经超过70.0%,吸附量也达到了17.9 mg/g。30min之后,去除率和吸附量的变化趋于平缓,反应进行270min后,葵花籽壳对溶液中铀酰离子的去除率为78.1%;吸附量为19.5 mg/g。在210min之后,葵花籽壳对铀的去除率和吸附量随时间的变化更小,可认为吸附反应达到了吸附平衡。

图7 时间对葵花籽壳吸附U(Ⅵ)的影响Fig.7 Effect of time on sunflower seed shells adsorption of U(Ⅵ)
葵花籽壳对铀酰离子的吸附主要在葵花籽壳的表面和孔隙的内表面,对于葵花籽壳表面的吸附只是液相中的铀酰离子转移到固体表面的过程,该过程所需的时间较短;而对于铀酰离子在葵花籽壳孔隙内表面的吸附则要有两个过程才能完成,首先是溶液中的铀酰离子通过扩散作用进入葵花籽壳的孔隙,接着才是孔隙中的铀酰离子吸附在孔隙的内表面上。与葵花籽壳表面的吸附相比在其内表面的吸附耗时更长,因此其对铀酰离子的吸附量随时间的增加缓慢的增加,直至达到平衡。
2.6 铀酰离子初始质量浓度对葵花籽壳吸附铀的影响
分别向7个100 m L的具塞锥形瓶中各加入50 m L初始质量浓度不同、p H均为5.0的铀溶液,然后各加入0.10g葵花籽壳,35℃下,在水浴恒温振荡器中振荡90min,反应完成后测定铀酰离子的浓度,并分析铀酰离子初始质量浓度对葵花籽壳吸附铀效果的影响,结果示于图8。由图8可知,随着溶液中铀酰离子初始质量浓度的增加,葵花籽壳对其的去除率不断减小,而吸附量不断增大。当溶液中铀酰离子的初始质量浓度为10 mg/L时,葵花籽壳对它的去除率达到了100%,吸附量为5.00 mg/g;当溶液中铀酰离子的初始质量浓度为100 mg/L时,葵花籽壳对其去除率为71.1%,吸附量为35.5 mg/g。由此可见,葵花籽壳对溶液中铀酰离子的吸附性能受初始质量浓度的影响很大;葵花籽壳适用于处理低浓度的含铀废水。
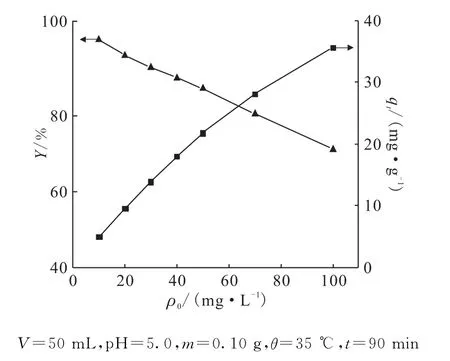
图8 铀酰离子初始浓度对葵花籽壳吸附U(Ⅵ)的影响Fig.8 Effect of U(Ⅵ)initial concentration on sunflower seed shells adsorption of U(Ⅵ)
当溶液中U(Ⅵ)的初始质量浓度较低时,U(Ⅵ)得以与吸附剂充分接触,溶液中所有的U(Ⅵ)均可以与吸附剂发生反应,因此去除率较高,但葵花籽壳的部分吸附位点未与铀酰离子结合,所以吸附量较小。溶液中铀酰离子初始质量浓度增加,单位质量的葵花籽壳对铀的吸附量显著增大,去除率却明显下降,原因是随着溶液中铀酰离子质量浓度的增大,导致溶液中铀浓度相对于葵花籽壳用量逐渐过量,当葵花籽壳对铀的吸附达到饱和之后,过量的未被吸附的铀酰离子就只能以游离态存在于溶液中,去除率降低;但是单位质量的葵花籽壳对铀的吸附量却变大,即吸附量增大。
2.7 葵花籽壳吸附铀的动力学
吸附动力学研究可以提供关于吸附机制的信息,可以估算吸附速率,推测反应机理,推导速率表达式,建立合适的吸附动力学模型。动力学吸附可以用多种模型进行拟合,目前比较常用的是准一级吸附动力学模型(式(3))和准二级吸附动力学模型方程(式(4))。
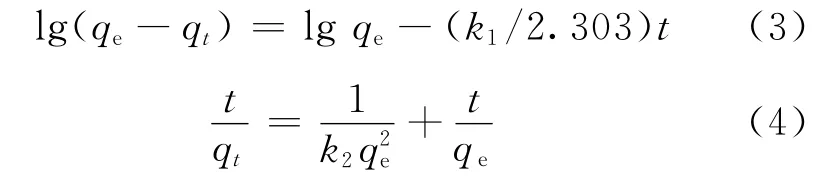
式中:qe,平衡吸附量,mg/g;qt,t时刻的吸附量,mg/g;t,振荡时间,min;k1,准一级吸附速率常数,min-1;k2,准二级吸附速率常数,g/(mg·min)。
准一级吸附动力学模型基于两个假定,一是吸附受扩散步骤控制,二是吸附速率正比于平衡吸附量与t时刻吸附量的差值;准二级动力学模型是基于假定吸附速率受化学吸附机理的控制,这种化学吸附涉及到吸附剂与吸附质之间的电子共用或电子转移[28]。准二级吸附动力学模型在模拟固态吸附剂吸附重金属离子的研究中得到广泛应用[29-31]。
本工作分别采用以上两种模型对葵花籽壳吸附铀的过程进行模拟,动力学模型参数列入表2,结果示于图9、10。由图9、10可知,准二级动力学模型的r2=0.999 8>0.980 7,证明拟合的很好;同时,通过准二级动力学模型计算所得理论平衡吸附量为19.755 mg/g,实验所得平衡吸附量为19.50 mg/g,二者非常接近,而与通过准一级动力学模型计算所得的理论平衡吸附量为3.207 mg/g,与实验结果相差很大。因此,准二级动力学模型能更好的描述葵花籽壳吸附铀的过程,此吸附过程为化学吸附。
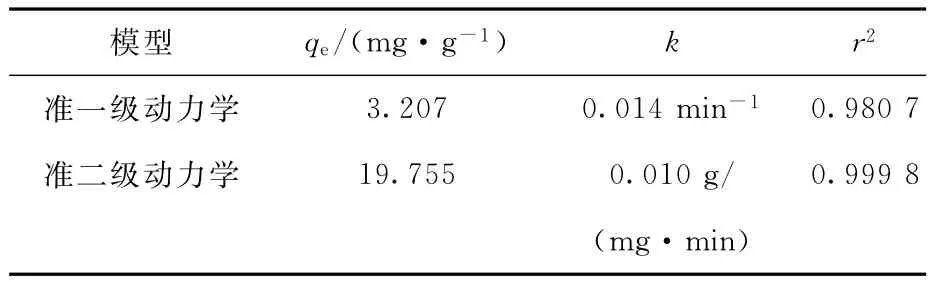
表2 葵花籽壳吸附铀的各动力学模型参数Table 2 Kinetic parameters of U(Ⅵ)adsorption on sunflower seed shells
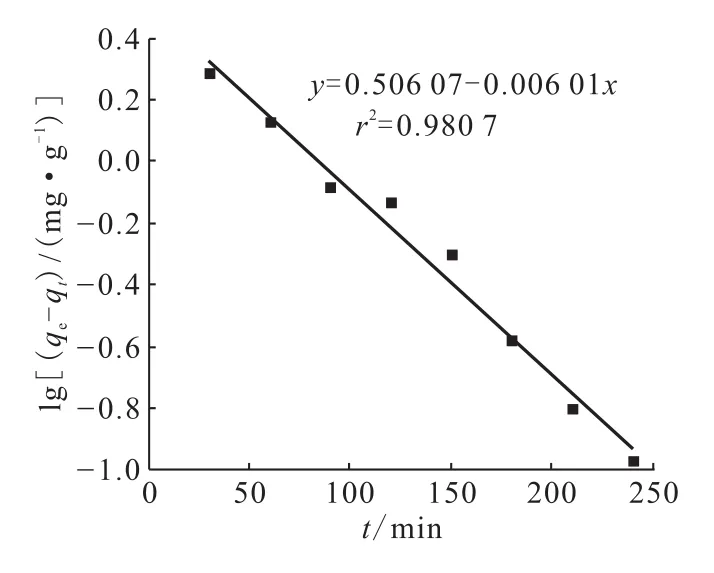
图9 准一级动力学模型Fig.9 Pseudo first-order model
2.8 葵花籽壳吸附铀的热力学
焓变ΔH(kJ/mol)、熵变ΔS(J/(k·mol))和吉布斯自由能变ΔG(kJ/mol)等吸附热力学参数更能较为直观地反映出吸附剂和吸附质分子之间以及吸附剂和溶剂之间的作用。ΔH、ΔS和ΔG可以通过公式(5)—(7)[32]计算。

式中:Kd,吸附分配系数,L/mg;ρ0、ρe,溶液中铀的初始和平衡时质量浓度,mg/L;R,理想气体常数,8.314 J/(mol·K);T,绝对温度,K;V,铀酰离子溶液的体积,m L;m,吸附剂的质量,mg。
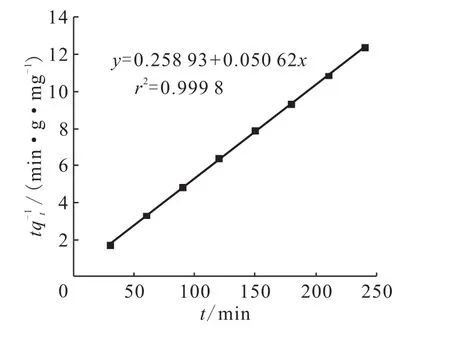
图10 准二级动力学模型Fig.10 Pseudo second-order model
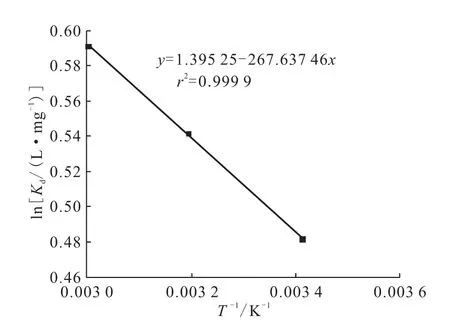
图11 ln Kd对1/T曲线Fig.11 Plot of ln Kdvs 1/T
用ln Kd对1/T作图,结果示于图11。通过拟合直线的斜率和截距以及公式(6)得到的各热力学参数列入表3。由表3可知,葵花籽壳吸附铀过程的ΔH为正值,表示葵花籽壳吸附铀的过程是吸热过程;ΔS为正值,表示该过程中在固液两相界面的不规则性,即自由度增加,这种随机性状态主要是因为金属螯合作用的螯合水分子的解放,是熵驱动过程[33];在三个温度条件下ΔG的值均为负,说明该过程可自发进行,并且温度的变化方向与ΔG绝对值的变化方向呈正相关,即温度升高,自发的程度也将越大。从表3还可知,ΔG在设定的三个温度下均为负值,表明该吸附过程是以熵而不是焓的变化为主[34]。

表3 葵花籽壳吸附铀的热力学参数Table 3 Thermodynamic parameters of U(Ⅵ)adsorption on sunflower seed shells
3 结 论
通过扫描电镜、红外光谱等方法对吸附铀前后的葵花籽壳进行表征;研究了时间、温度、p H、铀酰离子初始质量浓度、葵花籽壳用量等因素对葵花籽壳静态吸附的影响,并用动力学、热力学吸附数据进行了分析,其结论如下:
(1)扫描电镜分析表明,葵花籽壳表面粗糙多孔,孔结构分布连续而又均匀,孔道规则类似蜂窝状,孔洞还分布在葵花籽壳的内部并互相穿透,有利于吸附;
(2)葵花籽壳吸附铀的最佳p H为5.0~6.0;溶液p H=5.0,葵花籽壳质量浓度为1.00g/L时,饱和吸附量可达29.2 mg/g;在吸附反应进行30min后,葵花籽壳对铀酰离子吸附量也达到了17.9 mg/g,反应进行270min后,葵花籽壳对溶液中铀酰离子吸附量为19.5 mg/g;
(3)葵花籽壳吸附铀的过程符合准二级动力学模型,吸附过程是一个化学吸附过程;
(4)葵花籽壳吸附铀的过程,焓变为正值,反应是吸热过程;熵变为正值,葵花籽壳吸附铀时在固液界面的有序性减小;葵花籽壳对铀的吸附是自发进行的。
[1]刘芳,乔英云,巩志坚,等.农林废弃物的综合利用[C]∥第六届全国绿色环保肥料新技术、新产品交流会论文集.南京,中国腐植酸工业协会,2006.
[2]高慧.Characterization and mechanism of Cr(Ⅵ)removal from aqueous solutions by rice straw[D].长沙:湖南大学,2008.
[3]杨剑梅,高慧,李庭,等.稻草秸秆对水中六价铬去除效果的研究[J].环境科学与技术,2009,32(10):78-82.
[4]陈中兰,曾艳.多胺型稻草纤维素球的制备及其对水体中Zn2+的吸附性能[J].应用化学,2006,23(10):1116-1119.
[5]冯宁川,郭学益,梁莎,等.橘子皮化学改性及其对Cu(Ⅱ)离子的吸附性能[J].中国有色金属学报,2008,18(1):148-154.
[6]冯宁川,郭学益,梁莎,等.皂化交联改性橘子皮生物吸附剂对Cu2+的吸附[J].中南大学学报(自然科学版),2009,40(4):857-862.
[7]孙华雨,王天贵.橘子皮脱铬研究[C]∥中国环境科学学会学术年会优秀论文集.北京,中国环境科学学会,2007.
[8]韩香云,单学凯.香蕉皮吸附废水中铜、锌的研究[J].污染防治技术,2009,22(4):13-14,24.
[9]许彩霞,戴友芝,吴爱明.米糠和麦麸对水中Cr(Ⅵ)的吸附研究[J].水处理技术,2007,33(9):53-56.
[10]甄宝勤.玉米芯处理含镉废水的研究[J].化学与生物工程,2005,22(10):50-51.
[11]甄宝勤.玉米芯处理含锌废水的研究[J].化工技术与开发,2006,35(2):22-24.
[12]王文华,冯咏梅,常秀莲.玉米芯对废水中铅的吸附研究[J].水处理技术,2004,30(2):95-98.
[13]张庆乐,张文平,党光耀,等.玉米芯对废水重金属的吸附机制及影响因素[J].污染防治技术,2008,21(5):21-21,33.
[14]Christian V,Costodes T,Fauduet H,et al.Removal of Cd(Ⅱ)and Pb(Ⅱ)ions from aqueous solutions by adsorption onto sawdust of pinus sylvestris[J].J Hazard Mater,2003,105(1-3):121-142.
[15]何玉燕.改性锯屑对钙镁离子的吸附特性研究[J].能源与环境,2009,2:17-18,47.
[16]侯旭,廖学品,石碧.原位固化落叶松单宁对Cr(Ⅵ)的氧化还原吸附[J].林产化学与工业,2007,27(6):1-7.
[17]杨贯羽,张敬华,邹卫华,等.梧桐树叶吸附铜离子前后红外光谱分析比较[J].光谱实验室,2006,23(2):390-392.
[18]Harshala P,Shreoram J,Niyoti S.Uranium removal from aqueous solution by coir pith:equilibrium and kinetic studies[J].Bioresour Technol,2005,96(11):1241-1248.
[19]杨联敏,陈文纳.改性蔗渣纤维素水处理剂的合成及吸附性能研究[J].广西师范学院学报(自然科学版),2008,25(3):73-77.
[20]Huang L,Zeng G,Huang D,et al.Adsorption of lead(Ⅱ)from aqueous solution onto hydrilla verticillata[J].Biodegradation,2009,20(5):651-660.
[21]叶林顺,谢咏梅,刘慧璇,等.改性稻草吸附铜离子的动力学研究[J].环境科学与技术,2006,29(8):28-30.
[22]叶林顺,莫测辉.改性稻草吸附铜离子过程的内扩散机理[J].环境化学,2007,26(3):323-326.
[23]叶林顺,刘慧璇,谢咏梅,等.改性稻草吸附铜离子的热力学研究[J].环境污染与防治,2005,27(9):664-666.
[24]Montanher S F,Oliveira E A,Rollemberg M C. Removal of metal ions from aqueous solutions by sorption onto rice bran[J].J Hazard Mater,2005,117(2-3):207-211.
[25]张庆芳,杨国栋,孔秀琴,等.改性玉米芯吸附水中Cr6+的研究[J].广东化工,2009,36(4):122-123,147.
[26]Xu T,Liu X Q.Peanut shell activated carbon:characterization,surface modification and adsorption of Pb2+from aqueous solution[J].Chinese J Chem Eng,2008,16(3):401-406.
[27]Zhou L M,Chao S,Liu Z R.Selective adsorption of uranium(Ⅵ)from aqueous solutions using the ion-imprinted magnetic chitosan resins[J].J Colloid Interf Sci,2012,366:165-172.
[28]成芳芳.海藻酸纤维对重金属离子的吸附性能研究[D].青岛:青岛大学,2010.
[29]Zhu S J,Hou H B,Xue Y J.Kinetic and isothermal studies of lead ion adsorption onto Bentonite[J].Appl Clay Sci,2008,40:171-178.
[30]Ali T,Nadide D,Gulsin A,et al.Removal of fluoride from water by using granular red mud:batch and column studies[J].J Hazard Mater,2008,164(1):271-278.
[31]Gode F,Pehlivan E.A comparative study of two chelating ion-exchange resins for the removal of chromium(Ⅲ)from aqueous solution[J].J Hazard Mater,2003,100(1-3):231-243.
[32]Leyva-Ramos R,Geankoplis C J.Model simulation and analysis of surface diffusion of liquids in porous solids[J].Chem Eng Sci,1985,40(5):799-807.
[33]Mpofu V P,Mensah J A,Ralston J.Temperature influence of nonionic polyethylene oxide and anionic polyacrylamide on flocculation and dewatering behavior of kaolinite dispersions[J].J Colloid Interf Sci,2004,271:145-156.
[34]Donia A,Atia A,El-Boraey H,et al.Uptake studies of copper(Ⅱ)on glycidyl methacrylate chelating resin containing Fe2O3particles[J].Sep Purif Technol,2006,49(1):64-70.
Adsorptive properties of Sunflower Seed Shells forin Aqueous Solution
WANG Chang-fu,LIU Zhi-rong*,XUE Gui-rong,LAI Yi,WANG Yun,ZHOU Li-min
College of Chemical,Biological and Material Science,East China Institute of Technology,Nanchang 330013,China
Adsorption characteristics of sunflower seed shells have been studied for U(Ⅵ)removal from aqueous solution.The sunflower seed shells were characterized by elemental analysis,scanning electron microscopy,and FT-IR.Adsorption of U(Ⅵ)from aqueous solution by means of sunflower seed shells was studied in a series of batch experiments.The adsorption behavior of U(Ⅵ)onto the adsorbent was investigated as function of p H value,contact time,initial U(Ⅵ)concentration,temperature etc.The results show that the adsorption capacity is 29.2 mg/g at the p H=5.0 and 35℃with initial U(Ⅵ)mass concentration 50 mg/L and adsorbent dose 1.00g/L.
sunflower seed shells;uranium;adsorption
TL941.19
A
0253-9950(2016)02-0107-09
10.7538/hhx.2016.38.02.0107
2015-09-23;
2015-11-08
国家自然科学基金资助项目(11375043);江西省科技支撑计划资助项目(20133BBF60016,20151BBG7001)
王长福(1988—),男,甘肃武威人,硕士研究生,研究方向为放射性元素分离富集
*通信联系人:刘峙嵘(1969—),男,江西莲花人,博士,教授,主要从事功能环境材料制备及应用研究,E-mail:zhrliu@ecit.cn
