哌啶氮氧自由基与环糊精作用的电化学研究
2016-10-16张文彬赵贺贺
张文彬, 赵贺贺
(1.宜春学院化学与生物工程学院,江西宜春 336000; 2.江西省高校锂电新能源工程技术研究中心,江西宜春 336000)
β-环糊精(β-CD)分子是由7个葡萄糖基连接而成的具有筒状结构的分子,其内部疏水,外部具有亲水性能。β-CD可以包络有机、无机甚至气体分子等,形成的包络物具备特殊结构及特别功能,并广泛地应用于医药、环境、食品、有机合成及分析等领域[1]。因此,研究环糊精包络物的形成、结构及稳定性对这种新材料的应用推广有着重要意义。目前的研究方法主要有热重法[2]、荧光光谱法[3]、核磁共振法[4]及电化学方法。其中,电化学方法因具有简单易行、重现性好尤受关注,已经用于研究一系列有机物与环糊精之间的包络作用[5-10]。
氮氧自由基在生理pH值水溶液体系中稳定,早期主要被当成自旋标记物用来研究药物与生物大分子配体的相互作用[11]。研究表明,氮氧自由基能够捕获体内有害自由基,用于减少自由基引起的机体损伤,主要用于抗心肌缺血/再灌注损伤、抗辐射损伤、抗阿尔兹海默病、抗高血压及肥胖症等[12,13]。本文利用循环伏安法主要研究了2,2,6,6-四甲基哌啶-1-氧化物(TEMPO)哌啶氮氧自由基与β-CD的包络行为,然后通过电流法和电位法,分别测量了TEMPO与β-CD的包络比及包络常数。
1 实验部分
1.1 仪器与试剂
CHI650E电化学工作站(上海辰华仪器公司);FST-Ⅲ-10超纯水机(上海富诗特仪器设备有限公司)。
β-CD、2,2,6,6-四甲基哌啶-1-氧化物(TEMPO)、K2HPO4、KH2PO4,均购于上海阿拉丁有限公司;4-氨基-2,2,6,6-四甲基哌啶氧自由基(TP)购自比利时Acros公司,试剂均为分析纯,未经纯化直接使用。实验用水为超纯水。
1.2 电化学测试
玻碳电极先用Al2O3粉末进行抛光,然后经超纯水冲洗备用。电化学测试技术为循环伏安法。采用三电极体系:玻碳电极为工作电极,Ag/AgCl电极为参比电极,Pt片电极为辅助电极。所有电化学测试在室温下进行。
2 结果与讨论
2.1 氮氧自由基在玻碳电极上的伏安特征
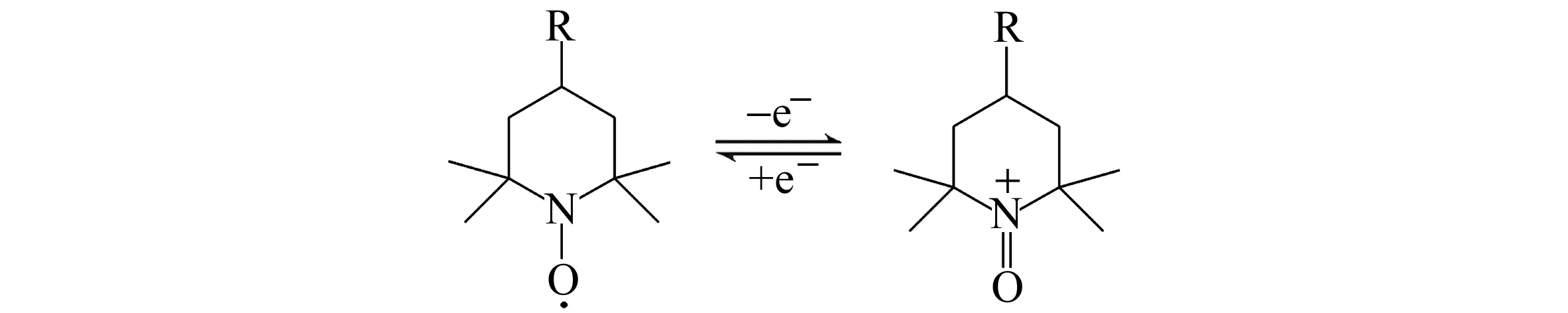
(1)
如式(1)所示,TEMPO以及TP在pH=7.4的磷酸盐缓冲溶液中均表现出可逆的电化学氧化行为(阴、阳极峰值电位相差70 mV左右),其中TEMPO的平衡电位为503 mV,而TP的氧化电位为593 mV,相对于TEMPO正移了90 mV。对于哌啶氮氧自由基,Baur等[14]的研究表明,4位取代官能团给电子能力越强,氧化电位越往正移。而对于吡咯烷氮氧自由基,Manda等[15]认为,3位取代基团给电子能力越强,电化学氧化过程反而更易发生,氧化电位更负。
2.2 β -CD与TEMPO的包络
2.2.1伏安特征由图2可知,当TEMPO水溶液中加入β-CD后,体系循环伏安图表现为峰电流减小,当TEMPO与β-CD的比例为1∶60时,电位由503 mV正移至531 mV,这可归因于TEMPO与β-CD通过疏水作用形成了包络物。从TEMPO的结构上看,亲水性的氮氧自由基为六元哌啶环的一部分,同时还被四个甲基围绕,所以TEMPO表现出较强的疏水性,而对于TP而言对位上的氨基表现出亲水性能,阻碍了TP分子进入β-CD内腔。自由基分子疏水链的存在使得某些氮氧自由基能够与环糊精形成包络物,这一点得到了电子顺磁共振(EPR)及电子自旋共振(ESR)实验的证实。汪汉卿等[16]通过EPR证明4-羟基-2,2,6,6-四甲基哌啶氧自由基、4-叠氮基-2,2,6,6-四甲基哌啶氧自由基及4-苯磺酰氧-2,2,6,6-四甲基哌啶氧自由基能够与β-CD相互作用而形成包络物,Birrell等[17]和Knyazev等[18]利用ESR技术证明脂肪酸氮氧自由基与CD之间存在包络反应。可以认为,β-CD与TEMPO形成的包络物,由于体积较大,表观扩散系数相对于TEMPO减小,所以峰电流减小,峰电位正移说明形成包络物后在电极上发生氧化还原反应所需要克服的活化能增大。
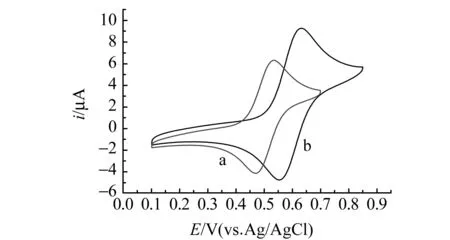
图1 1 mmol/L TEMPO(a)和TP(b)在pH=7.4磷酸盐缓冲溶液中的循环伏安图Fig.1 Cyclic voltammograms of 1 mmol/L TEMPO(a) and TP(b) in pH=7.4 phosphate buffer solution scan rate:50 mV/s.
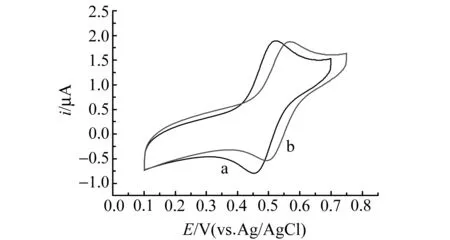
图2 TEMPO及其CD包络物在扫描速度50 mV/s时循环伏安图Fig.2 Cyclic voltammograms of TEMPO and its cyclodextrin inclusion complex with scan rate 50 mV/s a:2.0×10-4 mol/L TEMPO;b:a+1.2×10-2 mol /L CD.
2.2.2包络比及包络常数测量董绍俊等[5]指出,可以根据电位或者电流的变化来计算包络比及包络常数。对于TEMPO体系,可用以下方程式表示:

(2)
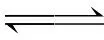
(3)
其中,m为包络比,令解离常数Kd为:
(4)
当[CD]≫[TEMPO]时,[CD]≈[CD]0,上式(4)结合能斯特方程有:
(5)
其中,DT-CD为TEMPO-CDm包络物扩散系数,DT为TEMPO的扩散系数,二者可以通过以峰值电流ip对扫描速度平方根v1/2作图而得。如图2(a)所示,TEMPO/CD体系表现出良好的可逆行为,满足下式:
ip=(2.69×105)AD1/2v1/2c0
(6)
其中,A为电极表面积,c0为电活性物质浓度。
图3为β-CD浓度为0 mol/L及12 mmol/L时ip与v1/2关系图,从图中可以看出,ip与v1/2表现出良好的线性关系。根据式(6),TEMPO-CDm包络物扩散系数与TEMPO的扩散系数比值DT-CD/DT可由线性拟合斜率值计算而得,有DT-CD=0.85DT,这也证明了前文所述峰值电流值减小是因为电活性物扩散系数变化导致。图4表明,对于TEMPO体系,实验结果发现△Ep与ln[CD]0呈良好线性关系,线性回归方程为:△Ep=127+20ln[CD]0,结合式(5)计算可得包络比m=0.78,可近似为1。Kd计算为6.47×10-3,包络常数Ks=1/Kd为154 L/mol。
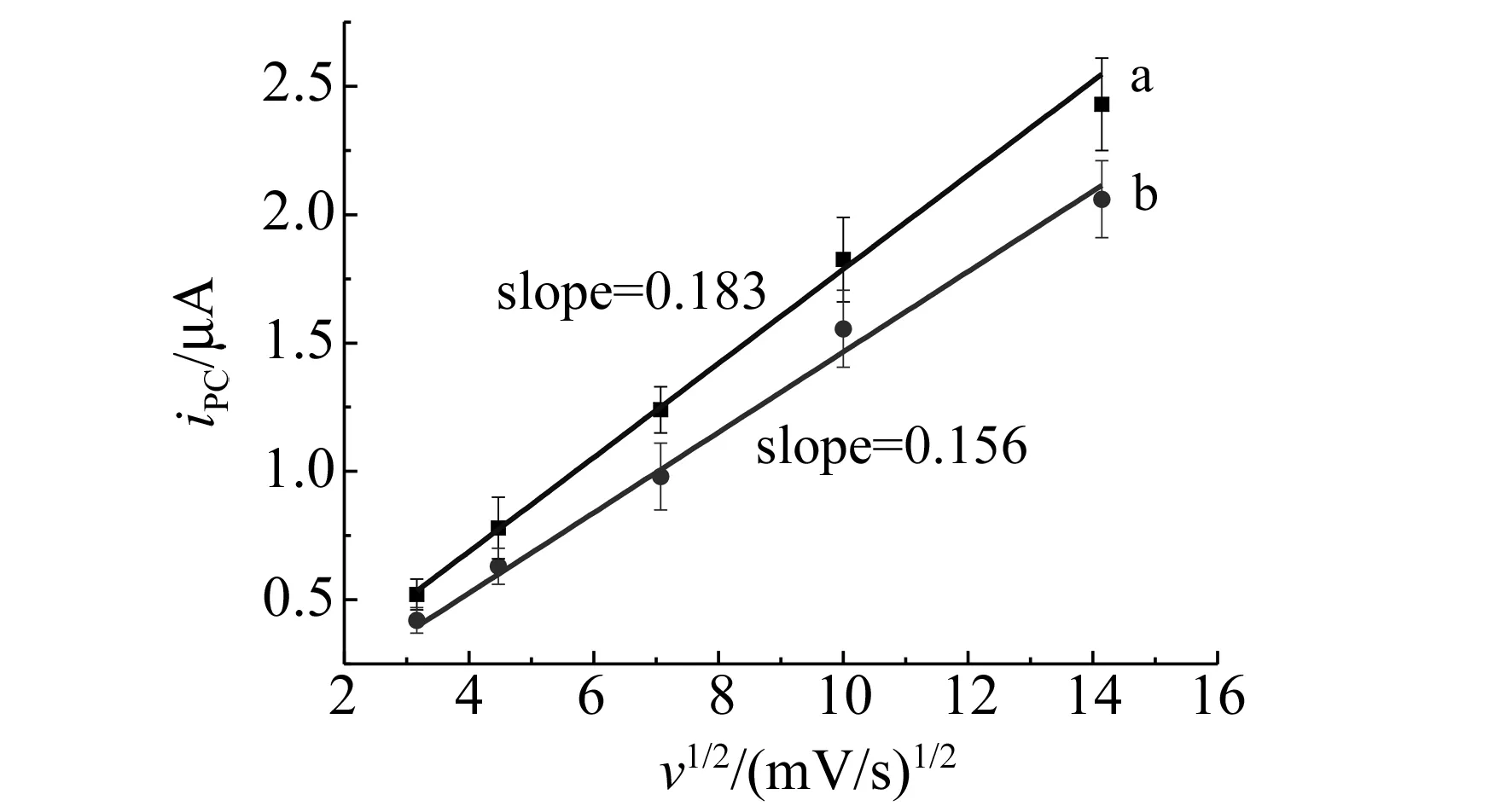
图3 不同浓度β -环糊精时扫描速度平方根v1/2与阳极峰值电流ipc关系Fig.3 Relationship between square root of scan rate v1/2 and cathodic peak current ipc at different concentration of β -cyclodextrin a:[CD]=0 mol/L;b:[CD]=12 mmol/L.

图4 TEMPO/CD水溶液体系中△Epa与ln[CD]0关系Fig.4 Relationship between△Epa and ln[CD]0 in the TEMPO/CD aqueous solution system
对于包络比为1∶1的β-CD/TEMPO体系,表观扩散系数Dobs可表示为:
(7)
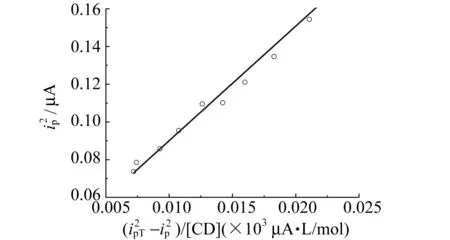
图5 TEMPO的β -CD包络物与关系Fig.5 Relationship between and of cyclodextrin inclusion complex containing TEMPO
结合式(6)可推导得
(8)
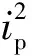
3 结论
作为一种常用的电化学技术,循环伏安法证明了可以用来研究β-CD与TEMPO的包络行为。结果表明β-CD与TEMPO可以形成超分子包络物,利用峰电流和峰电位的变化可以求出包络物的包络比和包络常数。通过电位法即△Epa与ln[CD]0关系式计算出β-CD与TEMPO的包络比为1∶1,包络常数为154 mol/L,接近于电流法计算的164 mol/L的结果。本文工作将为拓宽氮氧自由基在医药工业中的应用提供有益参考。
