高硅高铁粉煤灰制备SiO2的工艺研究
2016-10-14缪应菊沈秋玉连明磊
缪应菊,沈秋玉,周 钰,连明磊
(六盘水师范学院化学与化学工程系,六盘水 553004)
高硅高铁粉煤灰制备SiO2的工艺研究
缪应菊,沈秋玉,周钰,连明磊
(六盘水师范学院化学与化学工程系,六盘水553004)
以碳酸钠为活化剂活化粉煤灰,考察原料配方、焙烧条件(温度、时间)、酸浸条件(用量、浓度)、溶胶—凝胶条件(初始浓度、温度)对SiO2产率的影响。结果表明:(1)当m粉煤灰:m碳酸钠≥1∶1.8或焙烧温度超过850 ℃时,样品发生烧结无法从坩埚中取出,而致酸浸分解率和SiO2产率为零;(2) 粉煤灰在没有助剂条件下进行高温活化,酸浸分解率为24.13%,无SiO2产品;(3)盐酸浓度和溶胶-凝胶液的初始浓度对SiO2的产率基本无影响;(4)温度是影响溶胶-凝胶的显著因素;(5)最佳工艺条件为:m粉煤灰∶m碳酸钠=1∶1.2、焙烧温度800 ℃、焙烧时间2 h;凝胶-凝胶水浴温度94 ℃,SiO2的产率可达85.35%。
粉煤灰; SiO2; 工艺; 影响因素
1 引 言
粉煤灰是粉煤燃烧后的烟气中收捕下来的细灰,是燃煤电厂排出的主要固体废物之一,粉煤灰含有丰富的SiO2(23.1%~62.4%)、Al2O3(17.8%~30%)、Fe2O3(2.0%~7.1%)[1]等氧化物,可作为SiO2、Al2O3等提取的重要原料。目前,关于提取粉煤灰中SiO2的文献报道很多,但主要涉及粉煤灰中SiO2的纯度[2,3]、品质[4,5]、形貌结构[6,7]及提取工艺路线[8-10]的经济合理性等方面,对于粉煤灰中硅的产率的研究很少。
文章以高硅高铁粉煤灰[11]为原料,采用粉煤灰活化—盐酸酸浸—溶胶-凝胶的方法制备SiO2,以酸浸分解率及SiO2产率为评价指标,对SiO2提取过程中的诸多因素进行研究和分析,寻求合理的粉煤灰制备SiO2的工艺技术路线,以为粉煤灰提取SiO2的工业应用提供技术支持。
2 实 验
2.1实验试剂及仪器
试剂:粉煤灰,六盘水黔桂电厂;无水碳酸钠 (AR,重庆茂业化学试剂有限公司);盐酸(AR,重庆江川化工有限公司);无水乙醇(AR,天津市富宇精细化工有限公司)。
仪器:KQ-300DE数控超声波清洗机,昆山市超声仪器有限公司;TG1650-WS离心机,湖南赛特湘仪离心机仪器有限公司;DZ-88电热恒温真空干箱,上海跃进医疗器械厂;FA1004分析天平,上海上平责任有限公司;HWSK-5马沸炉,鹤壁市华通分析仪器公司;HH-S恒温水浴锅,金坛市恒丰仪器厂。
2.2实验方法
碳酸钠活化粉煤灰主要是形成硅铝酸盐等易溶于酸的产物,为提高粉煤灰中硅、铝的活性,以盐酸为酸浸液,考察了原料配方、焙烧温度、焙烧时间及酸浸液用量和浓度对硅、铝溶出率的影响,溶出率越高则SiO2产率也高,为研究硅酸溶液溶胶—凝胶条件对产率的影响,考察了溶胶液初始浓度和温度的影响,具体实验步骤见下:
(1)准确称取1∶1.2(质量比,下同)的粉煤灰(计m1)和碳酸钠于105 ℃的烘箱内干燥24 h,冷至室温后混合均匀置于瓷坩埚内在800 ℃马弗炉内焙烧2 h,焙烧结束后取出置于干燥皿中待用;
(2)将上述样品置于250 mL烧杯中,边搅拌边加入35 mL的3 mol/L的盐酸溶液,待溶解结束后,过滤、洗涤至中性,将滤渣置于105 ℃的烘箱内干燥24 h后,冷至室温称量计m2。
(3)将上述所得滤液放入恒温水浴锅中进行溶胶-凝胶,待溶胶-凝胶结束后,采用20 mL的1 mol/L的盐酸溶液进行二次酸浸并离心分离,将产物置于105 ℃的恒温真空干箱中干燥24 h,计m3。
2.3评价指标
工艺条件的优化以焙烧熟料的酸浸分解率和SiO2产品的产率进行评价,粉煤灰活化效果越好,酸浸分解率越高,其产率也高。分解率的计算式见式(1),产率的计算式见式(2)。
(1)
(2)
式中,η1、η2-粉煤灰分解率、SiO2产率,%;m0-SiO2理论质量,g;m1-粉煤灰质量,g;m2-酸浸残渣质量,g;m3-SiO2实验产量,g。
3 结果与讨论
3.1粉煤灰与碳酸钠质量配比的影响
粉煤灰和碳酸钠用量按1∶0、1∶0.6、1∶0.8、1∶1.0、1∶1.2、1∶1.4、1∶1.6、1.8、1∶2.0进行配比,除质量配比外其余过程均按1.2进行实验,结果见图1。
由图1可看出,当碳酸钠用量为0时,焙烧熟料的酸浸分解率为24.13%,且没有SiO2产品,说明酸浸液中基本没有硅化合物,仅高温活化粉煤灰并不能改变粉煤灰中硅的结构使之与盐酸发生反应进入溶液体系;随着Na2CO3用量的增加,粉煤灰的分解率和SiO2产率逐渐增加,当m粉煤灰∶m碳酸钠=1∶1.4时酸浸分解率为95.61%,SiO2产率为86.40%,当m粉煤灰∶m碳酸钠=1∶1.6时酸浸分解率和SiO2产率略有下降,当m粉煤灰∶m碳酸钠≥1∶1.8时,由于样品发生烧结无法从坩埚中取出进行酸浸,而致酸浸分解率和产率迅速降为零。
碳酸钠用量在0.6~1.4的范围内,酸浸分解率和产率略有增加,但增加幅度较缓,结合实验过程中焙烧熟料的蓬松度、从坩埚中取出的难易程度,及降低原料成本和保护焙烧设备的角度,建议粉煤灰与碳酸钠的质量配比采用1∶1.2较为适宜。此时,焙烧熟料的酸浸分解率为95.58%,SiO2产率为85.89%。
3.2焙烧温度的影响
考察焙烧温度在室温(~25 ℃)、650 ℃、700 ℃、750 ℃、800 ℃、850 ℃、900 ℃粉煤灰的酸浸分解率与SiO2产率的变化关系,除焙烧温度外其余过程均按1.2进行实验,结果见图2。由图2可看出:在25~800 ℃的范围内,焙烧熟料的酸浸分解率及SiO2产率随着焙烧温度的增加而增加,当焙烧温度≥850 ℃时,由于样品发生烧结无法从坩埚中取出进行酸浸,而致酸浸分解率和产率迅速降为零。经800 ℃焙烧后,焙烧熟料的酸浸分解率可达96.28%,SiO2产率为86.03%。
3.1中将粉煤灰原料在800 ℃的马弗炉中焙烧2 h后酸浸,酸浸分解率为24.13%,无SiO2产品;本考察条件下粉煤灰不焙烧直接酸浸,酸浸分解率为65.52%,也无SiO2产品。粉煤灰原料直接焙烧,酸浸分解率急剧下降,说明焙烧不能提高粉煤灰的活性,使粉煤灰中的矿物晶型发展得更稳定,不利于粉煤灰中各元素的溶出;当焙烧活化过程中有碳酸钠助剂参与时,酸浸分解率和SiO2产率均增加,说明高温活化过程中,碳酸钠的参与可改变粉煤灰中各元素的化学结构,使其易于与盐酸反应。
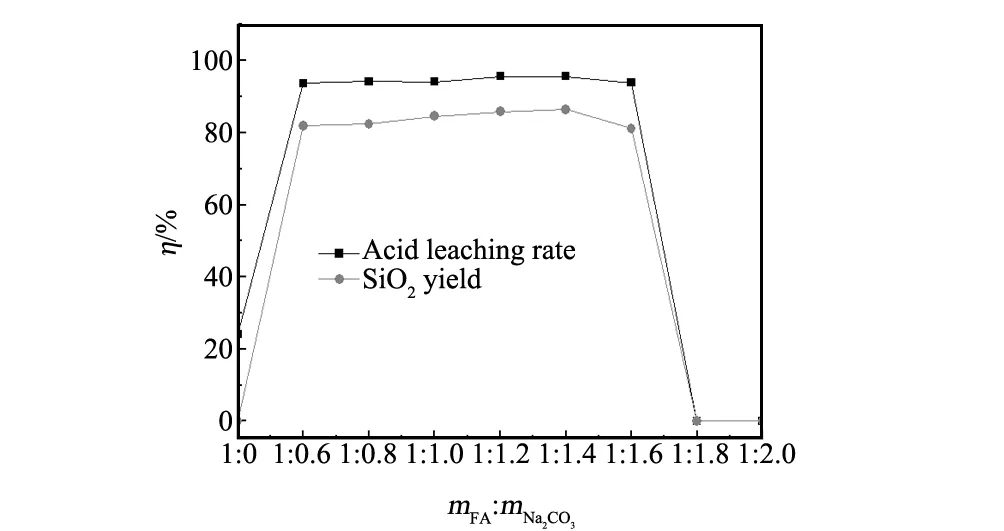
图1 物料配比对酸浸分解率及SiO2产率的影响Fig.1 Effect of material ratio on acid leaching rate and SiO2 yield
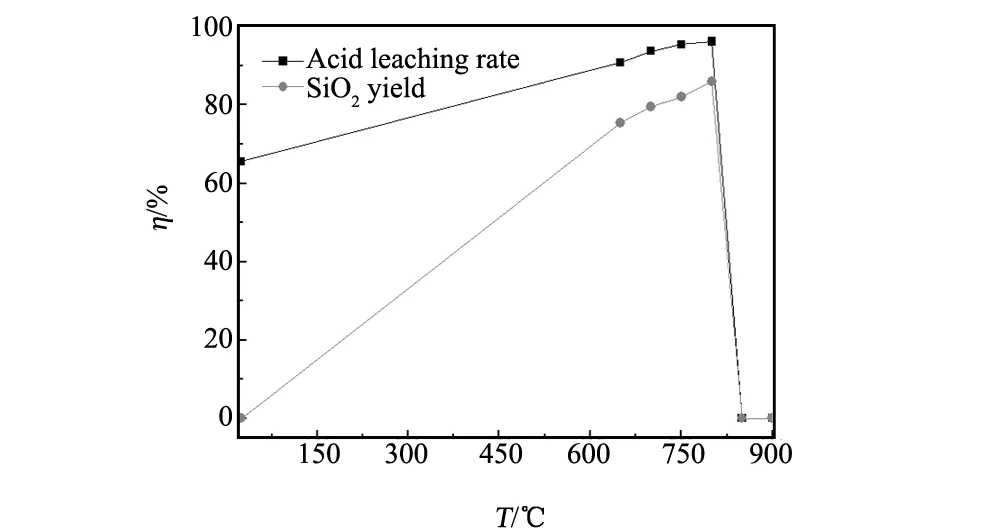
图2 焙烧温度对酸浸分解率及SiO2产率的影响Fig.2 Effect of calcination temperature on acid leaching rate and SiO2 yield
3.3焙烧时间的影响
将粉煤灰和碳酸钠按照1∶1.2的质量进行配比后,混合均匀置于800 ℃马弗炉内分别焙烧0 h、0.5 h、1 h、1.5 h、2 h、2.5 h、3 h,其余过程按照2.2进行实验,结果见图3。
由图3可看出:随着焙烧时间的延长,焙烧产物的酸浸分解率及SiO2产率也随之增大;当焙烧时间为2 h时,分解率和SiO2产率分别为95.87%、85.52%;当焙烧时间超过2 h后,分解率和SiO2产率略有降低。在0.5~3 h的时间范围内,焙烧产物的酸浸分解率变化幅度不大,但SiO2产率的变化幅度较明显,原因可能是在该焙烧时间范围内,在焙烧前期碳酸钠更容易与粉煤灰中的铁、铝等氧化物进行反应,随着活化程度的进行,一些结构比较稳定的硅氧化物参与到活化过程。
3.4酸浸液用量的影响
将5份m粉煤灰∶m碳酸钠为1∶1.2的混合物搅拌均匀后置于800 ℃的马弗炉内焙烧2 h,焙烧结束后向焙烧产物中分别加入3.0 mol/L 的盐酸溶液15 mL 、20 mL、30 mL、35 mL、40 mL,其余过程均按2.2进行实验,其酸浸分解率及SiO2产率如图4所示。
由图4可看出:焙烧产物在酸浸过程中,随着盐酸用量的增加酸浸分解率及SiO2产率均呈先增加后减少的变化趋势。是因为粉煤灰与碳酸钠焙烧过程中,粉煤灰中的硅、铝、铁等氧化物与碳酸钠反应生成可溶于酸的硅酸盐、铝酸盐或硅铝酸盐[2],当酸浸液用量小于35 mL时,酸浸反应不彻底,焙烧产物中大量可溶于酸的硅酸盐或铝酸盐或硅铝酸盐未充分溶解,导致分解率低以致于产率也低;当酸浸液用量为35 mL时,焙烧产物的可溶于酸的化合物以基本反应结束,分解率和SiO2的产率分别为95.47%、85.22%;当酸浸液用量超过35 mL时,酸浸体系中H+过量,有利于硅酸凝胶的形成[12]进入酸浸残渣,从而使酸浸分解率和SiO2的产率都下降。
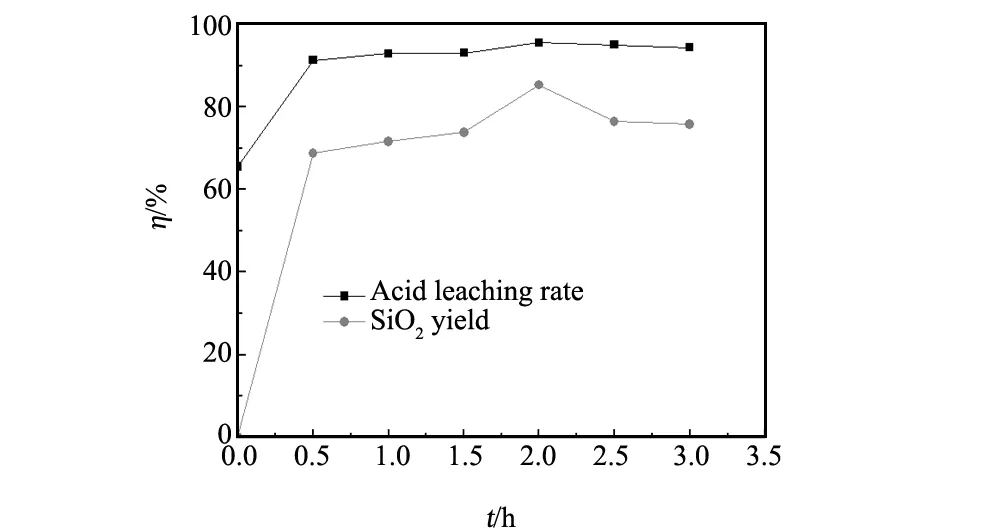
图 3 焙烧时间对粉煤灰分解率及SiO2产率的影响Fig.3 Effect of roasting time on acid leaching rate and the yield of SiO2
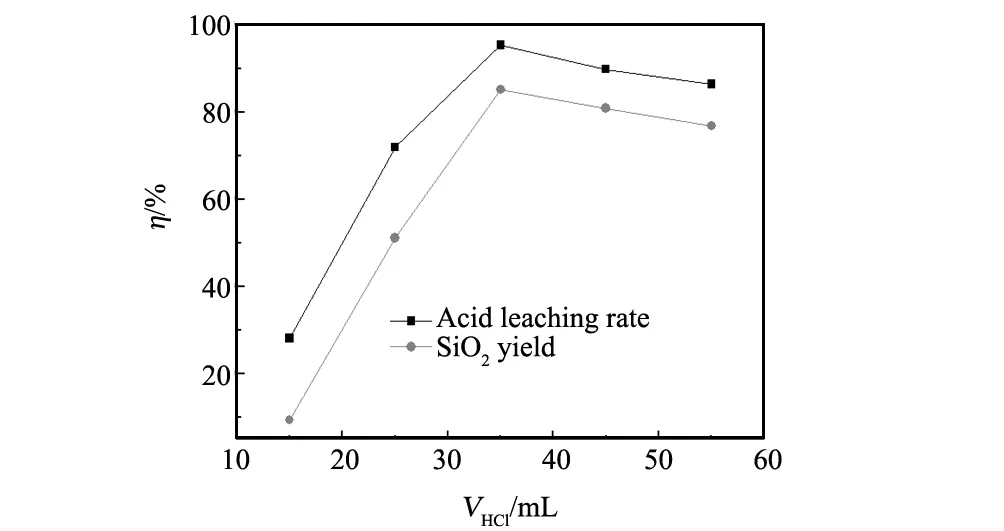
图4 盐酸用量对酸浸分解率及SiO2产率的影响Fig.4 Effect of hydrochloric acid dosage on acid leaching rate and the yield of SiO2
3.5盐酸浓度的影响
将5份m粉煤灰∶m碳酸钠为1∶1.2的混合物搅拌均匀后置于800 ℃的马弗炉内焙烧2 h,焙烧结束后向焙烧熟料中分别加入0.105 mol不同浓度∶1.5 mol/L、2.0 mol/L、2.5 mol/L、3.0 mol/L、3.5 mol/L的盐酸溶液,其余过程均按1.2进行实验,考察H+摩尔数相同的情况下,酸浸液浓度对分解率和产率的影响,实验结果见图5。
由图5可看出:在H+摩尔数相等的前提下,改变酸浸液的浓度,分解率和产率呈现增加后减小的变化趋势,酸浸分解率分别最高为95.63%最低93.45%,对应SiO2产率分别为85.05%和84.34%,变化幅度很小,与文献[13]报道一致。文献[3]报道当盐酸浓度为2.62 mol/L时,硅胶中的Al2O3含量较多,影响SiO2产品纯度和粒度,由于实验过程中对凝胶所得产品进行二次酸浸,因此可判断实验过程中酸浸液的浓度仅影响产品的粒度,对产品的产率影响可忽略不计。实验过程中,为缩短溶胶-凝胶的时间和虑液量,选择浓度略大的3.0 mol/L的盐酸进行实验。
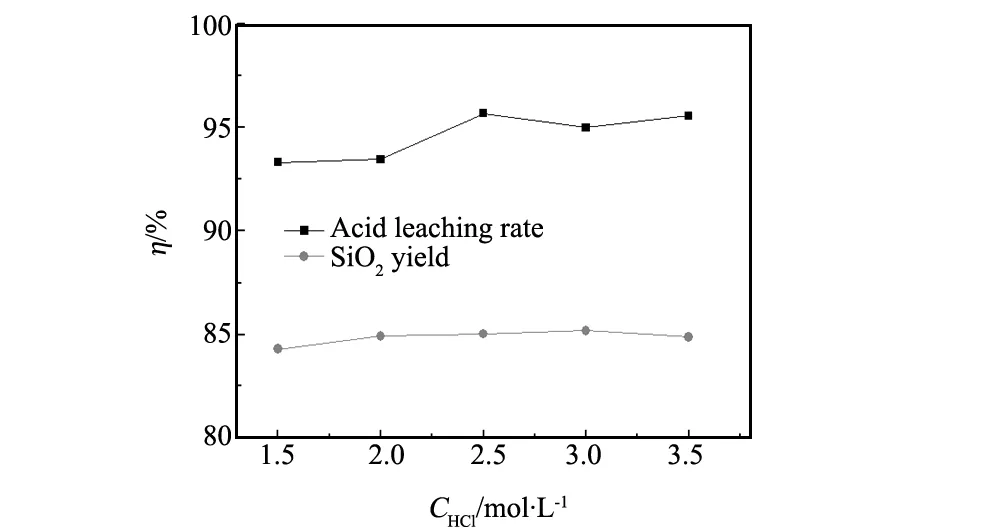
图 5 酸浸液浓度对粉煤灰分解率及SiO2产率的影响Fig.5 Effect of hydrochloric acid concentration on acid leaching rate and the yield of SiO2
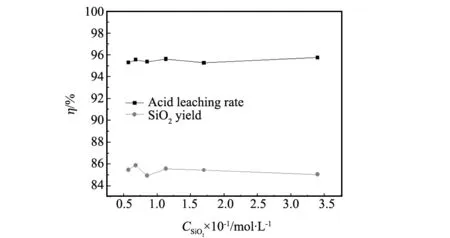
图6 相同分解率下溶胶-凝胶初始浓度对SiO2产率的影响Fig.6 Effect of initial concentration of sol-gel on the yield of SiO2
3.6溶胶-凝胶液液初始浓度的影响
在800 ℃、2 h的马弗炉中焙烧m粉煤灰∶m碳酸钠为1∶1.2的混合物6份,加入3 mol/L的盐酸溶液35 mL进行酸浸,过滤所得酸浸液分别用水稀释至50 mL、100 mL、150 mL、200 mL、250 mL、300 mL,并用浓度为1 mol/L的盐酸溶液调节pH值<0.5后进行溶胶-凝胶,其余过程均按2.2进行实验,分解率和SiO2的产率变化见图6。
由图6可看出:分解率的变化趋势和产率的变化趋势基本一致,且SiO2的产率与其初始浓度没有显著联系,结合实验中溶胶-凝胶过程结束的时间分析,凝胶-溶胶液的初始浓度仅与形成凝胶的时间有关,浓度越大凝胶时间越短,与文献[14]报道一致。实验过程中,从能耗角度考虑,选择3.5×10-1mol·L-1(溶液体积为50 mL)的初始浓度进行实验。
3.7溶胶-凝胶温度的影响
在800 ℃、2 h的马弗炉中焙烧m粉煤灰∶m碳酸钠为1∶1.2的混合物6份,加入3 mol/L的盐酸溶液35 mL进行酸浸,过滤所得酸浸液用水稀释至50 mL,并用浓度为1 mol/L的盐酸溶液调节pH值<0.5后进行溶胶-凝胶,考察室温(~25 ℃)、45 ℃、65 ℃、75 ℃、85 ℃、94 ℃,共6个溶胶—凝胶温度下分解率和SiO2的产率变化关系,其余过程均按2.2进行实验,结果见图7。
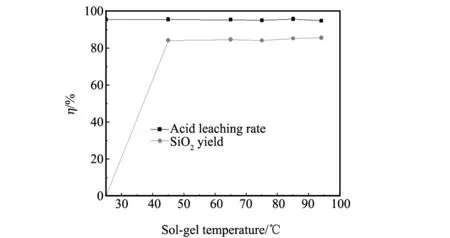
图7 相同分解率下溶胶-凝胶温度对SiO2产率的影响Fig.7 Effect of sol-gel temperature on the yield of SiO2
由图7可看出:在溶胶-凝胶的过程中,室温下没有SiO2产品,结合实验过程分析,将酸浸液室温放置24 h、36 h、1周均未见溶液溶胶-凝胶,且随着放置时间的延长,烧杯底部似有微量沉淀产生;当提高酸浸液溶胶-凝胶温度后,随着温度的提高,SiO2的产率没有显著变化,但溶胶产生的时间缩短且凝胶形成到凝胶结束的时间也缩短。
为确定溶胶—凝胶与温度关系更显著而不是浓度,在800 ℃、2 h的马弗炉中焙烧m粉煤灰∶m碳酸钠为1∶1.2的混合物,加入3 mol/L的盐酸溶液35 mL进行酸浸,过滤所得滤液用水稀释至50 mL,并用浓度为1 mol/L的盐酸溶液调节pH值<0.5后放置室温(~25 ℃)进行溶胶-凝胶,随着时间的推移12 h→24 h→36 h→72 h→1周,仅观察到烧杯底部有微量沉淀,但仍未观察到溶胶-凝胶的形成。由此可见,温度对体系的影响较为显著,在94 ℃的水浴条件下,溶胶-凝胶过程仅需约2 h,SiO2产率可达85.69%。
4 结 论
(1)考察粉煤灰原料配方和焙烧条件时,当m粉煤灰∶m碳酸钠≥1∶1.8或焙烧温度超过850 ℃时,样品发生烧结无法从坩埚中取出进行酸浸,而致酸浸分解率和产率为零;
(2)粉煤灰在没有助剂条件下进行高温活化,酸浸分解率为24.13%,无SiO2产品;
(3)盐酸浓度和溶胶-凝胶液的初始浓度对SiO2的产率基本无影响;
(4)温度是影响溶胶-凝胶的显著因素;
(5)SiO2制备的最佳工艺条件为:m粉煤灰∶m碳酸钠为1∶1.2、焙烧温度800 ℃、焙烧时间2 h时,用3.0 mol/L的盐酸进行酸浸,酸浸分解率为95.48%;溶胶-凝胶水浴温度为94 ℃时,SiO2的产率为85.35%。
[1] 钱觉时,吴传明,王智.粉煤灰的矿物组成(上)[J].粉煤灰综合利用,2001,(1):26-31.
[2] Halina M,Ramesha S,Yarmob M A,et al.Non-hydrothermal synthesis of mesoporous materials using sodium silicate from coal flyash[J].Mater.Chem.Phys.,2007,101(2):322-351.
[3] 王蕾,马鸿文,聂轶苗,等.利用粉煤灰制备高比表面积二氧化硅的实验研究[J].硅酸盐通报,2006,25(2):3-7.
[4] Bai G H,Teng W,Wang X G,et al.Processing and kinetics studies on the alumina enrichment of coal fly ash by fractionating silicon dioxide as nano particles[J].FuelProcessingTechnology,2009,(91):175-184.
[5] 李秀悌,姚志通,孙杰,等.利用粉煤灰制取白炭黑及其表面改性研究[J].功能材料,2010,41(6):939-942,947.
[6] 班卫静,周霞萍,柯一龙.粉煤灰短流程制取白炭黑的研究[J].洁净煤技术,2011,17(6):99-102.
[7] 李歌,马鸿文,刘浩,等.粉煤灰碱溶脱硅液碳化法制备白炭黑的实验与硅酸聚合机理研究[J].化工学报,2011,62(12):3580-3587.
[8] 荆富,伊茂森,张忠温,等.粉煤灰提取白炭黑和氧化铝的研究[J].中国工程科学,2012,14(2):96-106.
[9] 方俊.粉煤灰渣湿法制备水玻璃和白炭黑工艺研究[D].安徽:安徽理工大学学位论文,2013.
[10] Xu Z F,Zhang M X,Zhu J B,et al.Extraction of nano-α-Al2O3and SiO2from fly ash at low temperature conditions[J].IntegratedFerroelectrics,2013,147(1):8-16.
[11] 缪应菊,连明磊,胡江良,等.六盘水粉煤灰理化性质分析及资源化利用途径[J].无机盐工业,2014,46(7):8-10,46.
[12] 王梅,李辽沙,金霞,等.有盐体系中pH值对硅酸聚合度的影响[J].安徽工业大学学报(自然科学版),2007,24(2):143-145,149.
[13] 王星东,王亚军,杨武利,等.纳米沸石胶体化学性质的研究[J].化学学报,2003,61(3):354-358.
[14] 沈钟,赵振国,康万利.胶体与表面化学(第四版)[M].北京:化学工业出版社,2012.
Process of Preparing SiO2by High Iron and Silicon Fly Ash
MIAOYing-ju,SHENQiu-yu,ZHOUYu,LIANMing-lei
(Department of Chemistry and Chemical Engineering,Liupanshui Normal University,Liupanshui 553004,China)
Using sodium carbonate as activator, the mass ratio of sodium carbonate and fly ash, the roasting temperature and time, the dosage of hydrochloric acid, the concentration of hydrochloric acid, the Sol-gel initial concentration and water-bath temperature were investigated. The results showed that (1) whenmfly ash∶msodium carbonate≥1∶1.8 or calcination temperature above 850 ℃, the sample cannot be removed from the crucible, and the decomposition rate of acid leaching and the yield of SiO2is zero. (2) The high temperature activation of fly ash in the absence of auxiliaries, acid leaching rate of 24.13%, no SiO2products. (3) The initial concentration of the sol-gel solution and the concentration of hydrochloric acid had no effect on the yield of SiO2. (4) Temperature is a significant factor affecting the sol-gel experiments; (5) The optimum technological conditions were:mfly ash∶msodium carbonate=1∶1.2, calcination temperature 800 ℃, roasting time 2 h, the sol-gel water -bath temperature 94 ℃, the yield of SiO2can be up to 85.35% .
fly ash;SiO2;technology;influence factors
贵州省教育厅高等学校创新人才团队(黔教合人才团队字[2014]46);贵州省教育厅自然科学研究项目(黔教合KY字[2013]201);贵州省科技厅资助项目(黔科合J字LKLS[2013]25);贵州省教育厅特色重点实验室资助项目(黔教高发:2011-278)
缪应菊(1983-),女,副教授.主要从事固体废弃物资源化利用研究.
TQ175
A
1001-1625(2016)04-1260-05
