全基因组外显子测序技术在遗传性纤维蛋白原异常家系致病基因的克隆鉴定中的应用
2016-10-09刘晓娣张新友宋通微洪澄英
刘晓娣 张新友 宋通微 洪澄英

[摘要]目的研究采用全基因组外显子测序技术在遗传性纤维蛋白原异常家系致病基因鉴定中的应用价值。方法采集12例遗传性纤维蛋白原异常患者及其核心家庭成员外周血检测凝血指标,并提取其基因组DNA进行全基因组外显子测序,分析测序结果,探讨遗传性纤维蛋白原异常的分子机制。结果全基因组外显子测序结果显示:先证者A1、A4以及B2均为FGA基因g,1233G>A突变,A1的妹妹、A4的父亲以及B2的母亲均携带有相同的突变;A2、A7、B4和B5均为FGG基因g,10819G>A突变,家系成员中A2的母亲和外婆、A7的姐姐和女儿、B4的母亲和B5的母亲均携带有相同的突变;A3、A5、A6、B1和B3及其相关亲属共10例携带有FGB基因g,9692A>G突变。先证者及家系主要成员中发生Fg基因突变的成员APTT、PT和TT均明显延长,但Fg活性显著降低。结论遗传性纤维蛋白原异常可由多种Fg基因外显子突变导致,FGB和FGG外显子突变较为常见。
[关键词]遗传性纤维蛋白原异常;全基因组外显子测序;家系致病基因;基因突变
[中图分类号]R554.5
[文献标识码]A
[文章编号]2095-0616(2016)03-33-04
纤维蛋白原(Fgrinogen,Fg)能够在凝血酶作用下修饰成为纤维蛋白,在止血过程中发挥重要的生理作用,同时又可激活纤溶系统防止血栓的形成,Fg在集体出血与止血平衡中发挥重要的作用。遗传性异常纤维蛋白原血症(inheriteddvsfgrinogenemia)是人群中罕见的一种常染色体杂合显性遗传病,纯合显性遗传者少见,该病发病率低,患者多数仅表现为轻微隐匿性症状。Fg基因较为复杂,从分子发病机制上方能很好地研究和诊断遗传性异常纤维蛋白原血症。本研究于2015年1~8月针对我院收集的遗传性纤维蛋白原异常患者及其具有直接血缘关系的亲属和正常健康者,进行表型和基因分析,旨在从功能上探讨遗传性纤维蛋白原异常的分子发病机制。
1.资料与方法
1.1一般资料
选取遗传性纤维蛋白原异常患者及其具有直接血缘关系的亲属和正常健康者参与本研究。其中,已确诊的该疾病2个家系先证者共计12例,A家系7例,B家系5例先证者家系中的核心家系内成员共26例,A家系15例,B家系11例;正常健康者200例。12例先证者中有5例因消瘦原因就诊,生化检查表现为凝血酶原时间(PT)及凝血酶时间(TT)延长,活化部分凝血时间(Am)正常,纤维蛋白原(Fg)活性明显降低;3例先证者无临床症状,但易发生瘀斑、伤口愈合延迟,有自发流产史;4例先证者表现为经期经血过多,凝血较差,术前检查为TT显著延长,Fg活性下降。所有先证者平常均无自发出血、血栓病史,心脑、肝、肾功能均正常,所在家系中无近亲结婚史,所有成员亦无自发出血、血栓病史,心脑、肝、肾功能均正常。
所有患者在采集血液等样本和个人信息时均知情同意并签字,本研究经我院伦理委员会同意批准进行。
1.2研究方法
1.2.1样本收集及处理在知情同意的情况下,采集患者、家系成员静脉血,以0.109mol/L枸橼酸钠1:9抗凝,4℃下1500rpm离心15min,将血浆-进行分装于洁净冻存管中进行标记,冷冻于70℃超低温冰箱保存。提取所有研究对外周血细胞中基因组DNA进行外显子测序,-80%保存备用。
1.2.2家系基因分析通过QIAGEN公司生产的QIAamp DNA Blood Mini Kit提取从采集的血浆样本中提取研究对象的基因组DNA作为下步基因扩增的模板。家系基因分析采用测序方法找寻突变位点,测序方法为全基因组外显子测序。
根据美国国家生物技术信息中心(NationalCenter of Biotechnology Information,NCBI)基因库中公布的Fg基因序列(FGB ID:2244;FGA ID:2243;FGG ID:2266),利用Primer Premier 5.0软件设计23对引物以覆盖Fg基因的24个外显子区域及其启动子序列,其中FGA引物5对,FGB引物8对,GGG引物10对。将提取得到的DNA随机打断,将片段化的DNA分子在酶的作用下补齐随机打断造成的黏性末端而成为平末端,连接接头,通过NimbleGen外显子序列捕获芯片捕获目标外显子区域,检测其捕获效率;然后对捕获的目标片段进行PCR扩增,产物连接后随机打断,末端补平及加“A”碱基,连接测序接头,PCR扩增并检测序文库的质量,最后利用illumina公司NextSeq 500测序仪进行测序。
PCR扩增反应体系为:上下游引物各1.5uL、模板DNA 2uL、dNTP混合物2uL、10×PCR反应缓冲液2.5uL、Taq DNA聚合酶0.2uL、无菌超纯水15.3uL,总体积25uL。PCR扩增条件为:95℃预变性30sec→95℃变性30sec→52~63℃退火30sec→72℃延伸45sec。
1.2.3表型分析将采集的研究对象的外周血,以0.109mol/L枸橼酸钠1:9抗凝,4℃下3000rpm离心10min,取血浆检测凝血酶原时间(PT)、活化的部分凝血活酶时间(APTT)、凝血酶时间(TT)、Fg活性。
2.结果
2.1家系基因分析结果
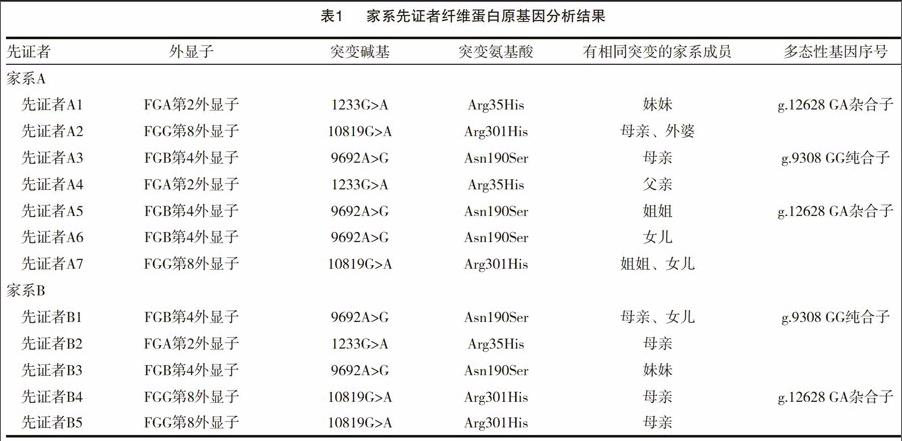
家系A和B中的12例先证者纤维蛋白原基因分析结果见表1,先证者A1、A4以及B2均为FGA基因第2外显子g,1233G>A突变,A1的妹妹、A4的父亲以及B2的母亲均携带有相同的突变;A2、A7、B4和B5均为FGG基因第8外显子g,10819G>A突变,家系成员中A2的母亲和外婆、A7的姐姐和女儿、B4的母亲和B5的母亲均携带有相同的突变;A3、A5、A6、B1和B3及其相关亲属共10例携带有FGB第4外显子g.9692A>G突变。家系其他成员及健康对照基因检测均未发现异常。见表1。
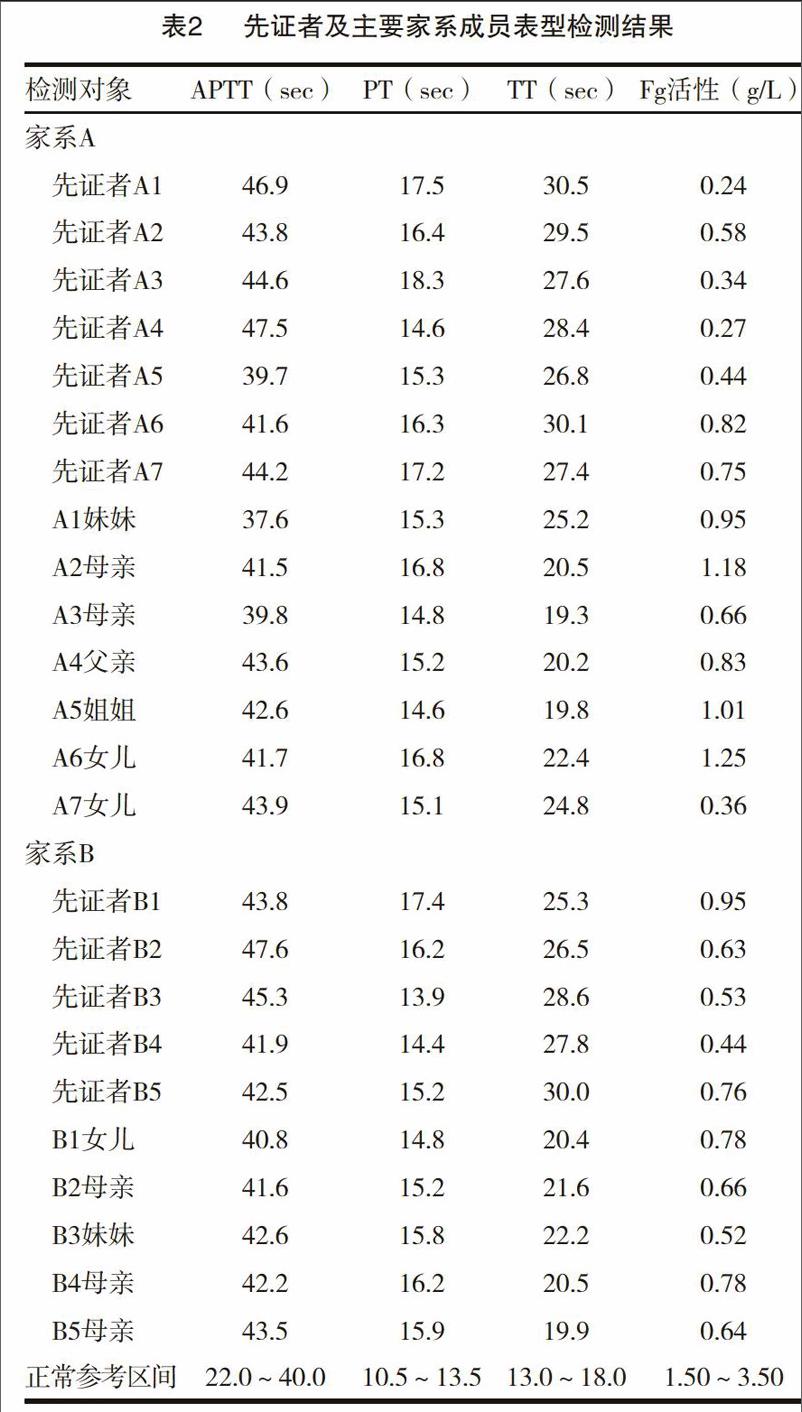
2.2先证者及主要家系成员表型检测结果
表2中为先证者及主要家系成员表型检测结果,可见所有先证者APTT、PT和TT等三项凝血指标均有明显延长,但Fg活性明显降低。经全基因组外显子测序确认发生基因突变的家系主要成员APqT、PT和TI"等三项凝血指标也存在明显延长,Fg活性明显降低的现象。其他家系成员和健康者四项指标均正常。
3.讨论
纤维蛋白原由3条同源多肽链Aα、Bβ、γ聚合而成的六聚物(AαBβ γ),这三条多肽链分别由FGA、FGB和FGG基因编码,且三个基因为同源基因,基因定位于4q28-4q31约50kb的染色体区域内,按5→3方向依次为FGG、FGA和FGB。三个基因中的任何一个发生突变均可导致纤维蛋白原出现数量及功能上异常,研究表明FGA基因突变占所有纤维蛋白原基因突变中的多数。纤维蛋白原异常对纤维蛋白肽释放、聚集、稳定性、交联,纤溶均能产生影响。遗传性异常纤维蛋白原血症是由于纤维蛋白原基因发生突变产生的一种纤维蛋白原结构和功能异常的遗传性疾病,常表现为APTT、PT和TT等凝血指标延长、Fg活性降低等。目前,基因突变检测是遗传性异常纤维蛋白原血症临床诊断的金标准,但在临床诊断时还需要分析其临床表现、凝血功能指标和家系情况。
外显子序列进展人类基因组序列的不足1%,单包含有85%以上的人类基因信息,人类多数遗传疾病均是由于相应基因外显子区域发生突变所致。全基因组外显子测序技术是近年来发展起来的用于寻找人类基因致病基因及发病机制的一种方法,李斌等利用全外显子组测序技术发现了基因c.1735 1736insT框移突变为Kallmann综合征为新的疑似致病性突变。
本研究中,先证者A1、A4以及B2均为FGA基因第2外显子g.1233G>A突变,A1的妹妹、A4的父亲以及B2的母亲均携带有相同的突变;A2、A7、B4和B5均为FGG基因第8外显子g.10819G>A突变,家系成员中A2的母亲和外婆、A7的姐姐和女儿、B4的母亲和B5的母亲均携带有相同的突变;A3、A5、A6、B1和B3及其相关亲属共10例携带有FGB基因第4外显子g.9692A>G突变。先证者及家系主要成员中发生Fg基因突变的成员APTT、PT和TT均明显延长,但Fg活性显著降低。
FGA基因g.1233G>A突变能导致Aα中的Arg35被His或者Cys替代,是纤维蛋白原异常中最常见的突变,能使影响凝血酶对纤维蛋白原肽的释放,抑制纤维蛋白聚合。FGB基因g.9692A>G突变可导致纤维蛋白原糖基之间可以通过相互排斥力使纤维蛋白网状结构更加稳定,从而调节纤维蛋白形成,糖基化影响纤维蛋白初限位的相互交联和纤维聚集,但由于这种改变没有影响到主要的聚集位点,纤维蛋白未受到关键影响,患者多无临床表现。FGG基因g.10819G>A突变常导致γ链中的Arg301发生变化。γArg301是纤维蛋白初纤维过程中D-D接触面上的重要位点之一,对于纤维蛋白网状结构形成所必需的,该位点的突变能够影响纤维蛋白正常结构和聚集功能,多数突变基因携带者无临床症状。
综上,遗传性纤维蛋白原异常可由多种Fg基因外显子突变导致,FGB和FGG外显子突变较为常见,这可能与地域有关。
