高炉渣制备系列精细化工品的技术研究
2016-09-26申星梅李辽沙武杏荣王平褚亮
申星梅,李辽沙,武杏荣,王平,褚亮
高炉渣制备系列精细化工品的技术研究
申星梅1,2,李辽沙1,武杏荣2,王平2,褚亮1
(1安徽工业大学教育部冶金减排与资源综合利用重点实验室,安徽 马鞍山 243002;2安徽工业大学冶金工程与资源综合利用安徽省重点实验室,安徽 马鞍山 243002)
以高炉渣为主要原料,在前期工作基础上,通过更进一步深入研究,开发出高炉渣制备系列精细化工品的完整工艺路线。采用硫酸酸解高炉渣的方法,获得产品石膏;制备超细硅酸铝的最佳水渣比为7:1,体系pH控制为4.0,通过加入铝片的方式进行除铁;制备镁铝尖晶石的最佳尿素质量百分比为65%,最佳除铁方法为向前体溶液中加入5%Na2S2O4。采用高炉渣制备得到的3种产品,其化学成分均符合相关标准。该工艺路线具有流程短、成本低等优点;渣中有价组分得以全部利用,无残渣排放,环境效益明显。
高炉渣;超细硅酸铝;镁铝尖晶石;石膏;除铁率
引 言
目前,我国高炉渣的利用率已接近100%,但传统技术含量不高的粗放式利用仍占较大比重,而技术含量高的利用相对较少,使渣中的多种有价组分没有得到合理利用,降低了其经济价值。事实上,高炉渣中含有大量的钙、硅、镁、铝等有价组分,可以用来制备附加值较高的产品。近年来,也不断出现了高炉渣高附加值利用的报道[1-5]。Maurizia等[3]利用高炉渣制备了硅溶胶,研究了渣粒度、浸出时间等因素对产品产率和纯度的影响;Brodnax等[6]利用高炉渣制备了硅酸钙吸收剂,研究了其吸附效果与比表面积的关系;Tsutsumi等[7]采用水热合成法,利用高炉渣制备了Al掺杂型雪硅钙石,研究了其对Cs+、Sr2+离子的吸附效果;Francis[8-9]制备了高炉渣基微晶玻璃,并研究了其结晶动力学;徐培君等[10]利用高炉渣制备了光催化剂,所得产品具有较高的光催化活性,且成本低廉;陆婷婷等[11]则利用高炉渣制备了聚硫酸铝硅絮凝剂。上述研究利用高炉渣中有价组分制备出附加值较高的产品,大大提高了其经济价值,实现了渣的高效利用。然而,渣中的有价组分并没有利用完全,仍有部分组分被排放,或尚未利用,造成资源的浪费和处理成本的增加。
基于此,本课题组针对高炉渣的全组分利用做了大量的前期工作[12],发现高炉渣中的主要组分可以用来制备超细硅酸铝和镁铝尖晶石。因此,本文在前期工作基础上,通过更进一步深入研究,开发出高炉渣制备系列精细化工品超细硅酸铝、镁铝尖晶石、石膏的技术,从而为高炉渣的全组分、高附加值利用奠定基础。
1 实验材料和方法
1.1 材料
高炉渣(取自马钢二铁厂,其化学成分如表1所示),硫酸、水玻璃、铝片、尿素、连二亚硫酸钠、高锰酸钾、硫酸锰。

表1 高炉渣的化学组成
1.2 仪器
粉磨机,SL301型,上海盛力仪器有限公司;精密增力电动搅拌器,JJ-1型,国华电器有限公司;数显恒温水浴锅,HH-S2型,金坛市文华仪器有限公司;高温循环油浴锅,GY-10L型,上海一凯仪器设备有限公司;精密pH计,PHS-2CW型,上海启威电子有限公司;数显电热干燥箱,202-4A型,上海阳光仪器有限公司;循环水真空泵,SHB-IV型,郑州长城科工贸有限公司;箱式炉,KSL-1400型,合肥科晶材料有限公司。
1.3 实验过程
(1)将取回的新鲜高炉渣干燥后,用粉磨机进行破粹至粒径为0.1~0.5 mm。称取50 g破碎后的高炉渣,将其加入水中,形成高炉渣悬浮液,水渣比分别控制为4:1、5:1、6:1、7:1和8:1(质量比)。在70℃恒温水浴和不断搅拌的条件下,向悬浮液中缓缓加入50 g浓硫酸,反应30 min后过滤。所得滤渣用稀硫酸洗涤后烘干,即得到石膏。
(2)向上述反应所得滤液中加入水玻璃溶液,调节体系pH分别至3.0、3.5、4.0、4.5、5.0、5.5、6.0和6.5。同时,加入5 g铝片。在70℃恒温水浴和不断搅拌的条件下,反应60 min后过滤。所得滤渣用水洗涤后烘干,即得到超细硅酸铝。
(3)向步骤(2)中所得滤液中加入质量百分比分别为25%、40%、50%、60%、65%和70%的尿素溶液。在100℃恒温油浴和不断搅拌的条件下,反应30 h后过滤,所得滤渣为镁铝尖晶石前体。将此前体加入水中,加入质量百分比分别为1%、3%、5%、8%和10%的Na2S2O4进行除铁。反应30 min后过滤,所得滤渣干燥后,置于1100℃马弗炉中煅烧2 h,即得到镁铝尖晶石。
2 实验结果与讨论
2.1 技术路线分析
高炉渣中含有大量的钙、硅、镁、铝组分,如表1所示。高炉渣的玻璃体含量较高,结构处在高能量状态,具有较高的活性。因此,采用硫酸酸解后,硅、镁和铝组分以、、的形式分别进入液相,而钙组分以CaSO4的形式进入固相,即石膏。含有硅、镁和铝组分的滤液1,在一定条件下陈化聚合后,硅和一部分铝组分进入固相,即超细硅酸铝,而镁和剩余铝组分进入液相。向含有镁、铝组分的滤液2中加入尿素溶液,一定条件下反应后,经过过滤、除杂,得到镁铝尖晶石前体。最后将此前体进行煅烧,即得到镁铝尖晶石。高炉渣制备系列精细化工品的技术路线如图1所示。
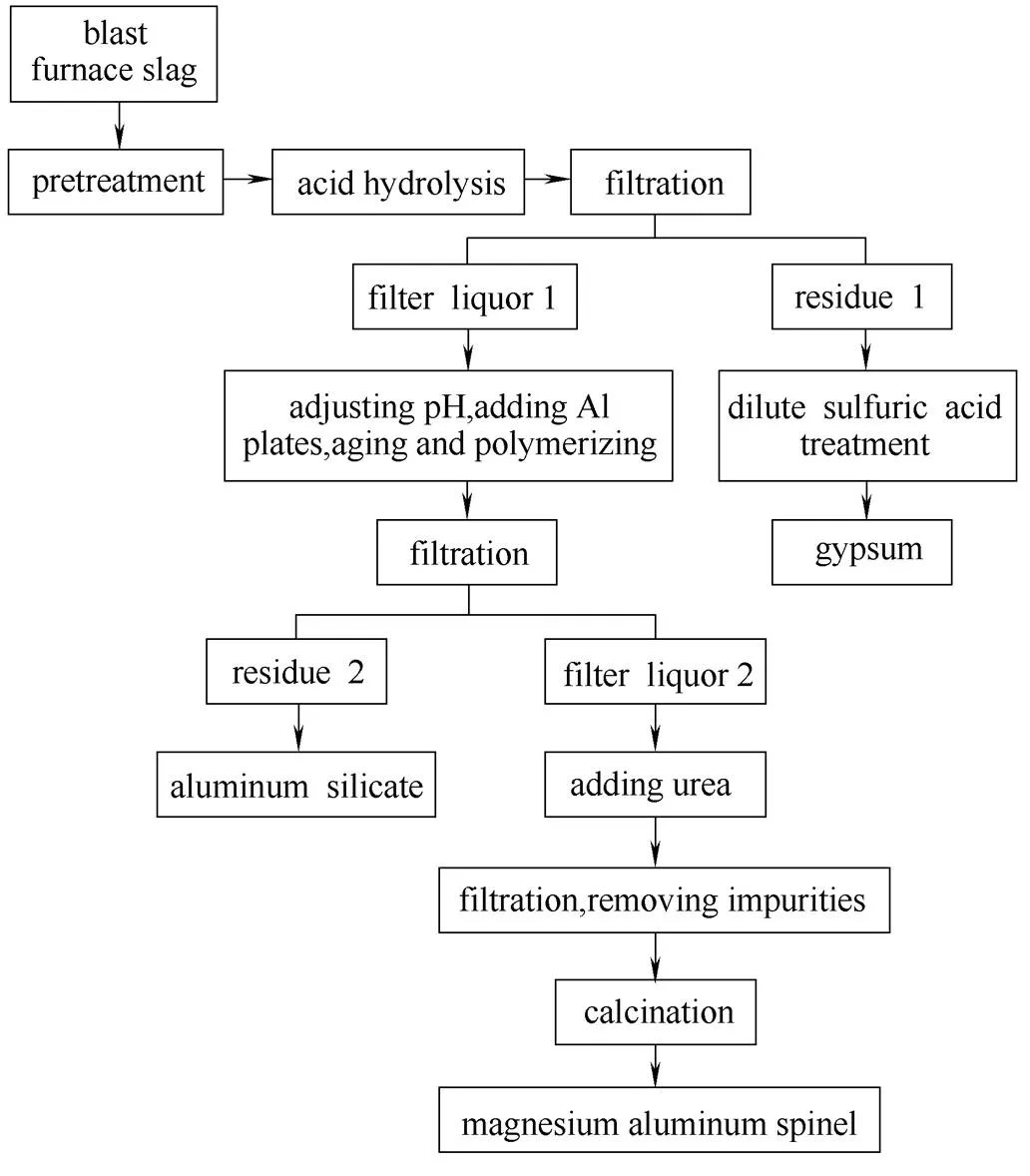
图1 高炉渣制备系列精细化工品的技术路线
2.2 超细硅酸铝合成过程
高炉渣硫酸酸解制备超细硅酸铝的过程中,高炉渣玻璃态结构中的硅酸根转化为单分子硅酸进入溶液,而Ca组分以CaSO4形式沉淀下来,为超细硅酸铝的合成提供了条件。高炉渣酸解反应属于固液两相反应,受固液相界面两侧传质速率控制。从化学活性及反应动力学来看,Ca2+向液相传质以及H+向固相传质的速率较快,而生成的硅溶胶向液相传质的速率较慢[13];另一方面,高炉渣中Ca组分含量较高,Ca2+迁移量大,其与硫酸反应快速生成CaSO4沉淀,再加上硅溶胶的生成,使体系的黏度上升,这就对H+向固相的传质及硅溶胶向液相的传质造成了阻碍,使硅酸形成的反应动力有所降低,同时使硅溶胶在高炉渣颗粒外层越积越厚,Ca2+的迁移速度也最终受到限制。因此,需选择合适的水渣比,以保证渣中的Ca组分快速进入沉淀相析出,Si、Al组分顺利进入液相。
图2是超细硅酸铝产率随水渣比的变化曲线。从图中可以看出,超细硅酸铝的产率随水渣比的升高呈先增大后减小的趋势。当水渣比4时,体系中硫酸的浓度较高,酸解反应较为剧烈,体系迅速黏稠;未反应的高炉渣被黏稠物覆盖,使Ca2+和H+向高炉渣表面扩散的速度大大降低,阻碍了高炉渣的酸解反应,使得产品产率较低(70.5%)。随着水渣比的逐渐升高,产品产率逐渐增大;当水渣比7时,产率达到最高(81.3%)。然而,当水渣比>7后,产品产率开始下降;这是因为,此时体系中H+浓度较低,到达高炉渣颗粒表面的H+数量大为减少,酸解反应进程缓慢,单位时间内形成的硅溶胶和铝的硫酸盐变少,产品产率降低。因此,最佳水渣比确定为7:1。
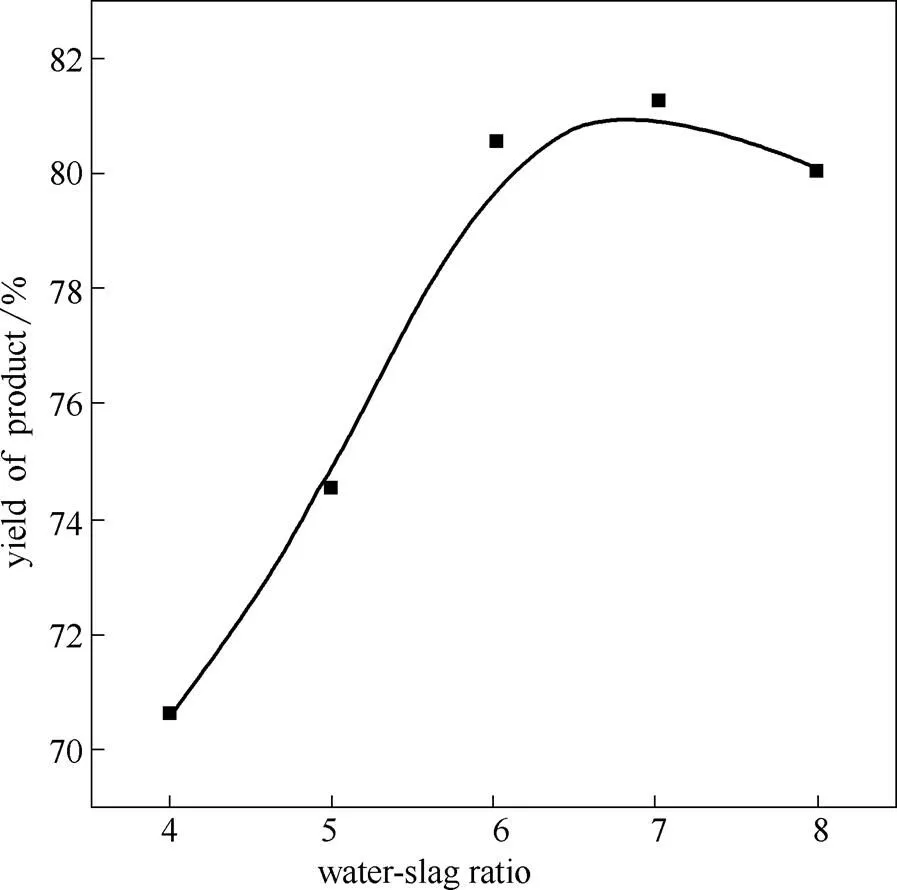
图2 超细硅酸铝产率随水渣比的变化曲线
图3是超细硅酸铝成分随pH的变化曲线。超细硅酸铝颗粒的生成可分为3个阶段,其主要化学反应如下
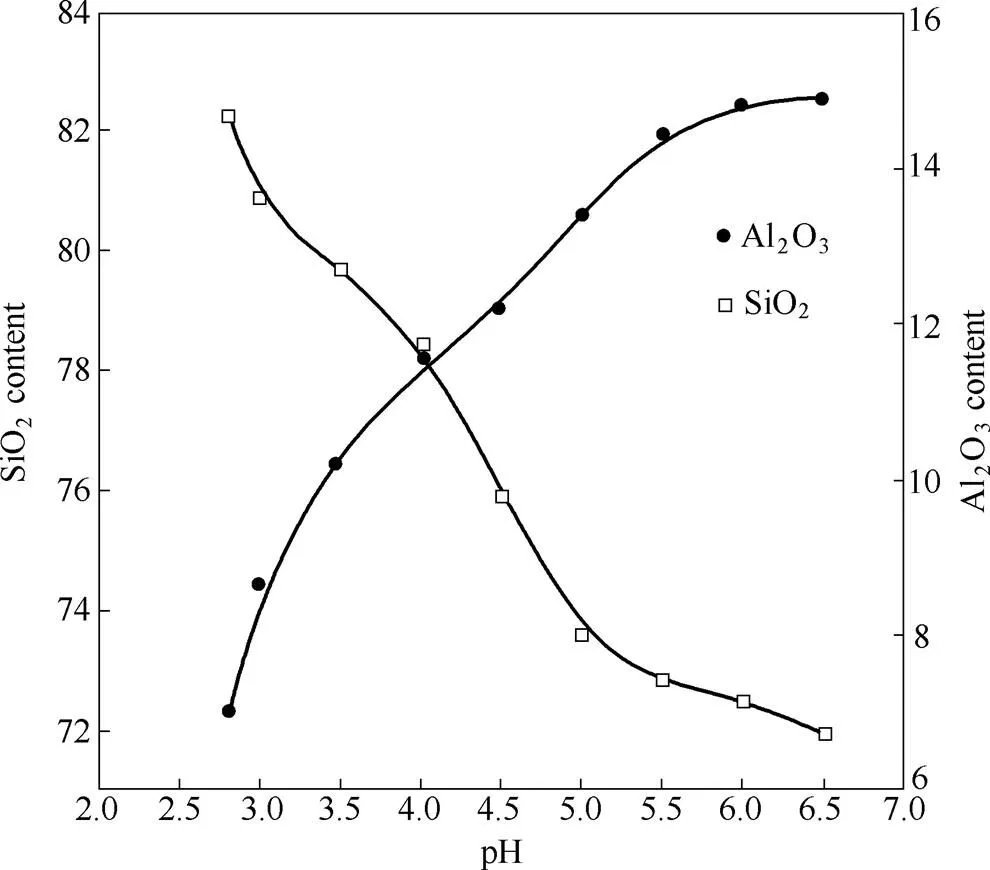
图3 超细硅酸铝成分随pH的变化曲线
高炉渣的Fe是必然会带入的杂质元素,也是最难去除的元素,它的存在对产品的白度和纯度都有影响。现行企业标准要求Fe2O3含量≤0.05%。图4是超细硅酸铝中Fe2O3含量随pH的变化曲线。可以看出,Fe2O3含量随pH升高而增大,且pH4.0时,Fe2O3含量较高(>0.10%)。Fe3+的初始沉淀pH为2.7,小于Al3+的初始沉淀值3.3,Al3+开始沉淀前,Fe3+已经开始沉淀。也就是说,Fe3+是产品中必然存在的杂质。因此,本实验采用加入铝片的方式,使Fe3+还原为Fe2+,Fe2+的初始沉淀pH为7.6,在本实验pH范围内(pH4.0)不沉淀,从而达到去除Fe3+的目的。其化学反应式为
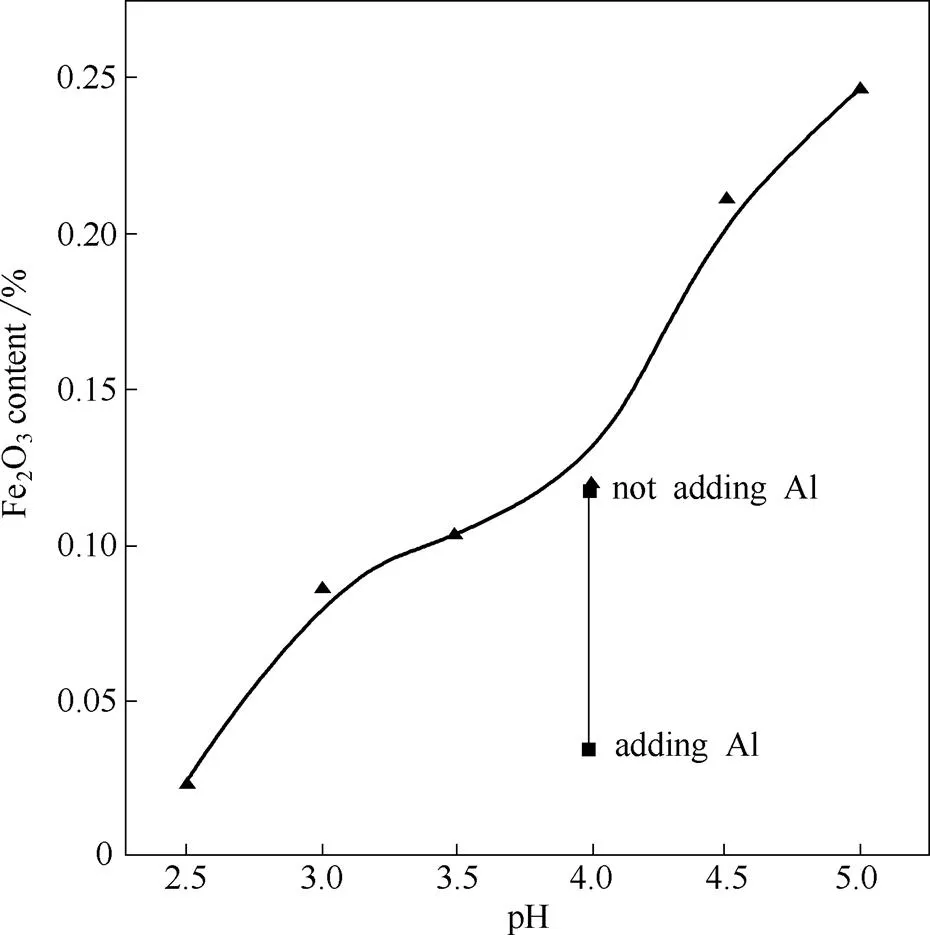
图4 超细硅酸铝中Fe2O3含量随pH的变化曲线
2.3 镁铝尖晶石制备过程
超细硅酸铝制备完成后,利用此过程分离出的滤液2制备镁铝尖晶石。首先分析滤液2的化学组成,将其水分蒸干后取残渣,用X射线荧光光谱仪进行测试,结果如表2所示。从表2中可知,滤液2中含有大量的Mg2+、Al3+,约占金属离子总含量的86%,是合成镁铝尖晶石的主要成分。
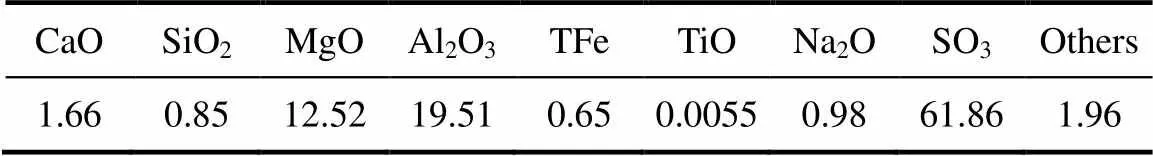
表2 滤液2蒸干后残渣的化学组成
向滤液2中加入尿素溶液,采用均匀沉淀法制备镁铝尖晶石前体,前体产率随尿素质量百分比的变化曲线如图5所示。从图中可以看出,前体产率随尿素质量百分比的增大而增大。尿素在本实验温度(100℃)下水解后,缓慢释放出,与滤液2中的Mg2+、Al3+反应,生成镁铝尖晶石前体。当尿素质量百分比较低(25%)时,其水解释放出的量较少,沉淀下来的Mg2+、Al3+就较少,则前体产率较低;随着尿素质量百分比的增大,其水解出的量增多,沉淀下的Mg2+、Al3+也越多,前体产率升高;当尿素质量百分比达到65%时,前体产率达到94%;再增加尿素质量百分比,前体产率增加不明显。因此,最佳尿素质量百分比为65%。

图5 镁铝尖晶石前体产率随尿素质量百分比的变化曲线
在超细硅酸铝制备过程中,体系中的杂质Fe3+还原为Fe2+,留在了滤液2中,进入镁铝尖晶石的制备过程。Fe2+在镁铝尖晶石制备过程中,会以Fe(OH)2形式随前体一起沉淀下来;而Fe(OH)2在空气中极不稳定,很容易氧化为Fe(OH)3,从而影响产品质量。因此,本实验采用了两种方法进行除铁。方法一是向制备好的前体中加入连二亚硫酸钠(Na2S2O4);方法二是向滤液2中加入高锰酸钾(KMnO4)。图6为镁铝尖晶石除铁率随Na2S2O4用量的变化曲线。从图中可以看出,产品除铁率随Na2S2O4用量的增加而逐渐增大。Na2S2O4具有较强的还原性,可将前体溶液中的Fe3+还原为Fe2+,其化学反应式如下
Fe2+在本过程pH范围(7.3左右)内不沉淀,仍以离子状态存在于液相中,经固液分离后得以去除。Na2S2O4用量越大,还原的Fe3+量越多,除铁率就越大,且Na2S2O4在碱性溶液中的除铁效果优于其在酸性溶液中的效果[17],而本实验的前体溶液呈弱碱性,有利于铁元素的去除。当Na2S2O4用量为5%时,除铁率达71%。当Na2S2O4用量大于5%以后,除铁率的增加不明显。因此,最佳Na2S2O4用量为5%。

图6 镁铝尖晶石除铁率随连二亚硫酸钠用量的变化曲线
图7为镁铝尖晶石除铁率随KMnO4用量的变化曲线。从图中可以看出,除铁率随KMnO4用量的增加而增大。KMnO4是强氧化剂,在酸性溶液中的氧化性最强。因此,选择向酸性的滤液2中加入KMnO4,将其中的Fe2+氧化为Fe3+,Fe3+生成Fe(OH)3沉淀,与滤液2分离;同时,Fe(OH)3还能与体系中生成的活性MnO2反应,生成棕色共沉淀Fe(OH)3·MnO2·H2O[18-20]。主要化学反应式如下
当KMnO4用量为0.2 g时,产品除铁率达95%。继续增加KMnO4用量,除铁率已无变化。因此,最佳KMnO4用量为0.2 g。
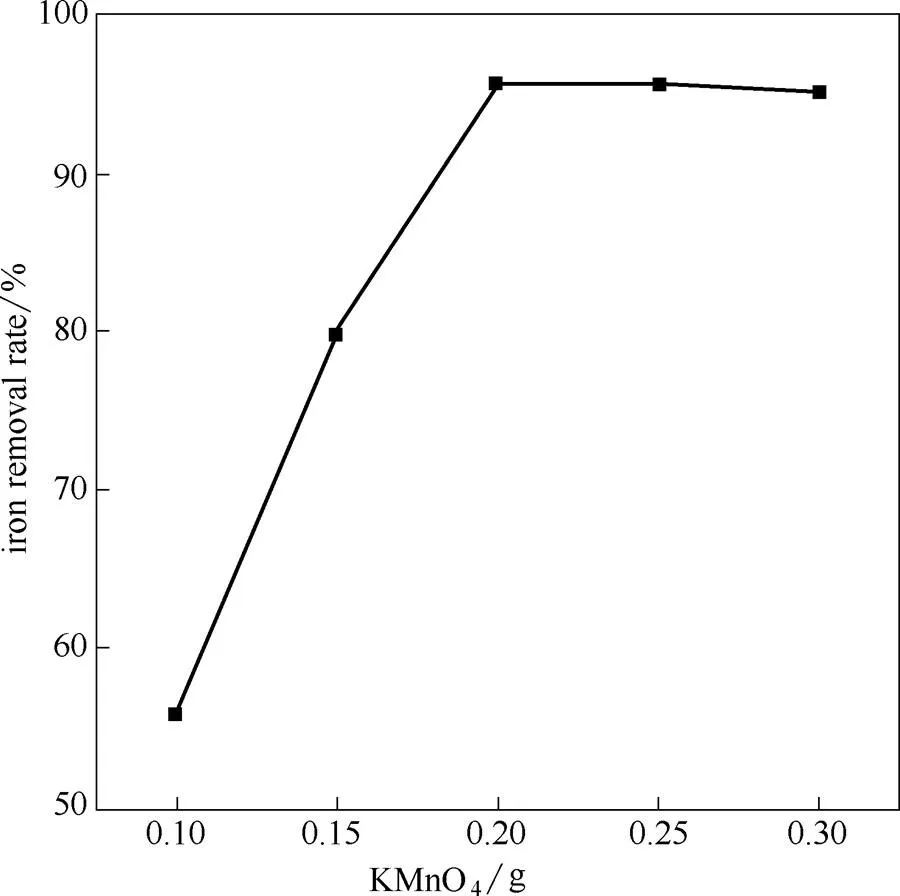
图7 镁铝尖晶石除铁率随高锰酸钾用量的变化曲线
从除铁效果上来看,KMnO4的除铁率可达95%,高于Na2S2O4的除铁率71%。然而,KMnO4的加入向体系中引入了锰离子,在后续均匀沉淀制备镁铝尖晶石前体的过程中,锰离子也会参与反应,随前体一起沉淀下来,从而影响产品的颜色与纯度。因此,本文选择最佳的除铁方法为向前体溶液中加入5%Na2S2O4。
2.4 产品的表征
按照本工艺流程的先后顺序,分别得到3种精细化工产品:石膏、超细硅酸铝和镁铝尖晶石。其中,石膏经热失重分析后可知,其硫酸钙含量为70%,化学式计算得出:CaSO4·2H2O;超细硅酸铝和镁铝尖晶石的化学成分如表3和表4所示。可以看出,超细硅酸铝的化学成分符合中国企业通用标准,镁铝尖晶石的化学成分符合GB/T 26564—2011的相关要求。
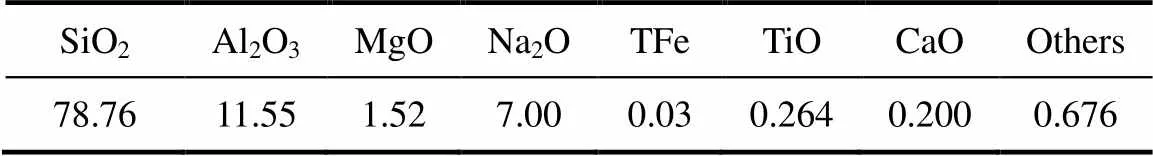
表3 超细硅酸铝的化学组成
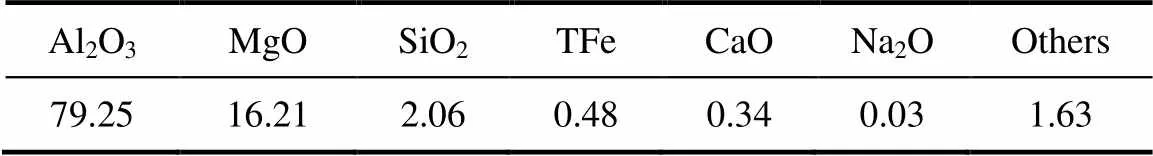
表4 镁铝尖晶石的化学组成
3 结 论
(1)采用硫酸酸解高炉渣的方法,获得产品石膏;制备超细硅酸铝的最佳水渣比为7:1,体系pH控制为4.0,通过加入铝片的方式进行除铁;制备镁铝尖晶石的最佳尿素质量百分比为65%,最佳除铁方法为向前体溶液中加入5%Na2S2O4。
(2)采用本工艺制备得到的3种产品,其化学成分均符合相关标准。该工艺路线具有流程短、成本低、消耗大量固体废弃物等优点;渣中有价组分得以全部利用,无残渣排放,环境效益明显;整个工艺路线可得到3种精细化工产品,工业化前景更广阔。
References
[1] DAS B, PRAKASH S, REDDY P S R,. An overview of utilization of slag and sludge from steel industries [J]. Resour. Conserv. Recy., 2007, 50: 40-57.
[2] FREDERICCI C, ZANOTTO E D, ZIEMATH E C. Crystallization mechanism and properties of a blast furnace slag glass [J].J. Non-Cryst. Solids, 2000, 273: 64-75.
[3] MAURIZIA S, SANDRA V. Recovery of silica gel from blast furnace slag [J]. Resour. Conserv. Recy., 2003, 40: 71-80.
[4] LIU H, LU H, CHEN D,. Preparation and properties of glass-ceramics derived from blast furnace slag by a ceramic-sintering process [J]. Ceram. Int., 2009, 35: 3181-3184.
[5] 苏洁, 陈莉荣, 刘文. 高炉渣制备聚硅酸硫酸铝铁混凝剂 [J]. 化工环保, 2015, 35 (1): 99-102.
SU J, CHEN L R, LIU W. Preparation of polysilic aluminum ferric sulfate coagulant from blast furnace slag [J]. Environmental Protection of Chemical Industry, 2015, 35 (1): 99-102.
[6] BRODNAX L F, ROCHELLE G T. Preparation of calcium silicate absorbent from iron blast furnace slag [J]. J. Air Waste Manage. Assoc., 2000, 50: 1655-1662.
[7] TSUTSUMI T, NISHIMOTO S, KAMESHIMA Y,. Hydrothermal preparation of tobermorite from blast furnace slag for Cs+and Sr2+sorption [J]. J. Hazard. Mater., 2014, 266: 174-181.
[8] FRANCIS A A. Conversion of blast furnace slag into new glass-ceramic material [J]. J. Eur. Ceram. Soc., 2004, 24: 2819-2824.
[9] FRANCIS A A. Non-isothermal crystallization kinetics of a blast furnace slag glass [J]. J. Am. Ceram. Soc., 2005, 88: 1859-1863.
[10] 徐培君, 刘红, 周志辉, 等. 高炉渣制备光催化剂及其催化活性的研究 [J]. 工业安全与环保, 2012, 38 (1): 84-87.
XU P J, LIU H, ZHOU Z H,. Preparation and photocatalytic activities of photocatalysts from high-iron slag [J]. Industrial Safety and Environmental Protection, 2012, 38 (1): 84-87.
[11] 陆婷婷, 李辽沙. 高炉渣制备聚硫酸铝硅絮凝剂 [J]. 安徽工业大学学报, 2010, 27 (3): 225-228.
LU T T, LI L S. Preparation of pass coagulant with high slag [J]. Journal of Anhui University of Technology, 2010, 27 (3): 225-228.
[12] 褚亮, 申星梅, 王莲贞, 等. 由高炉渣酸解废液制备镁铝尖晶石粉体 [J]. 过程工程学报, 2014, 14 (1): 157-161.
CHU L, SHEN X M, WANG L Z,. Preparation of magnesium aluminum spinel powder with waste solution from acid leaching of blast furnace slag [J]. The Chinese Journal of Process Engineering, 2014, 14 (1): 157-161.
[13] 李珍, 陈克勤. 大箕铺硅灰石酸法制备白炭黑工艺研究 [J]. 矿产保护与利用, 1999, 1 (1): 18-20.
LI Z, CHEN K Q. Experimental research on the preparation of white carbon black by acid treatment of wollastonite [J]. Conservation and Utilization of Mineral Resources, 1999, 1 (1): 18-20.
[14] 戴安邦, 江龙. 硅酸及其盐的研究(Ⅰ): 硅酸聚合的速度和机制 [J]. 化学学报, 1957, 23 (2): 90-98.
DI A B, JIANG L. Studies on silicic acid and its salts (Ⅰ): Rate of gelation and mechanism of polymerization of silicic acid [J]. Acta Chimica Sinica, 1957, 23 (2): 90-98.
[15] 戴安邦, 陈荣三, 朱屯. 硅酸及其盐的研究(Ⅶ): 一个较完全的N曲线 [J]. 南京大学学报, 1963, 7 (1): 20-29.
DI A B, CHEN R S, ZHU T. Studies on silicic acid and its salts (Ⅶ): A more complete N-curve [J]. Journal of Nanjing University, 1963, 7 (1): 20-29.
[16] 戴志诚, 刘洪章, 李添松, 等. 硅化合物的生产与应用[M]. 成都: 成都科技大学出版社, 1994: 146.
DAI Z C, LIU H Z, LI T S,. Production and Application of Silicon Compounds[M]. Chengdu: Chengdu University of Science and Technology Press, 1994: 146.
[17] 侯太鹏, 刘英魁. 除膨润土三价铁及增白研究 [J]. 非金属矿, 1999, 22 (5): 12-14.
HOU T P, LIU Y K. Research on removal of ferric iron from bentonite and its whitening [J]. Non-Metallic Mines, 1999, 22 (5): 12-14.
[18] 邹兴, 李艳, 邓彩勇. 硫酸锰溶液除亚铁的研究 [J]. 中国锰业, 2004, 22 (2): 22-24.
ZOU X, LI Y, DENG C Y. Removal of Fe2+from manganese sulphate with pyrolusite oxidizing agent [J]. China’s Manganese Industry, 2004, 22 (2): 22-24.
[19] 王娟珍, 薛长安, 王志勇, 等. 高锰酸钾应用于地下水除铁锰试验研究与探讨 [J]. 城镇供水, 2013, 3 (3): 78-80.
WANG J Z, XUE C A, WANG Z Y,. Experiment and research on removal of iron and manganese from groundwater by potassium permanganate [J]. City and Town Water Supply, 2013, 3 (3): 78-80.
[20] 陈国锋. 浙东水库水除铁除锰试验研究 [D]. 上海:同济大学, 2008.
CHEN G F. Pilot study on removal of iron and manganese from reservoir of east of Zhejiang province [D]. Shanghai: Tongji University, 2008.
Preparation of a series of fine chemicals by blast furnace slag
SHEN Xingmei1,2, LI Liaosha1, WU Xingrong2, WANG Ping2, CHU Liang1
(1Key Laboratory of Metallurgical Emission Reduction & Resources Recycling of Ministry of Education, Anhui University of Technology, Ma’anshan 243002, Anhui, China;2Anhui Province Key Laboratory of Metallurgy Engineering & Resources Recycling, Anhui University of Technology, Ma’anshan 243002, Anhui, China)
On the basis of previous works, preparation of a series of fine chemicals by blast furnace slag was researched further and deeply, and the process route was developed. The first product, gypsum, was obtained by sulphuric acid hydrolysis. The optimum conditions for preparing aluminum silicate were: water-slag ratio 7:1, pH 4.0 and adding small pieces of Al plates to remove iron. The optimum conditions for preparing magnesium aluminum spinel were: mass percent of urea 65% and amount of Na2S2O45%. The chemical composition of the three products was in accord with the relative standards. This process had the advantages of short flow, low cost,. Almost all valuable contents in the slag were used, and no residue was discharged. Thus, it had better environmental benefit.
blast furnace slag; aluminum silicate; magnesium aluminum spinel; gypsum; iron removal rate
supported by National Natural Science Foundation of China (51302003, 51274006), Anhui Science & Technology Department Foundation of China (1506c085003), Anhui Innovation Team Project of New Technology in Materialization of Metallurgical Solid Wastes and Ma’anshan Science & Technology Foundation of 2014.
date: 2016-02-29.
SHEN Xingmei, xxxxmx@126.com
TQ 170.9
A
0438—1157(2016)09—3988—07
10.11949/j.issn.0438-1157.20160220
国家自然科学基金项目(51302003, 51274006);安徽省科技厅项目(1506c085003);安徽省冶金固废材料化利用新技术创新团队项目;2014年马鞍山市科技计划。
2016-02-29收到初稿,2016-04-13收到修改稿。
联系人及第一作者:申星梅(1982—),女,博士,副教授。
