分散固相微萃取法测定水样中甲基紫的含量
2016-09-19段翔洋申江萍袁丽娜刘亚兰王柯新山西师范大学化学与材料科学学院山西临汾041000
段翔洋, 申江萍, 祁 嫒, 袁丽娜, 刘亚兰, 王柯新(山西师范大学 化学与材料科学学院,山西 临汾 041000)
分散固相微萃取法测定水样中甲基紫的含量
段翔洋,申江萍,祁嫒,袁丽娜,刘亚兰,王柯新
(山西师范大学 化学与材料科学学院,山西 临汾 041000)
建立了一种磁分散固相微萃取分光光度法检测水样中甲基紫含量的分析方法,主要考察了样品的pH值、吸附剂的用量、萃取与解析时间、解析剂的种类、解析剂用量以及离子强度对甲基紫萃取性能的影响。最优化条件下,线性关系在0.01~0.2 μg/mL的范围内良好,线性相关系数也较高(R2>0.99)。经检测,日内重复性5.3%,日间重复性4.9%。检出限为0.024 μg/mL,定量限为0.079 μg/mL。还研究了在湖水和鱼塘水中不同加标量的回收率,其中湖水的加标回收率在94.3%~101.0%,鱼塘水的加标回收率在85.4%~90.0%。
磁分散固相微萃取;甲基紫;分光光度法
甲基紫是三苯甲烷类化合物,在染料、制药和分析试剂等方面有广泛应用。此类染料组成复杂,性质稳定,色度高,水质波动大,可生化能力差,对人类及各种生物具有致畸、致癌和致突变的作用,对环境也造成了严重影响[2]。但由于它对鱼类的寄生虫病、水霉病等有良好的治疗效果,且价格较低,很多养殖户仍违规使用,因此,对甲基紫的残留监控问题很重要。
甲基紫的测定多采取气相色谱-质谱法[3]、高效液相色谱法[4]和液相色谱-质谱法[5]。但由于甲基紫禁止使用,因此在测定时,灵敏度越高越好。随着科技的发展,分析仪器虽有了很大进步,但为了提高灵敏度,在测定之前仍有必要进行分离与富集[6]。目前常用的分离富集方法有浊点萃取法[7]、固相萃取法[8]、旋转盘吸附萃取法[9]和溶剂萃取法[10]等。磁分散固相萃取作为一种新型的分析方法,具有材料易得,便于制备,操作简单,磁性强,成本低,又利于回收再利用等优点,是一种无毒无害的环境友好型方法。
本文提出一种磁分散固相微萃取分光光度法,以磁吸附剂为固相萃取剂,对废水中甲基紫的含量[11]进行测定研究。将磁吸附剂直接混合分散到溶液中,以便其充分接触,使吸附萃取效率提高,同时又可以用永磁铁将吸附材料从溶液中收回。该方法将样品的吸附和解析过程结合起来,通过对样品中分析成分和磁吸附剂吸附平衡的控制,使待测组分分离[12]。
1 实验
1.1试剂与仪器
乙醇(天津市光复科技发展有限公司)、丙酮(洛阳市化学试剂厂)、甲醇、甲基紫(天津市科密欧化学有限公司),分析纯;氯化钠(洛阳市化学试剂厂)、三酸缓冲溶液(Britton-Robinson buffer,0.04 mol /L)来调节溶液pH,蒸馏水,实际样品鱼塘水(取自山西师范大学校园),湖水(山西省临汾市汾河公园),用0.45 μm的滤膜过滤后,置于4℃条件下避光保存。
紫外分光光度计(varian australia澳大利亚),超声波清洗器(KH-500B型超声波清洗器),0.5 mL的石英比色皿。
1.2实验方法
1.2.1标准溶液的制备
精准称量0.100 0 g甲基紫样品,蒸馏水溶解后定容到100 mL容量瓶,配得1 000 μg/mL的甲基紫溶液。从中移取1 mL稀释成10 μg/mL的标准溶液。将配制好的溶液在4℃条件下避光存放。
1.2.2磁性材料的制备
将粘土(0.3 g)纯化后加入到24 mL的乙二醇中,之后将0.6 g的FeCl3·6H2O和1.2 g 的NaAc在环境温度下溶解到乙二醇溶液中。搅拌30 min,移动至50 mL聚四氟乙烯内衬的不锈钢高压釜内,温度设置为200℃,反应8 h,并自然冷却至室温。黑色沉淀于外部磁场作用下分离,将上清液倾析。用乙醇将得到的固体清洗并在60 ℃下真空干燥[13]。
1.2.3萃取过程
精确移取0.8 mL 10 μg/mL标准溶液,加蒸馏水定容到10 mL,称1.5 g的NaCl于比色管内,待其溶解后添加4 mg的磁性材料,超声分散后,静待10 min,用永磁铁把磁性材料吸到比色管底部,倒掉上清液。之后加入0.3 mL的甲醇进行解析,静置9 min,用磁铁将解析液和磁吸附材料分离,测量波长为582 nm时解析液的吸光度。
2 结果与讨论
2.1萃取条件的优化
为了得到磁吸附剂对甲基紫的最佳萃取条件,考察了样品基底的pH值、吸附剂的用量、萃取与解析时间、解析剂的种类、解析剂用量、以及离子强度对甲基紫萃取性能的影响。
2.1.1样品pH值的选取
溶液pH决定着吸附剂表面电荷及被分析物的存在形式,萃取效果将因此产生影响。甲基紫在不同的pH值时结构不同,pH<4时,阳离子是主要存在形式,pH>8时,稳定的中性分子是主要存在形式[14]。改变溶液pH为2到12(如图1所示),当3.00<pH<7.00 时,磁性材料的吸附能力随pH的升高而增大,且在 pH=6时达到最高。随着pH值的继续增大,吸附能力逐渐减弱。由此可得,甲基紫在弱酸性和中性条件更易被吸附,且环境水样本身也呈弱酸性,因此无需添加缓冲溶液。
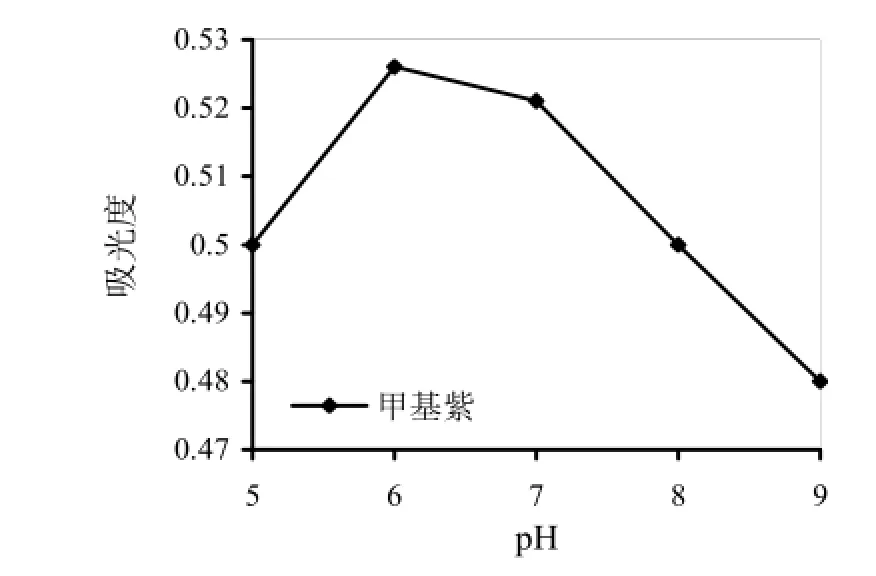
图1 pH值的影响
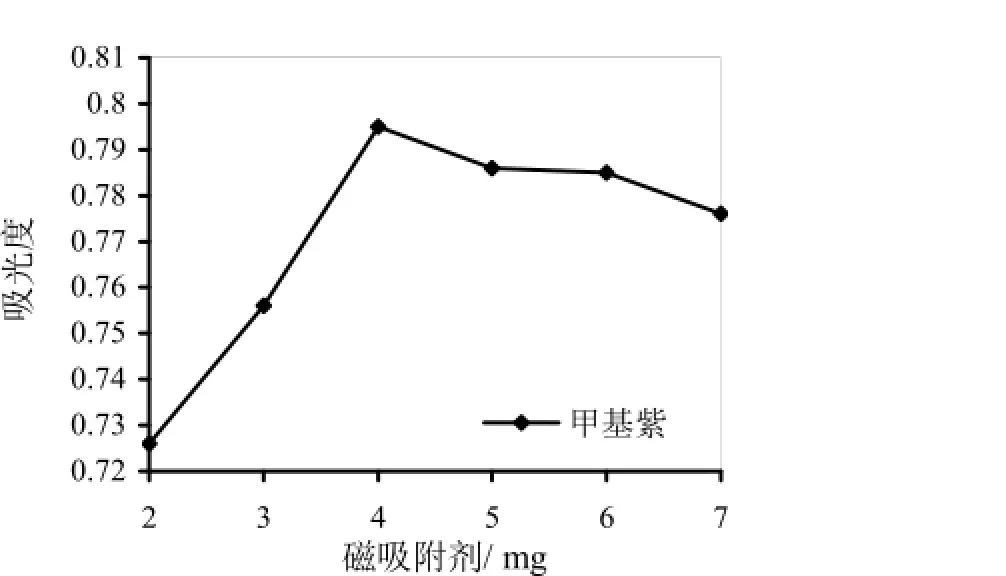
图2 吸附剂用量的影响
2.1.2磁性材料用量的影响
考察了磁性材料用量在2~7 mg时对甲基紫的萃取效率。从图2可以看出,萃取效果先增加后降低。开始时吸光度随着磁性材料用量的增加而增加,4 mg时达到最大,再增加用量,却有下降趋势。这是由于解析剂用量少而磁性材料太多,使得磁性材料无法与解析剂充分接触,导致一部分被吸附的甲基紫无法解析下来。因此,后续实验中磁性材料的用量为4 mg。
2.1.3萃取和解析时间的影响
在其他条件相同时,研究了萃取时间在2~16 min时的萃取效果(如图3所示),结果表明,延长时间,萃取性能逐渐提高,10 min时,萃取量达平衡,因此,选择10 min为最佳萃取时间。本实验萃取时间较短,可能是由于粘土增加了材料的亲水性,使磁性材料在水溶液中快速分散,缩短了萃取时间。本实验同时也就解析时间对吸附能力的影响进行了分析,考察了解析时间在3~18 min时的解析效果(如图4所示),经实验得出,9 min时解析效果最佳,9 min后的解析效果基本不变。说明9 min时已全部被解析,故解析以9 min为宜。
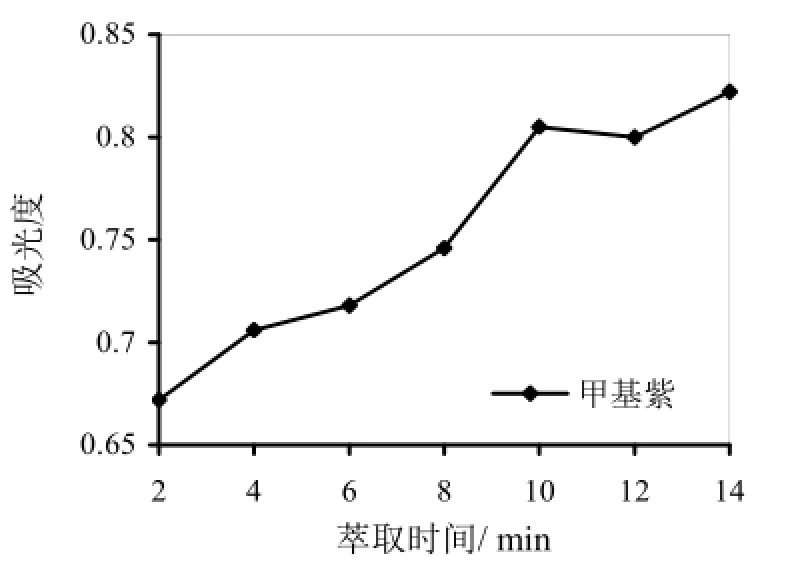
图3 萃取时间的影响
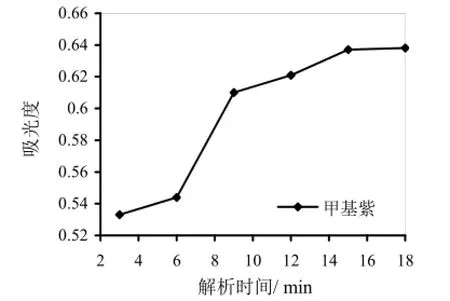
图4 解析时间的影响
2.1.4解析剂种类和用量的选择
甲基紫在有机溶剂中有较大的溶解度,且有机溶剂可以使分析物和磁吸附剂间的相互作用被破坏,所以,用有机溶剂来进行解析。本实验分别研究了以甲醇、丙酮、乙醇为解析剂时对甲基紫的解析性能,结果如图5所示,可见,在条件相同时,三者均可将甲基紫解析出来,但甲醇效果更好,萃取率更高,因此,以甲醇作为解析剂。本实验还考察了解析剂用量为0.3、0.6、0.9、1.2、1.5、1.8 mL时的解析效果。将解析后得到的上清液均稀释定容到1.8 mL,混合均匀后测量吸光度。可得,随着解析剂用量的增多,吸光度基本保持不变。因此,出于经济和环保方面的考虑,将解析剂用量定为0.3 mL。
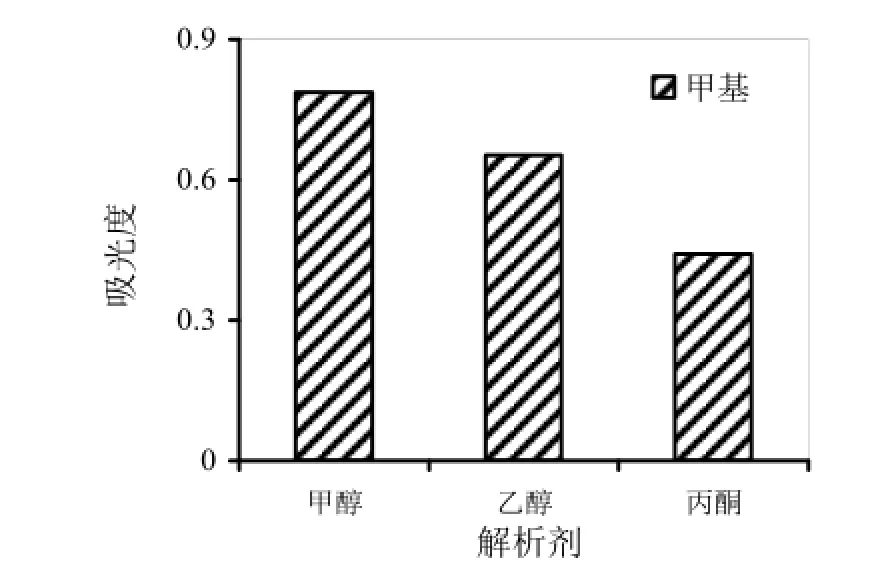
图5 解析剂的种类图
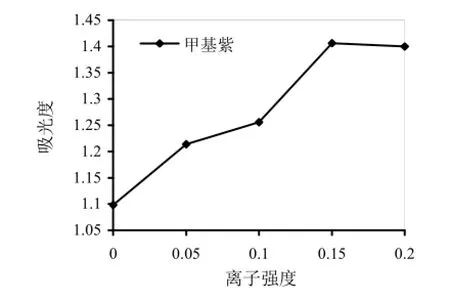
图6 离子强度的影响
2.1.5离子强度的影响
无机盐(如NaCl)加入到基底溶液中,不仅会使溶液离子强度增大,而且还会降低有机物的溶解度[15]。通过加入质量浓度为0、5%、10%、15%、20%的NaCl来改变基底溶液的离子强度,研究离子强度对萃取效率的影响(如图6所示)。随着盐溶液质量浓度的逐渐增加,萃取量增加,当质量浓度为15%时,效果最好。继续添加,吸光度却又下降,可能是形成的离子化物对溶解性能有影响。因此,选择质量分数为15%的盐溶液中萃取,性能最佳。
综上所述,磁性材料对甲基紫最优化的萃取条件是:pH值弱酸或中性,调节样品的离子强度为15%,磁吸附剂用量为4 mg,吸附与解析时间分别是10 min和9 min,以0.3 mL的甲醇进行解析。
2.2实验的线性范围
配置一系列浓度为0.005~0.200 μg/mL的甲基紫标准溶液,在最优化情况下做实验,测解吸液在 582 nm 处的吸光度,做工作曲线,得到y=5.379 7 c+0.024 5,线性关系于0.01~0.20 μg/mL浓度范围里良好,线性相关系数R2=0.997 5。分别以3倍和10倍的信噪比计算检出限(LOD)为0.024 μg/mL、定量限(LOQ)为0.079 μg/mL,同时,为了研究方法的重现性,对l 天内独立配制的样品及对连续4天独立配制的样品进行平行测定,计算得出日内相对标准偏差(RSD)是5.3%,日间相对标准偏差(RSD)是4.9%。因此,此次检测有好的重现性及灵敏度。
2.3样品及加标回收率的检测
还对湖水和鱼塘水进行了检测,在被测的湖水和鱼塘水中均没有检测到甲基紫,为了考察该方法在实际样品中的可行性,继续研究了在湖水及鱼塘水中不同加标量的回收率。其中,湖水在加标质量浓度是0.06、0.1、0.14 μg/mL时的加标回收率依次是98.0%、101.0%及94.3%,鱼塘水在相同浓度时的加标回收率依次是89.6%、85.4%和87.9%。说明该实验准确且具有可操作性。
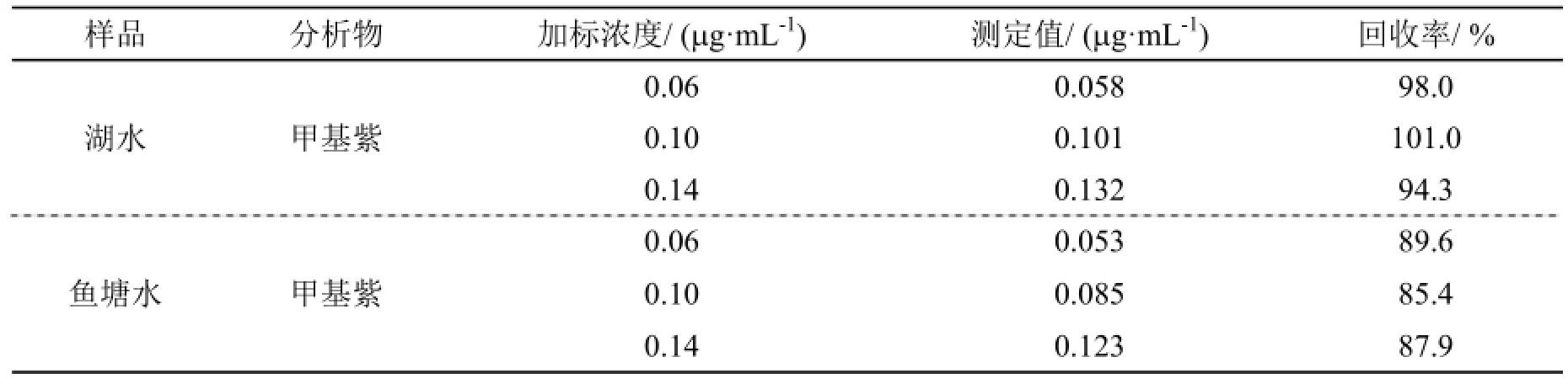
表1 环境水样中样品的检测
3 结语
本文建立了磁性材料富集吸附水中痕量甲基紫的磁分散固相微萃取分光光度法这一新型分析方法。结果显示,磁吸附剂对甲基紫有高的吸附萃取能力。在此基础上,还对实际水样进行了分析,回收率是85.4%~101.0%。本实验方法灵敏度高,且易于操作,成本低,无毒无污染,有很好的发展前景。
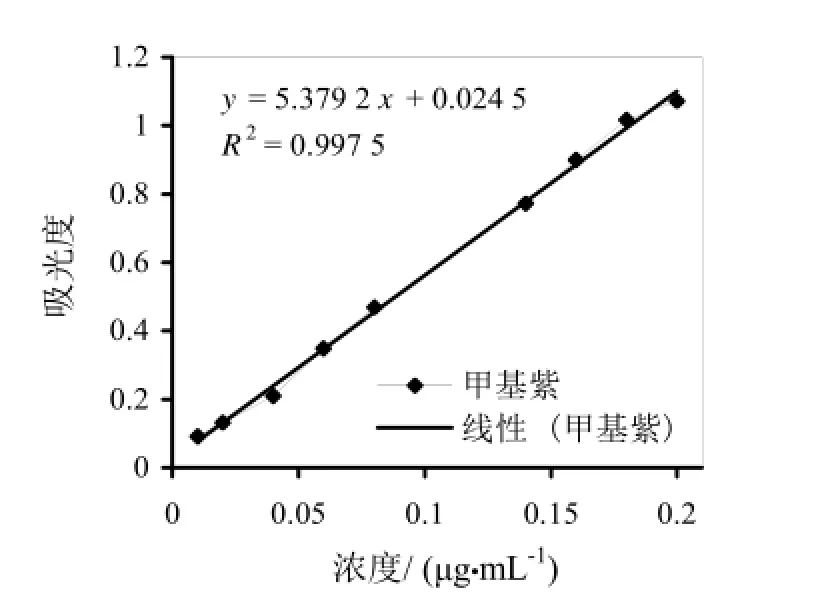
图7 工作曲线
[1] 高令飞, 蒋尊芳, 周继承, 等. 微波催化剂MgFe2O4-Fe2O3微波催化氧化降解结晶紫废水[J]. 湖南大学学报, 2015, 42(12): 74-79.
[2] 陈文华, 李刚, 许方程, 等. 染料废水污染现状及处理方法研究进展[J]. 浙江农业科学, 2014(2): 264-269.
[3] Zhang Hui, Wu Jie, Wang Zhongqiong, et al. Electrochemical oxidation of crystal violet in the presence of hydrogen peroxide[J]. Journal of Chemical Technology & Biotechnology, 2010, 85(11): 1436-1444.
[4] 张艺蓓, 岳田利, 乔海鸥, 等. 超高效液相色谱-串联质谱法检测鱼中孔雀石绿、结晶紫及其代谢物[J]. 食品科学,2014(10): 179-184.
[5] Dowling G, Mulder P P J, Duffy C, et al. Confirmatory analysis of malachite green, Leucomalachite green, crystal violet and leucocrystal violet in salmon by liquid chromatography-tandem mass spectrometry[J]. Analytica Chimica Acta, 2007, 586(1-2): 411-419.
[6] 肖芳, 郭岚, 柳英霞, 等. 一种基于磁性纳米材料 Fe3O4/C 吸附测定水样中痕量结晶紫的新方法吸附测定水样中痕量结晶紫的新方法[J/OL]. 食品科学,http://www.cnki.net/kcms/detail/11.2206.TS.20151221.1447.040.html.
[7] 陈建伟, 姚志云, 毛健伟, 等. 浊点萃取-高效液相色谱法测定虾肉中孔雀石绿和结晶紫残留的研究[J]. 南京农业大学学报, 2010, 33(1): 94-98.
[8] Guo Mingcheng, Shi Tianyu, Duan Yongheng, et al. Investigation of amino acids in wolfberry fruit (Lycium barbarum) by solid-phase extraction and liquid chromatography with preco lumn derivatization[J]. Journal of Food Composition & Analysis,2015, 42: 84-90.
[9] Manzo V, Navarro O, Honda L, et al. Determination of crystal violet in water by direct solid phase spectrophotometry after rotating disk sorptive extraction[J]. Talanta, 2013, 106: 305-308.
[10] 齐海静. 水产品中某些违禁物质的加速溶剂萃取——高效毛细管电泳检测方法研究[D]. 河北大学, 2013.
[11] 张金利, 郭翠梨, 陆红, 等. 活性碳吸附处理甲基紫废水过程研究——实验研究[J]. 天津大学学报, 2001, 34(4): 481-484.
[12] 孙会会. 分散固液微萃取方法及在汞形态分析中的应用研究[D]. 中国科学科技大学, 2012.
[13] Zheng Jinfeng, Wu Hao, Gao Nannan, et al. Extraction of pazufloxacin mesilate using magnetic attapulgite clay nanoparticles prior to determination by fluorimetric detectin[J]. 2016, 16(5): 183-191.
[14] 王炎. 膨润土对染料废水中的甲基紫吸附研究: 影响因素及最佳吸附条件探讨[J]. 建筑论坛, 2015, (17): 1856.
[15] 聂凤明, 刘丽琴, 潘伟, 等. 固相微萃取一气一质法测定纺织品中苯乙烯含量[J]. 染整技术, 2009, 31: 8-11.
Magnetic Dispersive Solid-phase Microextraction Method for Determining the Content of Methyl Violet in Water Sample
DUAN Xiang-yang,SHEN Jiang-ping,QI Ai,YUAN Li-na,LIU Ya-lan,WANG Ke-xin
(Shanxi Normal University School Of Chemistry And Material Science, Shanxi Linfen, 041000)
Magnetic dispersive solid phase microextraction coupled with spctrophotometry as a novel analyticalmethod was established to the determination of methyl violet in water samples. The effects of various parameters of the analytical method were investigated, including pH value, sorbent amount, extraction and desorption time, desorption solvent, desorption volume and ionic strength. Under the optimized experimental conditions, linearity was demonstrated with standards over the range 0.02~0.1 μg/mL with relative coefficient of 0.99. The RSDs for intar-day and inter-day were 5.3% and 4.9% respectively. The detection limit was 0.024 μg/mL and quantitation limit was 0.079 μg/mL. And the spiked recoveries of the proposed method in the lake and pond water samples were varies from 94.3% to 101.0% and 85.4% to 90.0% respectively. Thus the developed method was successfully applied to analysize methyl violet in the lake and pond water samples
magnetic dispersive solid phase microextraction; methyl violet; spctrophotometry
O661.1
A
1009-220X(2016)04-0023-06
10.16560/j.cnki.gzhx.20160401
2016-03-22
段翔洋(1994~),女,本科,从事样品前处理方向的研究。1047358370@qq.com
