毛细管电泳法同时分离检测饮料中的六种食品添加剂
2016-09-19代语林董婵婵何建波朱燕舞
代语林,董婵婵,邓 宁*,何建波,王 燕,朱燕舞
(合肥工业大学化学与化工学院,安徽合肥230009)
毛细管电泳法同时分离检测饮料中的六种食品添加剂
代语林,董婵婵,邓宁*,何建波,王燕,朱燕舞
(合肥工业大学化学与化工学院,安徽合肥230009)
建立毛细管电泳法同时测定饮料中苯丙氨酸、对羟基苯甲酸甲酯、肉桂酸、山梨酸钾、抗坏血酸和苯甲酸6种食品添加剂的分析方法。在Peakmaster 5.3软件对电泳参数模拟的基础上,考察了缓冲液浓度、pH值以及分离电压对6种食品添加剂分离效果的影响。结果表明,在检测波长214 nm,进样时间10 s的情况下,确定最佳电泳条件为40 mmol/L pH 9.0 Na2HPO4-H3PO4的缓冲液,分离电压12 kV。在此条件下,6种食品添加剂在20~160 mg/L范围内呈良好的线性关系(R>0.980 0),检出限为0.23~0.77 mg/L,加标回收率为97.3%~103.0%,相对标准偏差(RSD)为2.0%~3.8%,精密度试验结果相对标准偏差(RSD)为2.0%~3.8%,表明该方法操作简便、准确度高、精密度良好,能满足饮料中6种食品添加剂的检测需求。
毛细管电泳;Peakmaster 5.3软件;食品添加剂;饮料;分离检测
毛细管电泳(capillary electrophoresis,CE)法是以石英毛细管为分离通道,高压直流电场为驱动力的分离检测技术。食品添加剂是指为改善食品色、香、味等品质,以及为防腐和加工工艺的需要而加入食品中的人工合成或天然物质[1]。然而食品添加剂的过量使用,将会导致人体生理机能紊乱,给人体健康造成较大危害。因此,建立一种简单有效地检测食品添加剂的方法非常重要。目前,食品添加剂的检测方法常采用气相色谱(gas chromatography,GC)法[2]、高效液相色谱(high performance liquid chromatography,HPLC)法[3-5]和毛细管电泳法[6-8]。相对于GC法和HPLC法来说,CE法样品预处理简单,且具有分离效率高、试剂消耗量少、实验成本低等优点,因此被广泛应用于食品添加剂的分离检测。张礼春等[9]应用CE法分离检测苯甲酸、山梨酸、脱氢乙酸、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯和对羟基苯甲酸丁酯等7种防腐剂。LIU F J等[10]利用CE法分离检测了饮料中的柠檬酸、水杨酸、苯甲酸、山梨酸和抗坏血酸等5种有机酸。
建立CE法检测食品添加剂的过程中,通常需要通过实验考察电泳条件对分离的影响[11-12],因此方法建立的过程较长。Peakmaster 5.3是一款电泳软件,可用于预测分析物在毛细管区带电泳中的行为、计算背景电解质pH值和离子强度等[13-14],从而节约实验探索时间、降低分析成本。AZEVEDO M S等[15]应用Peakmaster软件对马来酸、丙二酸、甲酸和天门冬酸等10种有机酸进行电泳条件的模拟,在此基础上,优化实验条件,从而实现了10种有机酸的分离检测。
由于Peakm aster 5.3软件数据库中没有对羟基苯甲酸甲酯和山梨酸钾的相应参数,本研究应用Peakmaster 5.3软件对苯丙氨酸、肉桂酸、山梨酸、抗坏血酸和苯甲酸5种食品添加剂的电泳条件进行模拟。在参考模拟数据的基础上,进一步考察缓冲液浓度及其pH值、分离电压等电泳参数对6种食品添加剂分离的影响,确定分离检测6种食品添加剂的最佳电泳条件,建立同时分离检测苯丙氨酸、对羟基苯甲酸甲酯、肉桂酸、山梨酸钾、抗坏血酸和苯甲酸等6种食品添加剂的毛细管电泳法,为毛细管电泳法同时分离检测食品添加剂提供了思路和参考价值。
1 材料与方法
1.1材料与试剂
磷酸氢二钠(Na2HPO4)、磷酸(H3PO4,85%)、无水乙醇、苯甲酸、对羟基苯甲酸甲酯、山梨酸钾(均为分析纯):国药集团化学试剂有限公司;苯丙氨酸(99%):阿拉丁试剂有限公司;肉桂酸(99.5%):上海润捷化学试剂有限公司;抗坏血酸(99.7%):广东汕头西陇化工公司;水为实验室自制二次蒸馏水。名仁苹果醋饮料、锐澳鸡尾酒、百事可乐极度、可口可乐零度汽水、可口可乐怡泉柠檬味汽水、脉动和怡宝魔力维他命购自大型超市。
1.2仪器与设备
CL1020型高效毛细管电泳仪:北京彩陆科学仪器有限公司;紫外检测器、高压电源和CT-22色谱信号采集单元:上海千谱软件公司;内径50 μm未涂层石英毛细管:河北永年锐沣色谱器件有限公司;PHS-3CT型pH计:上海大中分析仪器厂;BSM-200.4型电子天平:上海卓精电子科技有限公司;KQ-100E型超声波清洗器:昆山市超声仪器有限公司;CZ-93自动双重纯水蒸馏器:上海亚荣生化仪器厂。
1.3方法
1.3.1溶液配制
标准溶液的配制:准确称取苯丙氨酸、抗坏血酸各100 mg于2个小烧杯中,用二次蒸馏水溶解并分别转移到2个50 m L容量瓶中,定容至刻度,配制成2 mg/m L的标准储备液。准确称取苯甲酸、山梨酸钾和对羟基苯甲酸甲酯各100 mg于3个小烧杯中,用无水乙醇溶解并分别转移至3个50 m L容量瓶中,定容至刻度,配制成2 mg/m L的标准储备液。准确称取200 mg的肉桂酸于小烧杯中,用无水乙醇溶解并分别转移至50 m L容量瓶中,定容至刻度,配制成4 mg/m L的标准储备液。分别用1、2、3、4、5和6表示苯丙氨酸、对羟基苯甲酸甲酯、肉桂酸、山梨酸钾、抗坏血酸和苯甲酸这6种食品添加剂,R1-2、R2-3、R3-4、R4-5、R5-6分别表示电泳谱图中出峰次序相邻食品添加剂之间的分离度。使用分离度作为分离程度的衡量标准,分离度R的计算公式如下:
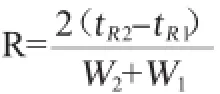
式中:tR为迁移时间,min;W为以时间表示的色谱峰底宽度;min;下标1、2分别代表相邻两个溶质。
缓冲溶液的配制:准确称取一定量的Na2HPO4于100m L烧杯中,用二次蒸馏水溶解,用0.01mol/LH3PO4溶液调节pH至9.0,并定容至50 m L容量瓶中,配制成40 mmol/L pH 9.0 Na2HPO4-H3PO4的缓冲液。
所有溶液在使用前进行超声脱气并用0.45 μm滤膜过滤。
1.3.2样品处理
对名仁苹果醋饮料、锐澳鸡尾酒、百事可乐极度、可口可乐零度汽水、可口可乐怡泉柠檬味汽水、脉动和怡宝魔力维他命试验样品分别进行超声处理,除去其中的气体,用二次蒸馏水进行适当的稀释,所得溶液用0.45 μm滤膜过滤后直接进样分析。
1.3.3石英毛细管电泳法操作条件
电泳条件:毛细管温度25℃,检测波长214 nm,进样高度10 cm,进样时间10 s。每次进样前熔融石英毛细管(50 μm×50 cm,有效长度42 cm)依次用1.0 mol/L HCl冲洗5 min、二次蒸馏水冲洗2 m in、1.0 mol/L NaOH冲洗10 m in、二次蒸馏水冲洗2 m in和缓冲液冲洗5 m in。每两次进样之间用缓冲液冲洗毛细管5 min。
2 结果与分析
2.1Peakmaster 5.3软件模拟
运用Peakmaster 5.3软件对苯丙氨酸、肉桂酸、山梨酸、抗坏血酸和苯甲酸混合体系进行毛细管电泳分离参数模拟,模拟实验参数如表1所示。

表1 Peakmaster 5.3软件模拟参数Table 1 Sim ula tion param eters o f Peakm aster 5.3
运行参数和缓冲液浓度及组成通过在软件界面输入相应数据和物质得到,系统参数是在运行参数设置之后运行软件得到。缓冲液分别选择含有三乙胺、三羟甲基氨基甲烷(Tris)和氢氧化钠(NaOH)与磷酸(H3PO4)进行模拟,模拟结果表明含有三乙胺和Tris的缓冲液都不能使模拟的5种食品添加剂出峰。最后使5种食品添加剂全部出峰并实现部分分离的缓冲液由80 mmol/L NaOH和40 mmol/L H3PO4组成,pH值9.436,电泳电压12kV。其中,山梨酸和苯甲酸在模拟条件下部分分离,需进一步进行电泳条件的优化试验。由于模拟得到pH值是9.436,因此实验中选择Na2HPO4溶液、H3PO4调节pH值,得到Na2HPO4-H3PO4缓冲液。
2.2电泳分离条件的确定
2.2.1缓冲液浓度的选择
在缓冲液pH 9.0、检测波长为214 nm、分离电压13 kV、进样时间10 s的条件下,缓冲液浓度从20 mmol/L逐步增大到60 mmol/L时,6种食品添加剂分离度以及迁移时间的变化情况见图1。

图1 缓冲液浓度对分离度(a)和迁移时间(b)的影响Fig.1 Effect of buffer solution concentration on the reso lution(a)and mobility time(b)
由图1a和图1b可知,随着Na2HPO4-H3PO4浓度的增大,6种食品添加剂之间的分离度逐渐增大且迁移时间也随之增大,这是由于缓冲液离子强度增加,毛细管内双电层厚度减小,引起电渗流下降[16]。当缓冲液浓度增大到40 mmol/L时,相邻食品添加剂之间的分离度都达到1.5以上,且在10 min内实现基线分离。继续增大缓冲液浓度,R3-4、R4-5的分离度<1.5,且迁移时间逐渐增大,由于毛细管内产生过多焦耳热的作用,导致峰形变宽,不利于分离。因此,选择40 mmol/L Na2HPO4-H3PO4溶液作为最佳缓冲液浓度。
2.2.2缓冲液pH值的选择
在缓冲液为40 mmol/L Na2HPO4-H3PO4、检测波长214 nm、分离电压12 kV、进样时间10 s条件下,缓冲液pH值在8.0~10.0范围内变化时对6种食品添加剂的分离度和迁移时间的影响,结果见图2。
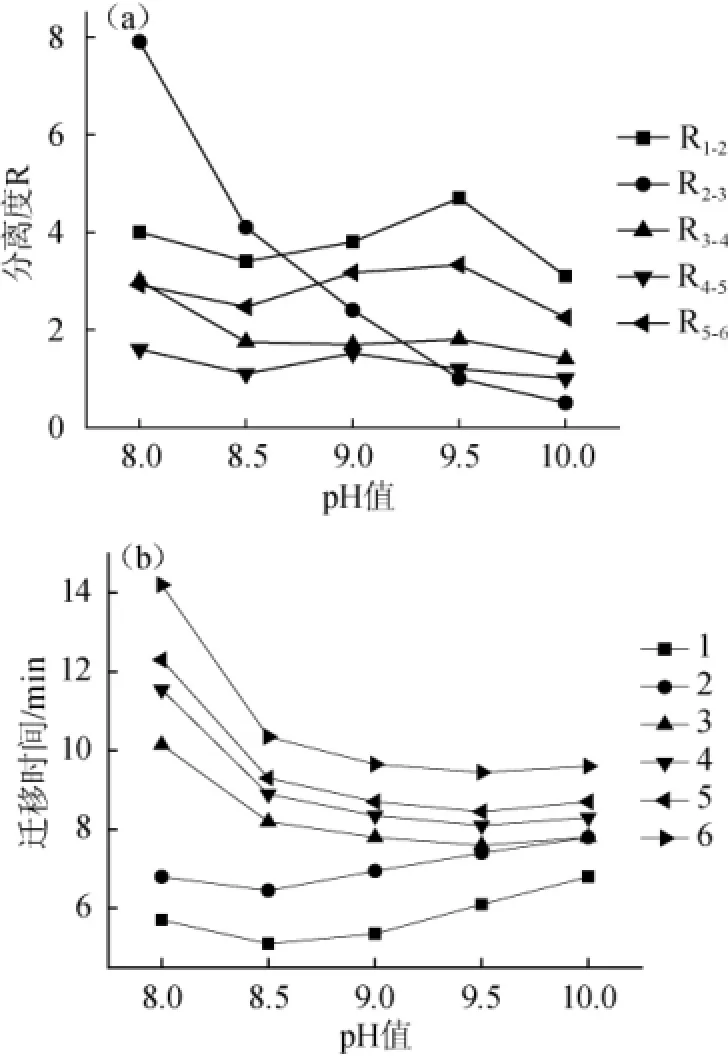
图2 缓冲液pH值对分离度(a)和迁移时间(b)的影响Fig.2 Effect of buffer solution pH on the resolution(a)and mobility tim e(b)
由图2可知,添加剂3、4、5和6的谱峰迁移时间随着pH值增大增大而减小,当缓冲液pH值为8.0和8.5时,由于添加剂3、4、5、6迁移时间较长,色谱峰出现展宽现象,而添加剂1和2的迁移时间在pH为8.5时最小,之后随着pH值的增大而增大;当缓冲液pH值为9.0时,被测物质峰形较好,并且大多数添加剂于10 min内实现了基线分离。当缓冲液pH值为9.5和10.0时,R2-3<1.5,不能实现基线分离;因此,在综合考虑分离度和迁移时间的情况下,选择缓冲液最佳pH值为9.0。
2.2.3分离电压的选择
在40 mmol/L pH 9.00 Na2HPO4-H3PO4、检测波长为214nm、进样时间为10 s的条件下,调节分离电压在6~18kV范围变化时对6种食品添加剂分离度和迁移时间的影响,结果见图3。
图3a中最下面一条曲线为R4-5曲线,说明在6种食品添加剂分析过程中,山梨酸钾和抗坏血酸最难以分离。R4-5只有在电压为12 kV时>1.5,即山梨酸钾、抗坏血酸只有在电压为12 kV时能实现基线分离。在分离电压为12 kV时,其他几种相邻食品添加剂之间的分离度均>1.5,达到基线分离。由图3可知,6种添加剂的迁移时间随着分离电压的增大而减小。综合考虑分离度和迁移时间的情况下,选择12 kV作为最佳分离电压。
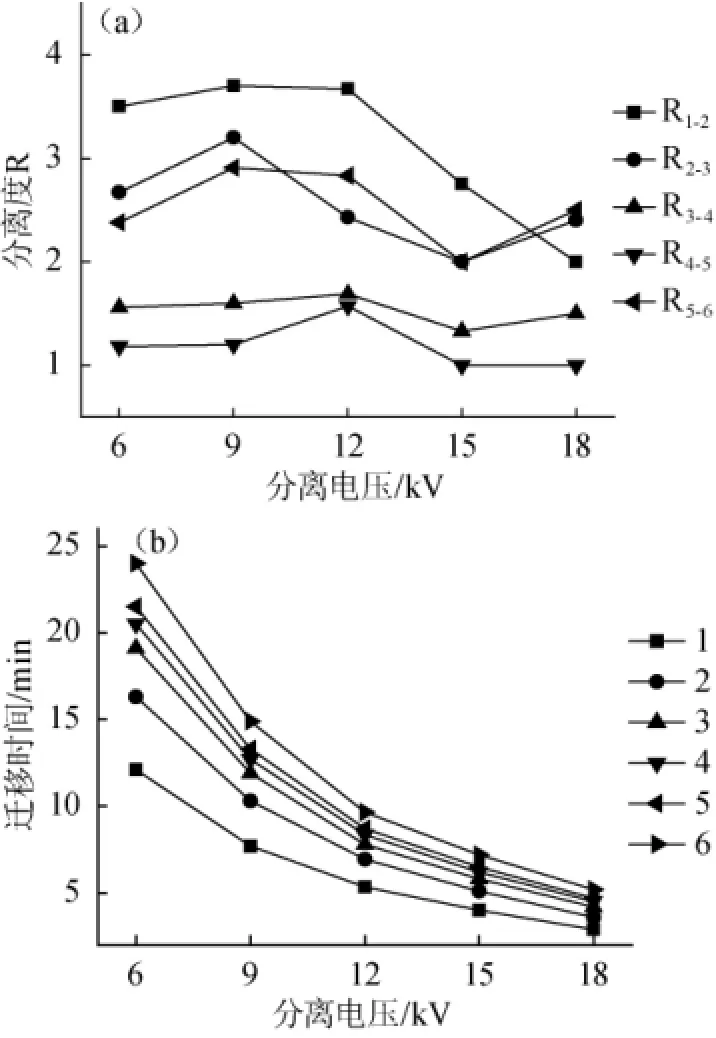
图3 分离电压对分离度(a)和迁移时间(b)的影响Fig.3 Effect of separation voltage on the resolution(a)and m obility tim e(b)
通过对电泳条件的优化,确定6种食品添加剂分离的最佳电泳条件为40 mmol/L pH 9.0 Na2HPO4-H3PO4缓冲液、分离电压12 kV,在此条件下,6种食品添加剂的毛细管电泳谱图如图4所示。由图4可知,6种食品添加剂在10 min内实现了良好地分离。

图4 6种食品添加剂毛细管电泳谱图Fig.4 Electropherogram of six food additives analysis by capillary eletrophoresis
2.3线性回归方程、相关系数、检出限和线性范围分析
在上述的最优电泳条件下,以峰面积(A)为纵坐标,食品添加剂标准品质量浓度(C)为横坐标,得到6种食品添加剂的标准曲线线性回归方程、相关系数(R)、检出限和线性范围,结果如表2所示。由表2可知,6种食品添加剂的线性相关系数(R)均>0.980 0,表明峰面积和6种食品添加剂的质量浓度呈良好的线性关系。6种食品添加剂的检出限为0.23~0.77 mg/L,定量分析的线性范围为20~160 mg/L。

表2 6种食品添加剂的线性回归方程、相关系数、检出限及线性范围Table 2 Linear regression equation,correlation coefficient,lim its of detection and linear ranges of six food additives
2.4加标回收率试验
为验证方法的准确性,以空白为对照,加入相同质量浓度的标准溶液,分别平行测定6次,根据加标量和测定结果计算其加标回收率和相对标准偏差(relative standard deviation,RSD),结果见表3。由表3可知,6种食品添加剂的加标回收率范围为97.3%~103.0%,RSD值为2.0%~3.8%,说明该方法准确度可靠,可满足饮料中6种食品添加剂的分析检测要求。
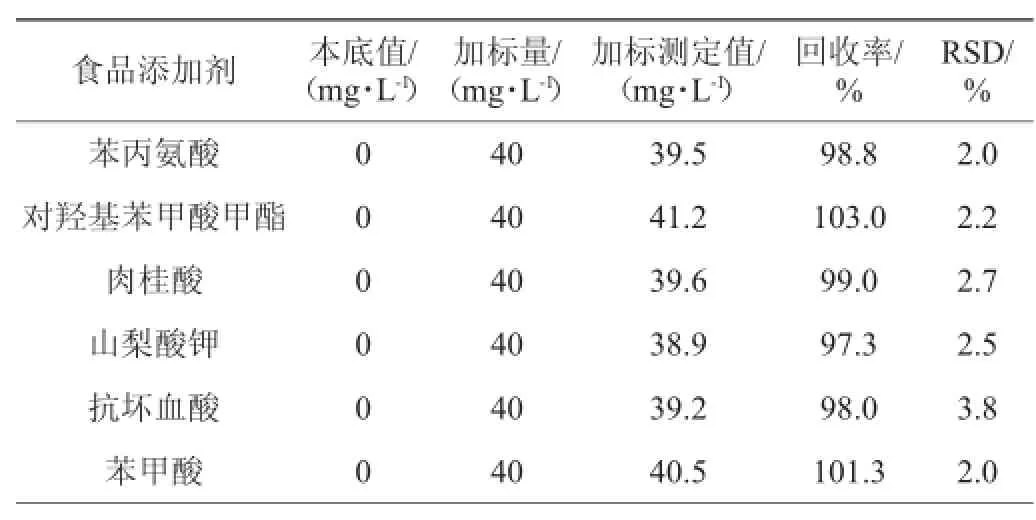
表3 加标回收率试验结果Table 3 Results of add ing standard recovery ra te experim ents
2.5精密度试验
准确量取标准品,分别平行测定6次,计算6种食品添加剂标准品测定值的平均值和相对标准偏差(RSD),结果见表4。由表4可知,测得6种食品添加剂标准品的相对标准偏差(RSD)为2.0%~3.8%,说明该方法精密度良好。
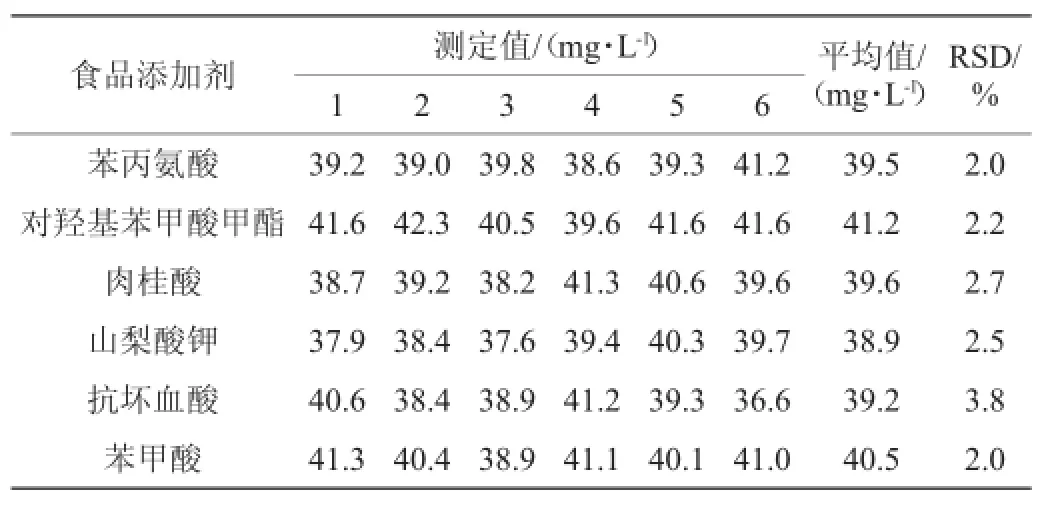
表4 精密度试验结果(n=6)Table 4 Results of precision experiments(n=6)
2.6样品中6种食品添加剂的分析
对名仁苹果醋饮料、锐澳鸡尾酒、百事可乐极度、可口可乐零度汽水、可口可乐怡泉柠檬味汽水、脉动和怡宝魔力维他命等7种市售饮料样品经过预处理之后,在最佳电泳条件下对其中的6种食品添加剂分别进行分析检测,每种饮料中6种食品添加剂含量的检测结果见表5。
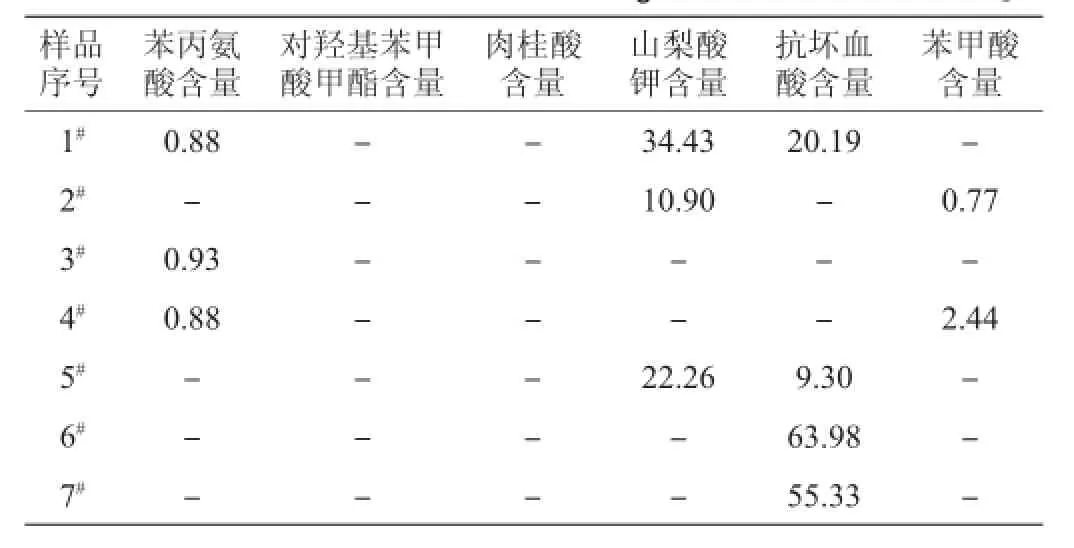
表5 7种饮料中6种食品添加剂的检测结果Table 5 Detection result of six food additives in seven kinds of beverages mg/L
由表5可知,1#、3#和4#饮料中,苯丙氨酸的含量分别为0.88 mg/L、0.93 mg/L和0.88 mg/L,1#、2#和5#饮料中,山梨酸钾的含量分别为34.43 mg/L、10.90 mg/L和22.26 mg/L,2#和4#饮料中,苯甲酸的含量分别为0.77 mg/L和2.44 mg/L,1#、5#、6#和7#饮料中,抗坏血酸的含量分别为20.19 mg/L、9.30 mg/L、63.98 mg/L和55.33 mg/L,所有添加剂的含量均符合国家相关标准[1],并且样品中检测到的添加剂均与该商品标签相对应。
3 结论
本研究应用Peakmaster 5.3软件对苯丙氨酸、肉桂酸、山梨酸、抗坏血酸和苯甲酸的混合样进行电泳条件的模拟,获得分离5种食品添加剂的缓冲液组成及浓度、pH值和分离电压。在此基础上,分别考察缓冲液浓度及pH值、分离电压等参数对6种食品添加剂分离的影响,在检测波长为214 nm、进样时间10 s的情况下,确定了分离检测6种食品添加剂的最佳电泳条件为40 mmol/L pH 9.0 Na2HPO4-H3PO4缓冲液,分离电压12 kV,在此电泳条件下,6种食品添加剂分离效果良好。结果表明,6种食品添加剂在20~160 mg/L范围内呈良好的线性关系(R>0.980 0),检出限为0.23~0.77 mg/L,加标回收率为97.3%~103.0%,相对标准偏差(RSD)为2.0%~3.8%,精密度试验结果RSD为2.0%~3.8%,该方法具有操作简单、快速、环境友好、检测结果可靠等优点,利于推广使用,因此具有较为广泛的应用前景,同时为毛细管电泳法分离检测食品添加剂提供参考。
[1]中华人民共和国国家卫生和计划生育委员会.GB 2760—2014食品安全国家标准添加剂使用卫生标准[S].北京:中国标准出版社,2014.
[2]SUN Y,WANG X Q,HUANG Y L,et al.Derivatization following hollow-fiber microextraction w ith tetramethylamonium acetate as a dual-function reagent for the determ ination of benzoic acid and sorbic acid by GC[J].J Sep Sci,2013,36(14):2268-2276.
[3]王骏,胡梅,张卉,等.超高效液相色谱快速测定饮料中的16种食品添加剂[J].食品科学,2010,31(2):195-198.
[4]马康,蒋孝雄,赵敏,等.高效液相色谱法同时测定软饮料中20种食品添加剂[J].分析化学研究报告,2012,40(11):1661-1667.
[5]黄永辉,余清,林钦,等.超高效液相色谱法同时测定碳酸饮料中的22种食品添加剂[J].分析测试学报,2011,30(8):877-882.
[6]郭芳芳,冯锋,白云峰,等.高效毛细管电泳-紫外检测法同时检测雪糕中多种添加剂[J].食品科学,2015,36(8):206-210.
[7]王丽芳,丁晓静,解娜,等.毛细管电泳法测定糖果及调制酒中10种人工合成色素[J].食品科学,2014,35(14):145-150.
[8]王钰,杨思文,代语林,等.毛细管电泳法分离检测饮料中的防腐剂[J].中国酿造,2014,33(4):124-128.
[9]张礼春,曾凯,高舸,等.高效毛细管电泳法同时测定饮料中七种防腐剂[J].分析实验室,2015,34(1):77-80.
[10]LIU F J,DING G S,TANG A N.Simultaneous separation and determ ination of five organic acids in beverages and fruits by capillary electrophoresis using diamino moiety functionalized silica nanoparticles as pseudo stationary phase[J].Food Chem,2014,145(7):109-114.
[11]陈桐,丁晓静,李一正,等.毛细管区带电泳-间接紫外法快速测定食品中的甜蜜素[J].色谱,2014,32(6):666-671.
[12]龙巍然,岑怡红,王兴益,等.毛细管区带电泳法同时测定饮料中16种食品添加剂[J].色谱,2012,30(7):747-751.
[13]HRU KA V,TĚDRM,VELÁKOVÁ K,et al.Eigenmobilities in background electrolytes for CZE.V.Intensity(amplitudes)of system peaks[J].Electrophoresis,2006,27(23):4610-4617.
[14]张红医,梁佳丽,聂中原,等.Peakmaster软件计算毛细管电泳缓冲液pH和离子强度[J].计算机与化学,2008,23(4):43-46.
[15]AZEVEDO M S,PIRASSOL G,FETT R,et al.Screening and determination of aliphatic organic acids in commercial Brazilian sugarcane spirits employing a new method involving capillary electrophoresis and a semi-permanent adsorbed polymer coating[J].Food Res Int,2014,60(6):123-130.
[16]武汉大学主编.分析化学(下册)[M].第五版.北京:高等教育出版社,2007.
Simultaneous separation and determination of six food additives in beverage by capillary electrophoresis
DAI Yulin,DONG Chanchan,DENG Ning*,HE Jianbo,WANG Yan,ZHU Yanwu
(Schoo l of Chem istry and Chem ical Engineering,Hefei University of Technology,Hefei 230009,China)
The analysis method of simultaneous determ ination of six food additives(including phenylalanine,methylparaben,cinnam ic acid,potassium sorbate,ascorbic acid and benzoic acid)was established by capillary electrophoresis.On the basis of simulation parameters of electrophoresis by Peakmaster 5.3 software,the effect of buffer solution concentration,pH and separation voltage on separation of six food additives were investigated. The results showed that in the conditions of determine wavelength 214 nm,injecting time 10 s,the optimum electrophoresis conditions were determ ined as 40 mmol/L Na2HPO4-H3PO4,pH 9.0 and separation voltage 12 kV.Under the conditions,the six food additives had a good linear relationship in the range of 20-160 mg/L(R>0.980 0).The lim its of detection were 0.23-0.77 mg/L.The adding standard recover rate was 97.3%-103.0% and the relative standard deviation(RSD)was 2.0%-3.8%.The RSD of precision experiments results was 2.0%-3.8%.The method had simple operation,high accuracy and good sensitivity,which could meet the determination requirement of 17 kinds of six food additives in beverages.
capillary electrophoresis;Peakmaster 5.3 software;food additives;beverage;separation and determ ination
O 657.8
0254-5071(2016)05-0187-05
10.11882/j.issn.0254-5071.2016.05.039
2016-02-25
国家自然科学基金(21102030)
代语林(1990-),男,硕士研究生,研究方向为工业及仪器分析。
邓宁(1976-),女,副研究员,博士,研究方向为毛细管电泳、毛细管电色谱。
