基于酰腙和菲咯啉配体的镉、铜配合物的水热合成、晶体结构和性质
2016-09-18陈延民王景梅陈飞鹏陈雅心曾倩茹解庆范泉州师范学院化学与生命科学学院泉州362000
陈延民 王景梅 陈飞鹏 陈雅心 曾倩茹 解庆范(泉州师范学院化学与生命科学学院,泉州 362000)
基于酰腙和菲咯啉配体的镉、铜配合物的水热合成、晶体结构和性质
陈延民王景梅陈飞鹏陈雅心曾倩茹解庆范*
(泉州师范学院化学与生命科学学院,泉州362000)
合成了一种酰腙类[ONO]三齿Schiff碱5-溴水杨醛缩噻吩-2-甲酰腙(H2Brsth),并以菲咯啉(Phen)为第二配体通过水热反应制备了两种金属配合物[Cd2(μ-Brsth)2(Phen)2] (1)和[Cu(Brsth)(Phen)] (2),经元素分析、红外光谱、紫外光谱、荧光光谱、热重分析和X射线单晶衍射分析对它们进行了表征。1的晶体属单斜晶系,C2/c空间群,晶胞参数a=2.116 36(13) nm,b=1.163 35(7) nm,c= 1.872 43(12) nm,β=100.981(2)°,V=4.525 6(5) nm3,Z=4;2的晶体属三斜晶系,P1空间群,晶胞参数a=0.911 7(2) nm,b=1.089 4(3) nm,c=1.272 9(3) nm,α=64.923(4)°,β=82.006(5)°,γ=67.768(5)°,V=1.059 6(5) nm3,Z=2。1是一种双核配合物,Cd的配位环境为畸变的八体构型;2是一种单核配合物,Cu则处于四方锥配位环境。配合物1在443 nm激发光作用下可发射很强的绿色荧光,最大发射波长525 nm,而配体的荧光发射峰则位于475 nm。
配合物;席夫碱;晶体结构;水热合成
Schiff碱是一类应用广泛的有机配体,被广泛用于非线性光学材料、催化剂和生物模拟等方面[1-3]。酰腙则是一类特殊的Schiff碱,其中许多具有很好的生物活性,如抗氧化、抑菌、抗肿瘤等[4-6]。酰腙具有结构多变和与金属配位方式丰富多样的特点,其配位方式不仅与酰腙分子结构和金属离子的电子构型有关,还与溶剂、介质的酸碱度、反电荷阴离子和反应温度等反应条件有关[7-9]。在水热条件下往往可以改变反应物的反应性能,提高反应活性,有利于生长缺陷少的完美晶体,因此,水热合成法在功能材料和配合物等的制备方面发挥着独特的作用[10-12]。作为研究工作的延续,本文制备了一种新的酰腙类Schiff碱(Scheme 1),采用水热法分别合成了镉和铜的配合物[Cd2(μ-Brsth)2(Phen)2] (1)和[Cu(Brsth)(Phen)] (2),用元素分析、红外光谱、紫外光谱和X射线单晶衍射分析进行了表征,同时分析了它们的热稳定性和荧光性质。

Scheme 1
1 实验部分
1.1仪器与试剂
Elmentar Vario EL元素分析仪(德国);Nicolet公司is10型FT-IR红外光谱仪(美国);美普达UV-1800PC型紫外-可见分光光度计(上海);塞驰STA 409 PC型综合热分析仪(德国);Bruker Smart Apex CCD单晶衍射仪(德国);Varian CARY/Eclipse型荧光分光光度计(美国)。所用试剂均为分析纯,使用前未经处理。
1.2合成方法
1.2.1配体H2Brsth的合成
将10 mmol 5-溴水杨醛溶于40 mL热的无水乙醇中,10 mmol噻吩-2-甲酰肼溶于30 mL无水乙醇,在搅拌下将二者混合,并滴入0.5 mL冰醋酸,然后加热搅拌回流3 h,析出大量黄色固体。冷却,抽滤,室温下用浓硫酸真空干燥备用。对C12H8BrN2O2S的元素分析,实测值(理论值),%:C 44.41(44.46),H 2.45(2.49),N 8.57(8.63)。IR (KBr,cm-1):3 202(NH),1 623(C=O),1 600(C=N),1 584,1 477(C=C);1 320,1 271(Ar-O);963(N-N);841,733(Ar-H);720(C-S);629 (C-Br)。
1.2.2配合物1的制备
将0.1 mmol菲咯啉、0.1 mmol的酰腙配体、0.1 mmol乙酸镉和6 mL甲醇和2 mL蒸馏水置于内衬聚四氟乙烯不锈钢自动升压反应釜,在140℃下晶化2 d,冷却至室温,获得黄色块状晶体。对C48H30Br2Cd2N8O4S2的元素分析,实测值(理论值),%:C 46.85(46.81),H 2.41(2.46),N 9.05(9.09)。IR (KBr,cm-1):1 609(C=N);1 523,1 503,1 461,1 426(C=C);1278,1 174(Ar-O);946(N-N);854,812,743,727(Ar-H);703(C-S);640(C-Br)。
1.2.2配合物2的制备
以乙酸铜代替乙酸镉,其他同上,获得蓝色针状晶体。对C24H15BrCuN4O2S的元素分析,实测值(理论值),%:C 50.88(50.85),H 2.61(2.67),N 9.85(9.88)。IR (KBr,cm-1):1 601(C=N);1 589,1 532,1 503,1 455, 1 433(C=C);1 355,1 178 (Ar-O);934(N-N);845,810, 730,717(Ar-H);707(C-S);640(C-Br)。
1.3晶体结构测试
分别选取0.37 mm×0.27 mm×0.19 mm (1)和0.15 mm×0.06 mm×0.03 mm (2)的单晶置于Bruker Smart Apex CCD单晶衍射仪上,用经石墨单色器单色化的Mo Kα射线(λ=0.071 073 nm)分别在3.13°< θ<25.01°(1)和1.77°<θ<28.74°(2)范围内以φ~ω扫描方式于291(2) K下收集单晶衍射数据。全部强度数据均经Lp因子校正,并进行了经验吸收校正,晶体结构由直接法解出,对全部非氢原子坐标及其各向异性热参数进行全矩阵最小二乘法修正,氢原子由理论加氢法得到。晶体中无序的部分参照文献[13-14]处理。1和2的结构解析和精修采用SHELXTL[15]和Olex 1.2程序包[16]。晶体学数据详见表1。键长键角列于表2和3。
CCDC:1062986,1;1046224,2。
2 结果与讨论
2.1晶体结构
2.1.1[Cd2(μ-Brsth)2(Phen)2]的晶体结构
晶体结构分析表明,镉配合物1属单斜晶系,C/2c空间群。它由2个Cd2+、2个菲咯啉和2个酰腙配体组成,是一种具有C2对称性的双核配合物(图1),Cd1…Cd1i间距0.335 9(9) nm。每个Cd2+的配位数为6,处于畸变的CdN3O3八面体配位环境,Cd-N 和Cd-O键长为0.224 3(5)~0.234 6(5) nm,键角为70.9(2)°~170.1(2)°。酰腙配体以烯醇式提供1个羰基O(C20-O2为0.131 1(7) nm,比典型的C=O长)、1个亚胺基N和1个酚羟基O与Cd2+配位,形成1个五元环和1个六元环,其中,酚羟基O以μ桥联方式同时与另一个Cd2+配位,从而构成双核结构。酰腙的噻吩环与苯环二面夹角24°,而扭转角O2-C13-N3-N4、N3-N4-C14-C15和N4-C14-C15-C20分别为5.9°、172.1°和2.0°,说明酰腙基与水杨基存在较强的共轭作用。

表1 配合物1和2的晶体学数据Table 1 Crystallographic data for the compounds 1 and 2

表2 化合物1的主要键长及键角Table 2 Selected bond lengths (nm) and bond angles (°) for 1
双核基元分子内2个菲咯啉的二面角为18°,Cg1…Cg2i(Symmetry code:i-x+1,y,-z+1/2)质心间距0.388 5 nm (其中Cg1由C7C8C9C10N2C11构成,Cg2由C4C5C6C7C11C12构成),说明二者的π-π相互作用较弱。而双核基元分子间相邻的Phen相互平行,存在较强的π-π相互作用,Cg2…Cg3ii(Cg3由C1C2C3C4C12N1构成,Symmetry code:ii1-x,1-y,1-z)质心间距0.364 4 nm,垂直距离0.340 8 nm,芳环的这种堆积作用将双核基元沿c轴方向扩展为一维链(图3a)。分子间次级键C-H…O增加了一维链的稳定性,C3-H3…O2ii键长0.243 4 nm。而一维链间噻吩环与菲咯啉之间的边对面作用(C23-H23A…Cg1iii键长0.308 2 nm)(图3b),将配合物扩展为三维超分子化合物(图2)。

表3 2的主要键长及键角Table 3 Selected bond lengths (nm) and bond angles (°) for 2
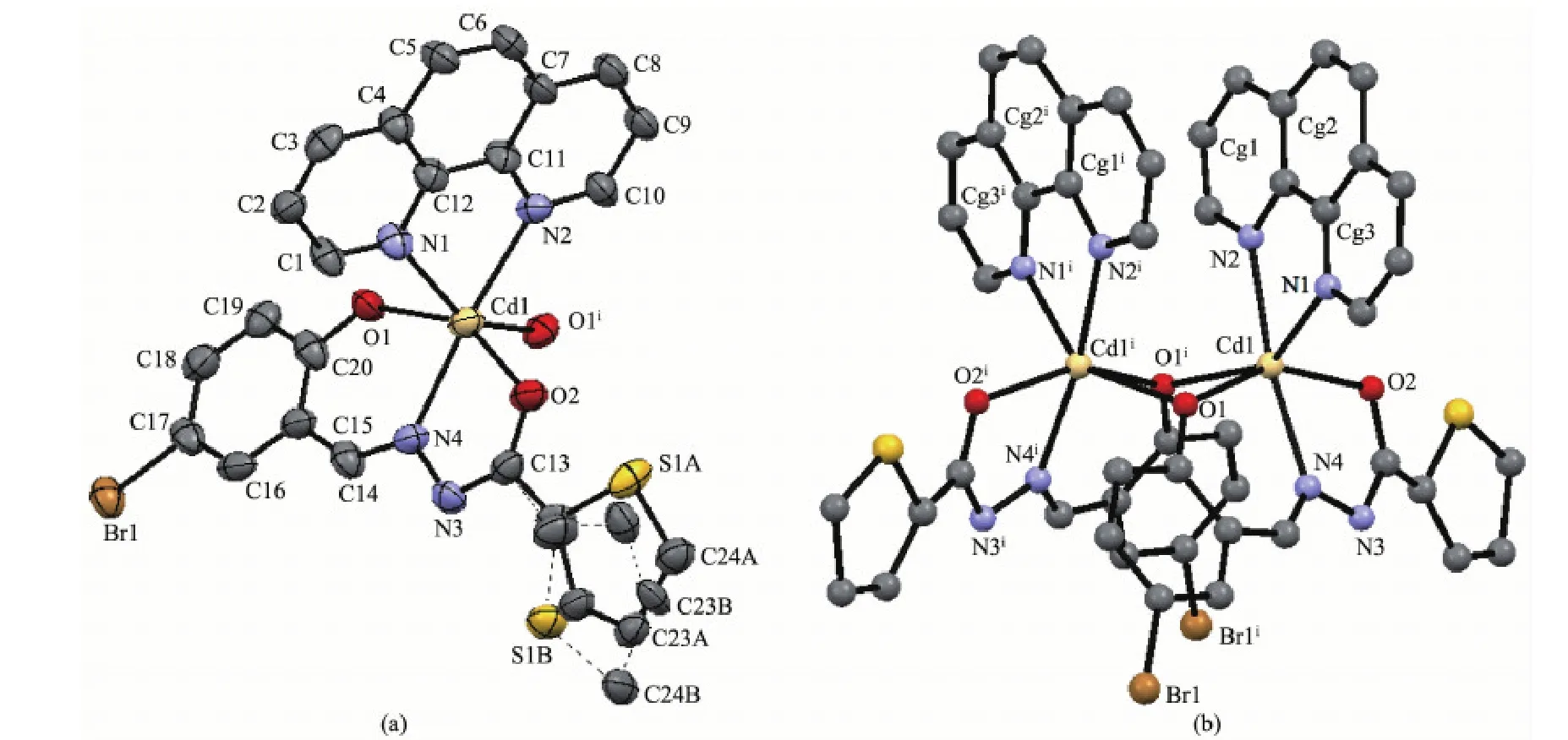
图1 配合物1的分子结构图Fig.1 Molecular structure of 1: (a) asymmetric unit at the 50% probability; (b) dinuclear structure

图2 配合物1沿a轴方向的堆积Fig.2 Packing diagram of complex 1 along the a axis
2.1.2[Cu(Brsth)(Phen)]的晶体结构
铜配合物晶体2属三斜晶系,P1空间群。它是一种单核配合物(图4),由1个中心离子Cu2+、1个菲咯和1个烯醇式的酰腙配体组成。Cu2+的配位数为5,与配位子形成畸变的CuN3O2四方锥配位几何构型,酰腙与中心金属离子配位形成近似平面的五元环和六元环。O1、O2、N1和N4位于锥底组成四边形,Cu-O键长为0.192 9(4)~0.199 0(4) nm,Cu-N键长为0.192 7(5)~0.203 0(5) nm。N4-O1-N1-O2扭转角为-4.96°,中心原子周围的键角为80.61(19)°~93.03(19)°,对角线键角为166.7(2)°~172.1(2)°;菲咯啉的1个氮原子N2位于锥顶,与邻位原子组成的键角为77.1(2)°~101.23(19)°,Cu1-N2键长为0.230 4 (6) nm。酰腙的噻吩环与苯环的二面角为9.8°。酰腙基与水杨基近乎共平面,扭转角C13-C18-C19-N4、N4-N3-C20-O1和C20-N5-N4-C19分别为0.4(9)°、2 (1)°和179.6(6)°。

图3 配合物1中分子间弱的相互作用Fig.3 Weak intermolecular interaction in 1

图4 配合物2的分子结构(椭球率50%)Fig.4 Molecular structure of 2 at 50% probability
Phen的所有原子几乎完全共平面,相邻结构基元的Phen相互平行,存在较强的π-π相互作用,质心间距分别为Cg2…Cg2i0.345 1 nm和Cg1…Cg1ii0.339 0 nm,其中,Cg1是N1/C1/C2/C3/C4/C12;Cg2 是C4/C5/C6/C7/C11/C12,Cg2与Cg2i及Cg1与Cg1ii所在平面夹角均为0.0°,这种芳环堆积作用将配合物沿a轴方向扩展为一维链(图5);同时Phen的Cg2平面与另一配合物结构基元的酰腙配体的噻吩环之间存在着C-H…π类型的次级键(图6),C23-H23…Cg2iii间距为0.280 48 nm。于是,配合物通过分子间的π-π作用和C-H…π作用形成一种二维超分子网络。

图5 配合物2通过π-π相互作用形成的一维链Fig.5 1D chain of 2 formed via π-π stacking interactions
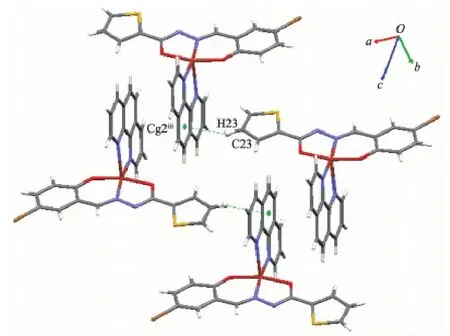
图6 配合物2分子之间的C-H…π相互作用Fig.6 Weak intermolecular C-H…π interaction in 2
2.2电子吸收光谱
配体及其配合物DMF溶液的电子吸收光谱见图7。酰腙配体H2Brsth在265 nm处的吸收带归属为芳环的π→π*电子跃迁;1和2在272和268 nm处的强吸收来自Phen配体的π→π*电子跃迁。H2L在294和306 nm处一对吸收峰与酚羟基O、亚胺基N和羰基O的n→π*电子跃迁有关,形成配合物1和2后,n→π*电子跃迁分别红移至312、324 nm和324、339 nm。H2Brsth在339和405 nm处的吸收带来自不同能级间的荷移跃迁(ILCT),而配合物1和2在405和404 nm的吸收强度与配体相比显著增强,这是因为配合物的形成增加了酰腙配体的刚性,而且可能荷移跃迁增添了L→M跃迁即LMCT成份。
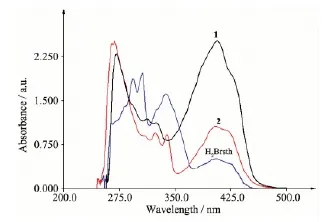
图7 H2Brsth配体及其配合物的紫外可见光谱Fig.7 UV-Vis spectra of H2Brsth ligand and thecomplexes
2.3荧光光谱
以DMF为溶剂考查了化合物的光致发光性能。酰腙配体可发射蓝色荧光,而酰腙配体由于以烯醇式与Cd2+配位,增加了配合物1中的酰腙整个分子的共轭程度,使发射光向长波位移而发射绿色荧光(图8)。H2Brsth和1的最大激发波长(λex)分别为405和443 nm,最大发射波长(λem)分别为475和 525 nm。具有顺磁性的Cu2+则对配体的荧光产生了淬灭作用。

图8 H2Brsth和1的荧光光谱Fig.8 Fluorescence spectra of H2Brsth and 1
2.4热稳定性
在N2气氛中以10℃·min-1升温速率考察了化合物的热分解行为(图9)。3个化合物在室温至800℃范围的分解均分为两阶段进行,配合物的热稳定性与酰腙配体相比显著提高。H2Brsth从252℃开始分解,至321.4℃快速失重58.39%;之后缓慢分解,至800℃残重10.02%。配合物1从348°开始分解,并快速失重,至405℃失重28.42%,相当于失去2个菲咯啉分子(理论计算值29.24%);配合物2从282℃开始分解,至460℃快速失重47.80%,相当于失去1个菲咯啉和噻吩残片(理论计算值46.4%)。至800℃,1和2的残重分别为34.79%和33.39%。

图9 化合物的热重分析图Fig.9 TGA curves of H2Brsth ligand and the complexes
[1] You Z L, Shi D H, Zhang J C, et al. Inorg. Chim. Acta, 2012,384(1):54-61
[2] HUO Yong-Qian(霍涌前), WANG Sheng-Wen(王升文), CUI Hua-Li(崔华莉), et al. Chinese J. Inorg. Chem.(无机化学学报), 2010,26(7):1274-1478
[3] Ebrahimipour S Y, Khabazadeh H, Castro J, et al. Inorg. Chim. Acta, 2015,427(1):52-61
[4] CHEN Yan-Min(陈延民), JIANG Xia(江霞), CHEN Guang-Hui(陈广慧), et al. Chinese J. Inorg. Chem.(无机化学学报), 2015,31(11):2159-2166
[5] WEI Tai-Bao(魏太保), LENG Yan-Li(冷艳丽), WANG Yong -Cheng(王永成), et al. Chinese J. Org. Chem.(有机化学), 2009,29(2):216-221
[6] XIE Qing-Fan(解庆范), GAO Ping-Zhang(高平章), CHEN Yan-Min(陈延民), et al. Chinese J. Inorg. Chem.(无机化学学报), 2014,30(10):2382-2388
[7] Khandar A A, Afkhami F A, Hosseini-Yazdi S A, et al. Inorg. Chim. Acta, 2015,427:87-96
[8] Yi L J, Xu G C, Zhang L, et al. Inorg. Chem. Commun., 2014,45:36-39
[9] HUANG Chao(黄超),WU Juan(吴娟), LIN Dong-Mei(林冬梅), et al. Chinese J. Inorg. Chem.(无机化学学报), 2015,31 (1):109-113
[10]Ying S M. Inorg. Chem. Commun., 2012,22:82-84
[11]Zheng C Z, Wang L, Liu J. J. Mol. Struct., 2012,1018(27): 78-83
[12]Ying S M. Inorg. Chim. Acta, 2012,387(30):366-372
[13]Sluis P V D, Spek A L. Acta Cryst., 1990,A46:194-201
[14]Müller P, Herbst-Irmer R, Spek A L, et al. Crystal Structure Refinement-A Crystallographer′s Guide to SHELXL. New York: Oxford University Press, 2006:63-96
[15]Sheldrick G M. SHELXTL, Program for X-ray Crystal Structure Solution and Refinement, University of Göttingen, Germany, 1997.
[16]Bourhis L J, Dolomanov O V, Gildea R J, et al. Acta Cryst., 2015,A71:59-75
Hydrothermal Syntheses, Crystal Structures and Properties of Cadmium/CopperComplexes with Acylhydrazone and Phenanthroline Ligands
CHEN Yan-Min WANG Jing-Mei CHEN Fei-Peng CHEN Ya-Xin ZENG Qian-Ru XIE Qing-Fan*
(College of Chemistry and Life Science, Quanzhou Normal University, Quanzhou, Fujian 362000, China)
Newly designed [ONO] tridentate hydrazone Schiff base ligand H2Brsth, derived from the condensation of 5-bromosalicylaldehyde and thiophene-2-formyl hydrazine, hydrothermally reacted with metal acetates and phenanthroline as co-ligand yielding two complexes [Cd2(μ-Brsth)2(Phen)2] (1) and [Cu(Brsth)(Phen)] (2), which were characterized by elemental analyses, FT-IR, electronic spectra, fluorescence spectra, TGA and single crystal X-ray diffraction. The X-ray diffraction analyses reveal that complex 1 crystallizes in monoclinic space group C2/c with a=2.116 36(13) nm, b=1.163 35(7) nm, c=1.872 43(12) nm,β=100.981(2)°, V=4.525 6(5) nm3and Z=4, while 2 crystallizes in the triclinic space groupwith a=0.911 7(2) nm, b=1.089 4(3) nm, c=1.272 9(3) nm,α= 64.923(4)°,β=82.006(5)°,γ=67.768(5)°, V=1.059 6(5) nm3and Z=2. The complex 1 is a binuclear ternary complex, in which Cd atoms locate in distorted coordination octahedron. The complex 2 is a mononuclear ternary complex with Cu atom in distorted square pyramidal coordination. The complex 1 exhibits strong green fluorescence with emission maximum of 525 nm at the excitation wavelength of 443 nm, while the ligand shows emission at 475 nm. CCDC: 1062986, 1; 1046224, 2.
complexes; Schiff base; crystal structure; hydrothermal synthesis
O614.24+2;O614.121
A
1001-4861(2016)03-0434-07
10.11862/CJIC.2016.043
2015-09-23。收修改稿日期:2015-11-30。
泉州师范学院学科建设资金和福建省大学生创新创业训练计划项目(No.201510399025,201510399030)资助。*通信联系人。E-mail:xqf360@163.com;会员登记号:S06N2113M1304(陈延民),S06N5449M1311(解庆范)。
