生物降解九资河茯苓多糖的HPLC图谱分析
2016-09-18王知龙张梦梦
王知龙,张梦梦,高 帆,叶 晶,吴 鹏
生物降解九资河茯苓多糖的HPLC图谱分析
王知龙,张梦梦,高帆,叶晶,吴鹏*
(黄冈师范学院 生命科学学院,经济林木种质改良与资源综合利用湖北省重点实验室,大别山特色资源开发湖北省协同创新中心,湖北 黄冈 438000)
通过柱前衍生化高效液相色谱(HPLC)法分析生物降解茯苓多糖的组分。选用黑曲霉HS-5液体发酵,生物降解茯苓多糖。粗多糖液经浓缩、Sevage法纯化、真空干燥处理得到多糖固体样品。利用红外光谱(IR)和紫外光谱(UV)分析鉴定多糖,采用PMP柱前衍生化HPLC法分析,通过与对照品的出峰时间比较,确定其分子中的单糖组成与含量分别为:甘露糖5.463%、鼠李糖8.970%、D-木糖52.809%。
茯苓多糖;生物降解;紫外光谱;红外光谱;高效液相色谱
茯苓(Poria cocos)是传统的药食两用食材,其味甘、淡、性平,具有利水渗湿、健脾和胃、宁心安神之功,是多种方剂及中成药的原料,又有“十药九茯苓”一说[1]。除了中医治疗药用外,还可制成多种保健食品[2-3]。因此,对茯苓的深度研究不仅具有学术价值,还具有实际生产意义。茯苓的有效成分主要为茯苓多糖[4],茯苓多糖具有抗肿瘤、增强机体免疫力、抗病毒、消石等作用,并广泛应用于医疗、保健和食品等方面[5-7]。茯苓主要分布在云南、湖北、安徽、山东、河南等省,其中湖北九资河茯苓以质量好,药用价值高,在国内外市场享有很高的声誉。目前,国内外对茯苓多糖的研究主要集中在其结构与活性的构效关系上,进而对其修饰改造,使其活性更强。本试验以九资河茯苓为原材料,采用生物降解法水解茯苓多糖,并采用柱前衍生化高效液相色谱(highperformanceliquidchromatography,HPLC)法对其结构组分进行分析研究,为九资河茯苓多糖的进一步研究和开发利用提供科学依据。
1 材料与方法
1.1材料与试剂
黑曲霉(Aspergillus niger)HS-5:黄冈师范学院食品加工技术实验室。浓硫酸、石油醚、无水乙醇、浓盐酸、三氟乙酸、醋酸酐、甲醇(色谱纯)、乙腈(色谱纯)、1-苯基-3-甲基-5-吡唑啉酮(1-phenyl-3-methyl-5-pyrazalone,PMP):国药集团化学试剂有限公司。
黑曲霉HS-5产β-葡聚糖酶培养基:大麦粉3%、酵母膏2%、碳酸钙0.3%、抗坏血酸0.1%、乙酸钠0.1%、硝酸铵0.14%、硫酸镁0.05%、硫酸亚铁0.000 1%、磷酸氢二钾0.1%。分装,灭菌,灭菌条件0.1 MPa、20 min。
1.2仪器与设备
RB-CJ-1ND型超净工作台:北京瑞邦兴业科技有限公司;TG16-WS台式高速离心机:湖南湘仪实验室仪器开发有限公司;D2F-6020真空干燥箱:上海景宏实验设备有限公司;UV2600紫外可见分光光度计、LC-20A高效液相色谱分析仪:岛津企业管理(中国)有限公司;SP-723型可见分光光度计:上海光谱仪器有限公司;Nicolet-6700傅立叶红外光谱仪:美国热电有限公司。
1.3方法
1.3.1原材料的预处理
九资河茯苓置于温度为105℃的烘箱进行烘干,至含水量不超过2%,将干燥后的茯苓用粉碎机进行粉碎,过60目筛,并收集过筛后的茯苓粉末,室温贮藏于密封塑料袋中备用。
缓冲液的配制:称取柠檬酸19.21g,加水溶解至1000mL容量瓶中,定容,得0.1 mol/L柠檬酸溶液;称取柠檬酸钠29.41 g加水溶解至1 000 mL容量瓶中,定容得0.1 mol/L柠檬酸钠溶液。
3,5二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)试剂的配制:称取3,5-二硝基水杨酸10 g,置于约600 mL水中,逐渐加入氢氧化钠10 g,在50℃水浴中(磁力)搅拌溶解,再依次加入酒石酸钾钠200 g,苯酚2 g和无水亚硫酸钠5 g,待全部溶解并澄清后,冷却至室温,用水定容至1 000 mL。过滤贮存于棕色试剂瓶中,于暗处放置7 d后使用。
1.3.2茯苓粗多糖的提取
根据文献[8-10]中得出的最佳工艺,本实验选用黑曲霉HS-5降解茯苓多糖。主要操作如下:
(1)β-葡聚糖酶液的制备
接种黑曲霉HS-5至β-葡聚糖酶培养基中,扩培,将扩培菌种接种于盛有50 mL发酵培养基的250 mL三角烧瓶中,置于30℃、200 r/min旋转式摇床上控温发酵,发酵48 h。过滤后得到粗酶液,采用硫酸铵分级沉淀、透析浓缩、采用Sephadex G-100柱层析对其进行分离纯化,得到了β-葡聚糖酶液。
(2)生物降解茯苓多糖
本试验通过改进郭雨桐等[18]的技术参数得到生物降解茯苓多糖的最优技术参数:反应温度55℃、时间120min、pH 5.0、β-葡聚糖酶量20 mL。在该参数条件下,用DNS法测得β-葡聚糖酶的酶活达20.03 U/mL,苯酚-硫酸法测得茯苓多糖的提取率为18.074%。
(3)DNS法测定β-葡聚糖酶酶活
本实验以葡聚糖为底物,DNS显色,光电比色法于波长520 nm处测定β-葡聚糖酶酶活。
酶活力定义:在本试验条件下,每分钟分解β-葡聚糖产生相当于l μmol葡萄糖所需的酶蛋白的量定义为一个酶活单位。此法测得β-葡聚糖酶的酶活达20.03 U/mL。
(4)粗多糖的提取
根据本项目前期研究结果,取2g茯苓粉末于锥形瓶中,加60 mL缓冲液(pH5.0),再加入20 mL酶液,最后以10 mL缓冲液清洗盛酶液的容器并倒入锥形瓶中。在55℃条件下反应120 min。反应结束后将采用高压蒸汽灭菌法将酶灭活,抽滤得到粗多糖液,然后采用旋转蒸发仪蒸发浓缩,低温真空干燥,从而得到茯苓多糖粗品。
1.3.3苯酚-硫酸法测定多糖含量
吸取1.0mL稀释样品液加入20mL试管中,再加入2mL 5%的苯酚、6 mL浓硫酸,放置30 min,于波长490 nm处测其吸光度值,对照标准曲线[13],计算多糖含量。
1.3.4茯苓多糖的纯化
粗多糖中含有较多的游离蛋白,在多糖的分离提取中,有机溶剂能够使游离蛋白变性沉淀,从而达到纯化的目的。
本实验采用Sevage法反复除蛋白:取茯苓多糖溶液4mL,加入1 mL氯仿和正丁醇(V(氯仿)∶V(正丁醇)=4∶1),充分振荡20min,离心去除水层与溶剂层交界的变性蛋白,反复数次,直至溶剂层与水的界面无乳白色沉淀为止。
1.3.5茯苓多糖的水解与衍生化[11-13]
(1)茯苓多糖的水解
取茯苓多糖样品40 mg于安瓿瓶中,再加入4 mol/L三氟乙酸溶液1mL,封管后于90℃水解8 h,得水解样品溶液,转移至EP管中离心,取上清液用0.3 mol/L氢氧化钠溶液调pH至中性。
(2)样品与单糖标品的PMP衍生化
精确称取半乳糖、葡萄糖和甘露糖各约0.018 g,鼠李糖约0.016 g,葡糖醛酸约0.019 g,木糖0.015 g溶于0.3 mol/L氢氧化钠溶液1.0 mL中,配制每种单糖的标准溶液(约为0.1 mol/L),分别取每种单糖的标准溶液100 μL混合,配制混和标准品溶液(每种单糖浓度约为1/60 mol/L)。取标准品溶液或茯苓多糖水解溶液50 μL于EP管中,依次加入PMP溶液(0.5 mol/L甲醇溶液)50 μL和0.3 mol/L氢氧化钠溶液50 μL,混匀后置于70℃水浴中加热反应30 min。取出室温放置10 min,再加入0.3 mol/L盐酸液60 μL中和至酸性,混匀后用0.5 mL三氯甲烷萃取,涡旋3 min,5 000 r/min离心15 min,小心弃去有机层(下层),萃取3次,5 000 r/min离心15 min,上清液加水至500 μL混匀,过膜后,用于HPLC分析。
1.3.6 HPLC分析单糖组成
色谱分析条件[14]:检测波长为250 nm。柱温为室温,流速1.0 mL/min,流动相:溶剂A,15%(V/V)乙腈+0.05 mol/L磷酸缓冲液(KH2PO4-NaOH,pH 6.9)、溶剂B,40%(V/V)。乙腈+0.05 mol/L磷酸缓冲液(KH2PO4-NaOH,pH6.9),时间梯度为0→10min→30min,相应浓度梯度为0→8%→20%溶剂B;进样体积10 μL。
1.3.7红外光谱分析
采用KBr压片法在Nicolet-6700傅立叶红外光谱仪波数400~4 000 cm-1范围进行扫描分析。
1.3.8紫外光谱分析
采用固体样品扫描法,用岛津UV2600紫外可见分光光度计进行扫描,扫描波长为190~600 nm。
2 结果与分析
2.1红外光谱结果分析
如图1所得的红外图谱显示,3 483 cm-1处强且宽的吸收峰是O-H与C-H的伸缩振动,为糖类物质的特征吸收;2 981 cm-1处的吸收峰是C-H的伸缩振动;1 585 cm-1处的吸收峰是O-H的弯曲振动吸收峰;1 442 cm-1和1 392 cm-1处的吸收峰是次甲基(=CH2)的变形吸收峰;1 267 cm-1是吡喃糖环C-O-C伸缩振动吸收峰;1 131cm-1是吡喃糖环的C-O吸收峰,1 080 cm-1和1027 cm-1是O-H的变角振动吸收峰,881 cm-1为β型糖苷键的吸收峰[15-17],740 cm-1为吡喃糖环的C-O-C的对称振动峰。586 cm-1和509 cm-1是C-CO的变形振动吸收峰。由此表明,提取的多糖样品是β-D-构型的多糖。

图1 茯苓多糖红外扫描图谱Fig.1 Infrared scanning spectrum of pachymaran
2.2紫外光谱分析
图2为生物降解法提取的茯苓多糖紫外扫描图谱,可见在波长204 nm处有典型的糖类物质特征吸收峰[16]。
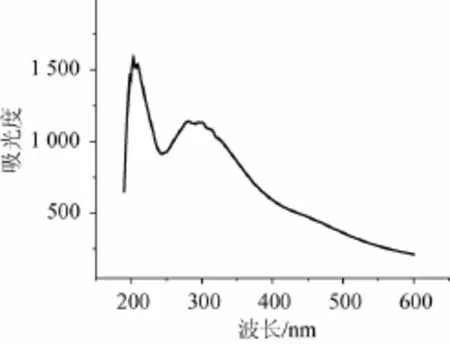
图2 生物降解得到的茯苓多糖的紫外吸收光谱Fig.2 UV absorption spectrum of pachymaran by biodegradation
2.3 HPLC分析单糖组成
生物降解茯苓多糖的多糖样品经过水解、PMP衍生化后,经高效液相色谱仪分析得到的色谱如图3所示;参照相同HPLC分析方法下屈贺幂[13]得出的混合标准单糖PMP衍生物高效液相色谱图,可知茯苓多糖样品HPLC色谱图中2.712 min处出峰对应的是PMP;4.065 min出的峰对应的是甘露糖;5.301 min处出峰对应的是鼠李糖;11.755 min时出的峰对应的是D-木糖。
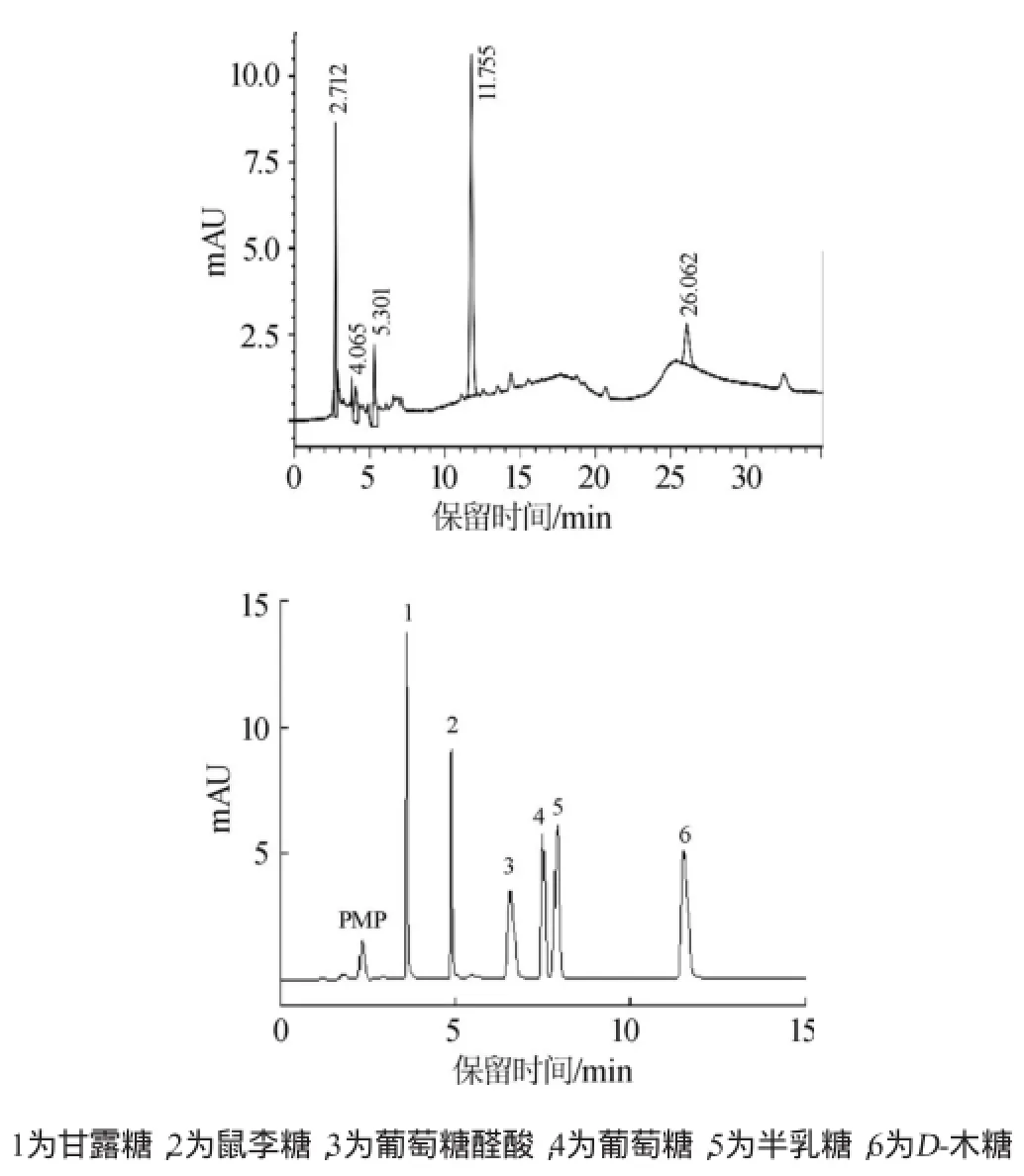
图3 混合标准单糖PMP衍生物高效液相色谱图Fig.3 HPLC chromatogram of mixed standard monosaccharide PMP derivative
根据色谱图中的出峰时间与峰面积,可以得出生物降解的九资河茯苓多糖含有的单糖组分与含量依次为:甘露糖5.463%、鼠李糖8.970%、D-木糖52.809%。
3 结论
多糖的提取方法有许多种,但是传统方法多糖提取率一般都不高而且提取时间较长。本试验选用黑曲霉液体发酵,定向高产β-葡聚糖酶为外源酶降解茯苓得到多糖溶液。β-葡聚糖酶可最大限度的将茯苓多糖中的葡聚糖聚合体降解为还原糖和寡糖,从而提高茯苓多糖的提取率,为茯苓多糖的开发利用提供依据。
经初步纯化后的茯苓多糖采用PMP柱前衍生化HPLC法分析,通过与对照品的出峰时间比较,最后确定其分子中的单糖。HPLC图谱分析结果显示,生物降解九资河茯苓多糖的单糖组成与含量为甘露糖5.463%、鼠李糖8.970%、D-木糖52.809%。
[1]冯亚龙,赵英永,丁凡,等.茯苓皮的化学成分及药理研究进展[J].中国中药杂志,2013,38(7):1098-1102.
[2]陈美珍,余杰,李鹰.茯苓、山药老年固体保健饮料的研制[J].食品工业科技,2000,21(2):36-38.
[3]路红波.茯苓保健鱼面的研制[J].食品工业,2011(7):55-57.
[4]牛爽,郝利民,赵树欣,等.茯苓多糖的研究进展[J].食品科学,2012,33(13):348-353.
[5]张敏,高晓红,孙晓萌,等.茯苓的药理作用及研究进展[J].北华大学学报(自然科学版),2008,9(1):63-68.
[6]侯安继,陈腾云,彭施萍,等.茯苓多糖抗衰老作用研究[J].中药药理与临床,2004,20(3):10-11.
[7]邵祥龙,苏日娜,李伟立,等.茯苓多糖抗肿瘤作用研究进展[J].北京中医药,2009,28(4):315-317.
[8]方华平.复合诱变选育β-葡聚糖酶高产菌株及其酶学性质的研究[D].合肥:安徽农业大学,2007.
[9]边超.酶水解制备水溶性茯苓多糖及其抗肿瘤活性的研究[D].武汉:华中农业大学,2006.
[10]徐光域,颜军,郭晓强,等.硫酸苯酚定糖法的改进与初步应用[J].食品科学,2005,26(8):342-346.
[11]吴建元,肖玉玲,孙曼春,等.柱前衍生化高效液相色谱法分析茯苓多糖的单糖组成[J].医药导报,2009,28(9):1213-1214.
[12]马耀宏,郑岚,杨俊慧,孟庆军,等.柱前衍生化HPLC法分析真菌多糖的单糖组成[J].食品科技,2012,37(1):254-260.
[13]屈贺幂.茯苓多糖的提取及其指纹图谱研究[D].长沙:湖南大学,2007.
[14]黄灿,王玉明,赵俊.抗肿瘤活性茯苓多糖的提取、纯化与结构分析[J].中草药,2012,43(11):2146-2149.
[15]莫清.茯苓多糖的化学修饰和生理性质的研究[D].杭州:浙江理工大学,2012.
[16]夏朝红,戴奇,房韦,陈和生.几种多糖的红外光谱研究[J].武汉理工大学学报,2007,29(1):45-47.
[17]颜军,陶涛,孙晓春,等.茯苓多糖的纯化及分子量测定[J].化学与生物工程,2011,28(3):88-90.
[18]郭雨桐,肖文军.β-葡聚糖酶降解茯苓多糖的效应[J].北方园艺,2011,24(9):18-22.
HPLC chromatogram analysis of Jiuzihe pachymaran by biodegradation
WANG Zhilong,ZHANG Mengmeng,GAO Fan,YE Jing,WU Peng*
(Hubei Collaborative Innovation Center for the Characteristic Resources Exploitation of Dabie Mountains,Hubei Key Laboratory of Economic Forest Germplasm Improvement and Resources Comprehensive Utilization,College of Life Sciences,Huanggang Normal University,Huanggang 438000,China)
The pachymaran components by biodegradation were analyzed by HPLC with pre-column derivatization.UsingAspergillus nigerHS-5 as fermentation strains to conduct liquid-state fermentation,pachymaran was degraded by biodegradation.Pachymaran solid sample was obtained by concentrating crude sugar,sevage purification and vacuum drying.Pachymaran solid sample was analyzed and identified by infrared spectroscopy(IR)and ultraviolet spectroscopy(UV),then using HPLC analysis with PMP column derivatization,by comparison with the peak time of the standard,the monosaccharide composition and contents were determined as follows:mannose 5.463%,rhamnose 8.970%,D-xylose 52.809%.
pachymaran;biodegradation;ultraviolet spectroscopy;infrared spectrum;HPLC
O657
0254-5071(2016)07-0139-04
10.11882/j.issn.0254-5071.2016.07.030
2016-03-03
湖北省自然科学基金项目(2013CFB472);校生物示范中心项目(zx201422)
王知龙(1994-),男,本科,研究方向为食品生物技术和农产品加工与贮藏。
吴鹏(1982-),女,副教授,博士,研究方向为食品生物技术和农产品加工与贮藏。
