糠醛对酿酒酵母GGSF16葡萄糖酒精发酵的影响
2016-09-18于志强伍时华赵东玲黄翠姬广西科技大学生物与化学工程学院广西柳州545006
于志强,伍时华,赵东玲,黄翠姬,易 弋(广西科技大学 生物与化学工程学院,广西 柳州 545006)
糠醛对酿酒酵母GGSF16葡萄糖酒精发酵的影响
于志强,伍时华,赵东玲*,黄翠姬,易弋
(广西科技大学 生物与化学工程学院,广西 柳州 545006)
研究了不同质量浓度糠醛对酿酒酵母GGSF16葡萄糖酒精发酵的影响,旨在为木质纤维素水解液酒精发酵提供参考和依据。以酵母浸出粉胨葡萄糖培养基替代木质纤维素水解液,调节糠醛质量浓度为0~2 g/L之间七个不同梯度,基于曲线下面积法考察糠醛对葡萄糖酒精发酵的影响。结果表明,随着糠醛质量浓度的增加酒精发酵周期延长,乙醇产率逐渐降低,但最终酒精度并没有明显差别;当糠醛质量浓度为0时乙醇产率最高,为3.24 g/(L·h);发酵周期最短,为6.94 h。
糠醛;葡萄糖;酒精发酵;酵母;曲线下面积
木质纤维素主要包含单糖聚合而成的纤维素和半纤维素。半纤维素的主要降解产物为木糖,在高温或高压条件下木糖将进一步降解为糠醛,糠醛为木质纤维素水解液酒精发酵的主要抑制剂[1-2]。而糠醛抑制酵母代谢的机理并不完全清楚,但已有研究表明,糠醛抑制了糖酵解过程中主要的酶的活性,包括己糖激酶、磷酸果糖激酶和磷酸丙糖脱氢酶[3]。此外,三羧酸循环及乙醇合成路径中的乙醇脱氢酶和乙醛脱氢酶同样受糠醛的影响[4]。在厌氧条件下,酵母利用糠醛转变成糠醇和甲酸[5]。这种转换最可能的途径是糠醛取代乙醛作为乙醇脱氢酶和乙醛脱氢酶的底物[6]。糠醛的抑制效果主要与酵母代谢利用糠醛的能力有关[6]。如果糠醛对酒精发酵的影响能够确定,便可通过特定的去毒方法、选择合适的菌种或者应用最优的工艺条件来提高发酵效率。
为了避免水解液中的其他成分对发酵产生影响或与糠醛产生相互作用,故将糠醛贮备液添加到酵母浸出粉胨葡萄糖培养基(yeast extract peptone dextrose,YEPD)中替代木质纤维素水解液进行酒精发酵,通过曲线下面积法(areaunder the curve,AUC)并对糖代谢曲线拟合[7-10],考察酒精发酵过程中的葡萄糖代谢、细胞生长及乙醇的生成受糠醛的抑制效果,从而为利用木质纤维素水解液酒精发酵奠定基础。
1 材料与方法
1.1料与试剂
1.1.1株
酿酒酵母GGSF16(Saccharomycescerevisiae GGSF16):由广西科技大学发酵工程研究所提供。
1.1.2养基
斜面活化培养基:葡萄糖20 g/L,蛋白胨20 g/L,酵母浸膏10 g/L,琼脂20 g/L,自然pH值。
种子培养基:葡萄糖20 g/L,蛋白胨20 g/L,酵母浸膏10 g/L,自然pH值。
YEPD发酵培养基:葡萄糖50 g/L,蛋白胨20 g/L,酵母浸膏10 g/L,自然pH值。
以上培养基和溶液均115℃高压蒸汽灭菌20min。
1.2器与设备
ZWYD-2402叠式恒温培养振荡器:上海智城分析仪器制造有限公司;LS-B35L-I立式压力蒸汽灭菌器:江阴滨江医疗设备有限公司;UV-1100紫外分光光度计:上海美普达仪器有限公司;SBA-40生物传感仪:山东科学院生物研究所;SW-CJ-TB标准净化工作台:苏州集团苏州安泰空气技术有限公司;M ikro220R台式冷冻离心机:天津奥特赛恩斯仪器有限公司;DW-86L386立式超低温保存箱:青岛海尔特种电器有限公司。
1.3法
1.3.1酵方法
种子培养:将实验室保存的斜面菌种接至斜面活化培养基中,32℃条件下培养1~2 d,待其斜面上长出白色菌苔即为菌种培养成熟。将活化的菌种转接至种子培养基中,32℃、160 r/min培养24 h后,经12 000 r/min离心5min,弃上清液,加入无菌水将酵母泥制成10倍浓缩种子悬液备用。
发酵流程:以10%的接种量(2m L高浓度种子液)将种子液转接至200m L YEPD发酵培养基中(500m L的锥形瓶),无菌操作将糠醛贮备液加入YEPD发酵培养基中,分别制成0、0.25 g/L、0.5 g/L、0.75 g/L、1.0 g/L、1.5 g/L、2.0 g/L质量浓度梯度,并以不添加糠醛作为对照组。初始酵母数在3.32×107CFU/m L左右,摇床160 r/m in,温度为32℃,发酵条件为非严格厌氧,用透气膜和牛皮纸包扎发酵。每个处理3个平行。发酵过程中每隔2 h取样并取其中一个平行用称重法测CO2质量损失,直至CO2质量损失<0.2 g时,即发酵结束。
1.3.2析方法
样品处理:取发酵液1m L,12 000 r/min离心5min,取上清液于-60℃冰箱冷冻,用于葡萄糖含量和乙醇生成数据分析;加入与抽取上清液等量的蒸馏水混合成菌悬液,用于测定酵母细胞OD值。
生物量的测定:使用UV-1100紫外可见分光光度计,将菌悬液稀释至合适倍数测定其在波长600 nm处的吸光度值。酒精度与葡萄糖含量采用SBA-40C生物传感分析仪测定,标准乙醇与葡萄糖含量分别为0.1%vol和1 g/L,将发酵上清液稀释合适倍数进样分析。
1.3.3线下面积与糖代谢曲线拟合
葡萄糖的代谢曲线及细胞OD值的生长曲线运用GraphPad Prism 5软件进行处理,并分别获得葡萄糖代谢曲线下面积及细胞生长曲线下面积,分别记做葡萄糖AUC与OD值AUC。
葡萄糖的代谢曲线运用Origin 8.0软件进行非线性曲线拟合,葡萄糖代谢方程拟合较好的主要有Boltzm ann S形函数和DoseResp S形函数,选择R2最大的函数作为其拟合方程,并以拟合方程分别计算出葡萄糖消耗一半与完全消耗的时间,记做t50与tend。
1.3.4定方法

2 结果和分析
2.1醛对糖代谢的影响
2.1.1醛对葡萄糖AUC的影响
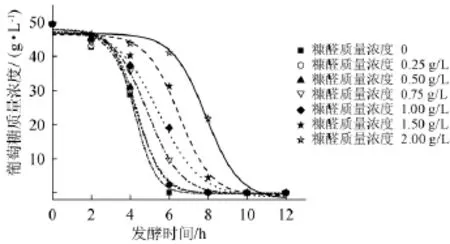
图1 不同糠醛质量浓度条件下酵母GGSF16葡萄糖消耗拟合曲线Fig.1 Fitting curve of glucose consum ption from S.cerevisiae GGSF16 w ith differen t furfural concentration

表1 糠醛浓度对酵母GGSF16葡萄糖代谢曲线面积的影响Table 1 Effec t of different furfural concentration on glucose m etabolism curve area from S.cerevisiae GGSF16
曲线下面积法能够直观、准确且定量的判断葡萄糖的利用情况,从而整体的评估发酵的好坏[10]。葡萄糖AUC越大说明葡萄糖利用速率越慢、糠醛对酵母细胞利用葡萄糖的抑制作用越强,反之亦然[10]。从图1可知,随着糠醛质量浓度的增大,葡萄糖的代谢速率不断降低,但对最终的残糖量影响不大。由表1可知,对照组的葡萄糖AUC值最小193.10±2.16,不同糠醛质量浓度条件下的葡萄糖AUC随糠醛质量浓度的增大而增大。当糠醛质量浓度为2.0 g/L时,葡萄糖AUC达到最大355.70±2.93。分别以不同糠醛质量浓度条件下的葡萄糖AUC与对照组的葡萄糖AUC比值发现,比值随着糠醛质量浓度的增大而增大。结果表明,抑制作用随着糠醛质量浓度的增大而不断增强[3-7]。当糠醛质量浓度分别为0.25 g/L与1.0g/L时,比值分别为1.04±0.008 7和1.31±0.004 1,表明糠醛质量浓度为0.25 g/L时,对酵母GGSF16利用葡萄糖的影响较小,而当糠醛质量浓度>1.0 g/L时,对葡萄糖的消耗具有明显影响[11]。
2.1.2醛对t50和tend的影响
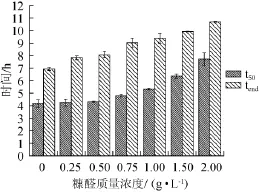
图2 不同糠醛质量浓度条件下t50和tend值Fig.2 t50and tendw ith different furfural concentrations
应用Origin 8.0软件对图1糖代谢曲线的拟合,可以分别计算出葡萄糖消耗一半和完全消耗的时间t50与tend。t50可以判断酒精发酵前期葡萄糖的消耗情况,tend则可以预测酒精发酵的结束时间[7],从而直观、定量的比较出不同浓度糠醛对酒精发酵结束时间的影响,结果见图2。由图2可知,t50和tend均随糠醛浓度的增大而增大。当糠醛质量浓度<0.5 g/L时,t50变化并不显著。表明糠醛在低浓度条件下对酵母GGSF16利用葡萄糖的影响较小,可能由于酵母本身对糠醛具有一定的耐受性[12]。当糠醛质量浓度>1.0 g/L时,t50与tend均随糠醛浓度增大而增大,tend与对照组相比分别增加了35.50%、43.15%和55.07%(见图2)。结果表明,随着糠醛浓度的增加,酒精发酵周期逐渐延长。
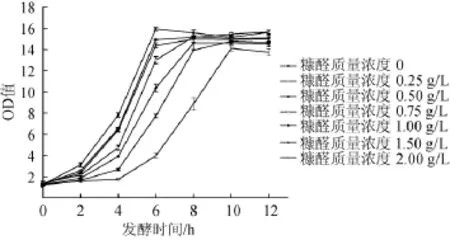
图3 不同糠醛质量浓度条件下酵母GGSF16细胞生长曲线Fig.3 Cellgrow th curve of S.cerevisiae GGSF16 a t different furfural concentrations
2.2醛对细胞生长的影响
测定细胞悬液的OD值能够简单、快速地评估微生物的生长情况[12]。与平板计数法相比更加适用、快速且廉价,因此一些作者已经采用OD值曲线下面积法来评估不同物质对细胞生长的抑制作用[13-16]。OD值AUC能够简单、直观且定量的比较细胞生长的情况[11]。OD值AUC越小则说明抑制成分对微生物生长抑制越明显,反之亦然[14]。由图3可知,随着糠醛浓度的增大,发酵前期细胞的生长速率逐渐降低,细胞的生长出现停滞且最终OD值逐渐减小。糠醛的存在抑制了乙醇脱氢酶的活性,乙醇脱氢酶有助于细胞排除乙醛,从而引起乙醛在细胞内部的积累,乙醛在细胞内部的积累被认为是细胞生长放缓或停滞的原因[17]。而在高浓度糠醛条件下会造成细胞的死亡可能是最终OD值随糠醛浓度的增大而减小的原因[18]。当糠醛质量浓度为2.0 g/L时,0~4 h的OD值增长量为0.49,而对照组在0~4 h的OD值增长量则为6.54。充分说明糠醛影响了细胞的繁殖与再生,且这种影响随着糠醛浓度的增大而增强。实验结果表明,糠醛在高浓度条件下,严重阻碍了细胞的生长。因此,高接种量可能是降低糠醛抑制作用的一种有效途径。由表2可知,不同糠醛浓度条件下的OD值AUC随糠醛浓度的增加而减小,糠醛浓度为0时,OD值AUC最大132.00±1.48。糠醛质量浓度为2 g/L时,OD值AUC最小75.58±0.83。说明糠醛浓度越高对细胞生长的抑制作用越强。糠醛的添加组与对照组的比值同样随糠醛浓度的增加而减小,当糠醛质量浓度为0.25 g/L和1.0 g/L时,比值分别为0.96与0.81,当糠醛质量浓度为0.25 g/L时,对细胞生长的影响较小,而当糠醛质量浓度>1.0 g/L时,细胞生长则明显放缓,表明糠醛阻碍了细胞的繁殖与再生,从而引起细胞生长的停滞[18]。与糠醛对葡萄糖代谢的影响一致,糠醛在低浓度条件下对细胞生长的影响较小;当糠醛质量浓度>1.0 g/L时,则对细胞生长具有明显影响。
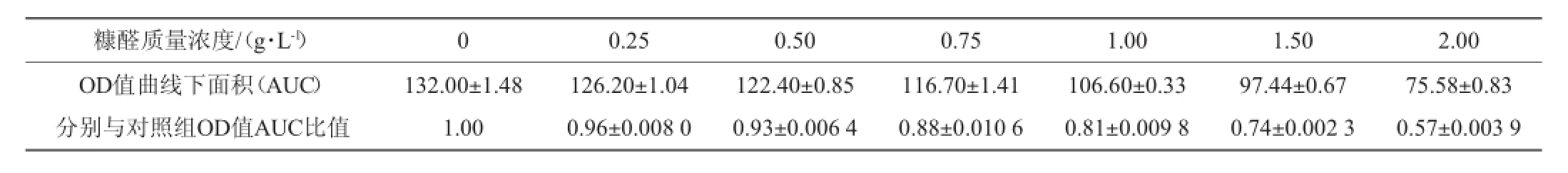
表2 糠醛质量浓度对酵母GGSF16细胞生长曲线下面积的影响Table 2 Effectof different furfural concentration on area under the curve of S.cerevisiae GGSF16 grow th
2.3醛对酒精生成的影响
糠醛对细胞生长的影响远大于对酒精生成的影响[18]。由图4与表3可知,随着糠醛浓度的增加,乙醇的生成速率逐渐降低,但对最终酒精度以及发酵效率影响不大。先前的研究同样表明,在糠醛存在的情况下,细胞的生长受到了明显的抑制作用,然而乙醇的产量仍旧维持在较高的水平[7,19]。但由于糠醛的加入延长了发酵周期,从而使得乙醇产率随着糠醛浓度的增大而逐渐降低(见表3)。当糠醛质量浓度为0时,乙醇产率最高为3.24 g/(L·h)。结果表明,随着糠醛浓度的增大乙醇产率逐渐降低、发酵周期逐渐延长,但对最终酒精度的影响不大。因此,尽可能的降低木质纤维素水解液中的糠醛浓度有利于酒精发酵的过程。
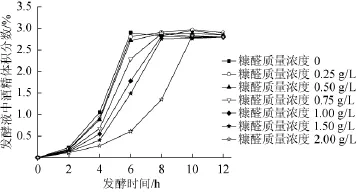
图4 不同糠醛质量浓度条件下酵母GGSF16酒精发酵过程中酒精生成曲线Fig.4 Alcohol production curve during the ferm entation process of S.cerevisiae GGSF16 from glucose at different furfural concentrations
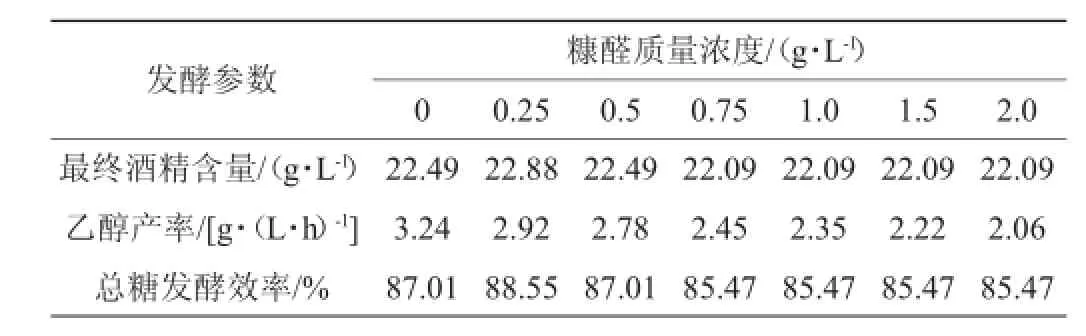
表3 糠醛质量浓度对酵母GGSF16葡萄糖酒精发酵参数的影响Table 3 Effectof different furfural concentrations on alcohol ferm entation param eters of S.cerevisiae GGSF16 from glucose
3 结论
本试验以调节不同浓度糠醛的YEPD发酵培养基替代木质纤维素水解液,通过对葡萄糖代谢曲线的拟合,分别得到了不同糠醛浓度条件下的发酵结束时间;并应用曲线下面积法整体评估了糠醛对发酵过程中几个重要参数的影响,在不同糠醛浓度条件下酵母GGSF16葡萄糖酒精发酵结果表明,糠醛浓度的增加会导致葡萄糖代谢和细胞生长逐渐减慢、乙醇产率逐渐降低、发酵周期逐渐延长,但最终酒精度并没有明显差别。当糠醛质量浓度为0时乙醇产率最高,为3.24 g/(L·h);发酵周期最短,为6.94 h。因此,在酒精发酵的过程中应尽可能的降低木质纤维素水解液中的糠醛含量。
[1]PALMQVIST E,HAHN-HÄGERDAL B.Fermentation of lignocellulosic hydrolysates.II:inhibitors andmechanisms of inhibition[J].Bioresource Technol,2000,74(1):25-33.
[2]DUNLOP A P.Furfural formation and behavior[J].Ind Eng Chem, 1948,40(2):204-209.
[3]BANERJEE N,BHATNAGAR R,VISWANATHAN L.Inhibition of glycolysis by furfural in Saccharomyces cerevisiae[J].Appl M icrobiol Biot,1981,11(4):224-228.
[4]TAHERZADEH M J,GUSTAFSSON L,NIKLASSON C,et al.Inhibition effects of furfural on aerobic batch cultivation of Saccharomyces cerevisiae grow ing on ethanoland/oracetic acid[J].Biosci Bioeng,2000,90(4):374-380.
[5]TAHERZADEH M,GUSTAFSSON L,NIKLASSON C,et al.Conversion of furfural in aerobic and anaerobic batch fermentation ofglucoseby Saccharomyces cerevisiae[J].BiosciBioeng,1999,87(2):169-174.
[6]ILONA SH,FCARL JOHAN,TAHERZADEH M J,et al.Effects of furfural on the respiratorymetabolism of Saccharomyces cerevisiae in glucose-lim ited chemostats[J].App l Environ M icrobiol,2003,69(7): 4076-4086.
[7]JORDIT,AMPARO G,FRANCISCO NOÉA L,etal.Differences in the glucose and fructose consumption profiles in diverse Saccharomyces w ine species and their hybrids during grape juice fermentation[J]. Int J Food M icrobiol,2009,134(3):237-243.
[8]左松,伍时华,张健,等.不同时间添加氮源对酵母GJ2008果糖与葡萄糖利用的影响[J].食品与发酵工业,2014(4):18-22.
[9]LICCIOLIT,CHAMBERSPJ,JIRANEK V.A novelmethodology independent of fermentation rate for assessment of the fructophilic character ofw ineyeaststrains[J].Ind M icrobiol Biotechnol,2011,38(7):833-843.[10]ARROYO-LÉPEZ FN,QUEROL A,BARRIO E.Application of a substrate inhibitionmodel to estimate the effect of fructose concentration on the growth of diverse Saccharomyces cerevisiae strains[J].Ind M icrobiol Biotechnol,2009,36(5):663-669.
[11]路鹏,沈世华,王丽莉,等.糠醛含量对乙醇发酵菌株Saccharomyces k luyveri生长的影响[J].现代化工,2006(S2):223-225+227.
[12]TAHERZADEH M J,NIKLASSON C,LIDÉN G.Conversion of dilute-acid hydrolyzates of spruce and birch to ethanol by fed-batch fermentation[J].Bioresource Technol,1999,69(1):59-66.
[13]MCMEEKIN T A,OLLEY JN,ROSST,etal.PredictiveM icrobiology:theory and application[M].New York:W iley,1993.
[14]ARROYO-LÓPEZ F N,BAUTISTA-GALLEGO J,DURÁN-QUINTANA M C,etal.Modelling the inhibition of sorbic and benzoic acids on a native yeast cocktail from table olives[J].Food M icrobiol,2008,25(4):566-574.
[15]BAUTISTA-GALLEGO J,ARROYO-LÓPEZ F N,DURÁN-QUINTANAM C,etal.Individualeffectsof sodium,potassium,calcium and magnesium chloridesaltson Lactobacilluspentosus and Saccharomyces cerevisiae grow th[J].JFood Protect,2008,71(7):1412-1421.
[16]LAMBERT R JW,PEARSON J.Susceptibility testing:accurate and reproducibleminimum inhibitory concentration(MIC)and non-inhibitory concentration(NIC)values[J].Appl M icrobiol,2000,88(5):784-790.
[17]PALMQVIST E,ALMEIDA JS,HAHN-HÄGERDAL B.Influence of furfuralon anaerobic glycolytic kineticsof Saccharomycescerevisiae in batch culture[J].Biotechnol Bioeng,1999,62(4):447-454.
[18]TIINA M,SANDHOLM M.Antibacterial effect of the glucose oxidase-glucose system on food poisoning organisms[J].Food M icrobiol,1989,8(2):165-174.
[19]JONESRP.Biologicalprinciples for the effectsof ethanol[J].Enzyme M icrob Tech,1989,11(3):130-153.
Effect of furfural on alcohol fermentation from glucose by Saccharomyces cerevisiae GGSF16
YU Zhiqiang,WU Shihua,ZHAO Dongling*,HUANG Cuiji,YIYi
(SchoolofBiologicaland Chemical Engineering,GuangxiUniversity ofScience and Technology,Liuzhou 545006,China)
The effect of different furfural concentration on alcohol fermentation from glucose by Saccharomyces cerevisiae GCSF16 wasexplored,which provided basic information for alcohol fermentation from lignocellulosic hydrolysate.YEPD medium was used instead of lignocelluloses hydrolysate,and the furfuralcontentwasadjusted to seven levels ranging from 0-2 g/L.Based on the areaunder curve,the effectof furfuralon thealcohol fermentation from glucosewasexplored.The results showed thatw ith the increase of furfural concentration,the fermentation period prolonged and the production of alcohol decreased,but no significant difference in alcohol content at the end.When the furfural concentration was 0,the ethanolyield was3.24 g/(L·h),and the fermentation period shortened to 6.94 h.
furfural;glucose;alcohol fermentation;Saccharomycescerevisiae;areaunder the curve
TS261.4
0254-5071(2016)01-0034-04
10.11882/j.issn.0254-5071.2016.01.008
2015-11-03
广西科技攻关项目(桂科攻0782003-2);广西高校科学技术研究项目(YB2014202)
于志强(1990-),男,硕士研究生,研究方向为纤维素酒精发酵。
赵东玲(1965-),男,工程师,博士,研究方向为微生物发酵。
