香元消痔巴布贴的质量标准研究
2016-09-16李文兵王洛临李智勇张诚光范宋玲
李文兵,王洛临,李智勇,张诚光,范宋玲
·炮制制剂·
香元消痔巴布贴的质量标准研究
李文兵,王洛临,李智勇,张诚光,范宋玲
目的:研究香元消痔巴布贴的质量控制标准。方法:采用薄层色谱法对制剂中地榆、黄柏进行定性鉴别,并用高效液相色谱法对制剂中的主药地榆进行含量测定。结果:薄层色谱斑点清晰,阴性对照无干扰;没食子酸在8.34~83.40 ng之间成良好的线性关系,平均回收率为99.14%, RSD为1.06%(n=6)。结论:该法灵敏、简便、准确和重复性好,可作为该制剂的质量控制标准。
香元消痔巴布贴;质量标准;高效液相色谱法;没食子酸
香元消痔膏是我院肛肠科内病外治的中医特色疗法,多年临床用于治疗痔疮的经验处方,具有疗效确切,毒副作用小等特点。课题组在前期临床应用研究基础上,针对其存在制备工艺粗糙、质量控制方法落后等不足,对该制剂的工艺、质量、剂型等进一步研究,以期将其研制成治疗痔疮的新药——香元消痔巴布贴。香元消痔巴布贴由地榆、黄柏、槐花、鱼腥草、元胡、乳香、没药、冰片等八味中药材组成,笔者对香元消痔巴布贴进行质量标准研究时,采用薄层色谱法对制剂中地榆、黄柏进行定性鉴别,并用高效液相色谱法对制剂中的主药地榆进行定量研究。现将研究结果报道如下。
1 仪器与试药
1.1仪器
1100型高效液相色谱仪、DAD检测器、四元梯度泵、G2170AA型数据处理软件系统(美国Agilent公司); Mettler-Toledo XS205DU电子分析天平(瑞士); KQ5200DE型数控超声波清洗器(昆山市超声仪器有限公司); CAMAG Reprostar薄层成像系统(瑞士CAMAG公司); CAMAG Automatic TLC Sampler4全自动薄层点样仪(瑞士);硅胶G薄层板(浙江省路桥四甲生化塑料厂)。
1.2试药
地榆对照药材(批号:121286-200402)、黄柏对照药材(批号:121510-200703) 、没食子酸对照品(批号:110831-200302)均购自中国药品生物制品检定所; 地榆、黄柏等中药均购于广州市药材公司(广东省第二中医院李庆勇副主任中药师鉴定,均为《中华人民共和国药典》2010年版收载的正品),香元消痔巴布贴(20140912、20141015、20141112广东省第二中医院自制); 甲醇为色谱纯,水为重蒸馏水,其余试剂均为分析纯。
2 薄层鉴别
2.1地榆的TLC鉴别[1]
取本品1贴,除去盖衬,剪碎,加10%盐酸溶液100 mL,超声处理30 min,滤过,滤液用盐酸饱和的乙醚萃取2次,每次20 mL,合并乙醚溶液,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液。另取地榆对照药材1 g,同法制成对照药材溶液。按处方比例,称取缺地榆的其它各药材,按制备工艺制成不含地榆的阴性样品,再按供试品溶液制备方法制成缺地榆阴性对照溶液。照薄层色谱法实验,分别吸取上述供试品溶液、对照药材溶液和阴性对照溶液各3 μL,点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以甲苯(用水饱和)-乙酸乙酯-甲酸(6:3:1)[2]为展开剂,展开,取出,晾干,喷以1%三氯化铁乙醇溶液。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,阴性对照无干扰,结果见图1。

图1 1~3.供试品 4.地榆对照药材 5.地榆阴性对照

图2 1~3.供试品 4.黄柏对照药材 5.黄柏阴性对照
2.2黄柏的TLC鉴别[3]
取本品1贴,除去盖衬,剪碎,加氯仿50 mL,水浴加热搅拌,滤过,残渣以少量氯仿分2次洗涤,挥干氯仿液,残渣连同滤纸置锥形瓶中,加甲醇30 mL,超声处理30 min,滤过,滤液蒸干,残渣加甲醇1 mL,作为供试品溶液。另取黄柏对照药材1 g,同法制成对照药材溶液。按处方比例,称取缺黄柏的其它各药材,按制备工艺制成不含黄柏的阴性样品,再按供试品溶液制备方法制成缺黄柏阴性对照溶液。照薄层色谱法[2010年版《中华人民共和国药典》(一部)附录VIB]试验,吸取上述供试品溶液、对照药材溶液和阴性对照溶液各3 μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(7:1:2)为展开剂,展开,取出晾干,置紫外灯下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,结果见图2。
3 没食子酸的含量测定
3.1色谱条件
色谱柱:Kromasil C18色谱柱(4.6 mm×250 mm,5 μm);流动相:流动相为甲醇-0.05%磷酸缓冲液(6:94);流速为1 mL·min-1;检测波长为272 nm;柱温25 ℃。
3.2对照品溶液的制备
精密称取没食子酸对照品置量瓶中,加甲醇制成每1 mL含没食子酸16.68 μg的溶液,作为对照品溶液。
3.3供试品溶液的制备
取本品半贴,除去盖衬,剪碎,加10%盐酸溶液60 mL,超声处理30 min,滤过,滤液用盐酸饱和的乙醚萃取2次,每次10 mL,合并乙醚溶液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。
3.4阴性对照溶液的制备
将处方中除去地榆,按制剂工艺制备供试品阴性对照品,按“3.3”项下方法制得阴性对照溶液。
3.5线性关系考察
精密量取没食子酸对照品储备液(16.68 μg·mL-1)各0.5 mL、1 mL、2 mL、3 mL、4 mL、5 mL,分别置5 mL容量瓶中,加甲醇稀释至刻度,摇匀,制成每1 mL含没食子酸1.668 μg、3.336 μg、6.672 μg、10.008 μg、13.344 μg、16.680 μg的对照品溶液。精密吸取上述对照品溶液各5 μL注入液相色谱仪,按上述色谱条件测定峰面积,以峰面积对数为纵坐标,进样量(μg)为横坐标进行线性回归,得回归方程为Y=10.2098X-0.0104(r=0.9998),结果表明,没食子酸在进样量为8.34~83.40 ng范围内线性关系良好。
3.6精密度试验
精密吸取上述对照品溶液5 μL,重复进样6次,按“3.1”项下色谱条件测定。结果,没食子酸峰面积的RSD为0.38%,表明仪器精密度良好。
3.7稳定性试验
取同一供试品溶液(批号: 20140912),分别于0 h、3 h、6 h 、12 h、18 h 、24 h,进样5 μL,按“3.1”项下色谱条件测定。结果,没食子酸峰面积的RSD为0.32%,表明供试品溶液在24 h内稳定性良好。
3.8重复性试验
按拟定的含量测定方法,取同一批样品(批号:20141015)6份,分别按“3.3”项下方法制备供试品溶液,按“3.1”项下色谱条件测定峰面积并计算含量。结果,没食子酸平均含量的RSD分别为0.88%,表明该方法重现性良好。
3.9回收率试验
取已知含量的样品(批号: 20141112)6份,分别精密加入一定量的没食子酸对照品,按“3.3”项下方法制备样品溶液,按“3.1”项下色谱条件测定,计算回收率,结果见表1。
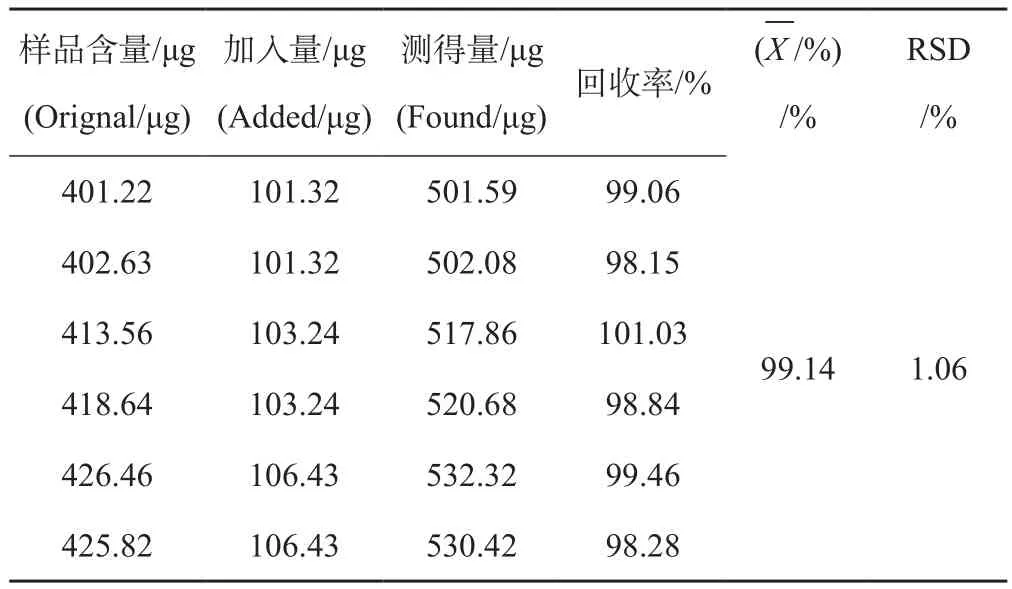
表1 没食子酸加样回收率试验结果(n=6)
3.10样品含量测定
取3批样品,分别按“3.3”项下方法制备样品溶液,按“3.1”项下色谱条件测定,进样量为5 μL,测定峰面积,计算样品含量。结果见表2。

表2 样品中含量测定结果(n=3)
4 讨论
在薄层定性研究时,鉴别黄柏曾以苯-乙酸乙酯-甲醇-异丙醇-浓氨试液(12:6:5:3:1)为展开剂[4],结果分离效果欠佳,色谱斑点不清晰,经过不断摸索试验,改用正丁醇-冰醋酸-水(7:1:2)为展开剂,结果分离效果较好,色谱斑点清晰,可作为黄柏的TLC鉴别方法。
在研究没食子酸的含量测定过程中,笔者进行流动相的选择时,曾以乙腈-0.01 mol/L磷酸溶液(5:100)[5]作为流动相进行试验,处方中的其他成分与没食子酸分离效果欠佳,采用甲醇-0.05%磷酸缓冲液为流动相,分离效果较好,然后经过不断调整两者的比例,最后确定甲醇-0.05%磷酸缓冲液(6:94),使没食子酸与其他成分完全分离,达到较佳的效果。
综上所述,本文所建标准可用于香元消痔巴布贴的质量控制。
[1] 陈淑映,黄健,庄学潮,等. 新型热熔压敏胶制备的伤科贴膏的薄层鉴别[J]. 云南中医中药杂志, 2013,34(2):44-46.
[2] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010:231.
[3] 乔 莉,焦正花,张小华,等. 铁箍膏巴布剂质量标准研究[J]. 中国中医药信息杂志, 2012,19(5):56-58.
[4] 孔繁晟,杨正奇,严春艳,等. 复方金黄痔疮软膏的薄层鉴别[J].中国实用医药,2009,4(33):18-19.
[5] 孙立立,江波,袁振海, 等. HPLC测定地榆饮片中没食子酸的含量[J].中成药,2006,28(8):1144-1147.
(责任编辑:傅舒)
Studies on quality control standard of Xiangyuan Xiaozhi cataplasm/
LI Wen-bing, WANG Luo-lin, LI Zhi-yong, ZHANG Cheng-guang ,FAN Song-lin//(GuangDong Second Traditional Chinese Medicine Hospital, Guangzhou 510095, Guangdong)
Objective: To study quality control standard of Xiangyuan Xiaozhi cataplasm. Method: Diyu and Huangbo in preparation were identified by TLC. The content of Diyu, the main active medicine in cataplasm was determined by HPLC. Result: The TLC spots were clear and negative control showed no interference. Linearity was found in the range of 8.34~83.40 ng for gallic acid with average recovery of 99.14% (RSD=1.06%, n=6). Conclusion: The method is sensitive, simple with good precise and reproducible, and can be used for the quality control of the cataplasm.
Xiangyuan Xiaozhi cataplasm; quality control standard; HPLC; gallic acid
R 284.1
A
1674-926X(2016)03-012-03
广东省中医药局立项资助科研课题(编号:20131117)
广东省第二中医院,广东 广州 510095
李文兵(1972-),男,硕士,主要研究方向:医院药学Tel:13660305488 Email:liwenbing312@163.com
2015-06-10
