酒西五味子与醋西五味子质量标准研究
2016-09-16肖芳黄勤挽谭茂兰范润勇
肖芳,黄勤挽,谭茂兰,范润勇
·炮制制剂·
酒西五味子与醋西五味子质量标准研究
肖芳,黄勤挽,谭茂兰,范润勇
目的:建立酒西五味子与醋西五味子的质量标准。方法:以五味子甲素为对照品进行酒西五味子与醋西五味子的薄层鉴别; 采用HPLC测定酒西五味子与醋五味子中五味子甲素的含量。分别对酒西五味子与醋西五味子水分、总灰分、酸不溶性灰分及水浸出物进行检测。结果:酒西五味子与醋西五味子薄层色谱分离度好,斑点清晰。根据样品测定结果,建议酒西五味子与醋西五味子水分分别不得超过13.0%、14.0%,总灰分均不得超过7.0%,酸不溶性灰分均不得超过2.0%,水浸出物含量均不得少于30.0%。五味子甲素进样量在0.3984~3.984 µg(r=1)其峰面积积分值与进样量有良好的线性关系,平均回收率为99.22%,RSD为1.08%,酒西五味子与醋西五味子中五味子甲素含量均不得低于0.2%。结论:所建方法操作简单,准确可靠,可用于评价酒西五味子与醋西五味子的质量。
酒西五味子;醋西五味子;质量标准;薄层鉴别;含量测定;五味子甲素
西五味子[1]为木兰科五味子属植物翼梗五味子Schisandrahenryi Clarke、红花五味子Schisandrarubriflora Rehd.et Wils.或柔毛五味子Schisandrapubescens Hemsl.et Wils.的干燥成熟果实。其具有收敛固涩,益气生津,补肾宁心等功效。酒西五味子多用于肾虚滑精,醋西五味子多用于咳嗽,遗精,泄泻。五味子甲素为西五味子的主要有效成分之一,具有一定的保肝作用[1]。目前酒西五味子与醋西五味子在《四川省中药饮片炮制规范》2002年版有收载,但尚未见其质量标准研究的相关文献报道。本实验对西五味子的薄层鉴别、检查(水分、总灰分、酸不溶性灰分、水浸出物) 及五味子甲素含量测定进行研究,旨在系统评价西五味子的两种炮制品质量,确保其临床用药安全、有效。
1 材料
1.1仪器
1200型高效液相色谱仪( 美国Agilent);BSA224S分析天平(德国Sartorius系列);BP211D十万分之一电子分析天平(德国Sartorius系列);SRIX-4-13箱式电阻炉(北京中兴仪器伟业有限公司);SHZDⅢ型循环水式多用真空泵 (巩义市予华仪器有限责任公司);UPH-I-10T优普超纯水器(成都超纯科技有限公司);RJ-TGL-16C型高速离心机(无锡瑞江分析仪器有限公司);ZF-90多功能暗箱式紫外透射仪(上海宝山顾村电光仪器厂)。
1.2试药与样品
五味子甲素对照品(供含量测定用),由中国食品药品检定研究院提供(批号:110764-201312);色谱级甲醇、水为超纯水;其他试剂均为分析纯。在成都荷花池中药材专业市场收集3个产地的3批西五味子药材,分别委托四川新荷花中药饮片股份有限公司、四川省中药饮片有限责任公司生产13批酒西五味子、醋西五味子样品,详见表1。
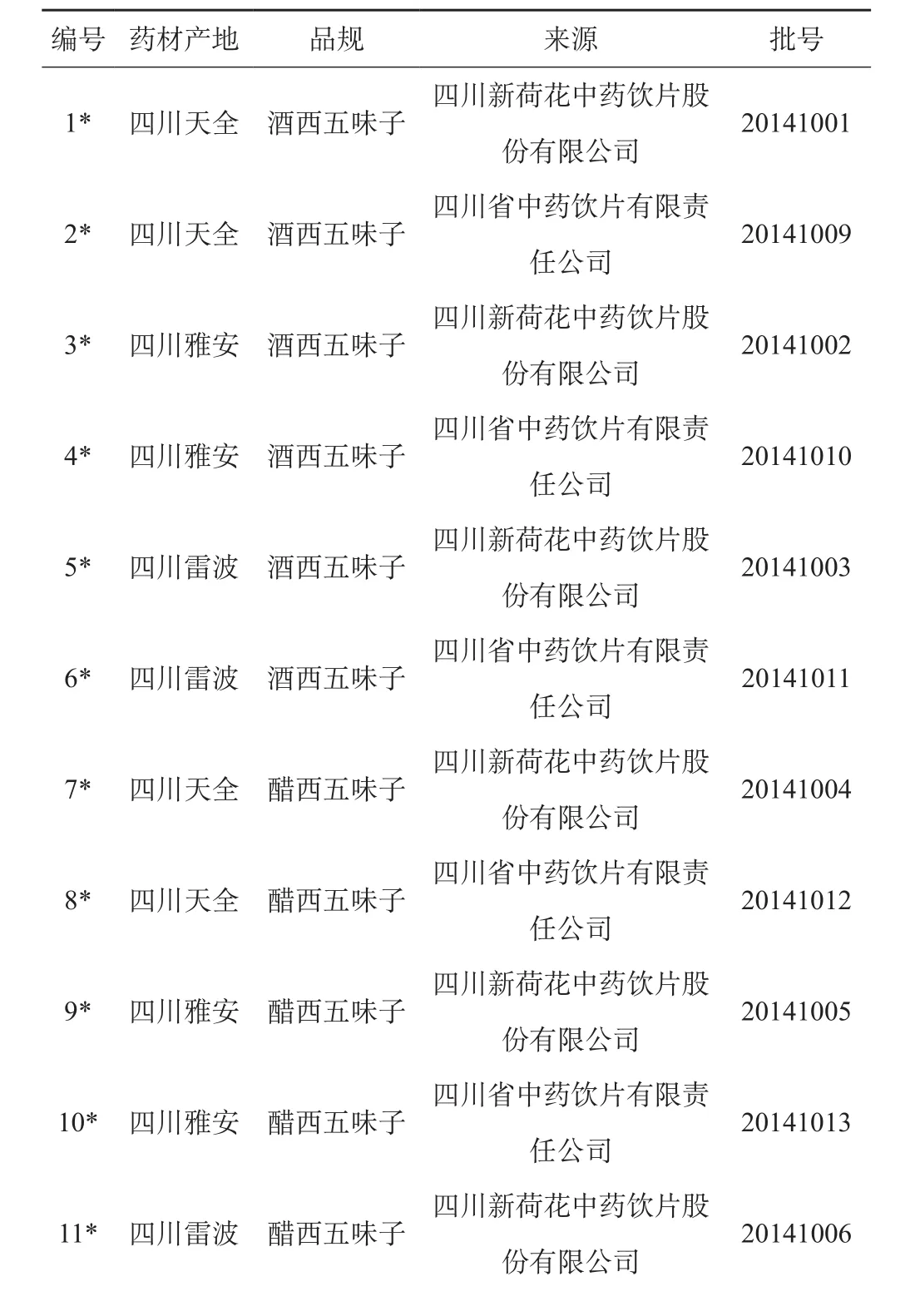
表1 酒西五味子、醋西五味子样品来源一览表

*注:样品1~样品12购买于成都荷花池中药材专业市场,委托四川新荷花中药饮片股份有限公司、四川省中药饮片有限责任公司进行酒制、醋制加工。
以上样品均经过四川省食品药品检验检测院黎跃成主任药师鉴定,为木兰科五味子属植物翼梗五味子SchisandrahenryiCLarke、红花五味子SchisandrarubrifLora Rehd.et WiLs.或柔毛五味子Schisandrapubescens HemsL.et Wils.的干燥成熟果实。
2 方法与结果
2.1显微鉴别
本品粉末棕色。石细胞单个或成群,表面观多角形、卵圆形、长椭圆形或不规则形。果皮表皮细胞表面观类多角形,垂周壁略成连珠状增厚,表面有角质纹理。
2.2薄层鉴别
2.2.1供试品溶液和对照品溶液的制备 分别取醋西五味子与酒西五味子品粉末1 g,加三氯甲烷20 mL,超声处理30 min,滤过,滤液蒸干,残渣加三氯甲烷1 mL使溶解,作为供试品溶液。另取五味子甲素对照品,加三氯甲烷制成每1 mL含1 mg的溶液,作为对照品溶液。
2.2.2TLC 试验 照薄层色谱法(《中国药典》2010年版一部附录ⅥB)试验,吸取上述两种溶液各2 µl,分别点于同一硅胶GF254薄层板上,以石油醚(30~60℃)-甲酸乙酯-甲酸(15:5:1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。本方法分离效果好,斑点清晰,重复性好。见图1。
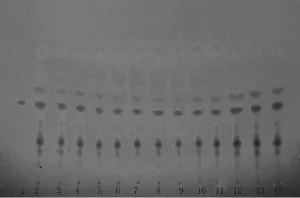
图1 酒西五味子、醋西五味子TLC图
2.3水分
按《中国药典》2010年版一部附录ⅨH 水分测定法第一法测定水分。测得6批酒西五味子与7批醋西五味子水分平均值分别为10.7%和11.7%。故暂定酒西五味子水分检查限度不得超过13.0%,醋西五味子水分检查限度不得超过14.0%。
2.4总灰分
按《中国药典》2010年版一部附录ⅨK 灰分测定法测定灰分。测得6批酒西五味子与7批醋西五味子灰分平均值分别为5.8%和5.7%。故暂定酒西五味子灰分检查限度不得超过7.0%,醋西五味子灰分检查限度不得超过7.0%。
2.5酸不溶性灰分
按《中国药典》2010年版一部附录ⅨK灰分测定法测定酸不溶性灰分。测得6批酒西五味子与7批醋西五味子酸不溶性灰分平均值分别为1.6%和1.7%。故暂定酒西五味子酸不溶性灰分检查限度不得超过2.0%,醋西五味子酸不溶性灰分检查限度不得超过2.0%。
2.6浸出物
按《中国药典》2010年版一部附录X A浸出物测定法项下热浸法测定浸出物含量,以水为溶剂。测得6批酒西五味子与7批醋西五味子水浸出物含量平均值分别为39.6%和41.3%。故暂定酒西五味子水浸出物含量不得少于30.0%,醋西五味子水浸出物含量不得少于30.0%。
2.7含量测定
2.7.1色谱条件 色谱柱:HypersiL C18(10 µm,250×4.6 mm),以甲醇-水(77:23)为流动相,流速:1 mL·min-1,检测波长为254 nm,柱温:25℃,进样量10 µl。结果见图2。
2.7.2对照品溶液的制备及线性关系考察 精密称取五味子甲素对照品适量,加甲醇制成每1 mL含0.3984 mg的溶液,即得五味子甲素对照品溶液。精密吸取五味子甲素对照品溶液(0.3984 g·L-1)1,2,4,6,8,10 µl,在上述色谱条件下,依次进样,以五味子甲素浓度(X)为横坐标,色谱峰面积积分值(Y)为纵坐标,绘制标准曲线,并计算线性回归方程为Y=1776.2X-16.951,r=1,结果表明五味子甲素在0.3984~3.984 µg范围内,其峰面积与进样量有良好的线性关系。
2.7.3供试品溶液的制备 分别取酒西五味子与醋西五味子样品粉末(过三号筛)约1.0 g,精密称定,精密加入甲醇25 mL,称定重量,超声提取30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
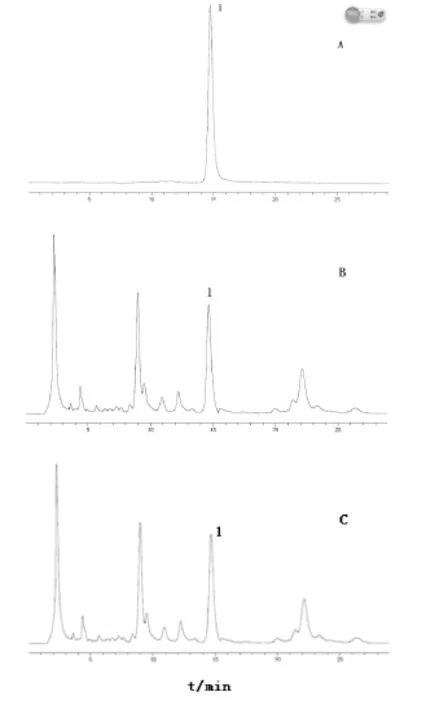
图2 酒西五味子和醋西五味子中五味子甲素HPLC图
2.7.4精密度试验 取0.3984 g·L-1的五味子甲素对照品溶液连续进6次,测定峰面积,结果峰面积值的RSD为0.24%。结果表明仪器的精密度良好。
2.7.5重复性试验 取6份同一批次样品(批号:20141001)各约1.0 g,精密称定,按“2.5.3”项下方法制备供试品溶液,结果测得五味子甲素含量的RSD为2.7%。结果表明方法的重复性良好。
2.7.6加样回收率试验 称取已知含量的样品(批号:20141001)约0.5 g,精密称定,共6份。分别加入五味子甲素对照品溶液(0.3984g·L-1)2 mL,依次测定,计算含量,并计算回收率,五味子甲素平均回收率为99.22%,RSD为1.08%。结果表明该方法回收率良好,符合HPLC 含量测定要求,见表2。

表2 加样回收率试验
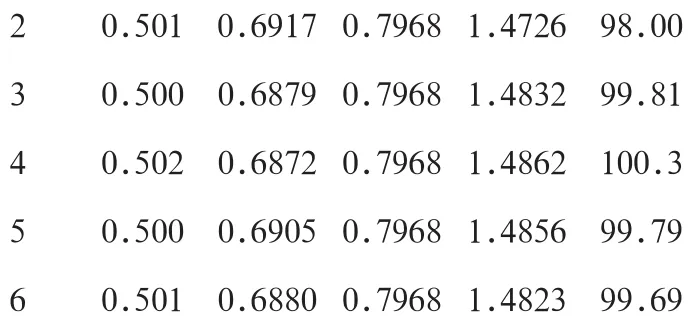
20·5010·6917 0·7968 1·472698·00 30·5000·6879 0·7968 1·483299·81 40·5020·6872 0·7968 1·4862100·3 50·5000·6905 0·7968 1·485699·79 60·5010·6880 0·7968 1·482399·69
2.7.7稳定性试验 取酒西五味子(批号20141001)供试品溶液,分别在0,2,4,6,8,12,24 h ,进样10 µl测定峰面积,计算得RSD为1.2%。结果表明供试品溶液在24 h内稳定性良好。
2.7.8含量测定 分别取各酒西五味子与醋西五味子样品粉末1.0 g,按“2.5.3”项下方法制备供试品溶液,按“2.5.1”项下色谱条件测定并计算百分含量,五味子甲素含量测定结果见表3、表4。酒西五味子、醋西五味子中五味子甲素平均含量( 按干燥品计算) 分别为0.22%、0.21%。根据测定结果,建议规定酒西五味子中五味子甲素含量不得低于0.2%,醋西五味子中五味子甲素含量不得低于0.2%。
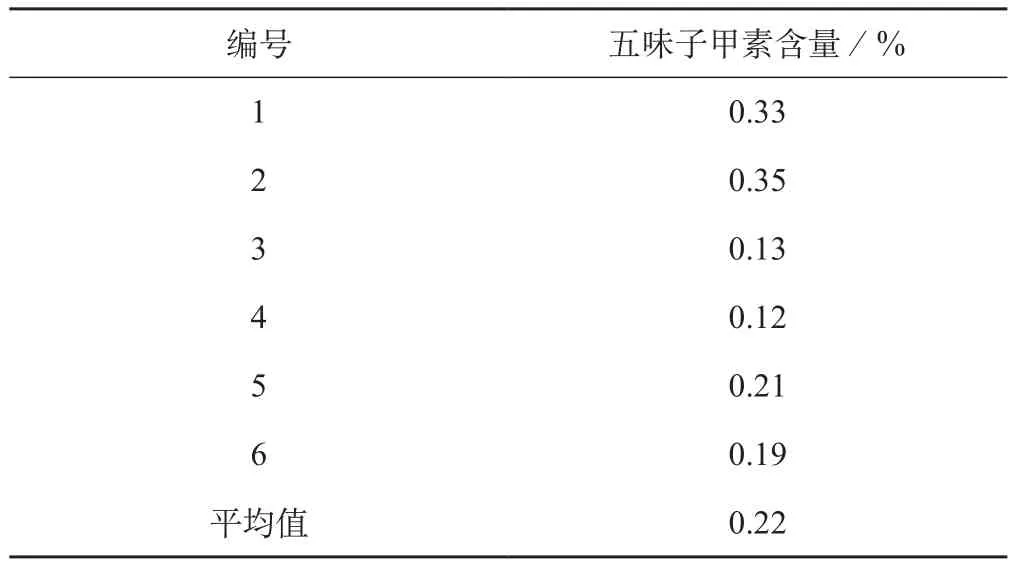
表3 酒西五味子中五味子甲素含量(n=3)
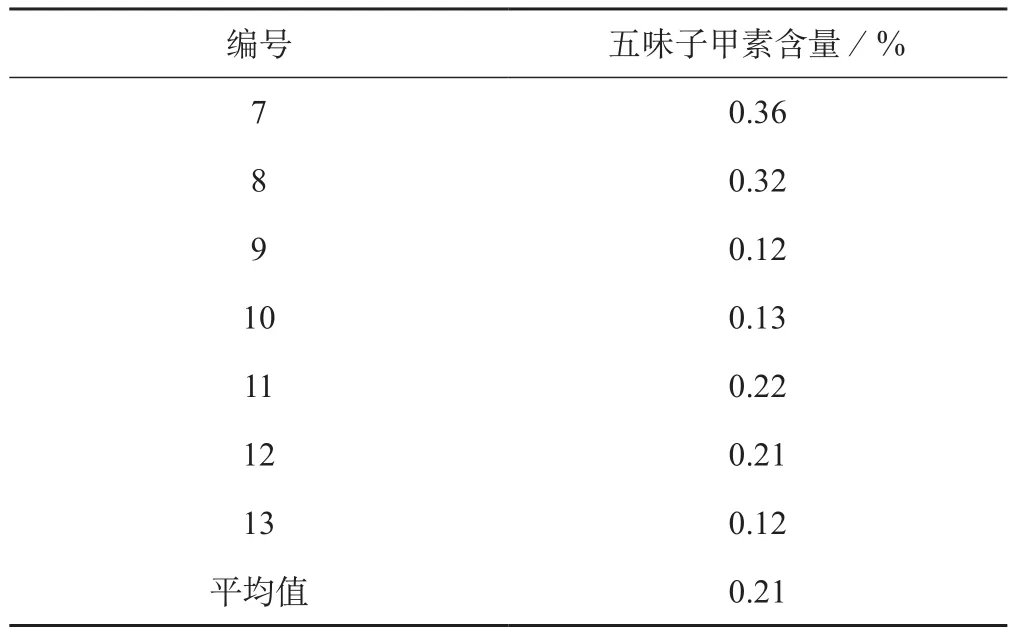
表4 醋西五味子中五味子甲素含量(n=3)
3 讨论
3.1本文参考相关文献报道[4~6],对西五味子中五味子甲素的提取工艺及含量测定所用流动相的选择进行筛选与优化。实验表明,以甲醇作为溶剂超声提取30 min效果最佳。与以无水乙醇或甲醇作为溶剂水浴回流提取方法相比,该方法更加简单易行,可操作性强,且含量测定结果表明,三种提取方法所得五味子甲素含量并无明显差异,所以选择该方法作为最佳提取方法。在流动相的选择上,本文对甲醇-水(85:15)、甲醇-水(90:10)、甲醇-水(77:23)三种流动相系统进行筛选,实验表明,在选用甲醇-水(85:15)与甲醇-水(90:10)作为流动相时,部分样品在与对照品相同保留时间处具有相应的色谱峰,但是部分样品却没有,说明应用此两种流动相系统建立的方法适应性不好,而甲醇-水(77:23)效果明显优于上述两种系统,其可重复性良好,结果准确,所以选择甲醇-水(77:23)作为西五味子中五味子甲素含量测定所用最佳流动相系统。
3.2实验所用酒西五味子与醋西五味子均按《四川省中药材标准》2002年版炮制项下方法获得,其炮制工艺大致为:取净西五味子,分别用黄酒或醋拌匀,蒸至透心,干燥。每100 kg西五味子,用黄酒或醋10 kg。实验还对西五味子药材生品与炮制品中五味子甲素含量进行比较,结果表明同一产地的西五味子药材分别经酒炙、醋炙加工后,其两种炮制品中五味子甲素含量与生品相较并无明显差异,说明酒炙、醋炙对西五味子中五味子甲素含量并无太大影响。而产自四川天全的西五味子药材相较其它产地五味子甲素的含量差异较大,产地不同、基原不同皆是影响其含量的因素,但由于单从外观的性状鉴别难于将西五味子的3个基原区分开,为区分西五味子药材优劣,保证其临床用药安全有效,不同基原的西五味子中有效成分含量测定值得进一步探究。
[1] 四川省药品监督管理局.四川省中药饮片炮制规范[M].成都:四川人民出版社,2002:350-351.
[2] 马永明,耿亚.浅谈南五味子[J].中国中医药现代远程教育,2013,11(9):103-104.
[3] 潘新,刘霞,蔡敏之.HPLC法测定五味子中五味子甲素含量[J].广东化工,2007,6(34):123-125.
[4] 倪琳,杨锡. HPLC法同时测定生脉饮中五味子醇甲、五味子甲素和五味子乙素[J].中成药,2012,34(5):872-875.
[5] 梁晓艳,梁旭霞,朱杰民. HPLC测定生脉饮中五味子甲素和五味子乙素的含量[J].广西中医学院学报,2010,13(3):48-49.
[6] 谭晓虹,王志宝,赵倩. HPLC测定南、北五味子中五味子甲素和五味子乙素的含量[J].中成药,2010,32(1):155-157.
(责任编辑:胡慧玲)
Study on quality standard for prepared Wuweizi with wine and prepared Wuweizi with vinegar/
XIAO Fang, HUANG Qin-wan, TAN Mao-lan, FAN Run-yong//(School of Pharmacy, Chengdu University of Traditional Chinese Medicine; Key Laboratory of Standardization for Chinese Herbal Medicine, Ministry of Education; National Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources, Chengdu 611137, Sichuan)
Objective: To establish the quality standard for prepared Wuweizi with wine and prepared Wuweizi with vinegar. Method: TLC was used to detect deoxyschizandrinin prepared Wuweizi with wine and prepared Wuweizi with vinegar. HPLC was adopted to determine deoxyschizandrin content. Moisture, ash, acid insoluble ash and aqueous extract were also measured. Result: TLC identification had a good resolution with clear spots. According to the measurement results, moisture in prepared Wuweizi with wine and prepared Wuweizi with vinegar should be less than 13.0% and 14.0%, respectively. The content of total ash should be less than 7.0 % and the content of acid insoluble ash should be less than 2.0%. The content of aqueous extract should be above 30.0%. Linear relation of deoxyschizandrin peak area integral to injection volume was good in the range of 0.3984~3.984 µg (r=1). The average recoveries were 99.22% with RSD of 1.08%. The contents of deoxyschizandrin were above 0.2%. Conclusion: The established standard is acceptable for quality evaluation of prepared Wuweizi with wine and prepared Wuweizi with vinegar.
Prepared Wuweizi with wine; Prepared Wuweizi with vinegar; quality standard; TLC identification; content determination; deoxyschizandrin
R
A
1674-926X(2016)03-005-04
四川省科技厅支撑计划(编号:2012FZ0017);成都市科技局课题(编号:12DXYB310JH);四川省教育厅青年基金(编号:10ZC051)
成都中医药大学药学院 中药材标准化教育部重点实验室 四川省中药资源系统研究与开发利用重点实验室省部共建国家重点实验室培育基地,四川 成都 611137
肖芳(1991-),女,在读硕士,主要从事中药炮制学研究Tel:18482177688 Email:329065965@qq.com
黄勤挽(1979-),男,博士,副教授,主要从事中药炮制学研究Tel:13982199974 Email:36190587@qq.com
2015-06-30
