槲皮素对糖尿病大鼠晶状体上皮细胞凋亡的影响*
2016-09-15刘鹃康刚劲康海军白梦天蒋燕韩茜
刘鹃,康刚劲,康海军,白梦天,蒋燕,韩茜
(西南医科大学附属医院眼科,四川泸州646000)
槲皮素对糖尿病大鼠晶状体上皮细胞凋亡的影响*
刘鹃,康刚劲,康海军,白梦天,蒋燕,韩茜
(西南医科大学附属医院眼科,四川泸州646000)
目的:探讨槲皮素对糖尿病大鼠晶状体上皮细胞(lens epithelial cells,LECs)凋亡的影响及机制。方法:将60只SD大鼠随机分为对照组、糖尿病组、槲皮素组,每组20只。糖尿病组、槲皮素组采用链脲佐菌素(streptozotocin,STZ)诱导制作糖尿病性白内障模型,糖尿病组和对照组予以常规饲料喂养,槲皮素组则予以50mg/kg/d槲皮素灌胃治疗。STE注射后4周、8周、12周检测大鼠血糖,观察大鼠晶状体混浊程度,HE染色观察大鼠晶状体上皮细胞,免疫组织化学检测大鼠LECs Bcl-2和Bax的表达,流式细胞术检测大鼠LECs凋亡率。结果:12周时糖尿病组、槲皮素组大鼠体重明显低于对照组(P<0.05),糖尿病组大鼠体重与槲皮素组之间无明显差异(P>0.05)。STZ注射后4周时、8周时、12周时对照组与糖尿病组、槲皮素组血糖比较差异具有统计学意义(P<0.05),糖尿病组与槲皮素组血糖比较无明显差异(P>0.05)。STZ注射后4周时、8周、12周时对照组、糖尿病组、槲皮素组大鼠晶状体混浊程度两两比较,差异均有统计学意义(P<0.05)。HE结果显示糖尿病组、槲皮素组均可见LECs形态不规则,胞质疏松,染色淡,后囊区晶状体纤维细胞见大量未被降解的细胞器。与对照组比较,糖尿病组和槲皮素组大鼠LECs Bcl-2蛋白表达下调,Bax蛋白表达增加,两组间比较差异具有统计学意义(P<0.05);与槲皮素组比较,糖尿病组大鼠LECs Bcl-2蛋白表达下调,Bax蛋白表达增加,两组间比较差异具有统计学意义(P<0.05)。STZ注射后4周、8周、12周时,各组之间LECs凋亡率两两比较,差异均有统计学意义(P<0.05)。结论:槲皮素对糖尿病大鼠LECs凋亡有一定的抑制作用,可延缓糖尿病性白内障的发生发展。
槲皮素;细胞凋亡;晶状体上皮细胞;糖尿病性白内障;Bcl-2;Bax
1 材料与方法
1.1 材料与分组
SD大鼠购自西南医科大学实验动物中心,散瞳后经数码裂隙灯显微镜检查晶状体透明、完整,体重150~180 g。60只SD大鼠随机抽取20只为正常对照组,剩余大鼠成功造糖尿病模型后随机分为糖尿病模型组和槲皮素干预组,每组20只。槲皮素购自华越洋生物公司;链脲佐菌素(streptozotocin,STZ)和戊巴比妥钠购自美国Sigma公司;兔抗大鼠Bcl-2和Bax多克隆抗体购自美国Bioworld进口分装;Annexin V-FITC/PI双染细胞凋亡检测试剂盒购自美国BD公司;其余试剂购自北京中杉金桥生物技术有限公司。
1.2 方法
1.2.1 糖尿病大鼠模型的建立与槲皮素干预
一次性腹腔注射STZ 65 mg/kg诱导糖尿病大鼠模型,72 h后尾静脉取血,空腹血糖≥16.7 mmol/L时为糖尿病造模成功,纳入实验组。对照组予以常规饲料喂养。糖尿病组和槲皮素组,STZ注射后第4 d开始槲皮素组大鼠予以槲皮素50 mg/kg/d灌胃。每周称重一次,调整槲皮素用量。分别于STE注射后4周、8周各组随机断髓处死5只大鼠,共30只,12周末处死剩余30只。
1.2.2 观察大鼠晶状体混浊情况
使用复方托吡卡胺滴眼液散瞳后,予以大鼠腹腔注射1%戊巴比妥钠麻醉,分别于4周、8周、12周时用数码裂隙灯显微镜对晶状体混浊情况进行观察、记录、拍照,分级标准参照Bahmani F等对晶状体混浊分级,共分为5级[2]:Ⅰ级:晶状体无混浊;Ⅱ级:晶状体轻度混浊,周边部出现空泡改变;Ⅲ级:晶状体中度混浊,周边部空泡向中心区域扩展,核出现雾状混浊;Ⅳ级:晶状体高度混浊,周边空泡扩展到核区,核雾状混浊加重;Ⅴ级:晶状体全混浊,发展为完全白内障。
“昆北”去声字“媚”唱调(《铁冠图·刺虎》【滚绣球】“俺佯娇假媚”,787)。该单字唱调的过腔是。其中即第一节级音性过腔,即第二节级音性过腔,为第三节级音性过腔。这个过腔即为“主调+级音+级音”两种不同音乐材料组合而成的多节型过腔。
1.2.3 HE染色
将石蜡切片常规脱蜡、水化;苏木素染色,蒸馏水冲洗至水变清;1%盐酸乙醇分化30 s,褪色至红色,蒸馏水过洗至恢复蓝色;0.5%伊红液染色2 min,蒸馏水冲洗;梯度酒精脱水、二甲苯透明;中性树胶、盖玻片封片。光学显微镜下观察、摄片。
1.2.4 免疫组织化学染色检测大鼠LECs Bcl-2、Bax表达情况
切片脱蜡后放在3%H2O2室温避光孵育10 min,PBS冲洗;切片置于染色架上,再放入0.01 mmol/L枸橼酸盐缓冲液容器中,加热至沸腾,15 min后取出容器,室温冷却30 min,PBS冲洗;滴加1滴5%BSA封闭游离结合位点,室温孵育30 min后弃去血清;滴加适当比例稀释的一抗(1∶100),在4℃冰箱中过夜,PBS冲洗;滴加适当比例稀释的生物素标记的二抗(1∶10),37℃水浴箱孵育30 min,PBS冲洗;滴加适当比例稀释的HRP标记的链霉亲和素,37℃孵育30 min,PBS冲洗;加新鲜配制的DAB显色,显微镜观察控制染色时间,见黄褐色斑时放入双蒸水中终止显色;自来水冲洗,苏木精复染,盐酸酒精分化,自来水冲洗;梯度酒精脱水,二甲苯透明;中性树胶、盖玻片封片;放入60℃烘箱中烤干,光学显微镜下观察摄片。
1.2.5 流式细胞术检测细胞凋亡
将摘除的晶状体用平衡液冲洗干净后,在显微镜下从赤道部环形撕取晶状体前囊膜,消化后用300目滤网制备成单细胞悬液;转移细胞至离心管中,1 000 r/min离心5 min,弃去培养液,PBS洗涤2次;加入预冷的结合缓冲液,调整细胞密度为1× 106/mL;按照Annexin V-FITC凋亡检测试剂盒说明书加入Annexin V-FITC液5 uL和PI 10 uL,轻轻充分混匀,室温(20°C~25°C)避光染色15 min;PBS洗涤多余染料后,在1 h内进行流式细胞仪检测。
1.3 统计学分析
采用SPSS 17.0软件对数据进行统计分析,计量资料采用x±s表示。多个样本均数之间比较采用单因素方差分析(ONE-WAY AONVA),两两比较采用LSD检验。等级资料等级秩和检验。P<0.05为差异具有统计学意义。
2 结果
2.1 大鼠晶状体混浊程度
各组大鼠晶状体混浊情况,见表1。在整个实验过程中,对照组始终保持晶状体透明、完整。STZ注射后4周糖尿病组、槲皮素组大鼠均开始出现不同程度的晶状体混浊,且晶状体混浊程度随实验进行逐渐加重。8周时,糖尿病组大鼠晶状体混浊程度较槲皮素组重。12周时,糖尿病组大鼠全部出现不同程度的晶状体混浊,槲皮素组大鼠晶状体混浊发展速度及混浊程度均较糖尿病组轻,实验结束仍未见1只晶状体发生Ⅴ级改变。4周、8周、12周时三组间晶状体混浊情况两两比较差异均有统计学意义(P<0.05)。
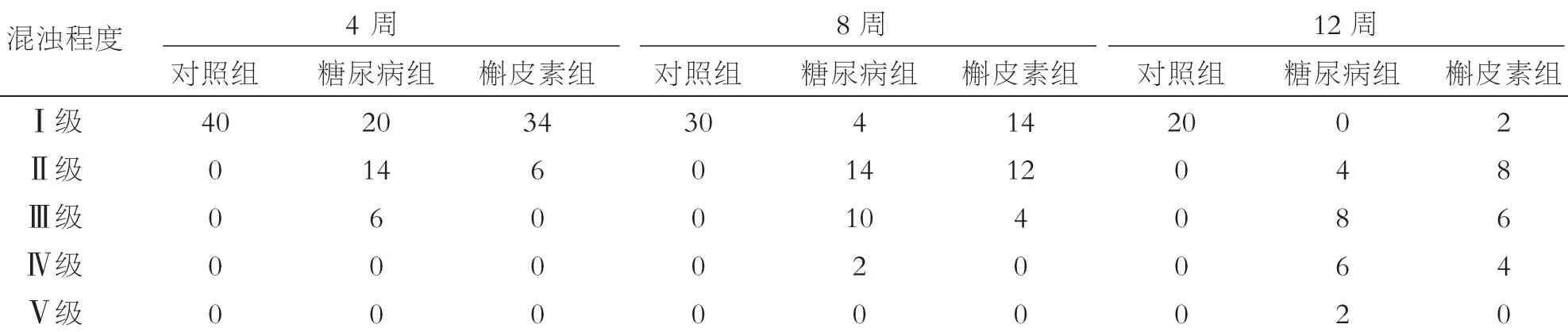
表1 在各时间点各组大鼠晶状体混浊程度(单位:只)
2.2 大鼠晶状体HE染色
对照组LECs形态规则,分布均匀,相邻细胞及与晶状体囊膜紧密结合,细胞核呈椭圆形,染色质均匀无凝缩,晶状体纤维细胞未见异常。而在糖尿病组、槲皮素组均可见LECs形态不规则,多呈扁平状或柱状,胞质疏松,染色淡,可见空泡,细胞核缩小,核内染色质不均匀、浓缩,后囊区晶状体纤维细胞见大量未被降解的细胞器,见图1。

图1 各组晶状体HE染色(×200)
2.3 大鼠晶状体上皮细胞Bcl-2、Bax表达情况
各组大鼠LECs Bcl-2、Bax表达情况。光学显微镜下观察阳性表达为细胞质中见黄色或棕黄色颗粒,否则为阴性。阳性细胞率=5个视野内阳性细胞总数/5个视野内细胞总数×100%,每张切片随机选择5个视野进行观察及记录阳性细胞率。规定阳性表达率:0%为阴性(-);1%~25%为弱阳性(+);26%~50%为阳性(++);>50%为强阳性(+++)。正常大鼠LECs均表达少量的Bcl-2、Bax,胞浆内均可见少量棕黄色颗粒。STZ注射后4周、8周、12周时槲皮素组Bcl-2蛋白的阳性表达较糖尿病组增强(P<0.05),但较对照组下降(P<0.05),同一时间点槲皮素组Bax蛋白的表达较糖尿病组下降(P<0.05),但较对照组增强(P<0.05)。见图2、3,表2、3。

图2 免疫组化显示Bcl-2的表达(×200)

表2 各组大鼠晶状体上皮细胞Bcl-2表达情况(n=5)
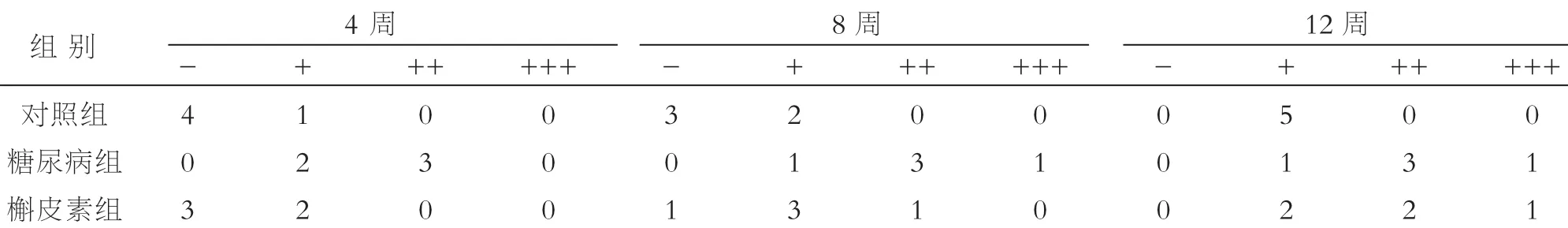
表3 各组大鼠晶状体上皮细胞Bax表达情况(n=5)
2.4 大鼠晶状体上皮细胞凋亡率
各组大鼠LECs凋亡情况,STE注射后4周、8周、12周时糖尿病组大鼠LECs的凋亡率显著高于对照组,而槲皮素组细胞凋亡率较糖尿病组显著降低,但仍高于对照组。各时间点三组之间两两比较差异有统计学意义(P<0.05),见表4。
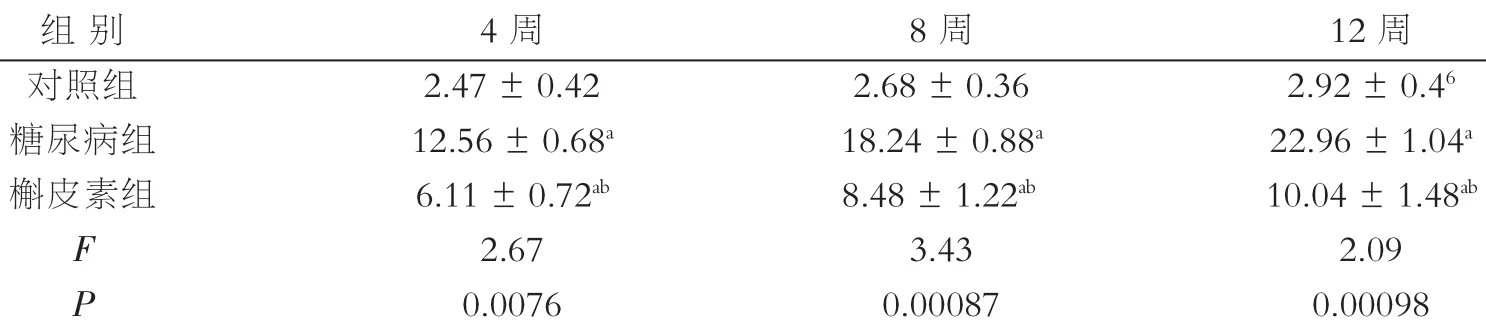
表4 各组大鼠晶状体上皮细胞凋亡率(%)

图3 免疫组化显示Bax的表达(×200)
3 讨论
糖尿病病人晶状体上皮细胞凋亡的发生发展是多种因素综合作用的结果,糖尿病最早攻击LECs,LECs能自主发生凋亡并可自我调节来抑制过度凋亡,而在高血糖刺激下产生的高氧化、高渗透压等将破坏LECs凋亡与增殖的平衡,从而引起LECs过度凋亡,并由此释放一系列物质产生级联反应,如Ca2+流入、半胱氨酸酶激活、晶状体蛋白变性、细胞骨架降解、水和电解质渗入等,晶状体的稳定性破坏,内坏境代谢失衡,最终导致白内障发生[1-3]。
槲皮素可通过抑制LECs的凋亡过程而对晶状体发挥保护作用。研究表明[4]槲皮素可明显降低老年性白内障的发病风险。紫外线诱导细胞凋亡是通过LECs DNA氧化性损伤引起的,槲皮素则可以在细胞遭受紫外线辐射前或后起到辐射防护的作用。Yao等[5]发现,紫外照射体外培养的LECs会诱导目标分子如p38蛋白、JNK蛋白的磷酸化,激活核转录因子NF-κB,MAPK家族等信号通路的活化,从而诱发LECs凋亡。Michael等[6]对大鼠晶状体紫外线照射发现,当LECs受到的损伤超过自我调节的能力时,细胞就会发生凋亡。Cao等[7]在观察DMSO和槲皮素共同作用于LECs的实验中发现,0.1 umol/L浓度的槲皮素可一定程度上抑制DMSO对LECs的破坏。Milackova I等[8]在动物实验中,大鼠晶状体在高糖中处理后,槲皮素衍生物可显著降低山梨糖醇的含量,认为槲皮素可能对高糖诱导的人LECs的凋亡有保护作用。本实验发现,同一时间点糖尿病组晶状体混浊程度均明显高于对照组,槲皮素组又轻于糖尿病组。并且糖尿病组LECs凋亡率明显高于对照组,而槲皮素组较糖尿病组低。表明随着糖尿病性白内障病情加重,LECs凋亡增加,予以槲皮素干预治疗糖尿病大鼠后,LECs凋亡程度降低,证实槲皮素在一定程度上可抑制LECs凋亡的发生发展。
Bcl-2家族是最早研究的凋亡相关基因,Bcl-2抑制细胞凋亡,Bax促进细胞凋亡,Bcl-2和Bax是主要的细胞凋亡调节蛋白,Bcl-2与Bax的比值决定着细胞的存亡,其它一切凋亡相关基因对细胞凋亡的作用都取决于Bcl-2与Bax比值的变化。因此,Bcl-2/Bax是目前细胞凋亡研究的热点之一,在细胞凋亡中决定细胞存活与凋亡的方向[9]。它们主要通过线粒体途径进行细胞凋亡的调节,Bcl-2主要在线粒体外膜执行功能,对于维持膜完整性起重要作用,而Bax破坏膜完整性。当细胞收到凋亡信号,被置换出来的Bax使线粒体膜通透性增加,促凋亡蛋白如cyt-c等及一些细胞因子进入细胞质,引起细胞凋亡。在此过程中Bcl-2和Bax以同/异二聚体的形式参与细胞凋亡的调节。当受到某种刺激(槲皮素干预)时,Bcl-2增多,将与Bax形成异二聚体,妨碍Bax之间形成同二聚体而使Bax减少,细胞免于凋亡;相反,若Bax增多,Bax形成同二聚体增多,细胞发生凋亡。有研究报道,转染Bcl-2能抑制如药物、加热、辐射等诱因引起的多种细胞凋亡[10]。Mao等[11]在动物实验中发现,Bcl-2通过减少β-晶状体蛋白,减弱H2O2诱导的兔LECs的凋亡。并且有研究证明[12],芦丁可下调Bax表达,上调Bcl-2表达,保护晶状体上皮细胞。已有研究者认为[13],Bax在硅油眼中对晶状体上皮细胞的凋亡起至关重要的作用。有研究者认为,通过改变Bcl-2/Bax的比值可能抑制糖尿病大鼠晶状体上皮细胞的凋亡[14]。本实验结果显示,糖尿病组与对照组比较,Bcl-2降低,Bax升高,表明Bcl-2和Bax的改变在糖尿病性白内障发生过程起重要作用,能起到调节LECs凋亡的作用。本实验通过免疫组化检测Bcl-2、Bax发现,高糖可引起晶状体上皮细胞凋亡。槲皮素组与糖尿病组比较,Bcl-2降低及Bax升高幅度更小,提示槲皮素通过引起Bcl-2和Bax的改变来抑制晶状体上皮细胞的凋亡。
综上所述,槲皮素对糖尿病大鼠LECs凋亡有一定的抑制作用,可延缓糖尿病性白内障的发生发展,作用机制可能是通过降低Bax的表达,增强Bcl-2的表达实现的。但槲皮素难溶于水,不利于机体吸收及利用,其溶剂的毒性也将限制其应用,如二甲基亚砜可导致溶血、肝肾毒性等,最近有将生物可降解的微粒与槲皮素共同制备成胶囊,不仅增加其吸收,还可延长槲皮素的释放周期;槲皮素对晶状体保护作用的研究尚不完善,确切的有效浓度、最大浓度、组织毒性等尚无定论;大部分研究仍处于临床前阶段,要广泛用于临床还需进一步在作用浓度、组织毒性、作用途径、剂型等方面进行探索和研究。
1.Kim J,Kim OS,Kim CS,et al.Accumulation of argpyrimidine a methylglyoxal-derived advanced glycation end product,increases apoptosis of lens epithelial cells both in vitro and in vivo[J].Exp Mol Med,2012,44(2):167-175.
2.Bahmani F,Bathaie SZ,Aldavood SJ,et al.Glycine therapy inhabits the progression of cataract in streptozotocininduced diabetic rats[J].Mol Vis,2012,18:439-448.
3.Li Y,Jia Y,Zhou J,et al.Effect of methionine sulfoxide reductase B1 silencing on high-glucose-induced apoptosis of human lens epithelial cells[J].Life Sci,2013,92(3): 193-201.
4.Ma Y,Gao W,Wu K,et al.Flavonoid intake and the risk of age-related cataract in China's Heilongjiang Province [J].Food Nutr Res,2015,11(59):29564.
5.Yao K,Zhang L,Zhang Y,et al.The flavonoid,fisetin,inhibits UV radiation-induced oxidative stress and the activation of NF-kappaB and MAPK signaling in human lens epithelial cells[J].Mol Vis,2008,14:1865-1871.
6.Michael R,Vrensen GF,Van Marle J,et al.Apoptosis in the rat lens after in vivo threshold dose ultraviolet irradiation[J].Invest Ophthalmol Vis Sci,1998,39(13):2681-2687.
7.Cao XG,Li XX,Bao YZ,et al.Responses of human lens epithelial cells to quercetin and DMSO[J].Invest Ophthalmol Vis Sci,2007,48(8):3714-3718.
8.Milackova I,Prnova MS,Majekova M,et al.2-Chloro-1,4-naphthoquinone derivative of quercetin as an inhibitor of aldose reductase and anti-inflammatory agent[J]. Enzyme Inhib Med Chem,2015,30(1):107-113.
9.Korkmaz D,Bastu E,Dural O,et al.Apoptosis through regulation of Bcl-2,Bax and Mcl-1 expressions in endometriotic cyst lesions and the endometrium of women with moderate to severe endometriosis[J].J Obstet Gynaecol,2013,33(7):725-728.
10.Huang YL,Chou CK.Bcl-2 blocks apoptosis signal of transforming growth factor in human hepatoma cells[J].J Biomed Sci,1998,5(3):185-191.
11.Mao YW,Xiang H,Wang J,et al.Human Bcl-2 gene attenuates the ability if rabbit lens epithelial cells against H2O2-induced apoptosis through down-regulation if the alpha B crystalline gene[J].J Biol Chem,2001,276(46): 43435-43445.
12.Zhou YF,Guo B,Ye MJ,et al.Protective Effect of Rutin Against H2O2-Induced Oxidative Stress and Apoptosis in Human Lens Epithelial Cells[J].Curr Eye Res,2015,41(7):1-10.
13.Zhu L,Zhao K,Luo D.Apoptosis Factors of Lens Epithelial Cells Responsible for Cataractogenesis in Vitrectomized Eyes with Silicone Oil Tamponade[J].Med Sci Monit, 2016,9(22):788-796.
14.Ou Y,Yuan Z,Li K,et al.Phycocyanin may suppress D-galactose-induced human lens epithelial cell apoptosis throughmitochondrialandunfoldedproteinresponse pathways[J].Toxicol Lett,2012,215(1):25-30.
(2016-05-30收稿)
Apoptotic effect of quercetin on len epithelial cells in diabetic rats
Liu Juan,Kang Gangjin,Kang Haijun,Bai Mengtian,Jiang Yan,Han Qian
Department of Ophthalmology,the Affiliated Hospital of Southwest Medical University,Luzhou,Sichuan Province 646000,China
Quercetin;Cell apoptosis;Lens epithelial cells;Diabetic cataract;Bcl-2;Bax
R776.1
A
10.3969/j.issn.1000-2669.2016.06.017
*西南医科大学附属医院国际合作课题(2011-43)
刘鹃(1988-),女,硕士,住院医师
康刚劲(1968-),女,硕士,教授。E-mail:929460414@qq.com
Astract Objective:To explore the apoptotic effect and the underlying molecular mechanism of quercetin on len epithelial cells in diabetic rats induced by STZ.Methods:60 SD rats were randomly divided into normal control group,diabetic model group and QUE treatment group,with 20 in each group.The rats in control group were maintained normally,and the other 40 rats were given intraperitoneal injection of 1%Stretozocin(STZ)to induce the diabetic cataract rats.The model group was maintained normally,and QUE group was given 50 mg/kg QUE by gavage every day.At 4,8,and 12 weeks after STZ injection,the blood glucose level was measured,the changes of lens opacity were evaluated,the morphology of LECs was observed by HE staining,the expression of Bcl-2 and Bax in LECs were analyzed by immunohistochemical,and the apoptotic ratio of LECs was measured by flow cytometry.Results:At 12 weeks,the average body weight in the model group and QUE group was significantly lower than that of control group(P<0.05),whereas there was no statistical difference between model group and treatment group(P>0.05).At 4,8,and 12 weeks,the blood glucose level in the model group and QUE group was significantly higher than in the control group(P<0.05),whereas there was no statistical difference between model group and treatment group(P>0.05).The degree of len opacity after STZ at 4th,8th,and 12th week was statistical different among groups(P<0.05),with the QUE group severer than control group(P<0.05)and model group severer than QUE group(P<0.05).HE results showed that LECs were irregular in morphology, loose and lightly stained in cytoplasm,contained many non-degraded organelles in the fibroblasts of the posterior capsule in both model group and treatment group.Compared with the control group,the protein expression of Bcl-2 in the model group and QUE group was reduced and the protein expression of Bax was up-regulated(P<0.05). Compared with the QUE group,the protein expression of Bcl-2 in the model group was reduced and the protein expression of Bax was up-regulated(P<0.05).At 4,8 and 12 weeks,the differences of the apoptotic rate in each group were statistically significant between any two groups(P<0.05).Conclusion:QUE can inhibit LECs apoptosis and delay the occurrence and the development of diabetic cataract in diabetic rats.
