壳聚糖和乙二胺改性Fe3O4磁性纳米粒子的制备及其对酸性品红的吸附特性
2016-09-13杨武,潘薇,郭昊
杨 武,潘 薇,郭 昊
(西北师范大学化学化工学院,甘肃兰州 730070)
壳聚糖和乙二胺改性Fe3O4磁性纳米粒子的制备及其对酸性品红的吸附特性
杨武,潘薇,郭昊
(西北师范大学化学化工学院,甘肃兰州730070)
采用SiO2包覆Fe3O4磁性纳米粒子,然后以戊二醛为交联剂使其与壳聚糖交联固化,得到了磁性壳聚糖复合纳米粒子(CMS),再经乙二胺改性制得乙二胺改性的磁性壳聚糖复合纳米粒子吸附剂(EDCMS),并将其用于对酸性品红溶液的吸附研究.考察了pH、吸附剂用量、吸附时间、初始浓度对吸附行为的影响.结果表明,吸附剂对酸性品红脱色率达98.04%以上,最大吸附量为284mg·g-1,吸附过程符合准二级速率方程和Freundlich等温模型.
Fe3O4纳米粒子;磁性吸附材料;壳聚糖;酸性品红;脱色
水是非常宝贵且有限的自然资源,是人类生活、生产活动中不可或缺的物质基础.但是随着我国印染工业的迅速发展,人们向环境水体中排放印染废水的数量也日益增多,对水环境造成了极大危害.因此研究开发染料废水的高效处理方法和技术显得尤为重要.在众多的染料废水处理方法中,吸附法作为一种廉价、高效的废水处理方法,在污水处理中占有重要地位[1-3].
Fe3O4磁性纳米粒子是一种具有吸附性能的纳米材料,但它易团聚,酸性条件下易被腐蚀,并且吸附能力较弱.为了克服这些缺点,本文利用正硅酸乙酯(TEOS)的水解反应在Fe3O4表面包覆上具有良好水溶性和化学性质稳定的SiO2.为了增强它的吸附能力可以通过物理或者化学的方法在磁性纳米粒子表面修饰氨基、巯基、羧基等官能团[4].壳聚糖是甲壳素脱乙酰化后的天然高分子聚合物,它来源丰富,存储量大而且无毒,具有良好的可降解性和生物相容性[5],因其分子中含有许多氨基,所以将壳聚糖复合在Fe3O4@SiO2磁性纳米材料上有利于对染料的吸附[6].最后用乙二胺对其进行再次氨基修饰,可以引进更多的氨基[7],大大提高了其对酸性品红的吸附能力.
1 实验部分
1.1仪器与试剂
壳聚糖(95%,青岛博益特生物材料有限公司),FeCl3·6H2O(天津光复科技发展有限公司);FeCl2·4H2O(天津凯信化学工业有限公司);戊二醛(上海中泰化学试剂有限公司);环己烷(莱阳双双化工有限公司);硅酸乙酯(天津天河化学试剂厂);环氧氯丙烷(济南万利玺化工有限公司);乙二胺(济南世纪通达化工有限公司).
真空干燥箱(DZF-6030A,上海一恒科技有限公司);恒温振荡器(上海启步生物科技有限公司);PHS-3C精密pH计;集热式恒温加热磁力搅拌器(西安莫吉娜仪器制造有限公司);UV757CRTVer2.00分光光度计(上海奥析科学仪器有限公司).
1.2吸附剂的制备1.2.1共沉淀法制备纳米Fe3O4准确称取5.41gFeCl3·6H2O和3.98gFeCl2·4H2O(即nFe2+/nFe3+=1∶1)置于烧杯中,加入100mL二次蒸馏水,60 ℃下搅拌均匀,在N2保护下加入25mLNH3·H2O,反应30min后,离心分离,产物用水洗至中性,再用无水乙醇洗涤数次,在真空干燥箱中干燥24h.
1.2.2SiO2包覆磁性纳米粒子Fe3O4@SiO2的制备称取0.5gFe3O4纳米粒子于60mL无水乙醇和20mL蒸馏水的混合液中,超声分散1h.加入5mL不同浓度的TEOS乙醇溶液、4mL25%的氨水,反应6h,确保TEOS分解产生的SiO2最大限度地包覆于Fe3O4表面.过滤,用无水乙醇和蒸馏水反复洗涤数次,以除去未反应的试剂,用磁铁将其从中分离,于60 ℃条件下真空干燥12h,产品标记为Fe3O4@SiO2.
1.2.3壳聚糖复合Fe3O4@SiO2磁性材料的制备将1g壳聚糖溶于100mL1%的醋酸中,加入0.5gFe3O4@SiO2,超声分散0.5h,再加入6mL25%的戊二醛溶液,磁力搅拌4h,生成的凝胶于60 ℃真空干燥24h,研细后依次用1%醋酸溶液、热水、冷水洗涤,干燥,产品标记为CMS.
1.2.4氨基修饰磁性材料的制备在上述制得的CMS中加入80mL异丙醇和2mL环氧氯丙烷(溶于40mL体积比为1∶1的丙酮/水混合液中),于60 ℃条件下搅拌反应24h,过滤分离后,将50mL体积比为1∶1的乙醇/水混合液加入其中,紧接着再加入2.5mL乙二胺,混合物于60 ℃下搅拌反应12h.产物过滤、洗涤,60 ℃真空干燥12h,产品标记为EDCMS.
1.3吸附量的计算
利用紫外分光光度法测定不同pH、不同吸附剂添加量、不同反应时间及不同初始浓度条件下,经吸附剂处理后的模拟染料废水的吸光度,依据(1)和(2)式计算脱色率和吸附量:
(1)
(2)
其中,qe为吸附量(mg·g-1);η为脱色率(%);Ce为吸附平衡时染料的浓度(mg·L-1);C0为染料的初始浓度(mg·L-1);V为溶液的体积(L);m为复合吸附剂的干重(g).
2 结果与讨论
2.1复合材料的表征
2.1.1磁性复合材料的红外光谱壳聚糖,Fe3O4,SiO2,CMS和EDCMS的红外光谱图见图1.壳聚糖在3 437cm-1附近的特征吸收峰为N—H和O—H键的伸缩振动,在2 920和2 880cm-1处的特征峰为C—H键的伸缩振动,在1 662,1 603和1 385cm-1处的吸收峰分别为酰胺Ⅰ带,酰胺Ⅱ带和CH3的变形振动[10].Fe3O4在582cm-1处出现了Fe—O键的伸缩振动峰,而在Fe3O4@SiO2中,除了582cm-1处的吸收峰外,在1 209和1 095cm-1处出现了Si—O键的伸缩振动峰,表明SiO2成功包覆到了Fe3O4的表面[8-9].在CMS的红外谱图中,酰胺I带和酰胺Ⅱ带的峰明显减弱,而在1 641cm-1处出现了较强的C=N吸收峰,这是通过交联剂将CS交联到SiO2@Fe3O4上的直接证据[11].而Si—O键的伸缩振动峰则被CS中的C—N振动峰所覆盖[12].EDCMS中1 585cm-1处的较强吸收峰为C=O的伸缩振动峰,而2 800~2 900cm-1之间的吸收峰强度明显增加则表明乙二胺中—CH2—基团已经成功引入[13].

图1 壳聚糖(a),Fe3O4(b),SiO2@Fe3O4(c),CMS(d)和EDCMS(e)的红外光谱Fig 1 FTIR spectra of chitosan(a),Fe3O4(b),SiO2@Fe3O4(c),CMS(d) and EDCMS(e)
2.1.2改性前后复合吸附剂的形貌图2为Fe3O4(a),Fe3O4@SiO2(b),CMS(c)和EDCMS(d)的扫描电镜.从图2a可以看出,未改性的Fe3O4呈微小的颗粒状,用SiO2包覆后(图2b),颗粒变大,表面变得光滑,用壳聚糖改性后变为规则的球形,表面变得更加光滑,并且出现许多孔洞(图2c),这种结构对提高吸附剂的吸附性非常有利.氨基功能化后,EDCMS的形貌发生了显著的变化,呈现出立体网状空间结构(图2d), 这种结构更加有利于染料分子与其接触或者嵌入其内部,使吸附效果大大提高.

图2 Fe3O4(a),Fe3O4@SiO2(b),CMS(c)及EDCMS(d)的FE-SEM形貌Fig 2 FE-SEM micrographs of Fe3O4(a),Fe3O4@SiO2(b),CMS(c)and EDCMS(d)
2.1.3热重分析图3为吸附剂的热重分析曲线.从图可以看出,它们的失重百分比都随着温度的升高而逐渐降低,其中CMS和EDCMS的失重明显.300 ℃时,Fe3O4(a)的失重率约为0.66%,归因于表面物理吸附水的脱除[14],Fe3O4@SiO2(b)在70 ℃到200 ℃的重量损失主要是由于结晶水和内部水分子的失去,损失率约为22.7%.在CMS和EDCMS中,除了水的损失,在180 ℃开始主要表现为有机组分的脱除和高分子聚合物的分解[10],失重率约为87.8%和83.1%.本实验中各材料失重率的不同说明在进行每一步实验时,材料的组成都发生了变化,也就是说,实验的每一步都有新的物质包覆到磁性纳米粒子上.
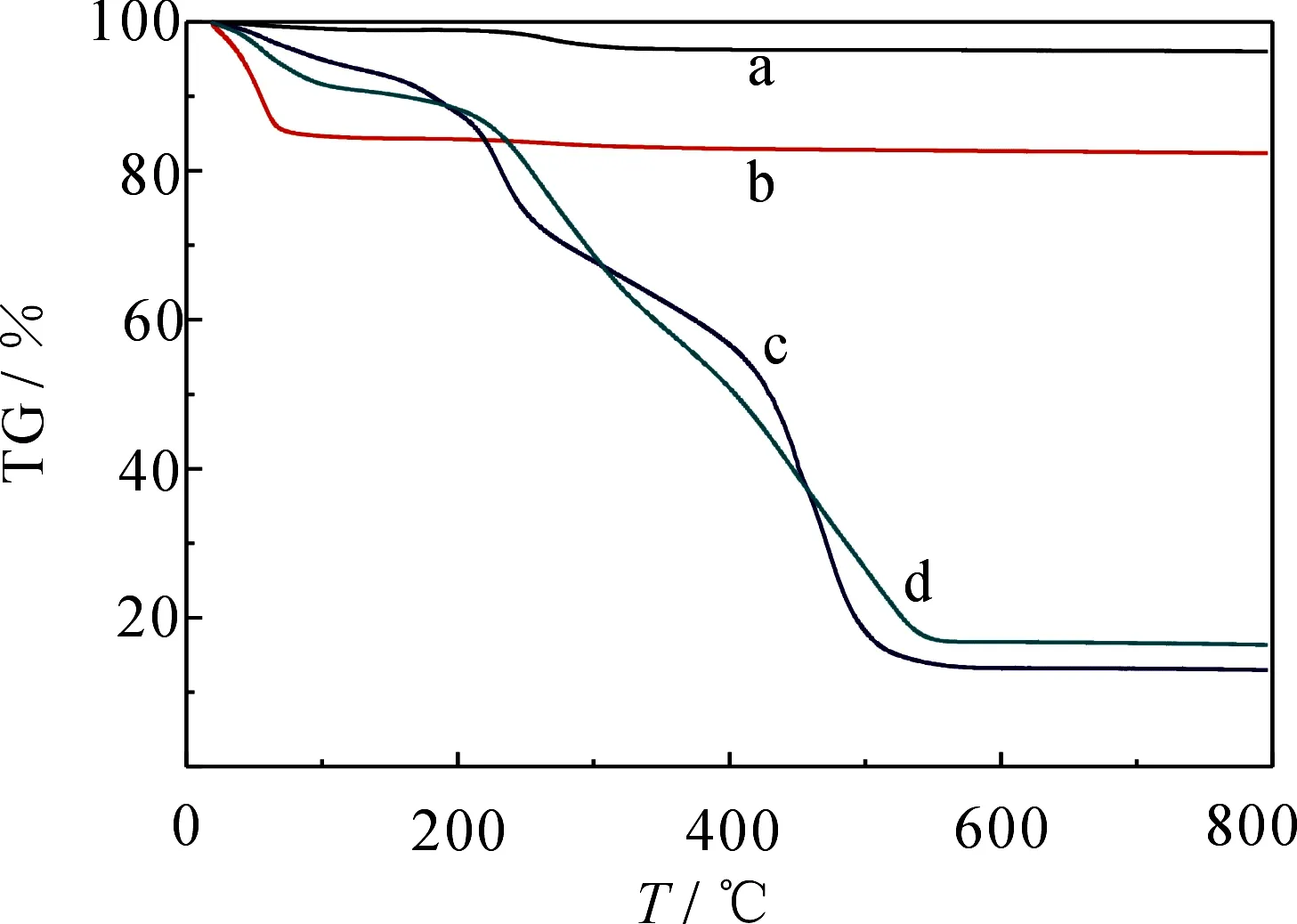
图3 Fe3O4(a),Fe3O4@SiO2(b),CMS(c)和EDCMS(d)的热重分析曲线Fig 3 Thermogravimetric curves of Fe3O4(a),SiO2/Fe3O4(b),CMS(c) and EDCMS(d).
2.1.4XRD分析图4为吸附剂的XRD图谱.从图可以看出,改性前后,Fe3O4的主要衍射峰位置(2θ=30.24°,35.70°,43.31°,53.70°,57.27°,63.01°)没有明显变化,表现出良好的结晶性,表明有机改性对Fe3O4的结晶形态没有产生显著影响[15].
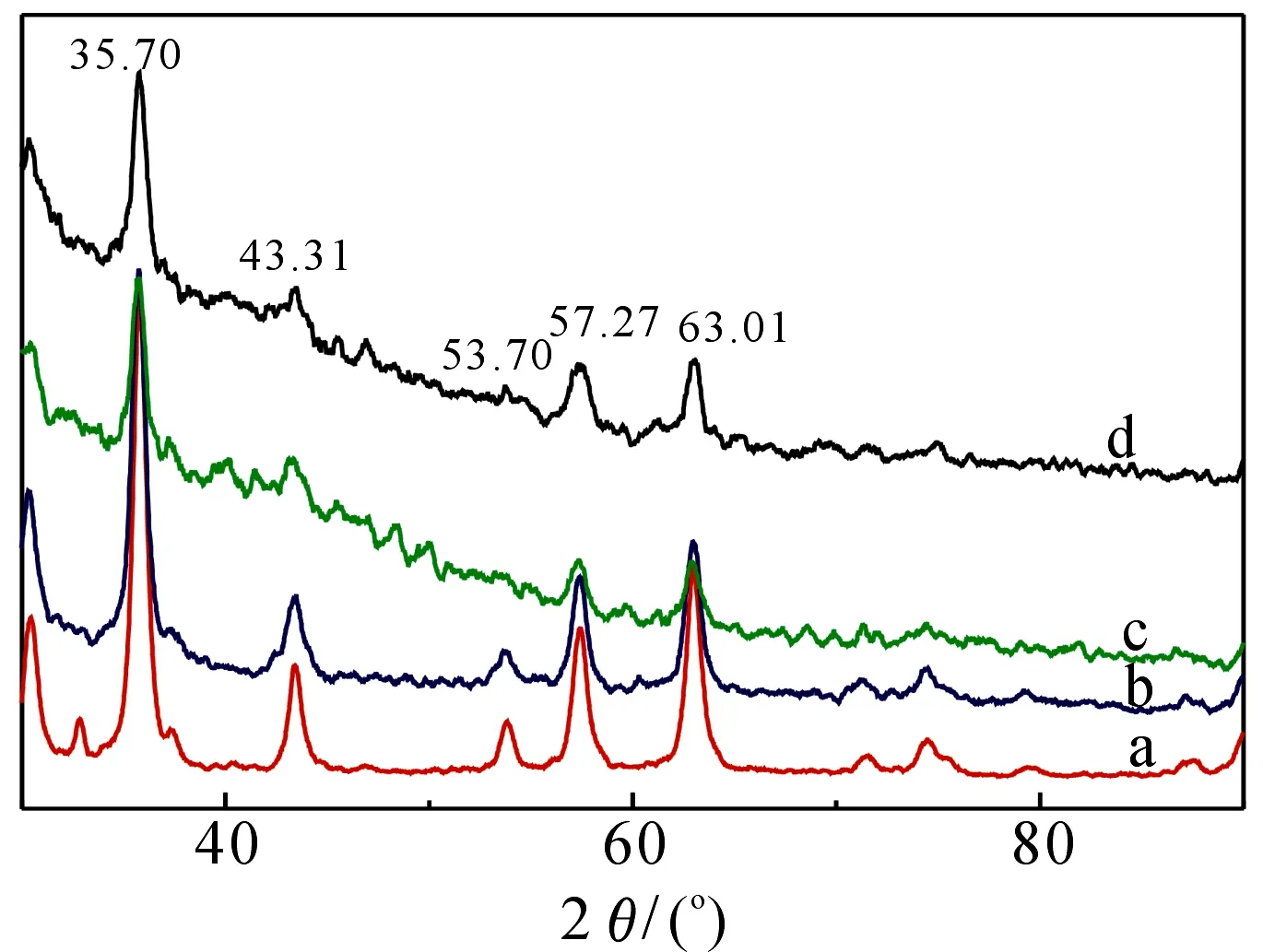
图4 Fe3O4(a),SiO2/Fe3O4(b),CMS(c) 和EDCMS(d)的XRD图谱Fig 4 XRD patterns of Fe3O4(a), Fe3O4@SiO2(b),CMS(c) and EDCMS(d).
2.2实验条件对吸附量的影响
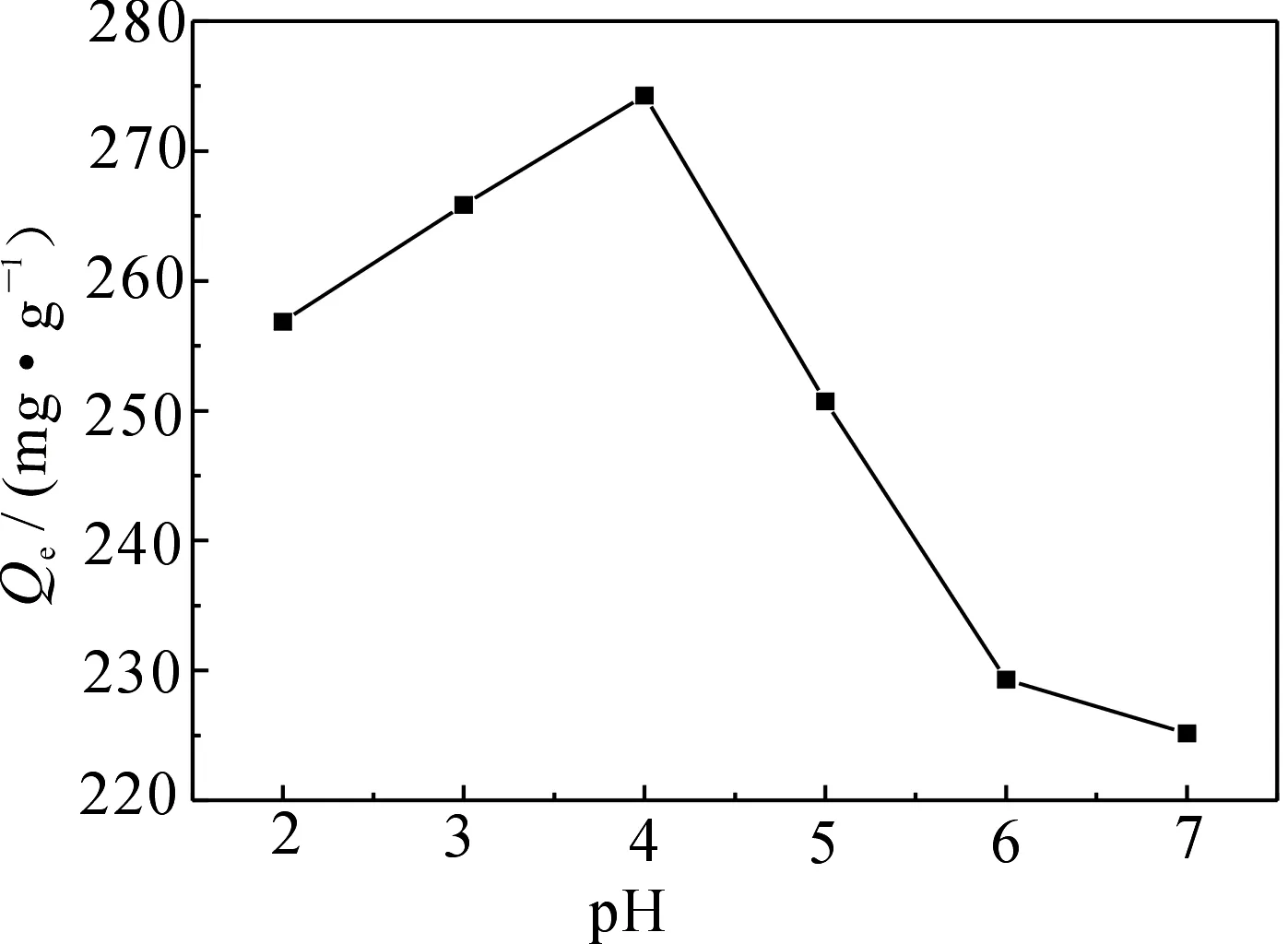
图5 pH对吸附量的影响Fig 5The effect of pH on the adsorption
2.2.2复合吸附剂用量对脱色率的影响吸附剂用量对酸性品红溶液脱色率的影响见图6.从图6可以看出,随着复合吸附剂加入量的增加,染料的脱色率迅速增加.当吸附剂达到20mg时,脱色率达到稳定,原因是随着吸附剂的加入,吸附活性位点会相应增加,吸附量增加.但是当吸附剂量增加到一定程度时,溶液中残留的染料浓度过低,无法再被吸附,所以脱色率不再增加,酸性品红的最佳吸附剂用量为20mg.
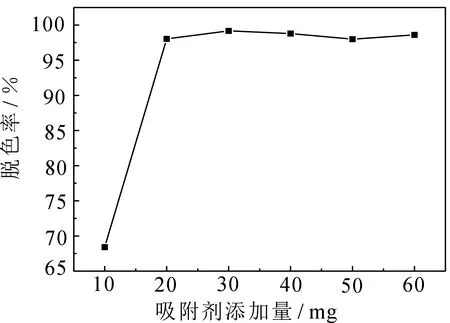
图6 吸附剂加入量对脱色效果的影响Fig 6 Effect of the adsorbent amountson the decolorization rate
2.2.3吸附时间对吸附量的影响移取体积为50mL,初始浓度为400mg·L-1的酸性品红溶液于不同锥形瓶中,各加入0.0500g吸附剂,分别振荡20,40,60,80,100,120,140,160min后,静置、离心,测定上清液吸光度,考察吸附时间对吸附量的影响,结果见图7.从图7可以看出,随着吸附时间的延长,吸附剂对酸性品红溶液的吸附量逐渐增大,当时间为120min时,吸附量达到稳定.
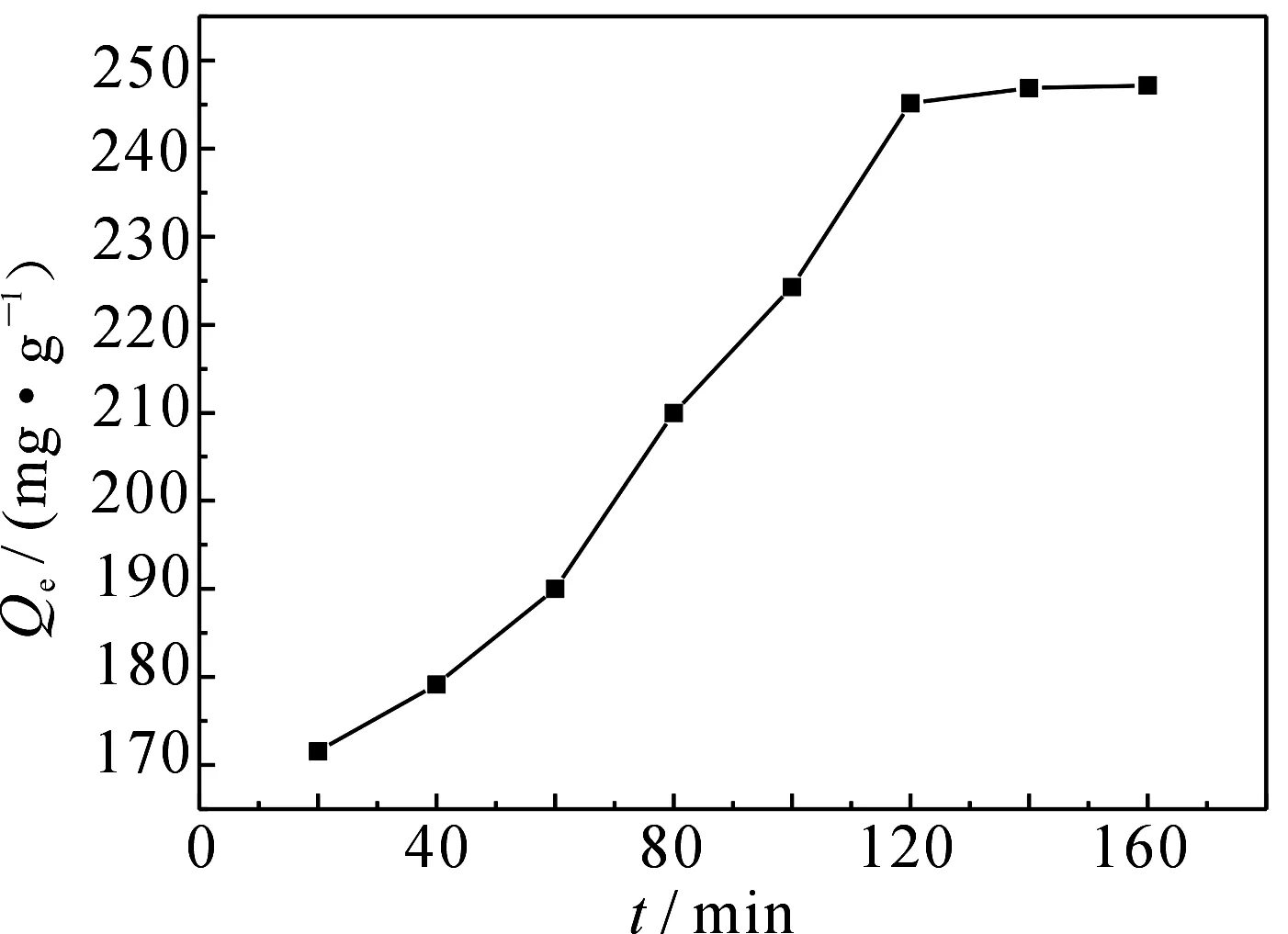
图7 吸附时间对吸附量的影响Fig 7Effects of contact time on the adsorption
2.2.4染料初始浓度对吸附量的影响用等质量的吸附剂对不同浓度的酸性品红溶液进行吸附.移取不同浓度的酸性品红溶液各50mL于锥形瓶中,分别加入0.0500g吸附剂,在25 ℃下振荡2h,静置、离心,测吸光度,考察吸附剂对不同浓度的酸性品红的吸附行为,结果见8.从图8可以看出,随着酸性品红溶液的浓度增大,吸附剂对酸性品红溶液的吸附量逐渐增大,当酸性品红的浓度达到400mg·L-1后,吸附量最大,并保持稳定.同时,从图8还可以看出,壳聚糖与磁性纳米粒子复合后,吸附量明显增加,达到了原磁性纳米粒子吸附量的2倍左右,当用乙二胺改性后,其吸附量更是得到了显著提升,达到了Fe3O4@SiO2的7倍以上.进一步说明随着氨基的引入,吸附剂对酸性品红的吸附性能越来越佳.
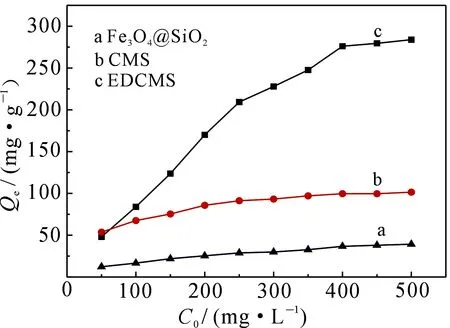
图8 初始浓度对吸附量的影响Fig 8Effect of the dye concentration on the adsorption
2.3吸附动力学
将酸性品红在复合吸附剂上的吸附过程分别用(3)式准一级动力学和(4)式准二级动力学模型进行拟合:
(3)
(4)
其中,qt,qe分别为t时刻和平衡后的吸附量(mg·g-1),k1为准一级吸附速率常数(min-1),k2为准二级吸附速率常数(g·mg-1·min-1).拟合结果见图9,相关参数见表1.
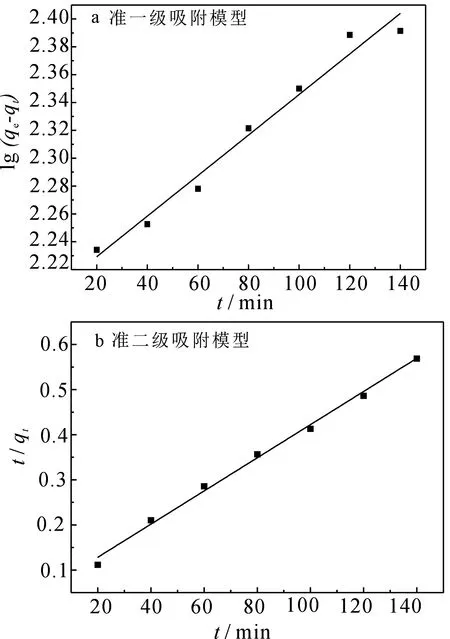
图9 复合吸附剂对酸性品红的吸附动力学曲线Fig 9 Adsorption dynamic curves of the compositeadsorbent to acid magenta表1 复合吸附剂对酸性品红的吸附动力学参数Tab 1 Kinetics parameter for adsorption of acidmagenta on the compound adsorbent

染料酸性品红准一级吸附速率方程k1/min-1 0.0035qe/(mg·g-1)158.5258R210.9781准二级吸附速率方程k2/(g·mg-1·min-1))0.0003qe/(mg·g-1)270.2703R220.9947
2.4吸附等温线
用Langmuir和Freundlich等温吸附模型分别对实验数据进行拟合:
(5)
(6)
其中,qm为单分子层的饱和吸附量(mg·g-1);KL为Langmuir吸附常数;KF和n分别为Freundlich有关吸附常数.分别以Ce/qe对Ce, lgqe对lgCe作图,拟合结果见图10,相关参数见表2.
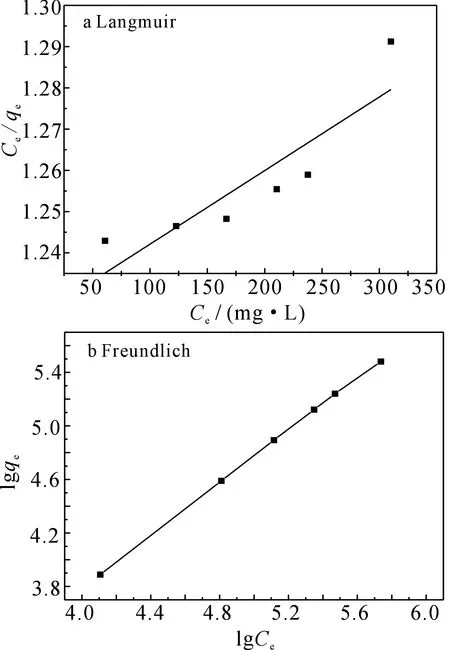
图10 复合吸附剂对酸性品红的Langmuir(a)和Freurdlich(b)吸附等温线Fig 10 Langmuir(a) and Freundlich(b) adsorptionisotherms of the composite adsorbent toacid magenta表2 吸附等温线的相关拟合参数Tab 2The fitting results of the adsorption isotherm

染料Langmuirqex/(mg·g-1)qm/(mg·g-1)KL/(L·mg-1)R21FreundlichKF/(mg·g-1)nR22酸性品红240.1114166.6670.0005180.78841.36421.01870.9997
3 结束语
成功制备了经壳聚糖和乙二胺改性的磁性纳米粒子复合吸附剂,并用于酸性品红染料的去除.在pH=4,吸附时间为2h条件下该吸附剂对酸性品红具有较高的吸附量.复合吸附剂对酸性品红的吸附过程符合Freundlich等温吸附模型和准二级吸附速率方程.该方法制备的复合吸附剂对酸性品红染料吸附效果良好,且易于分离,在染料废水的去除方面具有较好的应用前景.
[1]颜延国.两种磁性吸附材料制备及其染料吸附性能研究[D].哈尔滨:东北林业大学,2014.
[2]胡建邦,袁亚莉.氨基化改性Fe3O4/SiO2省略性材料的制备以及对铀的吸附研究[J].应用化工,2012,41(12):2068.
[3]宋昭峥,张建存,李宜坤.国外溶液型选择性堵水剂的研究进展[J].应用化工,2010,39(5):770.
[4]付雅观,钱杰,原观军,等.大庆油田二类油层聚合物驱前调剖深度探[J].西南石油大学学报(自然科学版),2007,29(4):122.
[5]杨武,姚文双,郭昊,等.聚甲基丙烯酸-g-壳聚糖/膨润土复合材料的制备及其对阳离子染料的吸附性能[J].西北师范大学学报(自然科学版),2015,51(3):64.
[6]MAM,ZHANGY,YUW,etal.Preparationandcharacterizationofmagnetitenanoparticlescoatedbyaminosilane[J].Colloids surfA,2003,212:219.
[7]周利民,尚超,刘峙嵘.乙二胺改性磁性壳聚糖纳米粒子对酸性染料的吸附特性[J].物理化学学报,2011,27(3):677.
[8]SAYINS,YILMAZM.SynthesisofanewcalixarenederivativeanditsimmobilizationontomagneticnanoparticlesurfacesforexcellentextractantstowardCr(VI),As(V),andU(VI)[J].J Chem Eng Data,2011,56,2020.
[9]LIZC,FANHT,ZHANGY,etal.Cd(Ⅱ)-imprintedpolymersorbentspreparedbycombinationofsurfaceimprintingtechniquewithhydrothermalassistedsol-gelprocessforselectiveremovalofcadmium(Ⅱ)fromaqueoussolution[J].Chem Eng J,2010,171,703.
[10]MONIERM,AYADDM,WEIY,etal.PreparationandcharacterizationofmagneticchelatingresinbasedonchitosanforadsorptionofCu(Ⅱ),Co(Ⅱ)andNi(Ⅱ)ions[J].React Funct Polym,2010,70,257.
[11]LEIZ,PANGX,LIN,etal.Anoveltwo-stepmodifyingprocessforpreparationofchitosan-coatedFe3O4/SiO2microspheres[J].J Mater Process Technol,2009,209,3218.
[12]NAJAFIM,YOUSEFIY,RAFATIiAA.Synthesis,characterizationandadsorptionstudiesofseveralheavymetalionsonamino-functionalizedsilicananohollowsphereandsilicagel[J].Sep Purif Technol,2012,85,193.
[13]QINR,LIF,CHENM,etal.Preparatianofchitosan-ethylenediaminetetraacetateenwrappedmagneticCoFe2O4nanoparticlesviazero-lengthemulsioncrosslinkingmethod[J].Appl Surf Sci,2009,256,27.
[14]WANGJ,ZHENGS,SHAOY,etal.Amino-functionalizedFe3O4@SiO2core-shellmagneticnanomaterialasanoveladsorbentforaqueousheavymetalsremoval[J].J Colloids Interf Sci,2010,349,293.
[15]RENY,ABBOODHA,HEFB,etal.MagneticEDTA-modifiedchitosan/SiO2/Fe3O4adsorbent:Preparation,characterization,andapplicationinheavymetaladsorption[J].Chem Eng J,2013,226,300.
(责任编辑陆泉芳)
Modification of the nano Fe3O4using chitosan andethylenediamineanditsadsorptionbehaviorforacidmagenta
YANGWu,PANWei,GUOHao
(CollegeofChemistryandChemicalEngineering,NorthwestNormalUniversity,Lanzhou730070,Gansu,China)
Acompositeabsorbent(EDCMS)basedonethylenediaminemodifiedmagneticchitosannanoparticlesispreparedthroughcoatingmagneticFe3O4nanoparticleswithSiO2,chitosanandethylenediamine,andthenusedtoadsorbacidmagenta.TheeffectsoftheexperimentalconditionssuchaspH,amountofabsorbents,contacttimeandinitialconcentrationontheadsorptionpropertiesaswellasthermodynamicsanddynamicsarealsoinvestigated.Theresultsshowthattheremovalrateofacidmagentaisabove98.04%andthemaximumadsorptionamountis284mg·g-1.Theadsorptionprocessobeysthepseudo-secondrateequationandtheFreundlichisothermaladsorptionmodel.
nanoFe3O4;magneticadsorbent;chitosan;acidmagenta;decolorizing
10.16783/j.cnki.nwnuz.2016.03.015
2015-10-08;修改稿收到日期:2016-01-09
国家自然科学基金资助项目(29875018)
杨武(1966—),男,甘肃西和人,教授,博士,博士研究生导师.主要研究方向为非线性化学.
E-mail:xbsfda123@126.com
O647.32
A
1001-988Ⅹ(2016)03-0078-06
