水系锂离子电池负极聚硫代苯醌的合成与电化学性能
2016-09-05蔡莉丽文越华曹高萍杨裕生北京化工大学理学院北京059北京防化研究院北京009
蔡莉丽 文越华 程 杰 曹高萍 杨裕生,(北京化工大学理学院,北京059;北京防化研究院,北京009)
水系锂离子电池负极聚硫代苯醌的合成与电化学性能
蔡莉丽1文越华2,*程杰2曹高萍2杨裕生1,2
(1北京化工大学理学院,北京110159;2北京防化研究院,北京100191)
通过硫化聚合的方法,以四氯苯醌(TCQ)为单体合成了聚硫代苯醌(PBQS)材料。本文改变S的加入量,探讨了不同摩尔比的S和Na2S对PBQS电极电化学性能的影响。当S和Na2S摩尔比为0.4时,形成两个氯原子被硫取代的PBQS-0.4稳定结构。PBQS-0.4电极放电比容量达到140 mAh∙g-1以上,显现出良好的循环稳定性和优异的倍率性能。而当S和Na2S摩尔比降至0.25时,氯取代不完全、聚合程度不高;S和Na2S摩尔比增至0.7:1时,聚合物中可能形成了不稳定的累积S―S键;上述两方面都导致电极性能明显下降。
水系锂离子电池;缩聚法;聚硫代苯醌;S和Na2S摩尔比;电化学性能
[Article]
www.whxb.pku.edu.cn
有机醌类聚合物的理论容量高(>200 mAh∙g-1),平均工作电压一般在2.0-2.5 V(vs Li/Li+)内,最高不超过2.8 V(vs Li/Li+),且在分子水平设计上通过聚合10、导电材料的原位复合等途径,可有效提高材料的导电性和循环稳定性;与通常的无机材料相比,有机醌类聚合物性能提升空间很大,具有用于水系锂离子电池负极材料的潜在应用前景。本文以四氯苯醌(TCQ)为起始原料,在一定温度下与含硫的多硫化钠发生缩聚反应,制备了聚合物醌电极材料-聚硫代苯醌(PBQS),且研究表明,S和Na2S的摩尔比对聚硫代苯醌的电化学性能有重要影响。为此,改变S的加入量,探讨了S和Na2S的摩尔比对所生成的聚硫代苯醌电极材料结构和电化学性能影响,对于醌类聚合物作为负极用于水系锂离子电池具有重要的研究和参考价值。
2 实验部分
2.1聚硫代苯醌的制备
将四氯苯醌(化学纯,98.0%)溶解在N,N-二甲基甲酰胺(DMF,分析纯,99.5%)中,TCQ和DMF的比例为0.03 g∙mL-1。四氯苯醌与硫化钠摩尔比1:4,将所需的Na2S(分析纯,98.0%,西陇化工有限公司)溶于水中,Na2S与水的比例是0.197 g∙mL-1,同时改变S(化学纯,99.0%,西陇化工有限公司)的加入量。将上述两种溶液混合均匀,80°C控温加热回流反应72 h,经过滤、洗涤、干燥得到PBQS材料。S和Na2S的摩尔比分别为0.25、0.4、0.7,对应制得的三个聚合物样品分别命名为PBQS-0.25、PBQS-0.4、PBQS-0.7。
2.2工作电极制备和电化学性能测试
将制备的电极活性材料PBQS、乙炔黑和聚四氟乙烯(PTFE)以质量比55:40:5混合后,擀压成片,裁成1 cm×1 cm的电极,活性物质担载量约2-3 mg∙cm-2左右,压在不锈钢网上制成工作电极,电解液为5 mol∙L-1LiNO3(分析纯,99.0%)水溶液(pH=7)。循环伏安(CV)测试在CHI 608D型电化学工作站(上海辰华仪器公司)上进行,采用三电极体系,其中用大面积活性碳作为对电极,饱和甘汞为参比电极,扫描速率为10 mV∙s-1,扫描范围为-0.8-0.2 V(vs SCE)。以活性物质担载量在10 mg∙cm-2的大面积(约2 cm×4 cm)活性炭为正极,与面积为(1 cm×1 cm)的PBQS负极组成两电极体系测试的充放电性能。为抑制正极析氧副反应影响,充电截止电压设定为1.1或1.2 V,放电截止电压为0 V。充放电测试在武汉Land CT2001A充放电测试仪上进行。电极放电比容量只按照活性物质的质量计算。
使用KBr压片法在Nexus670红外光谱仪(美国尼高力公司)上测试了TCQ和PBQS的红外光谱,扫描范围为500-2000 cm-1。采用Vario EL III元素分析仪(ElementarInc.,Germany)测试了三种PBQS样品中C、S、N三种元素的含量。
3 结果与讨论
3.1循环伏安测试
以不同摩尔比例的S和Na2S合成的PBQS和TCQ在5 mol∙L-1LiNO3溶液(pH=7)中的循环伏安曲线如图1所示。四氯苯醌单体的氧化还原峰型尖锐且对称,CV曲线重合度低,随着扫描次数增加,峰电流不断降低,材料出现溶解现象,电解液变黄。PBQS聚合物电极的峰型呈包峰状,但五次循环扫描的CV曲线都基本重合,说明四氯苯醌单体硫化聚合后电极极化有所增大,但循环稳定性显著提高。S与Na2S的摩尔比为0.25时,所制电极PBQS-0.25分别在-0.34、-0.089和-0.43、-0.21 V处出现两对氧化还原包峰,说明聚合物醌PBQS电极锂离子的脱嵌分两步进行。根据相关文献11-13以及循环伏安曲线的测试结果可知,PBQS材料的氧化还原机制如下:聚硫代对苯醌负极首先充电还原,得到一个电子,形成一价自由基负离子,嵌入一个锂离子;之后再得到第二个电子,形成二价自由基阴离子,嵌入第二个锂离子。放电氧化过程则相反,两个锂离子分别脱出,重新生成带两个羰基的聚硫代对苯醌。通过羰基和烯醇结构之间的转换实现锂离子的可逆嵌入和脱出。当S与Na2S的摩尔比例增至0.4时,低电位下的氧化、还原峰变弱,高电位下的氧化、还原峰进一步宽化且略向正移,但峰电流明显增大。当S与Na2S的摩尔比进一步增至0.7时,峰电流降至最低,峰电位进一步正移,且两步电子得失的氧化、还原反应过程已表现不明显,呈现一对氧化、还原包峰。
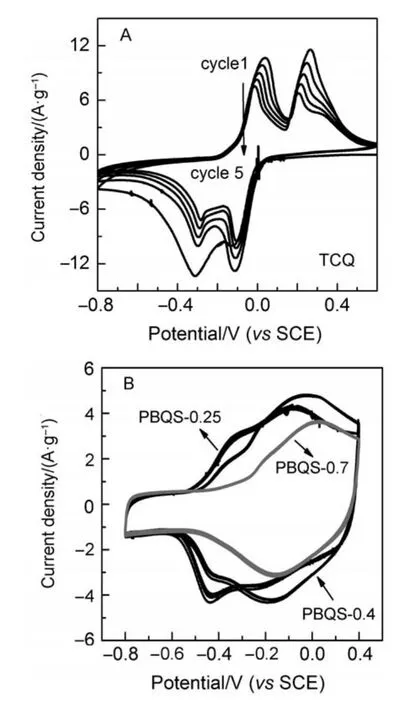
图1 四氯苯醌(A)和以不同摩尔比的S和Na2S制得的PBQS电极(B)前5次扫描的循环伏安曲线Fig.1 Cyclic voltammogram of the first five scanning with TCQ(A)and PBQS(B)electrodes prepared by different mole ratios of S to Na2S

图2 在电流密度为200 mA∙g-1时以不同摩尔比的S和Na2S制得PBQS聚合物电极的典型充放电曲线Fig.2 Typical charge and discharge curves of PBQS electrodes prepared by different mole ratios of S to Na2S atthe current density of 200 mA∙g-1(a)PBQS-0.25;(b)PBQS-0.4;(c)PBQS-0.7
3.2充放电性能
以容量过量的大面积活性碳电极为正极,聚合物醌PBQS电极为负极在5 mol∙L-1LiNO3水溶液中组成电池测试负极的充放电性能。图2为采用不同摩尔比的S和Na2S制得的PBQS电极在200 mA∙g-1电流密度下首次充放电曲线。为抑制析氧副反应的发生,保证充放电的库仑效率达到90%以上,电池充电截止电压设定为1.1或1.2 V。由图2中可见,聚合物醌PBQS电极的充放电曲线均呈倾斜状态,没有明显充放电平台。PBQS-0.4首次放电中值电压为0.55 V,高于材料PBQS-0.25和PBQS-0.7的中值电压0.50和0.51 V,说明电极PBQS-0.4的极化最小。S和Na2S的摩尔比为0.25时,聚合物电极PBQS-0.25的首次放电容量仅有96 mAh∙g-1,库仑效率为93%;提高S的含量,PBQS的首次放电比容量明显增大,均超过了100 mAh∙g-1,库仑效率接近100%。当S和Na2S的摩尔比为0.4时,电极PBQS-0.4的首次放电比容量达到138 mAh∙g-1;但是,将S和Na2S的摩尔比增至0.7时,放电比容量又出现一定程度的降低,PBQS-0.7的首次放电比容量仅为104 mAh∙g-1。
图3为采用不同摩尔比的S和Na2S合成的聚合物醌PBQS电极倍率性能。可见,在100 mA∙g-1电流密度下,电极PBQS-0.4初始放电比容量高达142 mAh∙g-1,电极PBQS-0.25和PBQS-0.7首次放电比容量分别为99和104 mAh∙g-1。10次充放电循环,放电比容量都出现一定程度的衰减,库仑效率低于90%。充放电过程中存在析氢副反应的影响,低电流密度下,析氢副反应电流所占比例较高,导致库仑效率低;提高电流密度,析氢副反应电流所占比例降低,从而库仑效率提高。因此,随着电流密度的增大,电极的库仑效率随之增至90%以上。当电流密度提高到500 mA∙g-1以上,库仑效率几乎接近100%。在电流密度达到1000 mA∙g-1时,S与Na2S的摩尔比分别为0.25、0.4、0.7时,所制得的PBQS电极放电容量分别降至85、120和90 mAh∙g-1。且当电流密度重新回至100 mA∙g-1时,电极PBQS-0.4的放电比容量可恢复至140 mAh∙g-1,而电极PBQS-0.25和PBQS-0.7的放电容量均有不同程度的降低。由此表明,S与Na2S的摩尔比为0.4时,合成的聚合物醌电极放电比容量最高,且倍率性能和稳定性均优于采用其它两种摩尔比的多硫化钠制备的PBQS电极材料。

图3 以S和Na2S不同摩尔比例制得的PBQS电极的倍率性能Fig.3 Specific capacity and coulomb efficiency vs cycle number of PBQS electrodes
以不同摩尔比的S和Na2S合成的PBQS电极材料循环性能如图4所示。可见,在200 mA∙g-1的电流密度下,三种PBQS电极的库仑效率均保持在95%以上。但是,放电比容量和稳定性差异明显。电极PBQS-0.25首次放电比容量仅有96 mAh∙g-1,随着循环次数的增加,放电比容量衰减较快,循环200次后已降至65 mAh∙g-1,容量保持率仅为67%。电极PBQS-0.4和PBQS-0.7稳定性有显著提高,充放电循环200次,容量保持率均达到80%以上,而PBQS-0.4电极具有更高的放电比容量,电化学性能更优。
3.3材料结构表征
通过电化学手段测试了上述三种PBQS材料的性能差异,为了更好研究它们的结构特点,采用傅里叶变换红外(FTIR)光谱定性分析官能团,并结合元素分析,来定量说明单体聚合过程中取代形式。
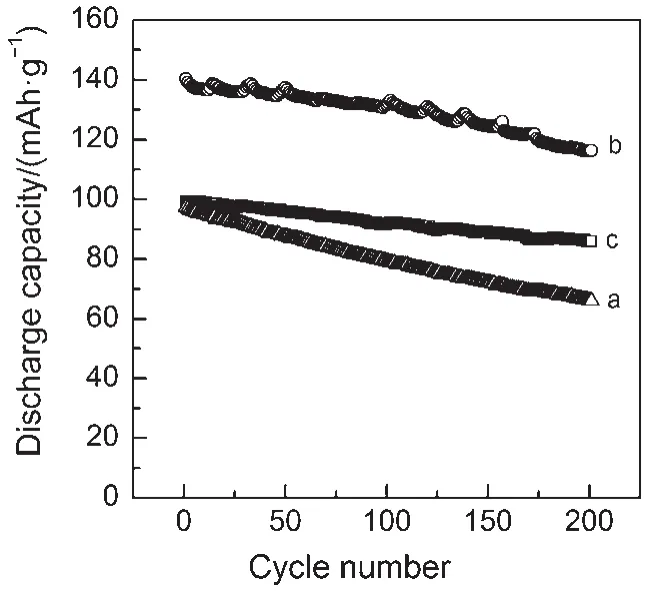
图4 以不同摩尔比的S和Na2S制得的PBQS电极循环性能Fig.4 Galvanostatic cycling of PBQS prepared by different mole ratios of S and Na2S
图5是四氯苯醌(TCQ)和三种PBQS材料的FTIR光谱图。从图中对比可以看出,对于四氯苯醌,在1566、1487 cm-1处的吸收峰是由苯环C=C伸缩振动引起的,在1685 cm-1处的强峰,是对苯醌上的羰基C=O伸缩振动的特征吸收峰;芳环的对位、邻位和间位同时被氯原子取代,在位于1103 cm-1处的强峰与C―Cl14的振动吸收相关。通过硫化单体聚合,在1529 cm-1处出现明显的苯环C=C伸缩振动吸收峰,苯醌上的C=O基特征峰向右偏移至1637 cm-1处,且部分氯被硫取代后,1103 cm-1处C―Cl的振动吸收弱化偏移,在1098 cm-1处出现芳环与S相连的特征吸收峰和C―Cl吸收峰相重叠的宽峰,此外吸收峰的宽化尤以硫含量较高的图5b和5c明显;同时硫化聚合物PBQS在526 cm-1出现较弱的S―S键的伸展振动吸收峰14。由此说明四氯苯醌单体与多硫化钠反应聚合,苯环上的氯原子并未完全取代,但多硫化钠中硫含量越多,硫化聚合的则越完全。为定量说明四氯苯醌硫化聚合过程中氯取代的程度,以下进行了元素分析。

图5 PBQS-0.25(a),PBQS-0.4(b),PBQS-0.7(c)和TCQ(d)的傅里叶变换红外光谱Fig.5 FTIR spectra for(a)PBQS-0.25,(b)PBQS-0.4, (c)PBQS-0.7,and(d)TCQ
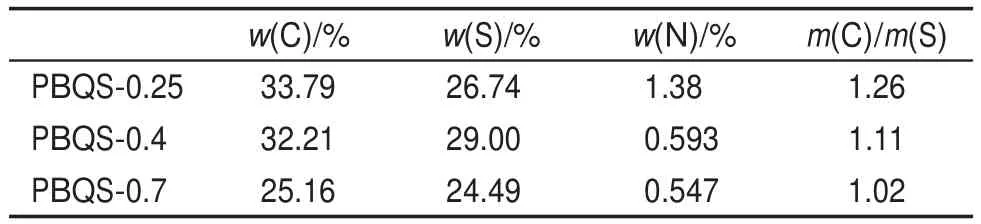
表1 以不同摩尔比的S和Na2S制得的PBQS元素分析Table 1 Element analysis of PBQS prepared bydifferent mole ratios of S to Na2S
表1为三个PBQS样品的元素分析结果。含有微量的N元素可能是由溶剂DMF未完全除去所致。如果四氯苯醌中两个氯原子被取代,则C/S的质量比为1.13。从表1中对比可知,当S与Na2S摩尔比为0.4时,C/S质量比为1.11,合成的PBQS-0.4聚合物的C/S质量比与四氯苯醌单体中两个氯原子被取代时最为接近。而当S与Na2S的摩尔比例为0.25时,S含量较少,C/S质量比增至1.26,取代不完全、聚合程度不高,充放电初始会有微量溶解导致比容量偏低,之后则趋于稳定。聚合物PBQS-0.7中由于S含量偏高,C/S质量比降至1.02,不仅导致循环伏安曲线中电极电位正移(见图1B),而且聚合物中可能形成了不稳定的累积硫硫键,充放电初始也会因少量硫硫键的断裂而导致比容量偏低,之后则趋于稳定。而S与Na2S的摩尔比超过0.7,则S再难溶于Na2S水溶液中。为此,四氯苯醌单体硫化聚合的合成路线的推测如图6所示。四氯苯醌的硫化聚合为阴离子亲核取代反应,因位阻排斥的作用,只在对位发生硫化取代聚合。聚合物-硫代聚苯醌中硫含量不确定,所以相应化学式中S的数量以y表示(见图6),以区别于多硫化钠Na2S1+x中S的含量。依据上述硫化聚合反应过程的测试确定,聚硫代苯醌化学式中y以1计算,得到PBQS理论比容量为224 mAh∙g-1。可见,实测比容量比理论比容量低大约40%。究其原因,电化学窗口问题是主要原因之一,水溶液与有机电解液相比,电化学窗口缩小约50%。但目前水系锂离子电池正极材料如最具应用潜力的LiMn2O4比容量低于120 mAh∙g-1,因此,聚合物醌即使实际比容量仅为理论比容量的40%-50%,在比容量上仍可与正极相匹配。此外,由于材料具有电子绝缘性、非多孔结构、颗粒粒度的影响等,导致材料的电化学活性未得以充分发挥,有待于进一步改进研究。
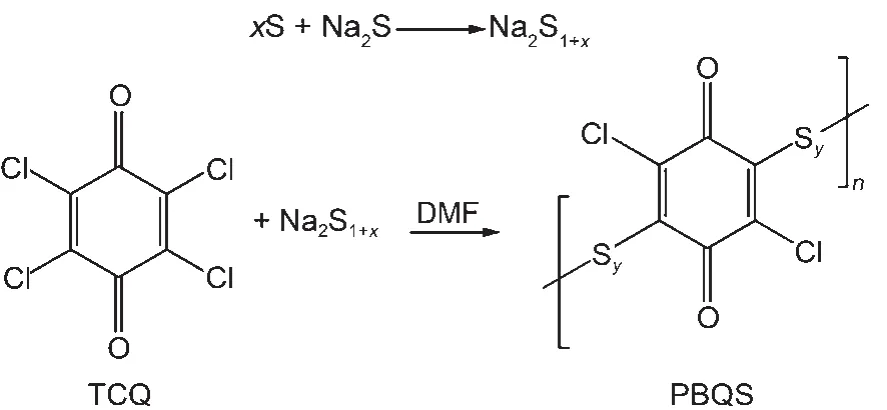
图6 PBQS的合成路线Fig.6 Synthetic route of PBQS
4 结论
通过硫化聚合的方法,以四氯苯醌为单体原料成功合成了硫代聚苯醌。虽然该醌类化合物聚合后的极化有所增大,但有效抑制了四氯苯醌电极在水介质中的溶解,使醌类化合物电极可用于近中性水体系。本文改变S的加入量,探讨了不同摩尔比的S和Na2S对所合成的聚硫代苯醌电极电化学性能的影响。结果表明,当S和Na2S的摩尔比为0.4时,形成两个氯原子被硫取代的PBQS-0.4稳定结构。PBQS-0.4电极放电比容量达到140 mAh∙g-1以上,显现出良好的循环稳定性和优异的倍率性能。而当S和Na2S摩尔比降至0.25时,氯取代不完全、聚合程度不高;S和Na2S摩尔比增至0.7时,聚合物中可能形成了不稳定的累积硫硫键;两方面都导致电极性能明显下降。
References
(1)Li,W.;Mckinnon,W.R.;Dahn,J.R.J.Electrochem.Soc. 1994,141,2310.doi:10.1149/1.2055118
(2)Li,W.;Dahn,J.R.;Wainwright,D.S.Science 1994,264, 1115.doi:10.1126/science.264.5162.1115
(3)Wang,H.B.;Huang,K.L.;Zeng,Y.Q.;Yang,S.;Chen,L.Q. Electrochim.Acta 2007,52,3280.doi:10.1016/j. electacta.2006.10.010
(4)Luo,J.Y.;Cui,W.J.;Ping,H.;Xia,Y.Y.Nature Chem.2010, 2,760.doi:10.1038/nchem.763
(5)West,R.;Powell,D.L.J.Am.Chem.Soc.1963,85,2577.doi: 10.1021/ja00900a010
(6)Tang,Z.Y.;Xu,G.X.Acta Phys.-Chim.Sin.2003,19,307.
[唐致远,徐国祥.物理化学学报,2003,19,307.]doi: 10.3866/PKU.WHXB20030405
(7)Xu,G.X.;Qi,L.;Wen,L.;Liu,G.Q.;Ci,Y.X.Acta Polymerica Sinica 2006,No.6,795.
[徐国祥,其鲁,闻雷,刘国强,慈云翔.高分子学报,2006,No.6,795.]
(8)Liu,K.;Zheng,J.M.;Zhong,G.M.;Yang,Y. Electrochemistry 2009,15,245.
[刘凯,郑建明,钟贵明,杨勇.电化学,2009,15,245.]
(9)Song,Z.P.;Zhan,H.;Zhou,Y.H.Chem.Commun.2009,No. 4,448.doi:101039/B814515F
(10)Gall,T.L.;Reiman,K.H.;Grossel,M.C.;Owen,J.R. J.Power Sources 2003,119,316.doi:10.1016/S0378-7753 (03)00167-8
(11)Jeftic,L.;Manning,G.J.Electroanal.Chem.1970,26,195. doi:10.1016/S0022-0728(70)80303-5
(12)Boschi,T.;Pappa,R.;Pistoia,G.;Tocci,M.J.Electroanal. Chem.1984,176,235.doi:10.1016/S0022-0728(84)80321-6
(13)Chen,H.;Armand,M.;Demailly,G.;Dolhem,F.;Poizot,P.; Tarascon,J.M.ChemSusChem 2008,1,348.doi:10.1002/ cssc.200700161
(14)Dong,Q.N.Infrared Spectroscopy,1st ed.;Petroleum Chemical Industry Press:Beijing,1977;pp 181-197.
[董庆年.红外光谱法.第一版.北京:石油化学工业出版社,1977: 181-197.]
Synthesis and Electrochemical Performance of a Benzoquinone-Based Polymer Anode for Aqueous Lithium-Ion Batteries
CAI Li-Li1WEN Yue-Hua2,*CHENG Jie2CAO Gao-Ping2YANG Yu-Sheng1,2
(1Faculty of Science,Beijing University of Chemical Technology,Beijing 110159,P.R.China;2Research Institute of Chemical Defence,Beijing 100191,P.R.China)
Using the tetrachloro-p-benzoquinone(TCQ)monomer,poly(benzoquinonyl sulfide)(PBQS)was synthesized by a simple polycondensation reaction.The influence of the molar ratio of S to Na2S on the electrochemical performance of a PBQS anode was assessed by changing the amount of S added.The results showed that the electrochemical performance of PBQS strongly depended on the molar ratio of S to Na2S.When the molar ratio of S to Na2S was 0.4,two Cl were replaced by S,and PBQS with a stable structure was obtained. The discharge capacity of PBQS exceeded 140 mAh∙g-1.At the same time,PBQS displayed satisfactory rate capability and excellent cyclability.Conversely,when the molar ratio of S to Na2S was decreased to 0.25,Cl was not substituted completely and the polymerization degree was low.Upon increasing the molar ratio of S to Na2S to 0.7,an unstable S―S bond may form in the polymer.The above two factors degraded the electrode performance of these materials.
Aqueous lithium-ion battery;Polycondensation;Poly(benzoquinonyl sulfide);Mole ratio of S to Na2S;Electrochemical performance
1 引言
基于传统水溶液电池容易制取、成本低的优势,近年来出现了以水相电解液代替有机电解液的水系锂离子电池,以期解决长期困扰有机锂离子电池有关安全性和成本高的难点问题1,2。目前,水系锂离子电池正、负极材料大多参考有机锂离子电池的研究,结合水体系电解液的特点加以引入和改进。与正极材料相比,除析氢副反应影响外,还要考虑空气中氧甚至溶剂水的作用,负极材料的研制更加困难,循环稳定性也更难以保证3,4。与无机材料相比,有机物电极材料具有理论比容量高、廉价、可循环利用和高度可设计等优点,且无需高温烧结,碳排量低,具有绿色合成5的特点;加之有机物可通过聚合进一步提高材料的稳定性,已成为一类具有广泛应用前景的储能介质。有机醌类化合物在电化学反应过程中具有较好的结构稳定性,有望发展成为一类有竞争力的锂二次电池电极材料。目前,醌类聚合物作为正极材料应用于锂二次电池,相关研究日益增多6-8,Song等9通过1,5-二氯蒽醌与硫化钠发生硫化缩聚反应,合成聚硫化蒽醌材料,用于有机锂离子电池正极,比容量做到198 mAh∙g-1,且具有良好的倍率性能和循环稳定性,然而醌类聚合物作为水系锂离子负极材料却鲜有报道。
September 25,2015;Revised:January 4,2016;Published on Web:January 6,2016.*Corresponding author.Email:wen_yuehua@126.com;Tel:+86-10-66748543. The project was supported by the Beijing Key Laboratory ofAdvanced Chemical Energy Storage Technology and Material.
O646
10.3866/PKU.WHXB201601061
北京市先进化学储能技术与材料重点实验室资助项目
