13C-呼气诊断试剂甘氨酸[1-13C]的合成研究
2016-09-02李虎林姜永悦
邱 俊,李虎林, 姜永悦
(上海稳定性同位素工程技术研究中心,上海化工研究院,上海 200062)
13C-呼气诊断试剂甘氨酸[1-13C]的合成研究
邱俊,李虎林, 姜永悦
(上海稳定性同位素工程技术研究中心,上海化工研究院,上海200062)
该合成方法以乙酸[1-13C]为原料,经过Hell-Volhard-Zelinski反应和乙醇酯化得到2-溴乙酸乙酯[1-13C],接着经过Gabriel反应得到N-乙酸乙酯邻苯二甲酰亚胺[1-13C],然后再与肼解和盐酸水解得到13C-呼气试验诊断试剂甘氨酸[1-13C]。同时还探索了关键中间体乙酸乙酯[1-13C]合成工艺,考察了温度、红磷用量和缚酸剂等主要因素,得到了最优合成工艺,使得最终产物甘氨酸[1-13C]总收率为58.4%,化学纯度高于98%以上,13C原子丰度高于98%。
13C-呼气试验;甘氨酸[1-13C];Hell-Volhard-Zelinski反应;Gabriel 反应;合成工艺
目前13C-呼气试验已经较广泛地应用于消化不良等疾病的胃动力测定、胃动力药物的疗效观察、延缓胃排空药物不良反应的监测,以及胃部手术后的胃动力恢复情况评价[1]。同时也逐渐地应用于糖尿病胃轻瘫患者胃动力检测,合理地指导口服降糖药物的用量。以及特护患者及婴儿的胃动力检测,指导口服营养或胃管营养,这样可以减少特护时间,有效地避免脓毒败血症休克的发生[2]。
甘氨酸[1-13C]作为一种13C-呼气试验诊断试剂,在胃内不会分解吸收,以原型进入十二指肠后迅速被吸收并经肝脏代谢为13CO2排出,可作为检测胃对食物排空的示踪剂。因此,13C-甘氨酸呼气试验目前用于液体食物的胃排空速率的测定[3]。其优势在于稳定同位素碳13标记甘氨酸无放射性,可在短期内进行重复的检测;此外还具有操作简便,试验的灵敏度高、特异性好、重现性好等优点。因此甘氨酸[1-13C]在临床检测液体食物胃排空速率的应用中具有良好的发展前景[4-9]。
目前文献报道合成甘氨酸[1-13C]的方法主要是利用13C-甲基镁碳酸酯和硝基甲烷反应得到2-硝基乙酸[1-13C],再经过钯/碳加氢还原得到甘氨酸[1-13C],三步反应总收率为39.4%[10]。而本工作旨在开发另外一种简单高效的甘氨酸[1-13C]合成方法,主要采用乙酸[1-13C]为原料,先进行溴素溴化,然后与乙醇酯化,再与邻苯二甲酰胺钾盐反应得到N-乙酸乙酯邻苯二甲酰亚胺[1-13C],然后进行肼解和盐酸水解得到目标产物甘氨酸[1-13C],该方法与文献报道方法相比,具有原材料便宜,操作简单,成本低,收率更高等特点。
1 实 验
1.1仪器与试剂
ARX400核磁共振仪,美国Bruker公司;WRS-1B数字熔点仪,上海精密科学仪器有限公司;Waters液相色谱仪,美国Waters公司;MAT271气体同位素质谱计,美国Finnigan公司;RE-52B旋转蒸发仪,上海亚荣生化仪器厂。
乙酸[1-13C]:美国CIL公司,13C丰度98.5%;邻苯二甲酰胺钾盐:自制;溴素、红磷、水合肼:国药集团化学试剂有限公司;其他试剂和溶剂均为市售AR级。
1.2合成路线
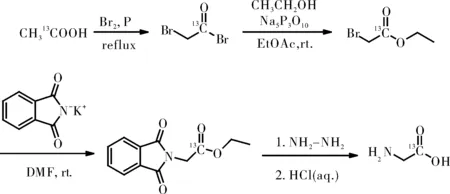
图1 甘氨酸[1-13C]合成路线
1.3合成方法
1.3.1溴代乙酸乙酯[1-13C]的合成[11]
在100 mL三口烧瓶上,安装球形冷凝管和溴化氢气体吸收装置(NaOH水溶液),在反应瓶中加入乙酸[1-13C] (3.05 g 50 mmol)、红磷(0.81 g,25 mmol),磁力搅拌下油浴升温至118 ℃,待稳定后缓慢滴加溴素(5.25 mL,100 mmol),滴完后保温反应,待红棕色褪去,颜色变成淡黄色后移去油浴,冷却至室温,加入50 mL乙酸乙酯,在5 ℃以下搅拌,分批缓慢加入三聚磷酸钠(9.2 g,25 mmol),加入完毕,在常温搅拌15 min,再将无水乙醇(3.45 g,75 mmol)置于恒压滴液漏斗中缓慢滴加,控制反应温度为室温,反应时间5 h,反应完成后过滤,滤液用饱和Na2CO3溶液洗涤至中性,二氯甲烷萃取水溶液。合并有机相用无水Na2SO4干燥过夜,过滤,浓缩蒸掉有机溶剂,得到亮黄色油状液体溴代乙酸乙酯[1-13C],产率为88.3%。1H-NMR (400 MHz, CDCl3, ppm): δ 4.24(q,J=7.6 Hz, 2H,-O-CH2), 3.82(s, 2H, Br-CH2-), 1.31(t,J=7.2 Hz, 3H,-CH3); IR值 (KBr, cm-1): 2963, 2861, 1741, 1465, 1170, 721。
1.3.2N-乙酸乙酯邻苯二甲酰亚胺[1-13C]的合成
在100 mL三口瓶中,加入4.18 g(25 mmol)溴代乙酸乙酯[1-13C]和25 mL DMF,然后再加入邻苯二甲酰亚胺钾盐4.55 g (25 mmol),室温下搅拌12 h,反应液倒入500 mL冰水中,有固体析出,过滤,滤饼用水洗(3×20 mL),固体在60 ℃真空干燥箱中烘6 h,得到5.17 g N-乙酸乙酯邻苯二甲酰亚胺[1-13C]白色固体产品,反应产率为84.1%。m.p.110~111 ℃;1H-NMR (400 MHz, CDCl3, ppm)) δ: 7.82~7.90 (m, 2 H), 7.72~7.77 (m, 2 H), 4.56 (s, 2H-N-CH2-C=O), 4.23 (q,J=7.2 Hz, 2H,-O-CH2), 1.30(t,J=7.2 Hz, 3H,-CH3); IR值 (KBr, cm-1): 3011, 2832, 1737, 1480, 1405, 1329, 1216, 705。
1.3.3甘氨酸[1-13C]的合成[12]
在100 mL三口瓶中,加入3.51 g (15 mmol) N-乙酸乙酯邻苯二甲酰亚胺[1-13C]、60 mL甲醇和30 mmol 85%的水合肼,反应加热回流,搅拌2 h,反应液冷却至室温,反应中有固体析出,过滤,滤饼用甲醇洗(3×20 mL),滤液蒸干得淡黄色固体,再加入50 mL盐酸(6 N),反应加热回流,搅拌2 h后,冷却到0 ℃,过滤除去析出物,减压蒸去盐酸水溶液,以2 mol/L NaOH水溶液中和至中性,在0 ℃放置过夜,析出的白色结晶固体,过滤,固体在60 ℃真空干燥箱中烘6 h,得甘氨酸[1-13C]纯品78.6%,液相色谱分析纯度:98.7%,同位素质谱分析13C原子丰度为98.1%。m.p. 232~234 ℃;1H-NMR (400 MHz, D2O, ppm) δ: 3.76 (s, 2 H, N-CH2-);13C-NMR (100 MHz, D2O, ppm) δ: 173.3(-CO-), 43.4(N-CH2-); IR值 (KBr, cm-1): 3106, 2605, 2172, 1597, 1395, 1333, 929, 685; M/z: 77.3 (M+H)+。
2 结果与讨论
2.1反应温度对溴代乙酸乙酯[1-13C]产率的影响
首先利用乙酸[1-13C]与溴素通过Hell-Volhard-Zelinski反应得到活性高的溴代乙酰溴[1-13C]中间体,然后中间体再与乙醇酯化得到溴代乙酸乙酯[1-13C],第二步反应常温下反应速率快,不易有副产物生成,在这里不做温度考察。因此主要考察第一步反应温度对溴代乙酰溴[1-13C]产率的影响,产物溴代乙酸乙酯[1-13C]反应收率利用HPLC峰面积计算。
选取溴化反应温度为80 ℃、90 ℃、100 ℃、110 ℃、118 ℃(乙酸沸点)。实验结果如表1所示。

表1 温度对溴化反应的影响aTable 1 The effects of temperature on brominationa
a乙酸(50 mmol)、红磷(25 mmol)、溴素(100 mmol)、无水乙醇(75 mmol)、三乙胺(25 mmol)。
从表1数据可以看出,在100~118 ℃范围内,温度的升高,溴代乙酸乙酯产率迅速提高。当温度达到118 ℃时,乙酸回流状态下,产率达到最高。因此118 ℃乙酸回流为最优反应温度条件。
2.2红磷用量对溴代乙酸乙酯产率的影响
众所周知,Hell-Volhard-Zelinski反应最为常用的催化剂为三溴化磷,然而三溴化磷的蒸气与液体都具有强烈刺激性和腐蚀性,不易称取和操作。故参考文献报道方法[11],选用性质稳定且相对便宜的红磷与溴素代替三溴化磷。实验证明,磷与溴素代替三溴化磷催化反应的效果相似。因此考察红磷的投入量对反应收率的影响,按照乙酸(3.0 g, 50 mmol),当量取红磷的投入量为0.2 equiv(0.32 g)、0.3 equiv(0.48 g)、0.4 equiv(0.65 g)、0.5 equiv(0.80 g)、0.6 equiv(0.96 g)。实验结果如表2所示。

表2 红磷用量对溴化反应的影响aTable 2 The effects of phosphorus dosage on brominationa
a乙酸(50 mmol)、溴素(100 mmol)、无水乙醇(75 mmol)、三乙胺 (25 mmol),118 ℃反应。
从表2中可以看出,红磷用量摩尔比从0.2 equiv逐步增加到0.5 equiv时,产率随之增加,当摩尔比为0.5 equiv时,产率达到最高82.6%。同时当红磷用量超过0.5 equiv时,对产品收率影响不明显。因此选择催化剂红磷用量摩尔比为0.5 equiv (0.8 g)。
2.3缚酸剂对溴代乙酸乙酯产率的影响
在溴代乙酰溴中间体与乙醇进行酯化反应中,需要加入碱作为缚酸剂中和反应中生成的溴化氢气体,使得酯化反应更完全。本论文将考察各种缚酸剂对酯化反应收率的影响。实验结果如表3所示。

表3 缚酸剂对酯化反应的影响aTable 3 The effects of acid-accepters on brominationa
a乙酸(50 mmol)、红磷(25 mmol)、溴素(100 mmol),无水乙醇(75 mmol)、缚酸剂(25 mmol),118 ℃反应。
从表3中可以看出,缚酸剂对酯化反应的影响比较大,不加缚酸剂反应产率相对较低,加入有机碱三乙胺和吡啶作为缚酸剂,虽然能得到较好的收率,但是存在后处理分离困难等缺点。当加入无机碱碳酸钠作为缚酸剂,产率反而相对较低,而利用三聚磷酸钠作为缚酸剂,产率则达到最高产率88.3%。根据机理上分析1 mol三聚磷酸钠吸附2 mol溴化氢,产物仍显碱性,反应依然能在碱性环境下进行,因此产率最高。因此选择无机碱三聚磷酸钠作为缚酸剂
2.4溴代乙酸乙酯[1-13C]最优合成工艺
综上所述,由乙酸[1-13C]为起始原料合成溴乙酸乙酯[1-13C]的优化条件为:乙酸[1-13C] (3.05 g, 50 mmol),红磷(0.80 g, 0.5 equiv),反应温度为118 ℃,溴素(5.25 mL, 100 mmol),三聚磷酸钠(9.2 g, 25 mmol)为缚酸剂,无水乙醇(3.45 g, 75 mmol),常温反应5 h,结束反应。在此最优条件下进行5次平行验证,考察反应重现性。实验结果如表4所示。
从表4可以看出,同样条件下的5次平行试验结果波动较小,目标产品溴乙酸乙酯[1-13C]的产率比较稳定。该优化反应条件其重现性和可靠性均较高。
3 结 论
(1)以乙酸[1-13C]为原料,先后经过Hell-Volhard-Zelinski反应、Gabriel反应和肼解等三步反应制备得到目标产物甘氨酸[1-13C],总收率为58.4%。
(2) 探索了关键中间体溴乙酸乙酯[1-13C]合成工艺,考察了温度、红磷用量和缚酸剂等主要因素,得到了最优合成工艺条件,5次平行试验结果显示该优化工艺具有重现性和稳定性。
(3) 甘氨酸[1-13C]经过熔点、LC、MS和IR检测,确认产品化学结构,化学纯度高于98%,13C原子丰度高于98%,13C同位素稀释效应小于0.5%。
[1]Perri F, Pastore Mr, Annsese V.13C-octanoic acid breath test for measuring gastric emptying of solids[J]. Eur Rev Med Pharmacol Sci, 2005, 9(5): 3-8.
[2]毛奇琦, 孙旭, 严惟力.13C-呼气试验一种有益的消化系统疾病检测方法[J]. 国际放射性医学核医学杂质, 2009, 3(3):129-133.
[3]Duan L, Braden B, Caspary W, Lembke B. Influence of cisapride on gastric emptying of solids and liquids monitored by13C-breath tests[J]. Dig Dis Sci,1995, 40(10):2200-2206.
[4]Maes B, Hiele M, Geypens B, Rutgeers P, Ghoos Y, Vanterrappen G. Pharmacological modulation of gastric emptying rate of solids as measured by the carbon labelled octanoic acid breath test: influence of erythromycin and propantheline[J]. Gut,1994, 35(3):333-337.
[5]Kure S, Korman SH, Kanno J, Narisawa A, Kubota M, Takayanagi T, Takayanagi M, Saito T, Matsui A, Kamada F, Aoki Y, Ohura T, Matsubara Y. Rapid diagnosis of glycine encephalopathy by13C-glycine breath test [J]. Annals of neurology, 2006, 59(5):862-867.
[6]黄晓璐, 曲新华, 蔡铭慈,等.13C-呼气试验在胃排空定量检查中的应用[J].中华全科医师杂志, 2009, 8(9): 645-646.
[7]Maes B, Ghoos Y F, Geypens B, et al. Combined13C-glycine/14C-octanoic acid breath test to monitor gastric emptying rates of liquids and solids[J]. Journal of Nuclear Medicine, 1994, 35(5):824-831.
[8]Scarpellini E, Abenavoli L, Balsano C, et al. Breath tests for the assessment of the orocecal transit time[J]. European Review for Medical and Pharmacological Sciences, 2013, 17(12):39-44.
[9]Maes B, Ghoos Y, Spitz B, et al. Gastric emptying rate of solids in non-dyspeptic pregnant women, using the13C-octanoic acid breath test[J].Gastroenterology,1993,104(4):A546-A546.
[10]Nakajima T, Nakayama K, Shimizu I. Synthesis of isotope-labelled [1-13C]-amino acids from13CO2[J]. J. Label. Compd. Radiopharm, 2007, 50(5):622-623.
[11]Iida K, Tokiwa S, Ishii T, et al. Synthesis of 5-[4,5-13C2]-and 5-[1,5-13C2] aminolevulinic acid[J]. J. Label. Compd. Radiopharm, 2002, 45(5): 569-576.
[12]郝永兵,祝振福,胡先明.甘氨酸叔丁酯的简便合成[J]. 广东化工, 2010, 40(3):134-135.
A Synthetic Method of the Diagnostic Reagent of13C-Glycine Breath Test
QIU Jun, LI Hu-lin, JIANG Yong-yue
(Shanghai Engineering Research Center of Stable Isotope, Shanghai Research Instituteofchemicalindustry,Shanghai200062,China)
The acetic acid [1-13C] was used as raw material to generate ethyl bromoacetate [1-13C] by Hell-Volhard-Zelinski reaction and esterification reaction. Subsequently, N-phthaloyl glycine ethyl ester[1-13C] was obtained from ethyl bromoacetate[1-13C] by Gabriel reaction, then reacted with hydrazine hydrate to produce the diagnostic reagent glycine[1-13C]. The influences of parameters, such as temperature, the mole ratio red phosphorus to acetic acid [1-13C], acid-accepters on the yield of products, were investigated, and the optimized conditions were obtained. The yield of glycine[1-13C] was above 58.4%, the purity≥98%, the abundance of 13C≥98%.
13C-breath test; glycine[1-13C]; Hell-Volhard-Zelinski reaction; Gabriel reaction; synthesis technology
邱俊(1984-),男,博士,工程师,主要从事同位素标记药物研发。
O628.2+1
A
1001-9677(2016)013-0084-03
