β-环糊精增敏橙黄IV分光光度法测定亚硝酸根离子*
2016-09-01陈小燕李和平刘万毅
陈小燕,李和平,李 冰,刘万毅
(宁夏大学化学化工学院,宁夏 银川 750021)
分析测试
β-环糊精增敏橙黄IV分光光度法测定亚硝酸根离子*
陈小燕,李和平,李冰,刘万毅
(宁夏大学化学化工学院,宁夏银川750021)

β-CD;橙黄IV;紫外-可见光谱法;增敏;亚硝酸根离子
亚硝酸盐常被用作食品着色剂和防腐剂,还用于织物的染色、漂白等[1]。但饮用水和食物中亚硝酸盐超过一定含量就会对人体有害,它会与胺类反应生成致癌的亚硝基化合物。所以美国公共卫生协会规定亚硝酸盐的饮用水限量为60 μg·L-1,可接受的每日摄入量小于0.07 mg·kg-1[2]。因此,在环境监测和食品加工中要对亚硝酸根离子进行严格地控制和监测。目前有许多关于测定亚硝酸盐的方法,如分光光度法[3-4],荧光光谱法[5-6],电化学法[7-8],色谱法[9]等。天然水和食品中亚硝酸根离子的测定主要用分光光度法,较经典方法是基于重氮化偶联反应和亚硝化反应。β-CD独有的“内疏水,外亲水”的中空斜截锥形的结构可与有机分子形成主客体包合物[10]。本研究在橙黄IV与微量亚硝酸根离子发生亚硝化反应[11]的基础上,加入β-CD与亚硝化产物通过氢键作用和疏水作用形成超分子包合物,使其明显提高体系的吸光度,达到增敏的效果。以期建立测定亚硝酸根离子的新的分析测试方法。
1 实验部分
1.1仪器与试剂
TU-1810SPC型紫外-可见分光光度计,北京普析通用仪器有限公司;HH-6型恒温水浴锅,北京长源实验设备厂;KQ5200DE型超声波清洗器,昆山市超声仪器有限公司;101A-1B型鼓风干燥箱,上海实验仪器厂有限公司;BSA224S型电子分析天平,赛多利斯科学仪器(北京)有限公司。
NaNO2标准溶液:用干燥过的NaNO2(分析纯)和蒸馏水配制0.2 g·L-1的储备液,100 mL溶液中加入氯仿0.4 mL以抑制细菌生长,避光冷存,使用时稀释为4 mg·L-1的工作液;橙黄IV(分析纯),分别用蒸馏水配制0.2 g·L-1和1.0×10-4mol·L-1的溶液;β-CD(化学纯),重结晶两次后配制0.01 mol·L-1的水溶液;HCl(分析纯),配制0.5 mol·L-1的水溶液; pH=1的KCl/HCl缓冲溶液:100 mL 0.2 mol·L-1KCl水溶液和194 mL 0.2 mol·L-1HCl溶液混合均匀。实验用水为蒸馏水。
1.2实验方法
1.2.1β-CD与橙黄IV包合物的形成
准确移取1.0×10-4mol·L-1橙黄IV溶液1.00 mL于10 mL的比色管中,加入1.00 mL的β-CD(0.01 mol·L-1)溶液,再加入pH=1的KCl/HCl缓冲溶液2.00 mL,加蒸馏水至刻度,混匀,超声5 min,室温静置30 min。另分别移取1×10-4mol·L-1的橙黄IV溶液1.00 mL和β-CD溶液1.00 mL于10 mL比色管中,按照相同步骤处理。以蒸馏水为参比,分别测定橙黄IV+β-CD、橙黄IV和β-CD三种溶液体系的吸光度。
1.2.2不同温度下橙黄IV和β-CD包合常数Ka的测定
移取1.0×10-4mol·L-1的橙黄IV溶液各1.00 mL于8支10 mL比色管中,依次加入0.01 mol·L-1的β-CD溶液0 mL、0.50 mL、1.00 mL、2.00 mL、3.00 mL、4.00 mL、5.00 mL、6.00 mL,再加入pH=1的KCl/HCl缓冲溶液2.00 mL,用蒸馏水稀释至刻度并摇匀,超声5 min,于恒温水浴中分别在298 K、308 K、318 K、328 K、338 K下静置30 min,根据不同温度下测定的溶液吸光度值与不加β-CD的吸光度值之差,再结合Hildebrand-Benesi方程[12-13],得出在不同温度下的稳定常数Ka列于表1中。
1.2.3β-CD对橙黄IV与亚硝酸根反应的影响
在25 mL比色管中,加入5 mL NaNO2标准溶液,0.2 g·L-1橙黄IV溶液2.00 mL,加水至10 mL,再加入0.5 mol·L-1HCl溶液2.0 mL,加入一定量的β-CD溶液,用蒸馏水定容至刻度并摇匀,静置15 min。以试剂空白为参比,用1 cm比色皿,在348 nm和526 nm波长处测定溶液吸光度(分别记为A348,A526)。以双波长叠加法计算吸光度A=A348+A526,通过吸光度确定加入β-CD的用量。
2 结果与讨论
2.1包合物的形成
在客体分子被包合后,最大吸收波长会红移或蓝移,而且吸光度会发生变化[12]。图1分别为橙黄IV(1.0×10-5mol·L-1)+β-CD(1.0×10-3mol·L-1)、橙黄IV(1.0×10-5mol·L-1)和β-CD(1.0×10-3mol·L-1)三种溶液的吸收曲线,可看出β-CD几乎没有吸收,而橙黄IV在加入β-CD后,最大吸收波长从529 nm 蓝移至448 nm。说明橙黄IV与β-CD形成了包合物。β-CD的内腔是疏水性的,所以极性大的化合物和带电的离子均不易进入β-CD的空腔[13]。由于橙黄IV分子的一端为疏水性的苯环,另一端的苯环上连有—SO3Na基团(见图2),所以极有可能橙黄IV疏水端的苯环被β-CD包合,包合反应式如图2。

图1 三种溶液的吸收曲线图
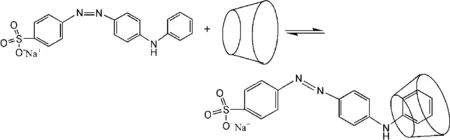
图2 橙黄IV和β-CD的包合反应方程式
2.2温度对橙黄IV和β-CD包合常数Ka的影响
运用紫外-可见分光光度法研究不同温度下的包合常数,测定最大吸收波长λmax=529 nm,假设橙黄IV和β-CD形成1:1的包合物,根据Hildebrand-Benesi方程及相应的数据处理,可得到1/ΔA~1/[CD]0的线性方程及包合常数(见表1)。

表1 不同温度下的包合常数
由表1可知,随着温度升高,包合常数呈减小趋势,说明升高温度不利于包合反应的进行。而且,由Hildebrand-Benesi方程得出橙黄IV和β-CD都形成了包合比为1:1的包合物。
2.3β-CD增敏橙黄IV测定亚硝酸根离子
2.3.1β-CD用量对吸光度的影响
在室温下,按1.2.3步骤加入其他试剂后,依次加入表2中不同量的β-CD溶液,由吸光度A,确定β-CD的最佳用量。

表2 加入不同量β-CD的溶液吸光度变化
由表2看出,随着β-CD加入量的增加,溶液的吸光度逐渐增大,这可能因为一部分橙黄IV先与NaNO2进行亚硝化反应,生成的-NO基团与已包合橙黄IV的β-CD的伯羟基形成氢键(图3),促使包合反应的进行,并使体系的吸光度增大。当β-CD加入量大于0.40 mL时,多余的β-CD不会产生吸收峰,吸光度趋于稳定,所以β-CD的最佳用量为0.40 mL,此时吸光度比不加β-CD增加0.228。

图3 β-CD与橙黄IV的亚硝化产物形成的氢键示意图
2.3.2橙黄IV用量的影响
按照步骤1.2.3的实验方法,考察不同橙黄IV用量对吸光度的影响,结果表明当0.2 g·L-1橙黄IV溶液用量为2.00 mL时,吸光度值最大,本实验选用0.2 g·L-1橙黄IV 2.00 mL(见表3)。

表3 橙黄IV用量的影响
2.3.3显色时间的影响
吸光度随显色时间的变化如图4所示,结果表明,当显色时间在10 min后,吸光度达到最大且比较稳定。故本实验显色时间在15 min。

图4 显色时间的影响
2.3.4工作曲线

2.3.5共存离子的影响

2.3.6样品回收率的测定
标准加入法测定回收率结果见表4。

表4 样品回收率的测定
3 结 论

[1]郭世珺,曾常春,李丽君. 亚硝酸钠化高铁血红蛋白的拉曼光谱量化检测研究[J]. 光谱学与光谱分析,2013,33(7):1805-1809.
[2]Yu-Xian Guo, Qing-Feng Zhang, Xincheng Shangguang, et al. Spectrofluorimetric determination of trace nitrite with o-phenylenediamine enhanced by hydroxypropyl-β-cyclodextrin [J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2013, 221 (101): 107-111.
[3]唐清华,陈玉静. 双波长催化光度法测定痕量亚硝酸根[J]. 分析科学学报,2010,26(3):370-372.
[4]董彦,吕春玲. 基于亚硝化反应分光光度法测定亚硝酸根[J]. 光谱学与光谱分析,2001,21(5):710-712.
[5]刘奇,魏静娟,王爱军. β-环糊精增敏中性红荧光猝灭法测定痕量亚硝酸根[J]. 分析试验室,2011,30(7):6-9.
[6]Feng Gao, Li Zhang, Lun Wang, et al. Ultrasensitive and selective determination of trace amounts of nitrite ion with a novel fluorescence probe mono[6-N(2-carboxy-phenyl)]-β-cyclodextrin[J]. Analytica Chimica Acta, 2005, 533 (1): 25-29.
[7]刘赵荣,王玉春,弓巧娟. 电化学掺铜(Ⅱ)类普鲁士蓝膜修饰电极的制备及其对亚硝酸根的测定[J]. 分析化学,2010,38(7):1040-1043.
[8]汪雪,李辉,吴敏,等. 石墨烯-壳聚糖/金纳米粒子修饰电极同时测定亚硫酸根和亚硝酸根[J]. 分析化学,2013,41(8):1232-1237.
[9]徐霞,应兴华,段斌武,等. 膜渗透与离子色谱联用技术测定蔬菜中亚硝酸盐和硝酸盐[J]. 分析化学,2007,35(11):1586-1590.
[10]陈鸿雁,陈善全,宋伟,等. β-环糊精与肉桂醇包结物的制备及包结性能的研究[J]. 化学研究与应用,2014,26 (4): 566-571.
[11]徐红,刘绍璞,罗红群. 橙黄IV分光光度法测定微量亚硝酸根[J]. 理化检验(化学分册),2006,42(11):949-950.
[12]Abdulilah Dawoud Bani-Yaseen, Abeer Mo’ala. Spectral, thermal, and molecular modeling studies on the encapsulation of selected sulfonamide drugs in β-cyclodextrin nano-cavity[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2014, 131: 424-431.
[13]童林荟. 环糊精化学—基础与应用[M]. 北京:科学出版社,2001.
Determination of Nitrite Ion by β-cyclodextrin Sensitizing Orange IV with UV-vis Spectroscopy*
CHEN Xiao-yan, LI He-ping, LI Bing, LIU Wan-yi
(School of Chemistry and Chemical Engineering, Ningxia University, Ningxia Yinchuan 750021, China)
A new method was developed for the determination of nitrite ion by β-cyclodextrin (β-CD) sensitizing orange IV being supramolecular inclusion of β-CD and orange IV. The result showed that 1:1(orange IV:β-CD) inclusion complexes were formed, higher temperature did not favor the inclusion reaction concluded from the binding constants at different temperatures. The inclusion of β-CD and nitrosation product from orange IV enhanced obsorbance, thus increased the sensitivity of the determination. Beer’s law was obeyed over the range of 0~0.82 μg·mL-1for nitrite ion.
β-CD; orange IV; UV-Vis spectroscopy; sensitization; nitrite ion
国家自然科学基金资助项目(21266025)。
陈小燕(1978-),女,高级实验师,主要从事有机合成及分析方面的研究。
O657.3
A
1001-9677(2016)01-0109-03
