厄洛替尼联合全脑放疗对非小细胞肺癌脑转移患者的临床疗效及预后影响
2016-08-31刘学啸杜德希田智峰程慧斐
刘学啸,杜德希,田智峰,程慧斐
(丽水市中心医院 放疗科,浙江 丽水 323000)
厄洛替尼联合全脑放疗对非小细胞肺癌脑转移患者的临床疗效及预后影响
刘学啸Δ,杜德希,田智峰,程慧斐
(丽水市中心医院 放疗科,浙江 丽水 323000)
目的探讨厄洛替尼联合全脑放疗(whole brain radiotherapy,WBRT)治疗非小细胞肺癌(non-small cell lung cancer,NSCLC)脑转移患者的临床效果及预后影响。方法选取2013年9月~2015年5月丽水市中心医院收治的NSCLC脑转移患者100例,根据患者是否使用厄洛替尼分为对照组54例和观察组46例,2组均给予WBRT治疗,对比2组患者的近期效果、远期预后及不良反应发生率。结果观察组的缓解率52.17%显著高于对照组27.78%,观察组总有效率91.30%显著高于对照组72.22%,差异均具有统计学意义(P<0.05);观察组的1年生存率52.17%(24/46)显著高于对照组29.63%(16/54),观察组中位生存时间9.0个月显著高于对照组6.0个月,差异均具有统计学意义(P<0.05);2组治疗过程中不良反应发生率差异均无统计学意义。结论厄洛替尼联合WBRT治疗NSCLC脑转移患者能够提高近期疗效及远期预后的效果。
厄洛替尼;放疗;非小细胞肺癌;脑转移;预后
非小细胞肺癌(NSCLC)是临床上较为常见的恶性肿瘤,相关研究显示NSCLC的发病率可达0.007%以上,且近年来有明显上升趋势[1],NSCLC的临床预后较差,病死率较高[2]。目前,放疗仍然是临床治疗NSCLC合并脑转移的主要方式,通过放疗可以促进脑组织中转移的肿瘤细胞凋亡,降低患者的病死率,改善远期生存时间。但全脑放疗的临床有效率较低,治疗有效率不足35%,且患者的五年生存率改善不明显,不良反应较多[3-4]。厄洛替尼是一种靶向治疗药物,可特异性地针对肿瘤细胞作用,抑制肿瘤的形成和生长[5]。本研究选取2013年9月~2015年5月丽水市中心医院收治的100例NSCLC脑转移患者,探讨厄洛替尼联合全脑放疗治疗NSCLC脑转移患者的临床效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2013年9月~2015年5月丽水市中心医院收治的NSCLC脑转移患者100例,根据患者是否使用厄洛替尼分为放疗组和放化疗组。其中对照组54例,男37例,女17例;年龄55~81岁,平均(68.9±11.3)岁;TNM分期均属于Ⅳ期;脑皮层电图(electrocorticogram,ECOG)评分:0~1分32例、2~3分22例;原发病灶病理:腺癌50例、鳞癌4例。观察组46例,男32例,女14例;年龄52~78岁,平均(67.1±10.3)岁;TNM分期均属于Ⅳ期;ECOG评分:0~1分28例、2~3分18例;原发病灶病理:腺癌42例、鳞癌4例。2组患者的年龄、性别、原发病灶病理类型、TNM分期、ECOG评分等一般资料比较差异无有统计学意义。本试验方案获患者知情同意并签署知情同意书,得到医院相关伦理委员会批准。
纳入标准:①经病理学证实为NSCLC的患者;②TNM分期属于Ⅳ期,ECOG评分0~3分;③放化疗治疗前患者的外周血白细胞(white blood cell,WBC)>4.0×109/L,血小板计数>100×109/L,中性粒细胞计数>1.5×109/L,血红蛋白(Hb)>100 g/L;④颅内具有可测量病灶。排除标准:①预计生存时间<4 w;②伴有严重的肝肾功能障碍;③伴有活动性感染、系统其他肿瘤;④未能完成治疗的患者。
1.2 方法
1.2.1 治疗方法:对照组采用美国VARIAN公司出产的Clinac ix数字化数控直线加速器进行放疗治疗,能量射线设置为6MX,采用三维适形放疗技术,单次放疗剂量为3 Gy,1次/天,5次/周,总放疗剂量为30 Gy/10 Fx。观察组在对照组的基础上联合进行厄洛替尼治疗,150 mg/d,1次/天,直至放疗结束。随访1年。
1.2.2 疗效评价指标:参照RECIST实体瘤疗效评价标准分为:完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD)。CR:可见病灶完全消失,维持一个月以上,无新病灶出现;PR:肿瘤最大直径及最大垂直直径的乘积缩小达到50%以上;SD:肿瘤最大直径及最大垂直直径的乘积缩小<50%,增大<25%;PD:患者出现一个或多个病灶的肿瘤最大直径及最大垂直直径的乘积>25%。缓解率=(CR+PR)/本组样本量×100%,总有效率=(CR+PR+SD)/本组样本量×100%。
1.2.3 不良反应:参照WHO不良反应5级分级标准:0度:无不良反应;Ⅰ度:轻度不良反应;Ⅱ度:中度不良反应;Ⅲ度:重度不良反应;Ⅳ度:有严重的并发症。Ⅰ度、Ⅱ度、Ⅲ度、Ⅳ度为发生不良反应。

2 结果
2.1 2组患者的近期疗效比较 观察组的缓解率52.17%显著高于对照组27.78%,观察组总有效率91.30%显著高于对照组72.22%,差异均具有统计学意义(P<0.05)。见表1。

表1 2组近期疗效比较[n(%)]Tab.1 Comparison of short-term efficacy between two groups[n(%)]
*P<0.05,与对照组比较,compared with control group
2.2 2组患者的预后观察比较 2组患者随访时间为4~12个月,对照组失访4例,观察组失访3例;观察组的1年生存率52.17%(24/46)显著高于对照组29.63%(16/54),观察组中位生存时间9.0个月显著高于对照组6.0个月,差异均具有统计学意义(χ2=5.260,Log Rank (Mantel-Cox)=7.724,P<0.05)。见图1。
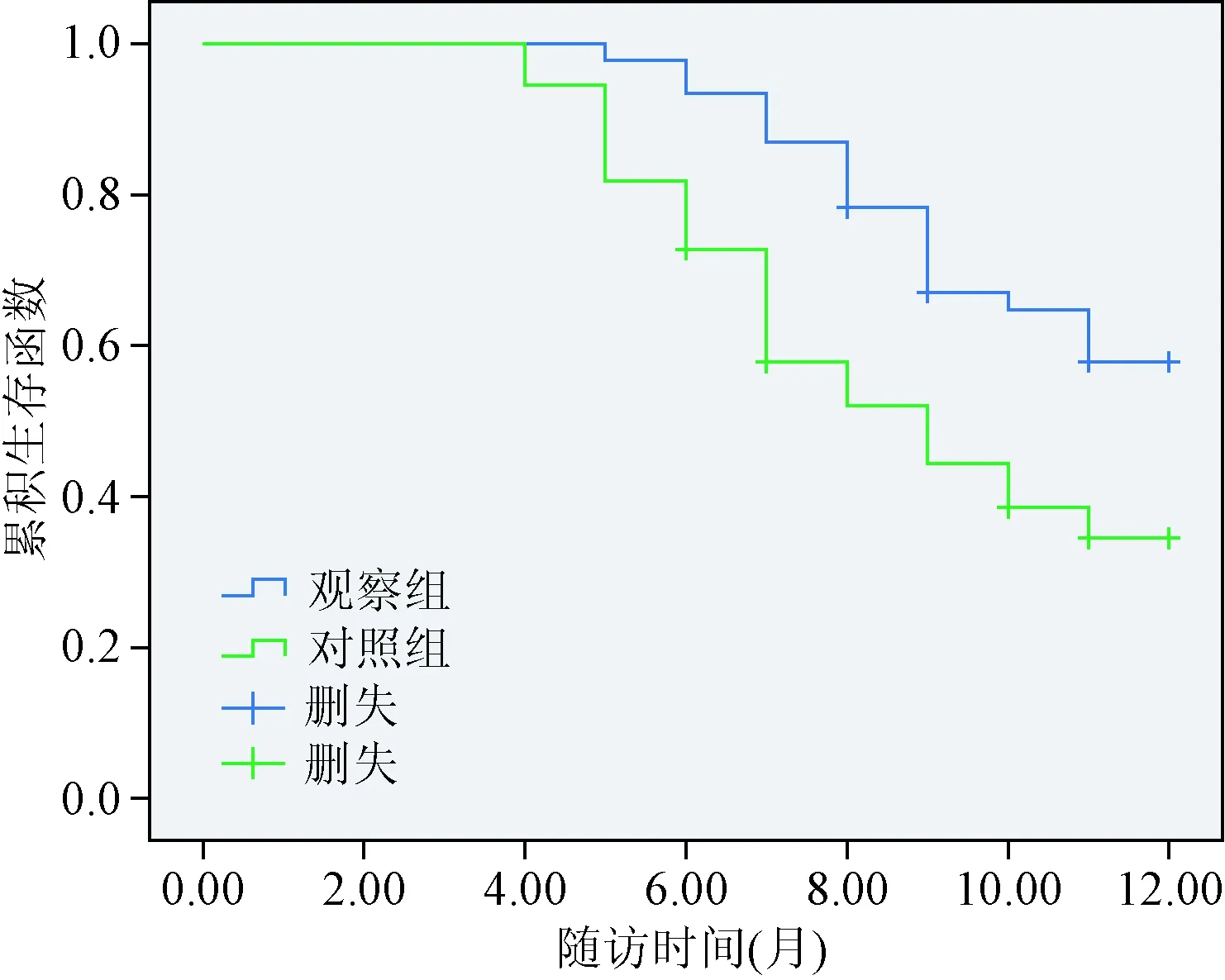
图1 2组患者生存函数图Fig.1 Survival function map of two groups
2.3 2组患者的不良反应情况 治疗过程中,2组不良反应发生率比较差异均无统计学意义。见表2。
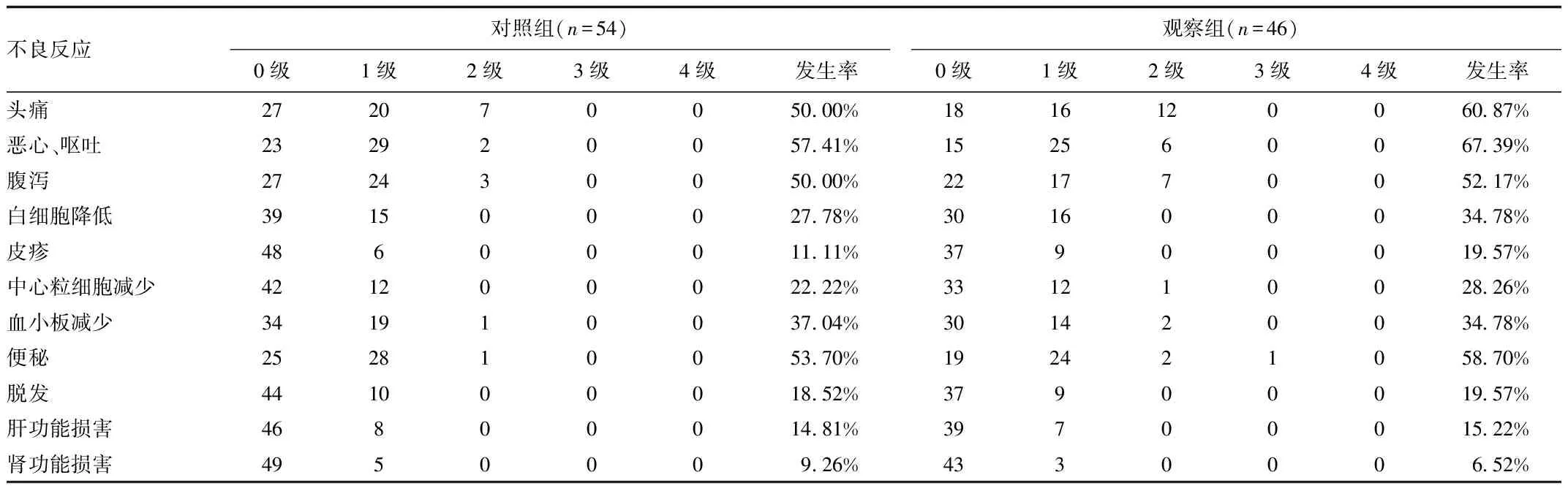
表2 2组不良反应发生率比较
3 讨论
NSCLC脑转移患者占NSCLC肿瘤的1%~3%,年发病率约为10~20人/100万,多发于中老年患者,在吸烟的男性人群中,其发病率更高[6]。对于NSCLC脑转移患者,放疗仍然是临床主要治疗方法,全脑放疗治疗可以显著改善患者脑组织压迫症状,并在一定程度上抑制疾病的进展[7- 8]。然而相关研究证实,NSCLC脑转移患者放疗治疗的复发转移率高,可达55%~90%[9],且放疗治疗后患者生存时间或者五年生存率无显著价值,患者的平均生存时间不足24个月[10-11],提示单纯全脑放疗治疗NSCLC脑转移患者的局限性。特别是对于复发转移以及临床评估不能彻底切除的NSCLC脑转移患者,全脑放疗治疗疾病缓解率不足15%,且放化疗严重的不良反应可加剧中枢神经系统远期后遗症[12]。
络氨酸激酶作为新型的分子靶向治疗靶点,在NSCLC患者血清以及外科手术术后切除病灶中的阳性表达率较高,特别是在鳞状细胞癌(鳞癌)、腺癌、大细胞癌等NSCLC中,络氨酸激酶的表达率可较基础水平上升3~4倍。络氨酸激酶与肿瘤细胞的生长、增殖有密切关系。厄洛替尼作为络氨酸激酶特异性的抑制物,可以通过影响基因转录水平的改变进而调控肿瘤细胞,抑制G1/S期跨越速度、稳定细胞增殖周期,进而抑制NSCLC细胞增殖。本次研究的创新性在探讨厄洛替尼联合全脑放疗治疗NSCLC脑转移患者的临床效果,以及临床安全性等问题。
本研究发现,在全脑放疗治疗的基础上联合厄洛替尼治疗可以改善脑转移患者的近期疗效,NSCLC脑转移患者的病情缓解率及治疗总体效率均明显高于对照组(P<0.05),提示联合厄洛替尼治疗NSCLC脑转移患者的重要意义。厄洛替尼可以通过抑制表皮生长因子或者络氨酸激酶受体,进而拮抗相关肿瘤信号通路激活导致的癌细胞复发和转移,抑制病情的进展,促进残留肿瘤细胞的凋亡,改善病情。杨金山等[13-14]通过前瞻性分析了82例样本量的NSCLC脑转移患者的临床资料,发现厄洛替尼联合全脑放疗可以提高15%的近期病情缓解率,并提高10%的临床总体治疗有效率,与本研究的结论基本一致。
对于联合厄洛替尼远期疗效的评估可以发现,厄洛替尼联合全脑放疗可以显著改善脑转移患者的生存时间和生存率,本研究结果显示,观察组的1年生存率52.17%显著高于对照组29.63%,观察组中位生存时间9.0个月显著高于对照组6.0个月,差异均具有统计学意义(P<0.05),提示厄洛替尼联合治疗在NSCLC中的作用,厄洛替尼可以通过抑制肿瘤复发,降低全脑放疗后肿瘤边缘病灶组织中残留的肿瘤细胞阳性率,进而改善远期生存预后。但需要注意的是,杨金山等的研究并未发现放疗联合厄洛替尼可以提高患者的中位生存时间,这与本研究的结论存在一定的差别,考虑可能是由于临床资料的纳入排除标准的不一、随访时间的不同等导致最终研究结论有所差别。最后,本研究发现,放疗联合厄洛替尼治疗的临床安全性较为可靠,患者的胃肠道反应及骨髓抑制等发生率并无明显上升的趋势。
综上所述,对于NSCLC发生脑转移的患者,在全脑放疗治疗的基础上联合厄洛替尼可以提高病情的近期及远期治疗效果,且临床安全性较为可靠。后续研究可以增加对于厄洛替尼治疗后MSCLC的复发率问题的研究。
[1] 鲍亮,赵弘卿,吕蕾.吉非替尼辅助治疗非小细胞肺癌脑转移临床观察[J].中国实用神经疾病杂志,2016,24(11):78-79.
[2] Courtin A, Smyth T, Hearn K, et al.Emergence of resistance to tyrosine kinase inhibitors in non-small-cell lung cancer can be delayed by an upfront combination with the HSP90 inhibitor onalespib[J].Br J Cancer,2016,25(5):90-92.
[3] 戴宇翃,孙越,张鹏.埃克替尼治疗30例非小细胞肺癌脑转移疗效及不良反应的初步分析[J].解放军医学杂志,2016,32(6):492-495.
[4] 胡潺潺,连相尧,朱翠敏,等.厄洛替尼对非小细胞肺癌脑转移细胞PC14/B侵袭转移能力的抑制作用[J].中国临床药理学杂志,2016,24(12):1118-1120.
[5] Lee AJX, Benamore R, Hofer M, et al.Leptomeningeal carcinomatosis in non-small-cell lung cancer: initial response to erlotinib followed by relapse despite continuing radiological resolution of disease[J].Oxford Medical Case Reports,2016,26(9):69-72.
[6] Shinde R, Cao X, Kothari S.Biopsy Procedures and Molecular Testing Utilization and Related Costs in Patients with Metastatic Lung Cancer[J].J Man Care & Spe Pharm,2016,22(10):1194-1203.
[7] 李豆豆,姜燕慧,毕卓菲,等.全脑放疗联合厄洛替尼治疗非小细胞肺癌脑转移的效果[J].广东医学,2015,25(15):2412-2414.
[8] 李沫,纪秀杰,周迪.厄洛替尼联合全脑放疗治疗非小细胞肺癌脑转移的临床疗效[J].中国老年学杂志,2015,24(18):5184-5186.
[9] 石远凯,孙燕,于金明,等.中国晚期原发性肺癌诊治专家共识(2016年版)[J].中国肺癌杂志,2016,22(1):1-15.
[10] 万欣,王军,曹峰,等.厄洛替尼加减脑部放疗治疗非小细胞肺癌脑转移临床观察[J].中国医师杂志,2016,18(5):653-658.
[11] 王建军,陈绍华,李国明,等.伽玛刀联合吉非替尼治疗非小细胞肺癌脑转移瘤的疗效分析[J].国际呼吸杂志,2016,36(8):576-579.
[12] Zhou Q,Yang J,Chen Z,et al.Serial cfDNA assessment of response and resistance to EGFR-TKI for patients with EGFR-L858R mutant lung cancer from a prospective clinical trial[J].J Hematol & Oncol,2016,9(1):102-104.
[13] 杨金山,魏传芳,吴晓阜.厄洛替尼辅助全脑放疗治疗肺癌脑转移的临床疗效[J].中国肿瘤临床与康复,2015,32(10):1200-1202.
[14] 占明,高宝安.颅脑放疗联合吉非替尼治疗肺癌合并脑转移老年女性患者的效果及不良反应[J].广西医科大学学报,2016,24(2):322-324.
(编校:苗加会)
PrognosisandclinicaleffectoferlotinibcombinedWBRTinpatientswithbrainmetastasesofnon-smallcelllungcancer
LIU Xue-xiaoΔ, DU De-xi, TIAN Zhi-feng, CHENG Hui-fei
(Department of Radiotherapy, Lishui Central Hospital, Lishui 323000, China)
ObjectiveTo investigate the prognosis and clinical effect of erlotinib combined WBRT in patients with brain metastases of non-small cell lung cancer.Methods100 cases of NSCLC patients from September 2013 to May 2015 in our hospital with brain metastases were collected,according to whether patients with erlotinib were divided into control group 54 cases and observation group 46 cases,both two groups were given WBRT treatment,the short-term effects, long-term prognosis and adverse reactions were compared between the two groups.ResultsThe remission rate in observation group 52.17% was significantly higher than control group 27.78%,the total effective rate in observation group 91.30% was significantly higher than control group 72.22%,the difference was statistically significant (P<0.05);The 1 year survival rate in observation group 52.17%(24/46) was significantly higher than control group 29.63%(16/54), the median survival time in observation group 9.0 months was significantly higher than control group 6.0 months, the difference was statistically significant (P<0.05); There was no significant difference between the two groups in the incidence of adverse reactions.ConclusionErlotinib combined with WBRT in the treatment of NSCLC patients with brain metastases can improve the prognosis of curative effect and long-term effect.
erlotinib; radiotherapy; non-small cell lung cancer; brain metastasis; prognosis
10.3969/j.issn.1005-1678.2016.10.014
刘学啸,通信作者,男,本科,主治医师,研究方向:肿瘤放疗,E-mail:liuxuexiao78@163.com。
R73
A
