CEUS与平面波超敏感血流显像分析甲状腺乳头状癌
2019-01-21刘晶华陈路增叶京明
刘晶华,陈路增*,陈 蕾,叶京明,王 彬,张 惠
(1.北京大学第一医院超声科,2.普通外科,北京 100034)
近年来,甲状腺癌的发病率显著上升,其中以甲状腺乳头状癌(papillary thyroid carcinomas, PTC)最为常见,占80%~90%[1]。新生血管在甲状腺癌的生长、局部侵犯和远处转移过程中具有重要作用[2]。CEUS可动态评估病灶内部和周边组织的血流分布和灌注特征[3]。平面波超敏感血流显像(planewave ultrasensitive imaging, AngioPLUS)可检测病灶微细血管内的低速血流信号[4]。本研究旨在对PTC的CEUS和AngioPLUS特征进行分析。
1 资料与方法
1.1 一般资料 选取2017年3月—11月于本院经手术病理确诊的83例PTC患者,男16例,女67例,年龄21~76岁,平均(44.7±12.7)岁。本研究经我院伦理委员会批准,所有患者均签署知情同意书。对多病灶患者选择最大病灶进行分析。
1.2 仪器与方法
1.2.1 仪器 常规超声及AngioPLUS采用SuperSonic Aixplorer诊断仪,L15-4、L10-2线阵探头,频率分别为4.0~15.0 MHz、2.0~10.0 MHz。CEUS选用GE Logiq E9超声诊断仪,L6-15探头,频率6.0~15.0 MHz。造影剂为声诺维,将5 ml生理盐水注入声诺维冻干粉中,反复用力振荡后形成微泡悬液备用。
1.2.2 方法 由2名具有8年以上工作经验的超声医师共同完成检查,意见不同时经协商达成一致。常规超声:测量病灶最大径;CDFI:观察病灶内部及周边有无血流信号。AngioPLUS:选择病灶纵切面及横切面,连续扫查病灶整体并存储连续多切面动态图像,实时观察病灶内部及周边有无血流信号及微细血流形态有无异常(纤细或粗细不均,走行纡曲、成角),并对比病灶内部与邻近正常甲状腺组织微细血流分布特征。CEUS:抽取1.0 ml造影剂快速经前臂浅静脉注入后,以5 ml生理盐水冲洗,连续实时观察至病灶及甲状腺实质内造影剂明显消退。观察病灶强化程度,对比CEUS病灶与邻近正常甲状腺组织强化程度,病灶强化程度低于邻近甲状腺组织为低增强(低增强组),病灶与邻近甲状腺组织强化程度相近为等增强(等增强组),病灶强化程度高于邻近甲状腺组织为高增强(高增强组)。于时间-强度曲线上测量病灶及邻近甲状腺组织峰值强度(peak intensity, PI),测量3次,取平均值。计算病灶与邻近甲状腺组织PI差值ΔPI(病灶PI平均值-邻近甲状腺组织PI平均值)。
观察CEUS显示病灶内强化程度与AngioPLUS显示的病灶内部微细血流分布特征的一致性:当低增强病灶内部微细血流少于邻近甲状腺组织、等增强病灶内部微细血流与邻近甲状腺组织相近,高增强病灶内部微细血流多于邻近甲状腺组织时,认为CEUS显示病灶内强化程度与AngioPLUS显示的病灶内部微细血流分布一致。
1.3 统计学分析 采用SPSS 19.0统计分析软件。对数据进行正态分析(Shapiro-Wilk检验)和方差齐性检验(Levene检验),计量资料以±s表示,采用单因素方差分析或Kruskal-Wallis检验比较各组间PI、ΔPI差异,组间两两比较采用Bonferroni法或Mann-Whitney检验。以Spearman相关性分析观察PI、ΔPI与CEUS显示病灶内部强化程度的相关性,以及CEUS显示病灶内部强化程度、PI和ΔPI与AngioPLUS显示的病灶内部微细血流分布特征的相关性,∣rs∣≤0.3为相关性较差;0.3<∣rs∣≤0.6为中度相关;0.6<∣rs∣≤0.8为相关性较高;∣r∣>0.8为高度相关。P<0.05为差异有统计学意义。
2 结果
83个PTC 病灶,最大径0.50~6.84 cm,平均(1.24±0.91)cm;56个病灶CDFI可探及血流信号,27个未探及血流信号。
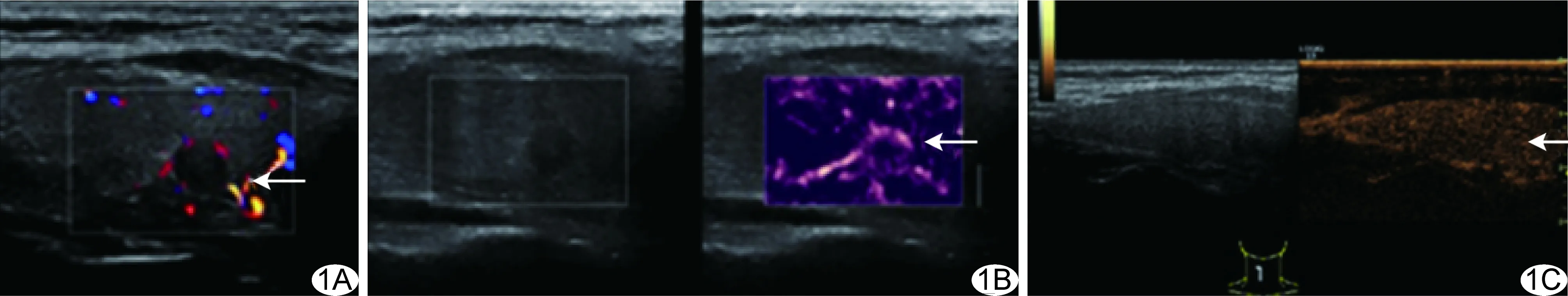
图1 患者男,58岁,PTC A.CDFI示病灶内部及周边点状、条状血流信号(箭); B.AngioPLUS示病灶内血流信号少于邻近甲状腺组织,病灶周边可见环绕血流信号(箭); C.CEUS示病灶呈等增强(箭),ΔPI=-0.53 dB

图2 患者女,65岁,PTC A.CEUS示病灶呈不均匀低增强(箭),ΔPI=-3.10 dB; B.AngioPLUS示病灶血流信号少于邻近甲状腺组织,病灶内部可见管径纤细、走行纡曲的穿支血管(箭)
2.1 CEUS 83个病灶均可见强化,其中低增强组53例,男9例,女44例,年龄21~72岁,平均(45.4±12.2)岁;等增强组24例,男6例,女18例,年龄28~76岁,平均(44.4±12.6)岁;高增强组6例,男1例,女5例,年龄29~74岁,平均(39.3±17.5)岁。
低增强组、等增强组及高增强组PI分别为 (-56.39±1.94)dB、(-52.65±2.26)dB及(-51.03±3.57)dB(F=34.97,P<0.001),其中低增强组PI小于等增强组及高增强组(P均<0.001),而等增强组PI与高增强组间差异无统计学意义(P=0.322)。低增强组、等增强组及高增强组ΔPI分别为(-2.96±1.43)dB、(-0.25±0.81)dB及(3.46±2.04)dB(χ2=52.35,P<0.001),其中低增强组ΔPI小于等增强组(Z=-6.45,P<0.001)和高增强组(Z=-3.99,P<0.001),等增强组ΔPI小于高增强组(Z=-3.73,P<0.001)。PI(rs=0.650,P<0.001)、ΔPI(rs=0.798,P<0.001)与CEUS显示病灶内部强化程度均呈正相关。
2.2 AngioPLUS 83个病灶均可见血流信号,其中60个病灶内部血流比邻近甲状腺组织少,14个与邻近甲状腺组织相近,9个比邻近甲状腺组织多;56个病灶以内部血流信号为主,26个病灶为内部加周边血流信号,1个病灶以周边血流信号为主。27个存在周边血流信号的病灶中,12个周边为环绕血流信号,15个周边为点状及短条状血流信号;而CDFI仅显示其中2个病灶周边为环绕血流信号,其余病灶周边为点状及短条状血流信号(图1)。83个病灶中,42个病灶内部可见纤细或粗细不均,走行纡曲、成角的异常血管,其中39个病灶为低增强,3个为等增强(图2);41个病灶内血管形态未见异常。
2.3 一致性分析 83个病灶中,CEUS显示66个病灶内强化程度与AngioPLUS显示的病灶内部微细血流分布一致,17个不一致。在53个低增强病灶中,52个病灶一致,1个不一致;24个等增强病灶中,11个一致,13个不一致;6个高增强病灶中,3个一致,3个不一致。CEUS显示病灶内部强化程度与AngioPLUS显示的病灶内部微细血流分布特征呈正相关(rs=0.768,P<0.001)。PI(rs=0.442,P<0.001)、ΔPI(rs=0.647,P<0.001)与AngioPLUS显示的病灶内部微细血流分布特征呈正相关。
3 讨论
CEUS通过显示病灶血流灌注可为诊断和鉴别诊断甲状腺癌提供依据[5-6]。超微血管显像技术能显示病灶内微细血管形态,已广泛用于鉴别诊断甲状腺良恶性结节及诊断甲状腺癌[7-9]。AngioPLUS是一种多普勒超声技术,通过非聚焦或称平面波原理及三维壁滤波原理检测微细血管内的低速血流。三维壁滤波技术能从时间、空间及振幅方面分析组织运动,有效分辨血流和组织信息[4,10]。本研究中,27个病灶CDFI未见血流信号,而AngioPLUS均显示存在血流信号,提示AngioPLUS可更为敏感地显示PTC微细血管内的低速血流信号,从而对病灶微细血管分布及形态是否异常进行判定。
本研究中,3组间ΔPI、PI差异均有统计学意义,PI、ΔPI与CEUS显示病灶内部强化程度呈正相关。既往主要依据医师主观判定病灶的强化程度,受人为因素干扰较大;而以ΔPI作为测量指标判定CEUS强化程度更为客观,有利于更准确地进行组间比较。杨萌等[1]指出,通过计算病灶与腺体达峰强度的差值,对仪器设置、血流动力学或造影剂剂量等方面的影响因素进行一定程度的矫正,有利于进行相对客观的组间比较及计量统计学分析。
本研究中,AngioPLUS显示12个病灶周边为环绕血流信号,而CDFI仅显示其中2个病灶周边为环绕血流信号。既往研究[11-13]发现甲状腺恶性结节主要为中央血流信号,而良性结节主要为周边血流信号;本研究结果与其不符,考虑为良性结节周边血流较粗大,CDFI即可显示,而多数PTC周边血流较细小,流速较低,CDFI不能显示或不能完整显示部分病灶周边血流,故多认为甲状腺恶性结节是以内部血流为主。本研究应用AngioPLUS后,提高了PTC周边血流信号的显示,可更好地显示出其周边的环绕血流信号。
田菊等[14]报道,甲状腺恶性肿瘤浸润并破坏病灶周围组织,滋养血管纤细或粗细不均,排列不规则,走行纡曲、成角。本研究中于42个病灶内可见到类似上述表现的新生血管,其中39个病灶为低增强,3个为等增强,提示PTC的CEUS表现为低增强可能与其内发育不良的新生血管有关。
本研究中,CEUS显示病灶内部强化程度与AngioPLUS显示的病灶内部微细血流分布特征均呈正相关,PI、ΔPI均与AngioPLUS显示的病灶内部微细血流分布特征均呈正相关,提示可通过AngioPLUS显示病灶内部微细血流分布特征间接评价其血流灌注。CEUS的缺点为费用较高、操作较复杂,且少数患者可能对造影剂过敏等。应用AngioPLUS,有助于超声医师更好地对甲状腺结节做出定性诊断。AngioPLUS操作简便、安全且不产生额外检查费用,还可实时、多切面观察病灶,发现病灶内异常的微细血管结构,有助于诊断PTC。与CDFI相比,AngioPLUS可更清晰地显示PTC病灶周边微细环绕血流信号,能否以此作为诊断PTC的依据尚待进一步研究。
