碘量法测定橙子维生素C的含量*
2016-08-25罗月生陈碧琼
严 苹, 罗月生, 陈碧琼
(1 西南医科大学临床医学院,四川 泸州 646000;2 西南医科大学基础医学院,四川 泸州 646000)
碘量法测定橙子维生素C的含量*
严苹1, 罗月生1, 陈碧琼2
(1 西南医科大学临床医学院,四川泸州646000;2 西南医科大学基础医学院,四川泸州646000)
采用碘量法测定泸州食用水果橙子中维生素C的含量。由于维生素C与I2可以发生氧化还原反应,利用其反应的定量关系得出维生素C的含量。实验结果表明,碘量法操作方便快速,反应条件易控制,仪器简单。试验的平均回收率为99.82%,相对标准偏差RSD=1.22%,线性回归方程为Y=2.1345X-0.1098,R2=0.9978。试验为橙子维生素C的测定提供了可靠方法,可用于一般机构对水果中维生素C含量的测定。
碘量法;测定;橙子;维生素C;含量
维生素C又名抗坏血酸(C6H8O6),纯品为白色结晶,无臭,味酸,易溶于水,不溶于氯仿或乙醚。维生素C具有防治坏血病的功能,能防止牙龈出血;促进胶原蛋白的合成,有利于组织伤口的愈合,防止癌细胞的扩散[1],促进芳香族氨基酸的代谢,延长机体寿命,增强机体抵抗外界刺激的能力,改善脂肪和类酯特别是胆固醇的代谢;维生素C在人体内不能合成,主要从膳食中获取[2]。维生素C广泛存在于各种蔬菜和水果中,且含量随品种和产地不同而异, 蔬果是人类维生素C 的重要来源。 因此,准确测定蔬果中维生素 C 的含量,对人们日常饮食具有重要的指导意义。实验选用当地盛产的橙子作为原材料进行研究。
1 实 验
1.1主要仪器和试剂
1.1.1仪器
电子天平,梅特勒-托利多仪器上海有限公司;榨汁机。
1.1.2试剂
草酸;抗坏血酸标准品;可湿性淀粉;碘;碘化钾;活性炭。均购自成都金山化学试剂有限公司,均为分析纯。
1.1.3样品
本实验根据前期问卷调查结果,选择泸州产橙子作为待测样品。
2 结果与讨论
2.1试验原理
维生素C具有二烯醇结构,还原性较强,在水溶液中易被空气和其它氧化剂氧化,生成脱氢抗坏血酸;在碱性条件下易分解,见光分解加速;在弱酸性条件下较稳定[3]。所以实验应在酸性条件下进行。
目前测定维生素C含量的常用方法有:2,6-二氯靛酚法[4]、紫外分光光度法[3]、碘量法[5]、高效液相色谱法等。本文采用碘量法对橙子中的维生素C含量进行测定,利用维生素C的还原性和碘的强氧化性,通过其反应的定量关系得出维生素C含量。该方法简单易行,效果好。
2.2试剂的配制及浓度标定
2.2.11%草酸溶液的配制
准确称取草酸10 g,先加少量蒸馏水溶解,然后定容至1000 mL室温保存以备用。
2.2.2维生素C标准溶液的配制
准确称取维生素C标准品500 mg,用1%的草酸振荡溶解,再用1%草酸溶液定容至500 mL。即得浓度为1 mg/mL的标准溶液。
2.2.31%淀粉溶液的配制
称取1 g淀粉,先用10 mL蒸馏水调匀,再加90 mL蒸馏水煮沸至透明,冷却后定容至100 mL容量瓶。
2.2.4I2标准溶液的配制
称取6 g KI,用少许蒸馏水溶解,然后加入1.3 g I2并使其完全溶解,转入1000 mL容量瓶中定容至刻度,得浓度约0.005 mol/L的碘标准溶液。置棕色瓶避光保存,备用。
2.2.5I2标准溶液的标定
准确移取维生素C标准溶液5 mL于锥形瓶中,加入20 mL 1%草酸溶液和1mL 1%的淀粉溶液,用I2标准溶液滴定至呈微蓝色且30 s内不褪色,记录消耗I2标准溶液的体积V1,同时做空白试验,记录消耗I2标准溶液体积V2,得出抗坏血酸消耗I2标准溶液体积VI2,计算I2标准溶液的浓度。结果见表1。

表1 碘标准溶液的标定Table 1 Titration of iodine standard solution
2.3标准曲线的绘制
分别准确移取维生素C标准溶液(1 mg/mL)5、20、40、60、80、100 mL,稀释至100 mL。再各取稀释液10 mL,加入20 mL 1%草酸溶液和1 mL 1%淀粉溶液,用I2标准溶液滴定,记录消耗I2的体积,每个溶液分别滴定5次取平均值,并扣除空白值[6],试验结果见表2。
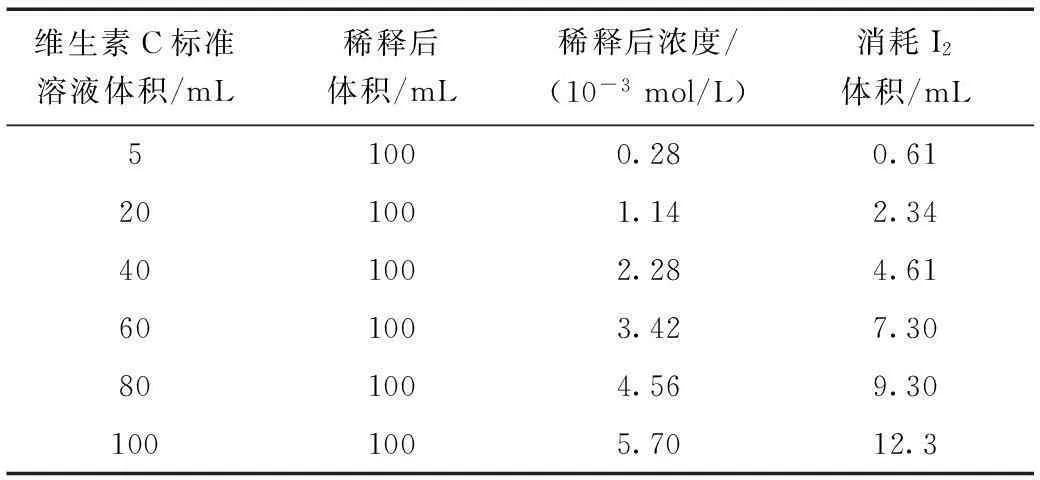
表2 维生素C标准溶液浓度与I2标准溶液体积Table 2 The ranation of Vitamine C concentration and I2 volume
将维生素C标准溶液浓度与消耗I2标准溶液的体积进行线性分析,得回归方程Y=2.1345X-0.1098,R2=0.9978。见图1。
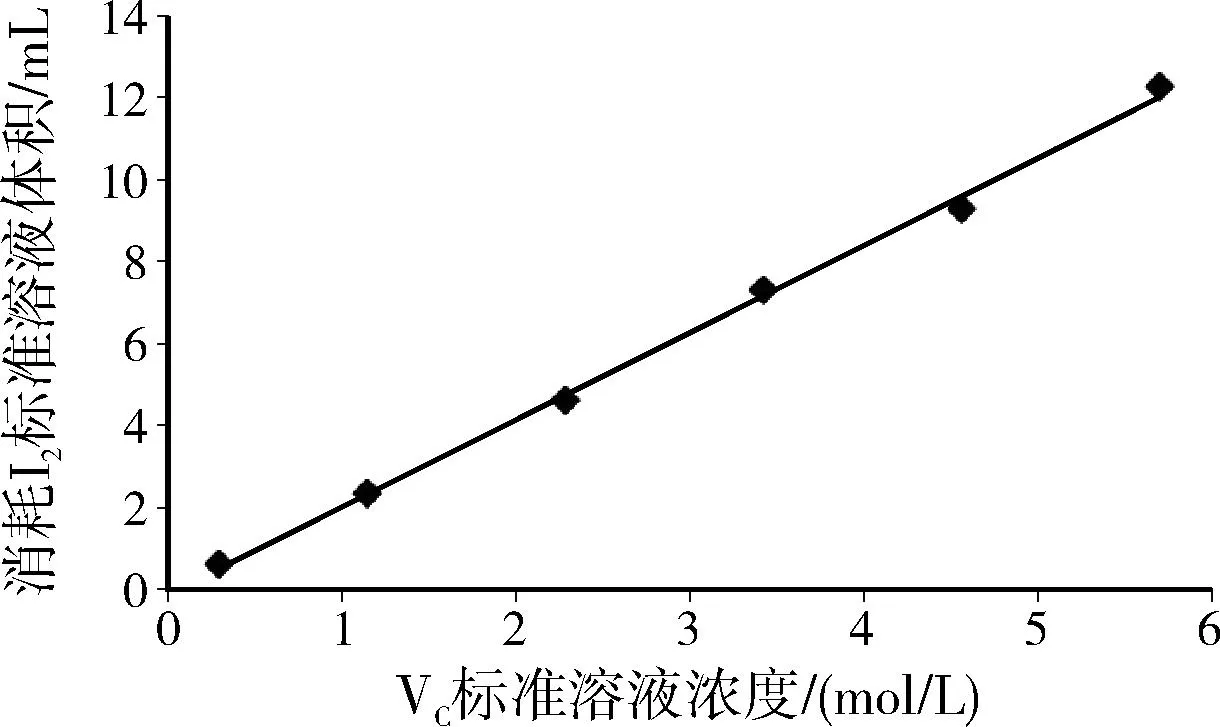
图1 维生素C标准溶液浓度与消耗I2体积的关系
2.4样品溶液的制备
将新鲜橙子去皮、去核,准确称取100 g置榨汁机中,加入40 mL草酸溶液,榨汁后将果汁倒入锥形瓶,再用10 mL草酸溶液清洗榨汁机一并倒入锥形瓶(为了减小实验误差,需加入活性炭脱色),量取最终所得果汁体积。
2.5样品中维生素C的含量测定
准确移取10 mL样品提取液,加入20 mL 1%草酸溶液和1 mL 1%淀粉溶液,用已标定准确浓度的I2溶液进行滴定,记录消耗的I2溶液的体积,重复滴定5次取平均值并扣除空白值。计算样品中维生素C的含量,计算公式:100 g样品中维生素C的含量=C(I2)·V(I2)·M(VC)·V(VC)/10。共测定4批次,结果见表3。
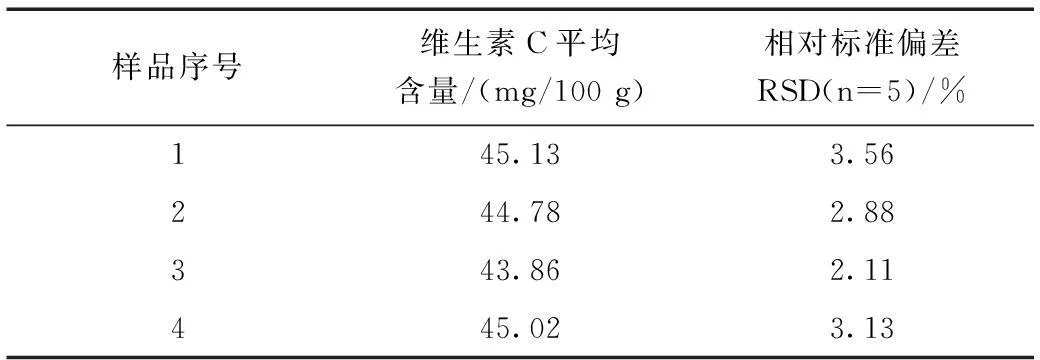
表3 橙子维生素C的含量Table 3 Vitamin C content of orange
2.6加标回收试验
准确移取已知含量的样品溶液四份,各加入一定质量的维生素C纯品,按前面测定方法测其消耗I2溶液的体积,计算回收率R:
式中:A——加入维生素C纯品后测得的总含量
B——样品中维生素C的含量
C——加入纯维生素C的量
测得平均回收率为99.82%,RSD(n=4)=1.22%,结果表明回收率较高。见表4。

表4 加样回收率测定Table 4 The result of recovery rate experiment
3 结论与讨论
本实验采用碘量法测定维生素C含量,操作简单易行,平均回收率为99.82%,RSD(n=4)=1.22%,回收率较高,方法可靠,可用于橙子维生素C的定量测定。实验发现,在酸性条件下,维生素C较稳定,由于溶液有颜色,试验中使用了活性炭脱色,效果较好。由于碘易挥发、见光易分解且碘离子易氧化等特点,碘标准溶液应现标定现用,还应做空白试验,扣除空白纸,以减少误差;操作还应尽量快速,以减小维生素C和碘等试剂不稳定带来的误差。
[1]H Hemila, Z S Herman. 维生素C 与感冒:对Chalmers综述的分析[J].中国临床营养杂志,2003,2(1):58-61.
[2]王征帆,杨艳丽.恒电流库伦分析法在水果VC含量测定中的应用[J].安徽农业科学,2008,36(10):3941-3942.
[3]吴春艳. 水果中维生素C含量的测定及比较[J]. 武汉理工大学学报, 2007,29(3):90-91.
[4]开启余.紫外分光光度法测定VC银翘片中维生素C含量[J].福建分析测试, 2015,24(3):35-37.
[5]王美荣. 直接碘量法定量测定维生素C[J]. 阴山学刊,2006,20(3):39-40.
[6]武文,詹秀环,宣亚文.碘量法测定蔬菜中维生素C的含量[J].安徽农业科学, 2009,37(21):9845-9846.
Determination of Ascorbic Acid in Orange by Iodimetry*
YAN Ping1, LUO Yue-sheng1, CHEN Bi-qiong2
(1 College of Clinical Medical, Southwest Medical University, Sichuan Luzhou 646000;2CollegeofPreclinicalMedicine,SouthwestMedicalUniversity,SichuanLuzhou646000,China)
This experiment adopted iodimetry to ascertain the concentration of Vc in orange. Vitamin C and I2can be quantitatively oxidized reduction reaction. It calculated the concentration of Vc in orange. This experiment showed that iodimetry was easy to operate. In this experiment, the average rate of recovery was R=99.82% and the standard linear equation was Y=2.1345X-0.1098, R2=0.9978.
iodimetry; determination; orange; ascorbic acid; concentration
四川省大学生创新创业训练计划项目(No:01070320);西南医科大学大学生创新创业训练计划项目(No:2014065)。
严苹(1994-),女,临床医学2013级13班学生。
陈碧琼(1969-),女,副教授。
O656.3
A
1001-9677(2016)014-0121-03
