二氧化硅/金复合膜修饰玻碳电极用于双酚A的检测
2016-08-19陈丽飞
黄 颖,陈丽飞
(福建师范大学 化学与化工学院,福建 福州 350007)
二氧化硅/金复合膜修饰玻碳电极用于双酚A的检测
黄颖*,陈丽飞
(福建师范大学化学与化工学院,福建福州350007)
该文制备了二氧化硅/金复合膜修饰玻碳电极(SiO2/Au/GCE),提出了一种简便检测双酚A(BPA)的电化学分析方法。 采用扫描电镜(SEM)和红外光谱(FT-IR)对SiO2和SiO2/Au的形貌和结构进行了表征,循环伏安法(CV)和交流阻抗法(EIS)研究了SiO2/Au/GCE的表面电化学特性,同时用CV、 计时库仑法(CC)、 控制电位电解库仑法、 线性扫描伏安法(LSV)和差分脉冲伏安法(DPV)等研究了BPA在SiO2/Au/GCE上的电化学行为,优化了实验参数,并得到电化学动力参数。 实验发现:SiO2/Au/GCE对BPA具有良好的电催化活性,BPA在该修饰电极上的氧化峰电流为GCE上的3倍,且BPA在SiO2/Au/GCE上的氧化过程为2电子2质子的完全不可逆电极过程。 在最佳条件下,BPA的氧化峰电流分别在0.01~0.50 μmol/L 和0.50~25 μmol/L浓度范围内呈良好的线性关系,检出限为1.9×10-8mol/L。 用于一次性手套中BPA含量的测定,回收率为98.9%~105.3%,与高效液相色谱法(HPLC)进行对照,结果满意。
二氧化硅/金复合膜;玻碳电极;双酚A;电化学行为
双酚A(Bisphenol A,BPA)是一种重要的化工原料,可作为聚碳酸酯PC的重要原料,并广泛存在于食物袋、 奶瓶等塑料制品中[1-2]。BPA属于内分泌干扰物(EDC),能够影响动物和人体的正常内分泌功能,对生态系统和人类健康具有潜在危险。因此,建立一种灵敏、 快速、 准确的BPA检测方法至关重要。 目前,BPA的检测方法主要有液相色谱法、 酶联免疫吸附法、 荧光法及相应的联用技术[3-8]。上述方法各有优点,但仪器设备昂贵、耗时长,而电化学方法灵敏、 快速、 简便且成本低。二氧化硅由于较高的化学稳定性、 表面活性和催化性能,在电催化和电化学分析方面具有较好的应用价值和前景[9-11]。 纳米金作为一种贵金属纳米材料,因具有纳米材料的表面、 量子尺寸效应,以及金属的导电性、 催化活性、 界面交互性等性质,可增加电极表面积和电子传递能力,而被广泛用作修饰电极材料。将纳米金作为电极修饰材料用于电活性物质的测定和分析已有文献报道[12-14],但将纳米金与二氧化硅复合膜修饰在电极上对BPA进行测定尚未见报道。本研究结合金和二氧化硅的优点,将二氧化硅/金复合材料制成膜,采用浸渍法将其修饰在玻碳电极表面。 该修饰电极用于BPA的电催化氧化行为研究,具有灵敏度高、 选择性和稳定性好等特点,可用于一次性手套中BPA的检测。
1 实验部分
1.1仪器与试剂
CHI660D电化学工作站(上海辰华仪器公司),三电极系统:玻碳电极(直径3 mm)或修饰电极为工作电极,Ag/AgCl为参比电极,铂丝电极为辅助电极;S-4800扫描电子显微镜(SEM,日本Hitachi公司);Nicolet 5700 傅立叶红外光谱仪(FT-IR,美国Nicolet 公司)。
双酚A(99.5%)、 氯金酸(HAuCl4·4H2O, 分析纯)、3-氨丙基三乙氧基硅烷(APTES,98%)购于阿拉丁公司;十四烷基二甲基苄基氯化铵水合物(BACH)购于百灵威化学试剂有限公司;甲醇(纯度>99.5%)、 无水乙醇(99.8%)、 甲醛(>99.5%)、 正己烷(>97.0%)、 氨水(分析纯)、盐酸(分析纯)购于上海国药集团化学试剂有限公司;水玻璃(SiO2∶Na2O=3.47∶1)购于福建沙县金沙白炭黑制造有限公司。实验用水为二次蒸馏水,其余试剂均为分析纯。
1.2球形二氧化硅的制备
在一定温度下,将一定体积的水玻璃加入到装有蒸馏水的圆底烧瓶中,搅拌条件下再加入少量BACH。30 min后,在剧烈搅拌条件下,加入一定体积的 2 mol/L HCl,使水解反应迅速进行。 以40 r/min继续搅拌一段时间,得白色凝胶。 将凝胶离心分离,洗涤、干燥,最后于一定温度下焙烧,得球形二氧化硅。
1.3金溶胶的制备
参照文献[15],采用柠檬酸钠还原法制备金溶胶纳米颗粒:搅拌条件下,在含有0.5 mL 1.0% HAuCl4的50 mL沸水中,加入1.0 mL 1.0%柠檬酸钠,继续加热使溶液颜色由黑色变至酒红色停止,冷却至室温后,将金溶胶置于4 ℃冰箱中保存,备用。
1.4SiO2/Au的制备
NH2-SiO2的制备参照文献[16]:将少量制得的SiO2分散在无水乙醇中,加热至80 ℃后,加入APTES,回流、过滤、无水乙醇洗涤,于80 ℃真空干燥6 h。SiO2/Au的制备参照文献[17]:取一定量的NH2-SiO2分散在金溶胶中,并加适量水,超声、 过滤,于50 ℃真空干燥12 h,200 ℃焙烧1 h。
1.5SiO2/Au/GCE的制备
将玻碳电极用直径为0.3 μm的Al2O3粉末抛光至镜面,再分别用无水乙醇和水依次超声清洗3 min,吹干备用。
根据文献[18]方法,取少量上述制得的SiO2/Au分散在5 mL水中,加入5 mL正己烷,超声3 min,形成正己烷-水界面,逐滴加入无水乙醇,使SiO2/Au在正己烷-水界面自组装成膜。 将玻碳电极浸渍于其中,取出自然风干即得SiO2/Au/GCE。
1.6样品的制备
以一次性PE手套为实验样品,参照文献[19]方法, 将样品剪碎,用水洗涤,自然晾干。称取1 g样品于20 mL甲醇中,在70 ℃恒温水浴锅中加热12 h,于室温下放置3 d后,离心洗涤3次,收集所有滤液至50 mL容量瓶中,用甲醇定容至刻度。
2 结果与讨论
2.1SiO2与SiO2/Au表征
SiO2和SiO2/Au的扫描电镜图如图1所示。制得的SiO2为球形,分散性好(图1A)。 而SiO2/Au中出现SiO2微球团聚及粘连现象(图1B),这可能是因为金溶胶起到了粘合剂的效果。

图1 SiO2(A)和SiO2/Au(B)的扫描电镜图Fig.1 SEM micrographs of SiO2(A) and SiO2/Au(B)

图2 SiO2(a)、 NH2-SiO2(b)和SiO2/Au(c) 的红外光谱图Fig.2 FT-IR spectra of SiO2(a), NH2-SiO2(b) and SiO2/Au(c) wavenumber range of 400-4 000 cm-1;samples diluted by KBr (weight ratio of 1∶100) before analysis
图2为SiO2(a),NH2-SiO2(b)与SiO2/Au(c)的FT-IR谱。 曲线a中,3 444.5 cm-1和1 630.9 cm-1处的吸收峰为SiO2中存在的游离水和吸附水的伸缩振动峰[20]。 1 089.5,801.4,463.7 cm-1处的吸收峰分别为SiO2中Si—O—Si键的不对称伸缩振动峰、 对称伸缩振动峰和弯曲振动峰[21]。 曲线b于1 565.7 cm-1处出现一新的吸收峰,为N—H的弯曲振动峰[22],表明氨基已成功修饰在SiO2表面。 而在曲线c上,N—H的弯曲振动峰移至1 545.6 cm-1且强度减小,说明N—H的弯曲振动受到金溶胶的影响,金溶胶能键合到SiO2表面。
2.2工作电极的表征
图3为GCE(a)和SiO2/Au/GCE(b)在1 mmol/L [Fe(CN)6]4-/3-+500 mmol/L KCl溶液中的循环伏安图。 与GCE相比,[Fe(CN)6]4-/3-在SiO2/Au/GCE上的氧化还原电流有较大提高,且氧化还原峰峰电位差(ΔEp)降至35 mV。 结果说明SiO2/Au的存在增加了电极的电活性面积,提高了电化学反应的电子转移速率。
为进一步研究修饰电极的电化学性能,考察了GCE和SiO2/Au/GCE在1 mmol/L [Fe(CN)6]4-/3-+500 mmol/L KCl溶液中的交流阻抗图。如图3插图所示,SiO2/Au/GCE(b)的阻抗弧半径明显小于GCE(a),说明GCE上SiO2/Au良好的电化学性能显著加快了电极表面[Fe(CN)6]4-/3-的电子传递。
2.3BPA的电化学行为

图3 不同电极的循环伏安图Fig.3 Cyclic voltammograms of different electrodes insert:Nyquist plots of different electrodes;solution: 1 mmol/L[Fe(CN)6]4-/3-(1∶1) containing 500 mmol/L KCl;a.GCE,b.SiO2/Au/GCE; scan rate:100 mV/s;frequency range:0.1-105 Hz

图4 50 μmol/L BPA在GCE(a)和SiO2/Au/GCE(b) 上的循环伏安图Fig.4 Cyclic voltammograms of 50 μmol/L BPA at GCE(a) and SiO2/Au/GCE(b) in 0.1 mol/L PBS(pH 8.0) insert:cyclic voltammograms of GCE(c) and SiO2/Au/GCE(d) in 0.1 mol/L pH 8.0 PBS;scan rate:100 mV/s
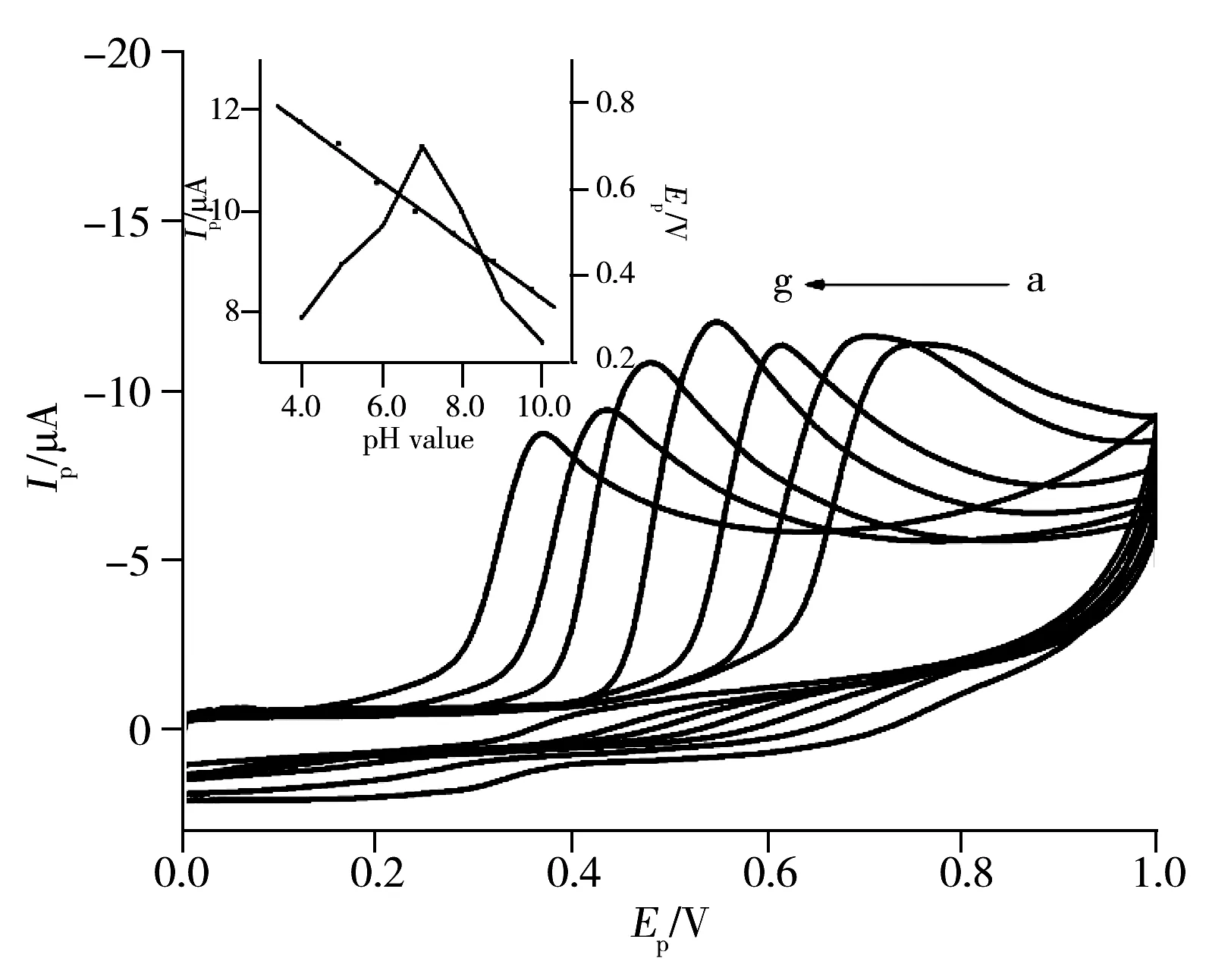
图5 50 μmol/L BPA在SiO2/Au/GCE上于 不同pH值下的循环伏安图Fig.5 Cyclic voltammograms of 50 μmol/L BPA at SiO2/ Au/GCE under different pH values pH value(a-g) :4.0,5.0,6.0,7.0,8.0,9.0,10.0; insert: influence of pH value on oxidation peak current and potential of 50 μmol/L BPA;scan rate:100 mV/s
图4为GCE(a,c)和SiO2/Au/GCE(b,d)在0.1 mol/L的PBS缓冲溶液(pH 7.0)和含有50 μmol/L BPA的PBS溶液中的循环伏安图。 由图4可知,在0~1 V电位范围内,不加BPA时(图4插图),未出现氧化还原峰,表明电极自身和空白底液均不存在电化学活性物质;将50 μmol/L BPA加至PBS缓冲溶液后(见图4),在GCE和SiO2/Au/GCE上均观察到1个氧化峰,且氧化峰电流大小关系为Ipa(b)>Ipa(a),而在反向扫描过程中均未出现还原峰,表明BPA在电极上的电化学行为完全不可逆。 BPA在SiO2/Au/GCE上的Ip是GCE的3倍,同时氧化峰电位负移30 mV,表明SiO2/Au/对BPA的电化学氧化过程具有良好的电催化活性。
2.4实验条件的优化
2.4.1SiO2/Au膜厚度研究发现制备SiO2/Au膜过程中,乙醇用量决定膜的厚度,进而影响电极性能。 采用CV法研究了乙醇用量对BPA氧化峰电流的影响,结果发现当乙醇用量从1 mL增至4 mL时,BPA的氧化峰电流逐渐增加,此后继续增加乙醇用量,氧化峰电流则开始下降。 故选择乙醇用量为4 mL。
2.4.2pH值的影响在SiO2/Au/GCE上,考察了50 μmol/L BPA在不同pH值PBS缓冲溶液中的循环伏安行为。 如图5所示,当pH值从4.0增至7.0时,氧化峰电流逐渐增大,而pH值继续增至10.0时,峰电流逐渐降低,因此选择最佳pH值为7.0。
图5插图为BPA的氧化峰电位与pH值的关系图。 氧化峰电位与pH值之间的线性回归方程为Epa(V)=-0.064 3 pH+1.011,r=0.998 0。 即当pH值逐渐增大时,氧化峰电位以64.32 mV/pH的速率负移,该值与等电子等质子传递的理论值59 mV/pH接近,表明BPA在SiO2/Au/GCE上的氧化是等质子等电子的完全不可逆过程。
采用控制电位电解库仑法测定电化学反应的电子转移数(n)。 对5 mL 1 μmol/L BPA 的PBS溶液(pH 7.0)和试剂空白溶液平行测定3次,得QBPA和Qblank的平均值分别为2.661×10-3C和1.699×10-3C。根据法拉第定律[23]:n=ΔQ/(FcV),式中c为BPA的浓度(mol/L),V为溶液体积(L),F为法拉第常数(C/mol),ΔQ(单位为C)为参与反应的物质的电解电量(ΔQ=QBPA-Qblank)。由此公式计算可得n=2。 综上可知BPA在SiO2/Au/GCE上的氧化过程为2电子2质子的完全不可逆电极过程。
2.4.3扫速的影响在SiO2/Au/GCE上,用CV考察了扫速对50 μmol/L BPA氧化峰电流的影响。 结果显示,在0.03~0.3 V/s范围内,随着扫速的增加,氧化峰电流逐渐增加,且氧化峰电流(Ipa,μA)与扫速(v,V/s)成正比,其线性方程为Ipa=47.04v+0.980 3,r=0.997 7,表明BPA在SiO2/Au/GCE上是完全不可逆的吸附控制过程。
2.4.4富集电位与时间的影响采用恒电位技术考察了-0.3~0.1 V电位区间50 μmol/L BPA在SiO2/Au/GCE上氧化峰电流的变化,发现富集电位为-0.1 V时电流响应最大。 同时研究了富集时间的影响,结果表明在120 s内,BPA的氧化峰电流随着富集时间的增加而逐渐增大,当富集时间大于120 s后,氧化峰电流呈下降趋势。 因此实验选择富集电位为-0.1 V,富集时间为120 s。
教育和体育行政部门应加强体育场馆资源使用方面的指导,鼓励学校以灵活的形式把场馆资源向学生开放,搭建学校交流和评比平台,开展体育俱乐部建设评比、学校场馆资源使用效益考核等活动,提高学校体育场馆管理水平,促进学生参加课外体育锻炼。
2.5计时库仑法
在1 mmol/L [Fe(CN)6]4-/3-+500 mmol/L KCl溶液中,用计时库仑法测定了GCE和SiO2/Au/GCE的有效表面积。GCE和SiO2/Au/GCE的Q~t1/2直线斜率分别为62.31 μC/s1/2和 136.1 μC/s1/2。 根据Anson方程[24]:Q=(2nFAD1/2cπ-1/2)t1/2+Qdl+Qads(Qads=nFAГs) ,式中A表示电极的有效表面积,n为电子转移个数,D为扩散系数,Qads为被吸附物质的法拉第电量,Qdl为双电层电量,可采用背景扣除以除去。 已知在[Fe(CN)6]4-/3-溶液中,n为1,D为7.6×10-6cm2/s,可计算得GCE和SiO2/Au/GCE的A分别为0.207 6,0.453 3 cm2,表明SiO2/Au/GCE的有效表面积明显提高。
用计时库仑法进一步测定了GCE和SiO2/Au/GCE在PBS缓冲溶液(pH 7.0)和含有50 μmol/L BPA的PBS溶液中的扩散系数(D)和表面吸附量(Гs)。 经背景扣除后,发现BPA的总电解电量Q(μC)与t1/2之间呈良好的线性关系,线性方程如下:GCE:Q=21.84t1/2+0.313 3,r=0.998 2;Au/SiO2/GCE:Q=66.94t1/2+5.916,r=0.997 2。
根据Anson方程的斜率和截距,可计算得BPA在GCE上的D和Гs分别为9.333×10-5cm2/s和7.821×10-12mol/cm2,而在SiO2/Au/GCE上的D和Гs分别为1.839×10-4cm2/s和 6.763×10-11mol/cm2。说明SiO2/Au/GCE对BPA的吸附性能优于GCE。
2.6标准电子转移速率常数ks
BPA在SiO2/Au/GCE上为完全不可逆的电化学氧化过程,ks的计算可依据Velasco方程[25]:ks=2.415 exp[-0.02F/(RT)]D1/2(Epa-Epa/2)-1/2v1/2, 式中Epa表示峰电位,Epa/2表示半波电位。 通过线性扫描伏安法(LSV)测得BPA在GCE上的|Epa-Epa/2|平均值为86 mV,D=9.333×10-5cm2/s,v=100 mV/s。 由此可计算得ks=0.011 55 cm/s。同样用LSV可测得BPA在SiO2/Au/GCE上的|Epa-Epa/2|平均值为36 mV,代入数值计算得D=1.839×10-4cm2/s,v=100 mV/s,ks=0.025 05 cm/s,表明Au/SiO2较高的吸附能力和导电性使BPA在SiO2/Au/GCE上的电极反应过程较快。
2.7重现性、稳定性与选择性
在最佳条件下,用同一支SiO2/Au/GCE对10 μmol/L BPA平行测定10次,得峰电流值的相对标准偏差(RSD)为3.9%。 用8支新制备的SiO2/Au/GCE对10 μmol/L BPA进行测定,得RSD为4.5%。 SiO2/Au/GCE分别在4 ℃冰箱中放置10,20,30 d后,对10 μmol/L BPA进行测定,BPA的氧化峰电流分别为初始值的95%,93%和89%。 说明该电极具有较好的重现性和稳定性。
2.8标准工作曲线
在优化实验条件下,采用差示脉冲伏安法(DPV)测定不同浓度BPA在SiO2/Au/GCE上的氧化峰电流(Ipa)。 实验结果显示,BPA的氧化峰电流(Ipa,μA)随浓度的增大而增大,并分别在0.01~0.50 μmol/L和0.50~25 μmol/L范围内与其浓度(c, μmol/L)呈良好的线性关系。 线性回归方程分别为Ipa=4.126c-0.017 76(r=0.999 6)和Ipa=0.063 60c+1.109(r=0.999 6)。根据第一个回归方程可计算得该方法的检出限(S/N=3)为1.9×10-8mol/L。
2.9实际应用
在优化实验条件下,用DPV测定一次性手套中的BPA,测得样品溶液中BPA的浓度为(0.35±0.053) μmol/L(n=3,RSD=3.8%)或4.0 μg/g。对样品进行3个浓度水平(0.30,0.60,0.90 μmol/L)的加标回收实验,测得加标回收率分别为105.3%,98.9%和103.6%,RSD分别为2.9%,3.2%和2.9%,说明SiO2/Au/GCE可用于BPA实际样品的测定。 为进一步证实本法的可行性,用HPLC测得样品中BPA的浓度为(0.31±0.019) μmol/L(n=3,RSD=2.1%)或3.5 μg/g。 计算得两种方法之间的Fcalculate和tcalculate分别为3.2和 1.6。 查表知,P=95%时,Fcalculate(3.2) 本文将导电性良好的金纳米粒与大表面积的球形二氧化硅复合修饰在玻碳电极上,制备了SiO2/Au/GCE,并研究了BPA在该电极上的电化学行为,建立了一种快速灵敏测定BPA的电化学方法。该电极具有制备简单、成本低、灵敏度高、稳定性好等优点,可用于一次性手套中BPA的测定。 [1]Li J H,Kuang D Z,Feng Y L,Zhang F X,Liu M Q.Microchim.Acta,2011,172:379-386. [2]Gao Y,Cao Y,Yang D G,Luo X J,Tang Y M,Li H M.J.Hazard.Mater.,2012,199/200:111-118. [3]Sungur S,Koroglu M,Ozkan A.FoodChem.,2014,142:87-91. [4]Feng Y,Ning B A,Su P,Wang H Y,Wang C H,Chen F S,Gao Z X.Talanta,2009,80:803-808. [5]Qiu C X,Xing Y H,Yang W M,Zhou Z P,Wang Y C,Liu H,Xu W Z.Appl.Surf.Sci.,2015,345:405-417. [6]Zhang X F,Zhu D,Huang C P,Sun Y H,Lee Y I.Microchem.J.,2015,121:1-5. [7]Deceuninck Y,Bichon E,Durand S,Bemrah N,Zendong Z,Morvan M L,Marchand P,Dervilly-Pinel G,Antignac J P,Leblanc J C,Le Bizec B.J.Chromatogr.A,2014,1362:241-249. [8]Zhao X,Zhang Z E,Zhang L,Peng S X,Cheng H.J.Instrum.Anal.(赵昕,张占恩,张磊,彭淑香,成昊.分析测试学报),2015,34(1):56-61. [9]Amini N,Gholivand M B,Shamsipur M.J.Electroanal.Chem.,2014,714/715:70-75. [10]Dehdashtian S,Gholivand M B,Shamsipur M,Karimi Z.Sens.ActuatorsB,2015,221:807-815. [11]Dai X X,Qiu F G,Zhou X,Long Y M,Li W F,Tu Y F.Anal.Chim.Acta,2014,848:25-31. [12]Ma X Y,Chen M F.Sens.ActuatorsB,2015,215:445-450. [13]Mazloum-Ardakani M,Dehghani-Firouzabadi A,Sheikh-Mohseni M A,Benvidi A,Mirjalili B-B F,Zare R.Measurement,2015,62:88-96. [14]Afkhami A,Bahiraei A,Madrakian T.Mater.Sci.Eng.C,2016,59:168-176. [15]Bu Y,Park S J,Lee S W.Curr.Appl.Phys.,2014,14:784-789. [16]Bai Y,Yang H,Yang W W,Li Y C,Sun C Q.Sens.ActuatorsB,2007,124:179-186. [17]Wang T,Ma W H,Shangguan J N,Jiang W,Zhong Q.J.SolidStateChem.,2014,215:67-73. [18]Liu T,Li D S,Zou Y,Yang D R,Li H L,Wu Y M,Jiang M H.J.ColloidInterfaceSci.,2010,350:58-62. [19]Yin H S,Zhou Y L,Xu J,Ai S Y,Cui L,Zhu L S.Anal.Chim.Acta,2010,659:144-150. [20]He S,Huang D M,Bi H J,Li Z,Yang H,Cheng X D.J.Non-Cryst.Solids,2015,410:58-64. [21]Minju N,Abhilash P,Nair B P,Mohamed A P,Ananthakumar S.Chem.Eng.J.,2015,269:335-342. [22]Selvakannan P,Swami A,Srisathiyanaranan D,Shirude P S,Pasricha R,Mandale A B,Sastry M.Langmuir,2004,20:7825-7836. [23]Chauke V,Matemadombo F,Nyokong T.J.Hazard.Mater.,2010,178:180-186. [24]Zhang Y,Wang L T,Lu A B,Shi X Z,Wang C M,Duan X J.Electrochim.Acta,2012,80:77-83. [25]Fu Q C,Zheng S H,Ji L S,Lai M F,Xu C M,Huang Y.J.Instrum.Anal.(傅清晨,郑少华,纪老三,赖鸣凤,许彩满,黄颖.分析测试学报),2013,32(5):586-591. Detection of Bisphenol A on SiO2/Au Composite Membrane Modified Glass Carbon Electrode HUANG Ying*,CHEN Li-fei (College of Chemistry and Chemical Engineering,Fujian Normal University,Fuzhou350007,China) A simple and novel electrochemical method was presented for the detection of bisphenol A(BPA) using spherical silica and gold nanoparticles composite film modified glass carbon electrode(SiO2/Au/GCE).The morphology and structure of SiO2and SiO2/Au were characterized by scanning electron microscopy(SEM) and Fourier infrared spectrometry(FT-IR).Electrochemical impedance spectroscopy(EIS) and cyclic voltammetry(CV) were used to investigate the surface electrochemical property of SiO2/Au/GCE.The electrochemical behavior of BPA on SiO2/Au/GCE was studied by CV,chronocoulometry(CC),bulk electrolysis with coulometry,linear sweep voltammetry(LSV) and differential pulse voltammetry(DPV).The experimental parameters such as the thickness of film,accumulation time,pH value and scan rate were optimized,and some kinetic parameters were obtained.The results demonstrated that BPA had a good electrocatalytic activity on SiO2/Au/GCE,and the oxidation peak current at the modified electrode was 3 times as high as that at GCE.The electrooxidation of BPA on SiO2/Au/GCE was adsorption controlled,and was totally an irreversible electrode process accompanied by a two-electron and two-proton electrode reaction.Under the optimal conditions,the oxidation peak current for BPA was linear in the concentration ranges of 0.01-0.50 μmol/L and 0.50-25 μmol/L with a detection limit(S/N=3) of 1.9×10-8mol/L.The proposed method was successfully applied in the determination of BPA in disposable glove with recoveries of 98.9%-105.3%.The results were consistent with those obtained by high performance liquid chromatography(HPLC). spherical silica and gold nanoparticles composite film;glass carbon electrode;bisphenol A(BPA);electrochemical behavior 2015-12-05; 2016-01-13 黄颖,博士,教授,研究方向:毛细管电泳与电分析化学,Tel:0591-22868166,E-mail:huangying@fjnu.edu.cn doi:10.3969/j.issn.1004-4957.2016.07.007 O657.1;O625.31 A 1004-4957(2016)07-0819-063 结 论
