英夫利昔单抗治疗类风湿关节炎的临床研究
2016-08-15薛红霞
黄 睿,薛红霞,张 宁
110004
英夫利昔单抗治疗类风湿关节炎的临床研究
黄睿,薛红霞,张宁*
中国医科大学附属盛京医院风湿免疫科,沈阳
[摘要]目的探讨英夫利昔单抗治疗类风湿关节炎的临床疗效,为临床合理用药提供参考。方法回顾性分析我院风湿免疫科2013年10月至2015年6月收治的30例患者应用英夫利昔单抗治疗类风湿关节炎的情况,观察患者治疗前后症状、体征及实验室检查等情况。结果治疗后患者的血沉和CRP明显降低,病情活动情况明显减轻。30例患者中,1例出现局部注射反应,2 d内可自动消失。其余患者未发现明显不良反应。结论英夫利昔单抗能明显改善RA等风湿免疫疾病的炎症反应,抑制关节破坏进展,改善患者的临床表现及预后。
[关键词]英夫利昔单抗;类风湿关节炎;
0 引言
类风湿关节炎(Rheumatoid arthritis,RA)是一种自身免疫性疾病,呈慢性进行性发展,多数及典型患者以累及周身小关节为主。有资料表明,RA在我国的患病率大约为0.32%~0.36%,在西方国家为1%[1]。RA患者关节滑膜组织化学分析提示,TNF-α存在其滑膜衬细胞层,尤其是血管翳与软骨交界处[2-3];RA患者经治疗病情缓解后,患者血清TNF-α水平可随其他有关RA活动性指标的改善而明显降低。英夫利昔单抗作为一种新型可治疗类风湿关节炎的生物制剂,在临床实践中正逐步得到推广应用。英夫利昔单抗(Infliximab)是一种针对TNF-α,人鼠嵌合的单克隆抗体,和人体中多种形式的TNF-α具有很强的结合能力,可以有效阻断TNF-α的病理作用,以达到治疗疾病的目的,同时还具有较高的耐受性及安全性,因此是治疗RA的新选择。本研究通过回顾性分析应用英夫利昔单抗的RA患者的临床资料,观察英夫利昔单抗的临床疗效。
1 资料与方法
1.1病例选择30例入选病例均来自2013年10月至2015年6月我院风湿免疫科门诊或住院部的RA患者。30例患者中男10例,女20例;年龄24~72岁,平均年龄(52.6±14.2)岁;病程4个月~50年,平均病程为(8.46±7.54)年。治疗前,向患者充分交代所用药物的常见不良反应和可能发生的不良事件,在获得患者书面知情同意后,确定为试验对象。入选标准:①均符合2010年美国风湿病学会/欧洲抗风湿联盟(ACR/EULAR)的RA分类标准;②用药前病情活动[病情活动的判断指标为:a.关节肿胀数≥6个;b.关节压痛数≥6个;c.晨僵持续时间≥45 min;d.红细胞沉降率(ESR)≥28 mm/h和/或C反应蛋白(CRP)≥20 μg/mL];③所有患者使用非甾体抗炎药在应用英夫利昔单抗治疗前停用1个月以上,均使用慢作用药物(甲氨蝶呤)治疗前3个月已达稳定剂量。排除标准:①有严重心、肝、肾等重要脏器和血液、内分泌系统病变及病史者;②孕妇、哺乳期妇女;③活动性感染和/或具有高度感染机会的患者;④对英夫利昔单抗严重过敏者;⑤恶性肿瘤患者或有家族史的易感人群;⑥近1个月应用糖皮质激素者;⑦诊断有其他自身免疫疾病者。
1.2给药方法第0、2、6、10、16周,分别静脉给予Infliximab(类克),剂量为3 mg/kg。
1.3观察指标关节肿胀数(SJC)、关节压痛数(TJC)、ESR、CRP、类风湿因子(RF)、病情活动性评分(DAS28)等。
1.4疗效评估采用DAS28评分,DAS28 包括人体28个(组)关节的压痛计数,肿胀计数,ESR或CRP的水平以及患者的自身综合评估4个项目,应用公式加以运算,最后得出一个分数,用来评估类风湿性关节炎的疾病活动性。 DAS28的分数最低为0.7,最高为9。可按照 DAS28 将疾病的活动性分为4级,缓解(<2.6)、轻度活动(2.6~3.2)、中度活动(3.2~5.1)和重度活动(>5.1)。如果在接受治疗后,患者的DAS28降低>1.2,说明该治疗很有效果,DAS28降低0.6~1.2,说明有一些效果,如果DAS28降低<0.6或DAS28仍然在5.1以上,说明该治疗无效。
1.5不良反应随时记录不良反应发生的时间、严重程度、持续时间,采取措施及结果,是否需要终止治疗。
1.6统计学处理采用SPSS 13.0统计分析软件,组间比较采用配对样本的t检验方法,相关性检验采用直线相关分析并计算Pearson相关系数,P<0.05为差异有统计学意义。
2 结果
2.1Infliximab治疗RA前后各实验室指标的改善情况治疗16周后复查血沉、CRP等指标,同时再次对患者进行DAS28评分。结果表明,英夫利昔单抗可以明显降低类风湿关节炎患者的血沉和CRP,病情活动情况明显减轻。见表1。
2.2部分患者Infliximab治疗RA前后DAS28评分情况见表2。
2.3不良反应30例患者中,有1例出现局部注射反应,2 d内可自动消失。其余患者未发现明显的不良反应。

表1 Infliximab治疗RA前后各实验室指标的改善情况
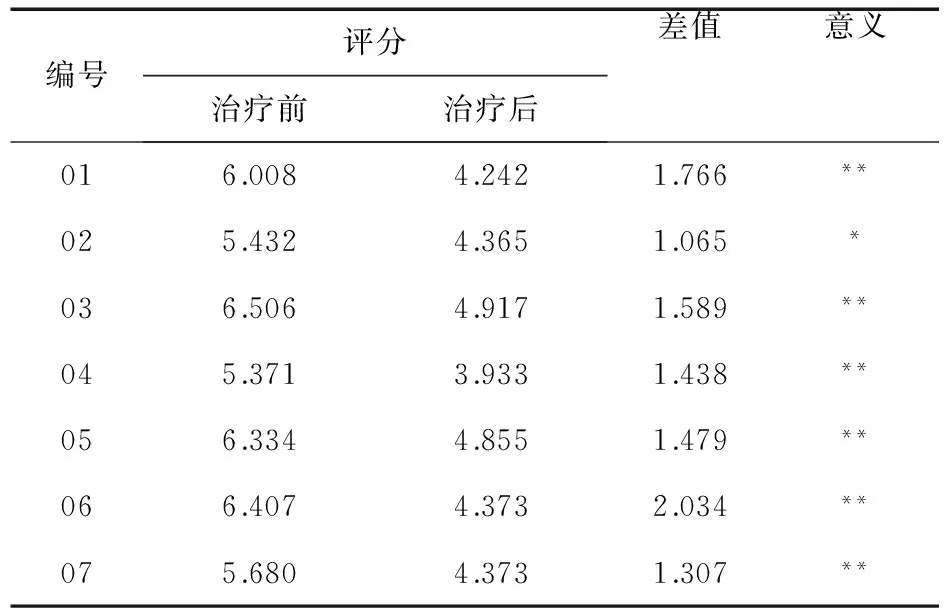
表2 部分患者Infliximab治疗RA前后DAS28评分情况
注:**表示治疗有明显疗效,*表示治疗有一些效果
3 讨论
RA是一种以慢性、进行性、反复发作且具有致畸性的对称性多关节炎为主要临床表现,可累及心脏、肺脏等重要脏器的全身性自身免疫性疾病,如能早期发现并且在早期对RA患者进行有效的干预,可以显著减少和延缓RA患者的关节侵蚀和破坏,降低其残疾甚至死亡的可能[4-6]。在生物制剂出现之前,仅有有限的几种药物可用于缓解病情进展,并且其效果显现并不明显或较为缓慢,且因其中大部分药物有相当的不良反应或严重的毒性反应,造成患者依从性较差,无法坚持服药,治疗效果更加不令人满意。
以往临床上治疗RA的药物主要是非甾体抗炎药(NSAIDs)、改善风湿病情药物及糖皮质激素。NSAIDs可以通过抑制环氧化酶(COX),抑制花生四烯酸转化为前列腺素,具有镇痛抗炎的作用。其起效快,可以改善关节炎症状,但不能控制病情发展,且对胃肠道,肾脏及心血管系统有一定的不良反应。由于NSAIDs不能控制病情发展,所以与改变病情的抗风湿药(DMARDs)合用,常用药物包括:甲氨喋呤、柳氮磺胺吡啶、来氟米特、羟氯喹等,虽然这些现有的药物在控制RA患者的炎症和疾病进展上起到一定作用,但这些药物起效慢,临床症状明显改善大约需要1~6周,毒副作用较多。临床观察也发现,即使患者遵照医嘱,按时按量用药,连续治疗5~10年,或者坚持更长的用药时间,疾病的活动指标在一定程度上得到明显的缓解和改善,但仍然不能阻止关节侵蚀和破坏的进展。除了上述药物以外,既往对于DEMARS药物效果不明显的RA患者大多加用小剂量激素。小剂量糖皮质激素能加速淋巴细胞凋亡,降低外周血嗜酸性粒细胞及单核细胞的数量并减弱中性粒细胞的吞噬作用,减少抗体的生成,从而达到降低免疫介导的炎症,控制自身免疫疾病症状的作用,但其具有一定的不良反应,并且效果有限,即使小剂量(5~10 mg/d)的泼尼松,长期连续口服也容易引起骨质疏松的发生,并且增加感染的机会。
TNF-α在正常人体内可由多种细胞产生,主要为单核/巨噬细胞分泌,其主要刺激因子包括细菌脂多糖、病毒、真菌、免疫复合物及其他细胞因子等;正常浓度下,其具有广泛的生物学活性,是目前发现的细胞因子中抗瘤作用最强的细胞因子;除对肿瘤细胞的增殖有直接抑制作用外,还可导致细胞坏死。肿瘤坏死因子对正常细胞的生长分化也有影响,同时可抗细菌和病毒,激活T 细胞,促进IL-21、IL-22 等的产生及分泌,诱发炎症反应等,此外,能摧毁肿瘤周围的血管上皮组织,形成血栓,阻断肿瘤的血液供应,导致肿瘤出血坏死。但其在高浓度时,超过生理量的TNF-α的产生和释放会打破机体的免疫平衡,与其他炎症因子如白介素等共同引起多种病理损伤。
英夫利昔单抗是一种生物制剂,是细胞因子TNF-α的抑制剂,TNF-α在RA患者中主要由血单核细胞和关节滑膜巨噬细胞分泌,也可由内皮细胞、淋巴细胞、平滑肌细胞、成纤维细胞、表皮细胞等产生。RA 患者TNF-α及TNFR 水平在血清、滑膜、滑液中均升高,尤其是病情严重及活动期患者,其浓度与RA患者疾病严重程度一致,是RA发病过程中重要的促炎性细胞因子,在RA发病过程中的主要机制包括以下几个方面:①诱导内皮细胞表达黏附分子,通过黏附分子介导促进白细胞与血管内皮的黏附,进而导致局部炎症;②TNF-α的高水平表达刺激滑膜的成纤维细胞、软骨细胞产生前列腺素E2,通过前列腺素E2在炎症的发生发展过程中起重要作用,促进骨质破坏和吸收,并可产生胶原酶,抑制骨胶原的合成;③促进软骨细胞分泌纤维蛋白溶酶激活剂,使纤维蛋白酶原转变成纤维蛋白,加速关节损伤;可增加滑膜、内皮细胞及成纤维细胞产生生长因子并释放,进而使血管翳形成,滑膜肥厚。血管翳具有很强的破坏性,是造成关节破坏和畸形的病理基础。同时,RA患者关节滑膜中的TNF-α可以通过下调人单核细胞亚铁血红素氧化酶-1(HO-1)的表达来促进炎症反应;以及通过下调相关编码基因的反式作用因子水平,以减少骨髓细胞HLA-DR的表达,进而降低骨髓细胞刺激T细胞的能力。因此,抑制TNF使得骨髓细胞恢复HLA-DR的表达,能够使T细胞介导的慢性炎症得到一定改善[7]。同时,TNF-α拮抗剂可竞争性结合细胞表面TNF受体,减少TNF-α和细胞表面TNF受体结合,使其不能发挥生理作用,减少了TNF-α介导的炎症反应[8]。通过以上多种途径,TNF-α拮抗剂比常用的DRAMS药物MTX能更快地减轻早期RA症状,延缓关节破坏[6]。同时有报道,英夫利昔单抗可以降低TNF-α、IL-1、INF-γ、IL-6等Th1型细胞因子的水平,同时增强IL-10等Th2型细胞因子的效应,这与MTX的作用机制各有侧重,因此两者联合用药可以互相补充,产生协同作用[9-10]。此外,英夫利昔单抗可以更强结合TNF-α,通过激活补体和抗体依赖的细胞毒性(ADCC)作用,特异性地溶解产生的活性细胞,使TNF-α失去生物活性,有效抑制体内TNF-α,达到治疗和预防RA的效果。最早有国外研究者认为,对于活动性RA,一般在选用1种以上传统的DMARD(常用MTX)之后,推荐选用TNF-α阻断剂。
MTX是临床上推荐RA患者的首选用药。MTX是一种周期特异性药物,抑制细胞内的二氢叶酸还原酶,通常情况下二氢叶酸可以在二氢叶酸还原酶的作用下生成四氢叶酸,四氢叶酸具有生理活性。甲氨蝶呤的常见和主要的不良反应包括肝功能异常,胃肠道不适,骨髓抑制,一般患者不良反应较轻,停药后多能恢复。但用药期间需监测肝功能、血常规等指标。也有研究表明,TNF-α阻断剂与其他DMARDs的应用效果优于传统单用DMARS药物[11]。目前,生物制剂已成功应用于RA的治疗,越来越多的患者使用生物制剂,大量的循证医学表明,它比传统的慢作用抗风湿药物能更快地达到疾病缓解,尤其对于处于中高活动度的RA患者,生物制剂可降低其活动性;且在疗效指标上也显著优于传统药物,在放射学改变上也表现出优势。
英夫利昔单抗与MTX药理作用不尽相同,两者联用使RA的临床症状快速缓解,关节功能状态明显改善,延缓软骨和骨质的破坏,还可以使部分患者停止使用药物后持续缓解。加用英夫利昔单抗后,弥补了传统DMARS药物起效较慢的缺点。而且,英夫利昔单抗与传统治疗RA的药物相比较,对人体的毒副作用更少,对于需要长期服药的患者来说,具有良好的耐受性。有文献报道,TNF-α拮抗剂最常见的不良反应为局部注射部位反应或感染[12-13]。英夫利昔单抗的不良反应较上述传统药物轻微。本试验30例患者中,仅有1例患者出现了注射部位的局部反应,但2 d后自然消失,未发现明显的感染。
但需要注意的是,有报道,TNF-α拮抗剂有可能增加机体发生严重感染、增加感染结核的危险性及引发肿瘤的可能[14-15]。本实验观察时间较短,病例数少,未发现患恶性肿瘤患者及新近结核感染,但在临床治疗中仍要密切观察患者的用药情况,尤其是不良反应情况。总之,英夫利昔单抗能明显改善RA等风湿免疫疾病的炎症反应,抑制关节破坏进展,改善患者的临床表现及预后。但对生物制剂长期治疗的安全性及不良反应有待进一步临床观察。
参考文献:
[1]葛均波,徐永健.内科学[M].第8版.北京:人民卫生出版社,2013:808-814.
[2]Bouchelouche K,Turkbey B,Choyke PL.PET/CT and MRI in bladder cancer[J].J Cancer Sci Ther,2012,(1):S14.
[3]Kirino Y,Takeno M,Murakami S,et al.Tumor necrosis factor alpha acceleration of inflammatory responses by down-regulating heme oxygenase 1 in human peripheral monocytes [J].Arthritis Rheum,2007,56:464-475.
[4]苏妍,徐高四,涂卫平,等.英夫利西单抗联合甲氨蝶呤治疗类风湿性关节炎的Meta分析[J].实用医学杂志,2014,30(13):2142-2147.
[5]杨文浩,刘宁,袁伟,等.类风湿关节炎患者心血管疾病危险因素调查[J].中国医药,2015,10(8):1107-1111.
[6]马中双,张育.NLRP3炎性体与类风湿关节炎相关性的研究进展[J].实用医学杂志,2014,30(13):2024-2026.
[7]Mueller RB,Skapenko A,Grunke M,et al.Regulation of myeloid cell function and major histocompatibility complex class II expression by tumor necrosis factor[J].Arthritis Rheum,2005,52:451-460.
[8]Nayak B,Dogra PN,Naswa N,et al.Diuretic 18F-FDG PET/CT imaging for detection and locoregional staging of urinary bladder cancer:prospective evaluation of a novel technique[J].Eur J Med Mol Imaging,2013,40(3):386-393.
[9]Lindén C,Bjrklund A.Living with rheumatoid arthritis and experiencing everyday life with TNF-α blockers[J].Scand J Occup Ther,2010,17:326-334.
[10]Sfikakis PP.The first decade of biologic TNF antagonists in clinical practice: lessons learned,unresolved issues and future directions[J].Curr Directions Autoimmunity,2010,11:180-210.
[11]Amri M,Sfar I,Skhiri H,et al.Anti-CCP antibodies,rheumatoid factors and anti-keratin antibodies:clinical value in established rheumatoid arthritis [J].Tunis Med,2011,89(3):231-235.
[12]Furst DE,Breedveld FC,Kalden JR,et al.Updated consensus statement on biological agents,specifically tumour necrosis factor alpha (TNFalpha) blocking agents and interleukin-1 receptor antagonist (IL-1ra),for the treatment of rheumatic diseases,2004[J].Ann Rheum Dis,2004,63:ii2-ii12.
[13]Vinay DS,Kwon BS.Targeting TNF superfamily members for thera-peutic intervention in rheumatoid arthritis[J].Cytokine,2012,57(3):305-312.
[14]Augustsson J,Neovius M,Cullinane-Carli C,et al.Patients with rheumatoid arthritis treated with tumour necrosis factor antagonists increase their sect1icipation in the workforce: potential for significant long-term indirect cost gains (data from a population-based registry) [J].Ann Rheum Dis,2010,69: 126-131.
[15]Daïen CI,Daïen V,Parussini E,et al.Etanercept concentration in patients with rheumatoid arthritis and its potential influence on treatment decisions: a pilot study[J].J Rheumatol,2012,39(8):1533-1538.
收稿日期:2015-12-31
基金项目:辽宁省自然科学基金(2014021081)
*通信作者
DOI:10.14053/j.cnki.ppcr.201603019
Clinical effect of infliximab in treatment of rheumatoid arthritis
HUANG Rui,XUE Hong-xia,ZHANG Ning*
(Rheumatism and Immunology Desect1ment,Shengjing Hospital of China Medical University,Shenyang 110004,China)
【Abstract】ObjectiveTo investigate the clinical effects of infliximab in the treatment of rheumatoid arthritis (RA) and provide references for rational clinical drug use.Methods30 patients at the Rheumatism and Immunology Desect1ment in our hospital were administered and were given infliximab to treat RA from Octorber 2013 to June 2015.The patients′ pre-and post-treatment symptoms,signs,and progression were reviewed.ResultsAfter infliximab treatment,ESR and CRP of the 30 patients reduced,and their conditions were significantly improved.One of the 30 patients displayed local reactions at the injection site,which disappeared spontaneously within 2 days.There were no adverse events among the remaining patients.ConclusionInfliximab can suppress the inflammatory reaction of RA and rheumatic immunological diseases,inhibit the progression of joint damage,and improve the clinical manifestations and prognosis of patients.
Key words:Infliximab; Rheumatoid arthritis
