高效液相色谱法测定复方氯甲霜中氯霉素及甲硝唑的含量
2016-08-12杨瑾莫国栋林丽曾维国李嘉良卢志军
杨瑾,莫国栋,林丽,曾维国,李嘉良,卢志军
(广东省中山市第二人民医院,广东 中山 528447)
高效液相色谱法测定复方氯甲霜中氯霉素及甲硝唑的含量
杨瑾,莫国栋,林丽,曾维国,李嘉良,卢志军
(广东省中山市第二人民医院,广东 中山528447)
摘要:目的对复方氯甲霜的质量标准进行再提高研究。方法色谱柱为AgiLent XDB-C18(150 mm×4.6 mm,5 μm);流速为1 mL·min-1;柱温为30℃;进样量为10 μL;氯霉素的流动相为甲醇-庚烷磺酸钠缓冲溶液(32∶68);紫外检测波长为277 nm;甲硝唑的流动相为甲醇-水(20∶80);紫外检测波长为320 nm。结果氯霉素、甲硝唑进样量分别在5.56~111.2,26.02~260.2 mg·L-1浓度范围内与峰面积呈良好的线性关系,r分别为1.000 0和0.999 6(n=6);平均回收率分别为103.8%,99.6 %,RSD分别为1.73 %和0.43%(n=9)。结论该方法简便快速、准确、重复性好,可用于该制剂中氯霉素及甲硝唑的含量测定。
关键词:色谱法,高压液相;氯霉素;甲硝唑
复方氯甲霜是我院皮肤科临床应用多年的自制制剂,该制剂由氯霉素、甲硝唑等组成,具有抗菌、消炎、杀螨、止痒、收敛等作用,用于治疗无渗出性皮炎、酒糟鼻、痤疮及螨虫引起的皮肤感染[1-6]。原质量标准仅对氯霉素、甲硝唑做了简单的化学鉴别,并无含量测定项。为进一步有效控制此制剂的质量,提高其标准,本试验参文献[7-10]方法,拟建立了以HPLC 法测定处方中主要成分氯霉素及甲硝唑的含量。结果表明,此方法简便、准确,可作为控制此制剂的质量指标。
1 材料
1.1仪器、试剂安捷伦1260 液相色谱仪, G1311C泵,G1329B自动进样器,G1314B紫外检测器,Eclipse XDB-C18色谱柱(150 mm×4.6 mm,5 μm),(Agilent)AT-330色谱柱恒温箱(天津奥特赛恩斯仪器有限公司),AUW220D电子天平(SHIMADZU),TDL-60B离心机(上海安亭科学仪器厂),AS20500A超声波清洗器(天津奥特赛恩斯仪器有限公司),甲醇为色谱纯,庚烷磺酸钠为分析纯,水为超纯水。
1.2试药氯霉素对照品(中国药品生物制品检定所,批号:130555-200602),甲硝唑对照品(中国食品药品检定研究院,批号:100191-200606),复方氯甲霜(中山市第二人民医院自制,批号:20140120、20140121、20140122)。
2 方法与结果
2.1氯霉素
2.1.1溶液的制备(1)供试品溶液:称取本品0.3 g,加流动相溶解,并转移至50 mL量瓶中,加流动相至刻度,摇匀,吸取10 mL浑浊液,离心(转速3 000 r·min-1,5 min),取出,吸取上清液,作为供试品溶液。(2)阴性对照溶液:按处方制备不含氯霉素的阴性对照制剂,精密量取阴性对照制剂,按供试品溶液制备项下方法制备,即得。(3)对照品溶液取氯霉素对照品10 mg,精密称定,置50 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,作为对照品储备液。
2.1.2色谱条件色谱柱:AgiLent XDB-C18(150 mm×4.6 mm,5 μm);流动相以甲醇-庚烷磺酸钠缓冲溶液(32∶68);流速为1.0 mL·min-1;柱温为30℃;检测波长为277 nm。取“2.1.1”项下对照品、供试品、阴性对照溶液进样测定,记录色谱图。在此色谱条件下,供试品中其他成分对氯霉素的测定无干扰,见图1。
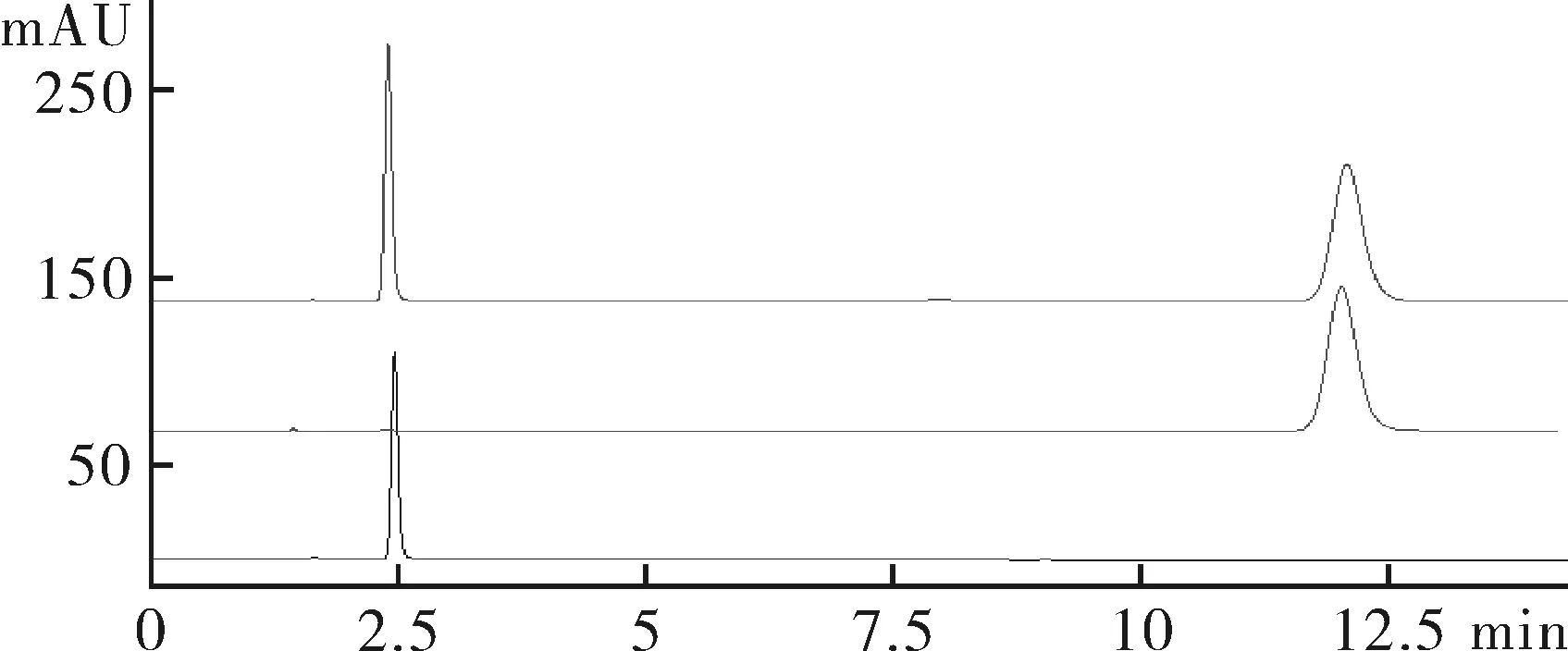
注:1为杂质峰,2为氯霉素峰;A为供试品,B为氯霉素对照品,C为阴性对照品。
图1氯霉素HPLC色谱图(277 nm)
2.1.3线性相关性试验精密量取“2.1.1(3)”氯霉素对照品贮备液1,2,2.5,5,10 mL分置10 mL量瓶中,用甲醇稀释至刻度,作为系列标准溶液,按上述色谱法,分别进样10 μL,记录色谱图。以标准溶液的浓度X(g·L-1)为横坐标,峰面积Y为纵坐标绘制标准曲线,氯霉素的回归方程为:Y=14.637X+0.000 2,(r=1.000 0)。结果表明:氯霉素在5.56~111.2 mg· L-1浓度范围内,与峰面积呈良好的线性关系。
2.1.4精密度试验取“2.1.1(3)”项下氯霉素对照品溶液,按上述色谱法,连续测定6次,记录色谱图。结果测得氯霉素峰面积RSD为1.08 %,表明采用上述色谱法测定本品含量精密度较高,可满足本品含量测定要求。
2.1.5重复性试验取供试品溶液(批号:20140120),按“2.1.1(1)”供试品溶液制备项下方法制备供试品,连续测定6次,按上述色谱条件测定,结果氯霉素RSD为0.18%,表明表明采用上述色谱法测定本品含量方法重复性良好,可满足本品含量测定要求。
2.1.6溶液稳定性试验取供试品溶液(批号:20140120),按上述色谱条件分别于0、2、4、6、12、24 h进行测定,记录色谱图。结果测得氯霉素RSD为1.26%,表明供试品溶液24 h内稳定性良好。
2.1.7回收率试验精密称取不含氯霉素的阴性样品9份,取已知含量的氯霉素对照品,按80%,100%,120%三个水平各配3份,按“2.2.1”项下方法制备供试品溶液,按上述色谱条件进样测定,并计算回收率。结果平均回收率为103.8%,RSD为1.73%(n=9)。
2.1.8含量测定取本品3批,按“2.2.1(1)”项下方法制备供试品溶液,按上述色谱条件分别进样测定,记录色谱图,按外标法计算含量,结果氯霉素标示百分含量分别为88.15%、87.66%、84.78%,符合标准要求(氯霉素含量应为标示量80.0%~110.0%)。
2.2甲硝唑
2.2.1溶液的制备(1)供试品溶液:称取本品2.5 g,加流动相溶解,并转移至100 mL量瓶中,加流动相至刻度,摇匀,吸取10 mL浑浊液,离心(转速3 000 r·min-1,5 min),取出,吸取上清液,作为供试品溶液。(2)阴性对照溶液按处方制备不含甲硝唑的阴性对照制剂,精密量取阴性对照制剂,按供试品溶液制备项下方法制备,即得。(3)对照品溶液取甲硝唑对照品10 mg,精密称定,置50 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,作为对照品储备液。
2.2.2色谱条件色谱柱:AgiLent XDB-C18(150 mm×4.6 mm,5 μm);流动相以甲醇-水(20∶80);流速为1.0 mL·min-1;柱温为30℃;检测波长为320 nm。取“2.2.1”项下对照品、供试品、阴性对照溶液进样测定,记录色谱图。在此色谱条件下,供试品中其他成分对甲硝唑的测定无干扰,见图2。
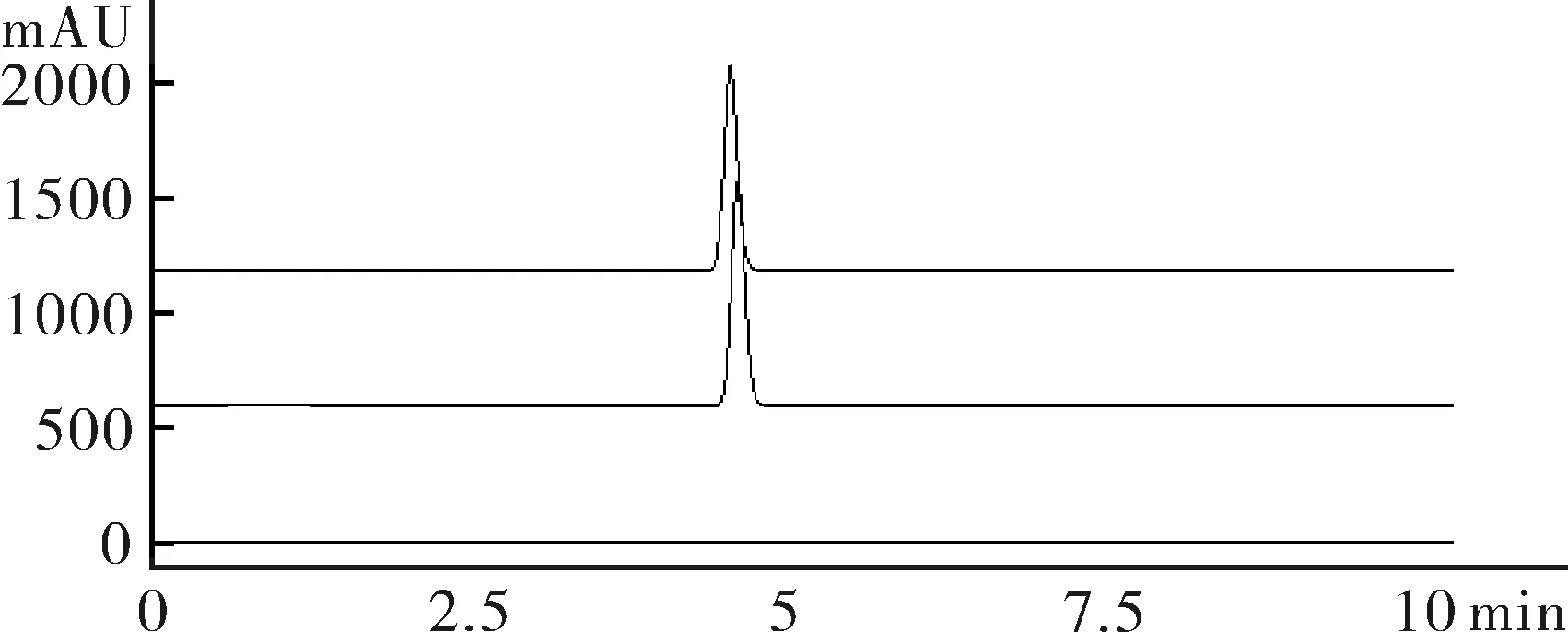
注:3为甲硝唑峰;D为供试品,E为甲硝唑对照品,F为阴性对照品。
图2甲硝唑HPLC色谱图
2.2.3线性相关性试验精密量取“2.2.1(3)”甲硝唑对照品贮备液1,2,2.5,5 mL置10 mL量瓶中,用甲醇稀释至刻度,作为系列标准溶液,按上述色谱法,分别进样10 μL,记录色谱图。以标准溶液的浓度X( g·L-1)为横坐标,峰面积Y为纵坐标绘制标准曲线,甲硝唑的回归方程为:Y=32.517X-55.993,(r=0.999 6)。结果表明:甲硝唑在26.02~260.2 mg·L-1浓度范围内,与峰面积呈良好的线性关系。
2.2.4精密度试验取“2.2.1(3)”项下甲硝唑对照品溶液,按上述色谱法,连续测定6次,记录色谱图。结果测得甲硝唑峰面积RSD为0.54%,表明采用上述色谱法测定本品含量精密度较高,可满足本品含量测定要求。
2.2.5重复性试验取供试品溶液(批号:20140120),按“2.1.1(1)”供试品溶液制备项下方法制备供试品,连续测定6次,按上述色谱条件测定,结果甲硝唑RSD为0.78%,表明表明采用上述色谱法测定本品含量方法重复性良好,可满足本品含量测定要求。
2.2.6溶液稳定性试验取供试品溶液(批号:20140120),按上述色谱条件分别于0、2、4、6、12、24 h进行测定,记录色谱图。结果测得甲硝唑RSD为1.47%,表明供试品溶液24 h内稳定性良好。
2.2.7回收率试验精密称取不含甲硝唑的阴性样品9份,取已知含量的甲硝唑对照品,按80%、100%、120%三个水平各配三份,按“2.2.1”项下方法制备供试品溶液,按上述色谱条件进样测定,并计算回收率。结果平均回收率为99.6 %,RSD为0.43%(n=9)。
2.2.8含量测定取本品3批,按“2.2.1(1)”项下方法制备供试品溶液,按上述色谱条件分别进样测定,记录色谱图,按外标法计算含量,结果甲硝唑标示百分含量分别为87.72 %、87.67 %、87.44%,符合标准要求(甲硝唑含量应为标示量80.0 % ~ 110.0 %)。
3 讨论
取甲硝唑和氯霉素对照品,分别加甲醇适量使溶解并稀释成每1 mL 中含10 μg 的溶液,照紫外-可见分光光度法在200 ~400 nm 波长范围内进行扫描,结果表明,甲硝唑在320 nm 波长处有最大吸收,氯霉素在277 nm 波长处有最大吸收。有文献选择278 nm作为检测波长,同时检测这两种物质,虽然方法简单,但是由于同一流动相及波长下,氯霉素和甲硝唑的响应值差别较大,峰形差,保留时间长,分析准确度有所降低。为使氯霉素和甲硝唑有较好的响应,所以本文分别采用不同流动相不同波长下测定氯霉素及甲硝唑的含量。
参考文献
[1]郝江华,郗宁,唐晓琳.小剂量强力霉素联合甲硝唑凝胶治疗酒渣鼻疗效观察[J].中国皮肤性病学杂志,2012,26(4):308-309.
[2]姜群.玫芦消痤膏加甲硝唑片剂外用治疗酒糟鼻疗效评价[J].黑龙江医学,2012,36(3):212-213.
[3]周圆,王方,柯萍,等.甲硝唑在皮肤科的应用[J].医学综述,2011,17(8):1207-1209.
[4]崔金环,王琛,徐颖,等.自制灭螨液体外杀螨及治疗人体面部蠕形螨病的临床研究[J].时珍国药,2012,23(12):3078-3079.
[5]董红霞.氯霉素酒精联合甲硝唑外用治疗皮肤痤疮的疗效观察[J].内蒙古医药,2013,7:131
[6]侯军才,马俊英,赵艳庚.欧龙马联合氯霉素硼酸粉在促进中耳炎干耳进程的临床应用价值探讨[J].安徽医药,2015,19(8):1589-1590.
[7]王浩,张霞,秦文涛.高效液相色谱法测定康肤霜中甲硝唑和氯霉素含量[J].药物鉴定,2011,20(1):27-28.
[8]赵建颖.高效液相色谱法同时测定复方甲硝唑搽剂中甲硝唑和氯霉素含量[J].中国药业,2012,21(20):40-41.
[9]张娜,徐强,周娟.RP-HPLC、紫外分光光度法及容量法测定甲硝唑的含量[J].韶关学院学报,2013,34(12):45-48.
[10] 徐莲琴,王玉华,郑亿,等.RP-HPLC 法测定复方甲硝唑涂剂中甲硝唑和醋酸泼尼松的含量[J].中国药房,2013,24(3):1218-1219.
doi:10.3969/j.issn.1009-6469.2016.07.014
(收稿日期:2016-02-28,修回日期:2016-04-17)
Quality specification standard of Chloramphenicol Metronidazole Cream
YANG Jin,MO Guodong,Lin Li,et al
(SecondPeople’sHospital,Zhongshan,Guangdong528447,China)
Abstract:ObjectiveTo improve quality standards of Chloramphenicol Metronidazole Cream.MethodsChloramphenicol andmetronidazole were assayed by HPLC.AgiLent XDB-C18(150 mm×4.6 mm,5 μm) was used at the rate of 1.0 mL·min-1.The injection volume was 10 μL and the column temperature was set at 30 ℃.277 nm and 320 nm were selected asthe detection wavelengths forchloramphenicol and metronidazole respectively,and themobile phasesweremethanol-sodiumheptanesulfonate(32∶68)forchloramphenicol and methanol-water(20∶80)formetronidazole,respectively.ResultsA good linearrelationship was established between the peak response and the concentration of chloramphenicol and metronidazole over the range of 5.56~111.2 mg·L-1(r=1.000 0) and 26.02~260.2 mg·L-1(r=0.999 6) respectively.The mean recoveries of chloramphenicol and metronidazole were103.8 %(RSD=1.73%)and 99.6 %(RSD=0.43%),respectively.ConclusionThe method is simple,accurate and repeatable,which can be used for the determination of Chloramphenicol Metronidazole Cream.
Key words:Chromatography,High Pressure Liquid;Chloramphenicol;Metronidazole
