N-甲基-D-天冬氨酸受体抑制剂盐酸美金刚对老年性痴呆大鼠β-淀粉样前体蛋白及β分泌酶表达的影响
2016-08-12吴芳
吴芳
(重庆三峡中心医院神经内科,重庆 404000)
N-甲基-D-天冬氨酸受体抑制剂盐酸美金刚对老年性痴呆大鼠β-淀粉样前体蛋白及β分泌酶表达的影响
吴芳
(重庆三峡中心医院神经内科,重庆404000)
摘要:目的探讨N-甲基-D-天冬氨酸(NMDA)受体抑制剂盐酸美金刚对老年性痴呆(AD)大鼠β-淀粉样前体蛋白(APP)及β分泌酶(BACE1)表达的影响。方法30只SD大鼠随机数字表法分为假手术组、模型组、治疗组(盐酸美金刚组);除假手术组外,其余两组大鼠海马注射10 μg β-淀粉样蛋白(Aβ)1-40构建AD大鼠模型,治疗组大鼠腹腔注射10 mg·kg-1·d-1盐酸美金刚,其余两组给予等量生理盐水,连续给药14 d,并于第1、3、7、14 天采用Morris水迷宫实验检测大鼠的空间学习记忆能力,于14 d处死大鼠取血及海马组织。ELISA法检测血清及海马组织中Aβ含量,western blot及RT-PCR法检测海马组织中APP和BACE1蛋白及mRNA表达量。结果与假手术组比较,模型组大鼠水迷宫潜伏期延长,Aβ含量显著提高,APP及BACE1蛋白及mRNA含量显著提高,均差异有统计学意义(P<0.01);与模型组比较,治疗组大鼠水迷宫潜伏期缩短,Aβ含量显著降低,APP及BACE1蛋白及mRNA含量显著下降,均差异有统计学意义(P<0.01)。结论盐酸美金刚能通过阻断APP裂解,从而抑制AD大鼠海马组织中Aβ沉积。
关键词:阿尔茨海默病;美金刚;受体,N-甲基-D-天冬氨酸;淀粉样前体蛋白分泌酶类;大鼠,Sprague-Dawley
阿尔茨海默病(Alzheimer’s Disease,AD)又称老年性痴呆,是一种中枢神经系统退行性疾病,其临床主要病理特征为老年斑形成,神经元缠结及丢失。β淀粉样蛋白(β-amyloid protein,Aβ)是老年斑的主要成分,在脑内沉积可引起神经元的丢失死亡[1-3]。Aβ的形成是神经细胞膜上β-淀粉样前体蛋白(APP)在β分泌酶(BACE1)作用下产生的[4]。因此,通过抑制APP降解,能有效的抑制Aβ形成,从而缓解AD患者老年斑形成。盐酸美金刚是是一种新型的,低中度亲和力,电压依赖的N-甲基-D-天冬氨酸(NMDA)受体非竞争性抑制剂,已被美国FDA批准用于中、重度AD患者的治疗。同时临床研究也已证实盐酸美金刚对中、重度AD患者具有显著疗效,且盐酸美金刚治疗AD患者的机制主要集中于能够拮抗NMDA受体,从而阻滞NMDA引起的谷氨酸兴奋性损伤,减轻细胞凋亡,改善学习记忆功能[5-7]。而对于盐酸美金刚是否能通过阻止APP裂解,进而抑制Aβ生成还未见报道。因此,本研究拟通过构建AD模型大鼠,通过腹腔注射给予盐酸美金刚,检测治疗前后大鼠海马组织中APP,BACE及Aβ含量的变化。
1 材料与方法
1.1材料
1.1.1实验动物30只SD大鼠,体重(200±20)g,清洁级,购自上海斯莱克实验动物有限责任公司,合格证(SCXK(沪)2012-0002)。室内温度控制在(23±2)℃,大鼠自由饮食和摄水。
1.1.2主要试剂及仪器盐酸美金刚购自丹麦灵北药厂,批号:D1420011991;大鼠Aβ1-40检测试剂盒(上海丰寿实业有限公司,批号:fs-3558);兔抗APP,BACE1单克隆抗体(美国Epitmics公司);迷你双垂直电泳仪,迷你转印电泳仪(北京六一仪器厂);ChemiDocTM XRS凝胶成像系统(美国Bio-Rad公司)。
1.2方法
1.2.1模型制备[4]大鼠用10%水合氯醛腹腔注射麻醉,固定,剔除大鼠头部毛发,碘消毒。参考相关文献,沿着小鼠大脑矢状线切开皮肤,使颅骨暴露,并用牙科钻钻开颅骨使脑膜暴露出来,将微量注射器垂直插入,缓慢注射2 μL Aβ1-40(10 μg),5 min注射结束,并留针5 min。用牙科泥封堵住后,常规缝合头部皮肤并消毒。假手术组注入等量生理盐水,其余步骤与模型组一致。
1.2.2分组及给药[8-9]大鼠随机数字表法分为假手术组、模型组、盐酸美金刚组,于术后24 h对模型动物注射10 mg·kg-1·d-1盐酸美金刚,其余两组给予等量生理盐水,连续给药14 d。大鼠处死,并取血分离出血清用于Aβ的检测,后心脏灌注生理盐水取出大脑,并于冰上分离出海马组织,用于RT-PCR及western blot检测。
1.2.3认知功能测定[9]采用Morris水迷宫实验检测大鼠的空间学习记忆能力。整个认知功能测试过程中,保持实验室内灯光,物品摆放位置的不变,以排除环境因素对实验动物的干扰。
1.2.4血清及海马组织中Aβ含量检测根据试剂盒说明书检测血清及海马组织中Aβ含量。
1.2.5RT-PCR根据trizol试剂盒(Invitrogen)说明书提取海马组织总RNA,并检测RNA纯度。通过一步法RT-PCR试剂盒将RNA逆转录成cDNA并进行PCR扩增,获取5 μL扩增产物用于下一步2%的琼脂糖胶进行检测并拍照。引物分别加入25 μL PCR反应体系中,反应条件为94 ℃变性45 s,59 ℃复性45 s,72 ℃延伸60 s,共35个循环。引物如表1。

表1 RT-PCR引物
1.2.6western blot海马组织经匀浆后,加入组织裂解液,离心获得总蛋白。根据BCA试剂盒对蛋白浓度进行测定。蛋白上样,SDS凝胶电泳,湿法转膜。一抗孵育,4℃过夜;二抗室温孵育1-2 h。膜上滴加ECL曝光液,凝胶成像系统中曝光。采用Quantity one软件对各抗体条带灰度值进行统计。

2 结果
2.1各组大鼠Morris水迷宫逃避潜伏期如表2所示,与假手术组比较,模型组大鼠水迷宫潜伏期延长,差异有统计学意义(P<0.01);与模型组比较,治疗组大鼠水迷宫潜伏期缩短,差异有统计学意义(P<0.01)。
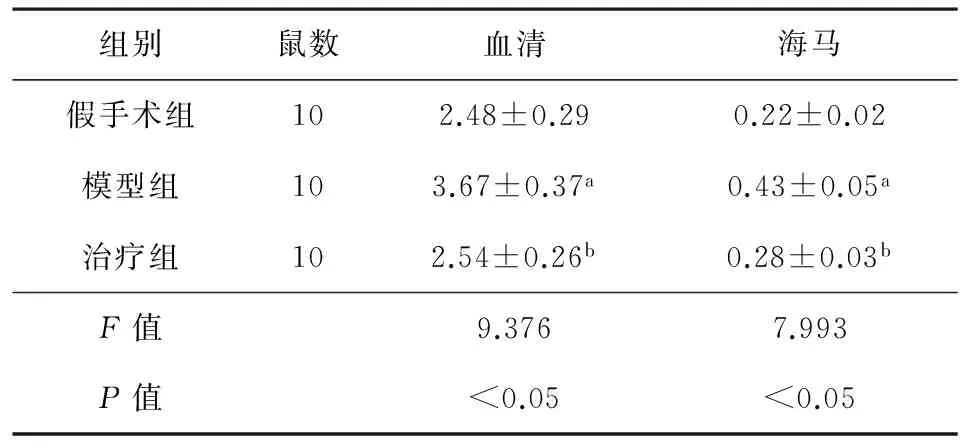
2.2各组大鼠血清及海马组织中Aβ含量的测定如表3所示,与假手术组比较,模型组血清及海马组织中Aβ含量显著提高;与模型组比较,治疗组血清及海马组织中Aβ含量显著降低;均差异有统计学意义(P<0.01)。
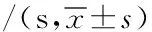
表2 各组大鼠Morris水迷宫逃避潜伏期
注:与假手术组比较,aP<0.01;与模型组比较,bP<0.01。
表3各组大鼠血清及海马组织中Aβ含量的测定
组别鼠数血清海马假手术组102.48±0.290.22±0.02模型组103.67±0.37a0.43±0.05a治疗组102.54±0.26b0.28±0.03bF值9.3767.993P值<0.05<0.05
注:与假手术组比较,aP<0.01;与模型组比较,bP<0.01。
2.3各组大鼠海马组织中APP及BACE1蛋白含量的测定如图1、表4所示,与假手术组比较,模型组血清及海马组织中APP及BACE1蛋白含量显著提高;与模型组比较,治疗组血清及海马组织中APP及BACE1蛋白含量显著降低;均差异有统计学意义(P<0.01)。

图1 各组大鼠海马组织中APP及BACE1蛋白含量的测定表4 各组大鼠海马组织中APP及BACE1蛋白 含量的测定±s

组别鼠数APP/GAPDHBACE1/GAPDH假手术组100.13±0.010.12±0.01模型组100.49±0.05a0.46±0.05a治疗组100.26±0.02b0.25±0.02bF值15.29112.524P值<0.01<0.01
注:与假手术组比较,aP<0.01;与模型组比较,bP<0.01。
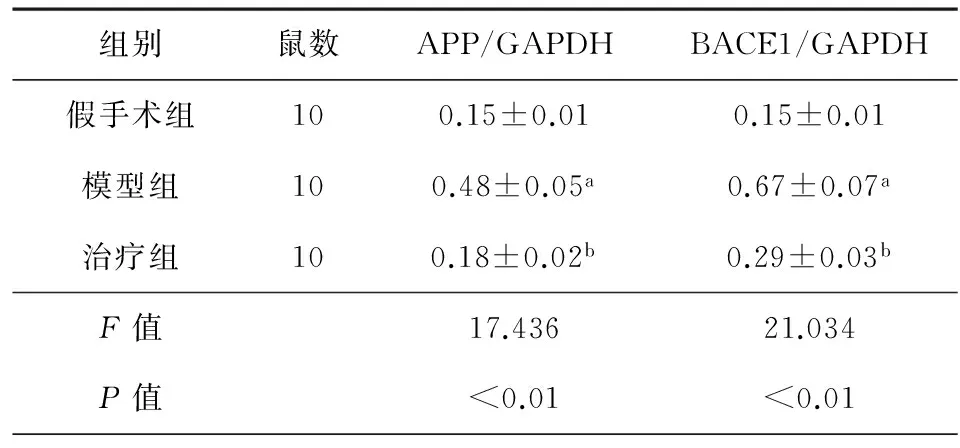
2.4各组大鼠海马组织中APP和BACE1 mRNA含量的测定如图2、表5所示,与假手术组比较,模型组血清及海马组织中APP及BACE1 mRNA含量显著提高;与模型组比较,治疗组血清及海马组织中APP及BACE1 mRNA含量显著降低;差异均具有统计学意义(P<0.01)。

图2 各组大鼠海马组织中APP及BACE1 mRNA 含量的测定表5 各组大鼠海马组织中APP及BACE1 mRNA 含量的测定±s
组别鼠数APP/GAPDHBACE1/GAPDH假手术组100.15±0.010.15±0.01模型组100.48±0.05a0.67±0.07a治疗组100.18±0.02b0.29±0.03bF值17.43621.034P值<0.01<0.01
注:与假手术组比较,aP<0.01;与模型组比较,bP<0.01。
3 讨论
盐酸美金刚是美国批准用于治疗AD的谷氨酸NMDA受体非竞争性抑制剂,其治疗中、重度AD患者疗效显著。同时国内学者赵宝敏等[9]发现盐酸美金刚能改善血管性痴呆大鼠学习记忆能力,并能上调NR1,NR2A,NR2B。孙玉华等[10]也发现盐酸美金刚能清除血管痴呆大鼠海马区自由基,减轻组织损伤,并上调脑源性神经营养因子(BDNF)表达从而保护神经元。而盐酸美金刚对于AD模型大鼠的治疗作用机制尚未见报道。所以本研究拟通过构建AD模型大鼠,并通过盐酸美金刚进行干预,从而探讨盐酸美金刚治疗AD的相关机制。首先通过Morris水迷宫实验证实盐酸美金刚能显著的缩短水迷宫潜伏期。
老年斑是AD病理学特征之一,大量存在于AD患者的大脑皮层及海马区。Aβ是老年斑的主要成分,是AD发生,发展的促进因素,能导致神经元缠结及神经元缺失,因此由Aβ诱导的细胞或动物模型常作为AD模型进行相关研究,也说明了通过清除Aβ的沉积能阻止AD的发展[4,11]。Aβ是由APP裂解产生的。APP是种Ⅰ型跨膜糖蛋白,定位于人染色体21q21.2,表达于中枢神经细胞,在生理水平下能维持细胞与细胞间及细胞与细胞外间质间的信号,参与神经细胞信号识别、细胞粘附,凋亡及神经保护等生理过程。其氨基酸具有保守生长因子样区域,通过α、γ或β、γ等分泌酶的剪切,参与多种靶蛋白的调控。APP转基因动物亦常作为AD动物模型进行研究[12]。在正常生理状况下,APP主要通过α途径进行代谢,不产生Aβ,在病理状况下通过β途径,在BACE1等酶作用下,裂解产生Aβ,从而导致AD的发生[13]。BACE1广泛存在于多种组织中,其中脑组织中的皮层、海马及小脑中表达较高,而在胶质细胞中表达量几乎没有。已有研究证实BACE1反义寡核苷酸能够显著抑制APP的β裂解[14]。同时也有研究证实BACE1-/- AD小鼠认知功能得到显著改善,并使Aβ形成减少[15]。因此通过抑制BACE1表达,进而抑制APP的β裂解,最终减少Aβ形成,不失为治疗AD的一种有效策略。
所以,本研究通过Aβ注射SD大鼠海马,从而构建AD大鼠模型,并于术后24 h腹腔注射盐酸美金刚,连续给药14 d后,取血及海马组织,ELISA法检测血清及海马组织中Aβ含量,结果表明模型组中Aβ含量显著提高,而盐酸美金刚能显著的降低AD大鼠血清及海马组织中Aβ含量。因此我们进一步检测Aβ来源物及生成关键酶,即APP和BACE1蛋白及mRNA含量,western blot及RT-PCR结果均表明盐酸美金刚能显著降低AD大鼠海马组织中APP和BACE1表达。
综上所述,盐酸美金刚能显著的降低AD大鼠血清及海马组织中Aβ的形成,并能下调海马组织中APP及BACE1蛋白与mRNA的表达,从而说明盐酸美金刚通过抑制BACE1表达,从而阻止APP的β裂解,减少Aβ的产生,从而达到治疗AD大鼠的目的。
参考文献
[1]Bloom GS.Amyloid-beta and tau:the trigger and bullet in Alzheimer disease pathogenesis [J].JAMA Neurol,2014,71(4):505-508.
[2]孙灵芝,阮志刚,刘靖,等.Aβ和tau蛋白从独立学说到联合学说-老年性痴呆的研究进展[J].神经解剖学杂志,2012,28(4):419-422.
[3]Kaya G,Gunduz E,Acar M,et al.Potential genetic biomarkers in the early diagnosis of Alzheimer disease:APOE and BIN1 [J].Turk J Med Sci,2015,45(5):1058-1072.
[4]韩玉生,侯志涛,纪显玥,等.姜黄素调控β-分泌酶基因表达抑制老年性痴呆大鼠Aβ蛋白生成的机制[J].中医学报,2015,30(4):536-538.
[5]陈宗胜,孙中武.血管性认知功能障碍治疗研究进展[J].安徽医药,2015,19(3):409-412.
[6]殷健,冯岩,卢骏,等.盐酸美金刚治疗阿尔茨海默病的临床研究进展[J].实用药物与临床,2012,15(4):232-235.
[7]万有才.盐酸美金刚联合其他药物治疗阿尔茨海默病的应用进展[J].中国药房,2011,22(4):379-380.
[8]田爽,王维平,王丽娜,等.盐酸美金刚对癫痫大鼠海马GSK-3β表达的影响[J].中风与神经疾病杂志,2011,28(10):931-934.
[9]赵宝敏,张楠,程焱.盐酸美金刚对血管性痴呆大鼠N-甲基-D天冬氨酸受体的影响[J].中华老年心脑血管病杂志,2015,17(3):303-306.
[10] 孙玉华,许予明,贺维亚.盐酸美金刚干预对血管性痴呆大鼠海马脑源性神经营养因子的表达及氧化应激水平的影响[J].中国老年学杂志,2014,34(4):1006-1007.
[11] 刘玲,王淑英.芍药苷对Aβ-(25-35)诱导PC12细胞氧化损伤的影响[J].中国中药杂志,2013,38(9):1318-1322.
[12] Rockenstein E,Desplats P,Ubhi K,et al.Neuro-peptide treatment with Cerebrolysin improves the survival of neural stem cell grafts in an APP transgenic model of Alzheimer disease[J].Stem Cell Res,2015,15(1):54-67.
[13] 郑嵋戈,阮志刚,刘靖,等.β-淀粉样蛋白的代谢机制[J].神经解剖学杂志,2011,27(3):344-348.
[14] Devi L,Ohno M.Effects of BACE1 haploinsufficiency on APP processing and Abeta concentrations in male and female 5XFAD Alzheimer mice at different disease stages [J].Neuroscience,2015,307:128-137.
[15] Cole SL,Vassar R.The role of amyloid precursor protein processing by BACE1,the beta-secretase,in Alzheimer disease pathophysiology[J].J Biol Chem,2008,283(44):29621-29625.
doi:10.3969/j.issn.1009-6469.2016.07.006
(收稿日期:2016-02-09,修回日期:2016-04-01)
Effect of NMDA on the expression of APP and BACE1 in Alzheimer’s disease rats
WU Fang
(DepartmentofNeurology,SanxiaCentralHospital,Chongqing404000,China)
Abstract:ObjectiveTo explore the effect of N-methyl-D-aspartate(NMDA) receptor inhibitor(memantine) on the expression of amyloid precursor protein(APP) and β-secretase(BACE1) in Alzheimer’s disease(AD) rats.MethodsThirty SD rats were randomized into three groups:sham operation group(n=10),model group(n=10),treatment group(memantine group)(n=10).The AD rats model was built by injecting 10 μg β-amyloid protein(Aβ)1-40 to hippocampus.The rats received intraperitoneal injection of 10 mg·kg-1·d-1memantine for 8 d in treatment group,while the rats were given the same amount of normal saline in normal and model group.The spatial learning and memory ability of rats was detected by Morris water maze test in 1,3,7,and14 d.The level of Aβ in serum and hippocampus was examined by ELISA method.The expressions of APP and BACE1 protein and mRNA in hippocampus were assayed by Western blot and RT-PCR.ResultsCompared with ham operation group,the escape latency in the water maze training prolonged,the level of Aβ in serum and hippocampus increased,and the expressions of APP and BACE1 protein and mRNA in hippocampus were upregulated in model group with statistically significant difference(P<0.01).Compared with model group,the escape latency in the water maze training decreased,the level of Aβ in serum and hippocampus decreased,and the expressions of APP and BACE1 protein and mRNA in hippocampus were downregulated in treatment group with statistically significant difference(P<0.01).ConclusionsThese results suggested that memantine could inhibit the APP cleavage,thereby inhibiting Aβ deposition of hippocampal tissue in AD rats.
Key words:Alzheimer disease;Memantine;Receptors,N-Methyl-D-Aspartate;Amyloid precursor protein secretases;Rats,Sprague-Dawley
