阿伐那非类似物的合成与表征
2016-08-09田红潮肖咏梅杨亮茹屈凌波
田红潮,毛 璞,肖咏梅,杨亮茹,屈凌波
(河南工业大学 生物工程学院,河南 郑州 450000)
0 引言
勃起功能障碍(ED)是一种常见的男性疾病并且患病率随着年龄的增长而增加.磷酸二酯酶5抑制剂(PDE5i)被推荐作为治疗ED的一线药物[1],阿伐那非是新兴的磷酸二酯酶5抑制剂的一种.根据GOSS的调查,ED在美国的发病率为33.7%[2].保守估计,全球有1.5亿的男性有不同程度的ED,2025年将翻一番达到3.22亿人[3].根据张庆江等对北京、广州、重庆进行的调查,发现中国≥40岁人群ED患病率高达40.2%[4].阿伐那非(avanafil,StendraTM)是一种于2012年4月获US-FDA批准用于治疗ED的口服速效的高选择性磷酸二酯酶5抑制剂(PDE5i)[5].与其他PDE5i相比,阿伐那非选择性更高,起效更快,副作用更少[6],预计将会有非常大的市场前景.基于此,很有必要研发其仿制药,并在其基础上开发出药效更好、副作用更小、廉价易得的类似药,基于阿伐那非的结构(结构式见图1),合成了阿伐那非的类似物(见图2).
本文按照酰胺缩合条件优化的方法[7]合成了8种未见文献报道的阿伐那非类似物.本研究以4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯(1)为原料,先进行酯的水解,再与R基团进行酰胺缩合反应,合成了8种阿伐那非类似物(如表1所示).所合成的产物均经1H NMR、13C NMR、ESI-MS得到验证.

图1 阿伐那非的结构式
1 实验部分
1.1 仪器与试剂
Bruker Avance 400型超导核磁共振仪,瑞士Bruker公司;ICPMS7700型电感耦合等离子体质谱仪,深圳华普通用科技有限公司;WQF-510型傅立叶变换红外光谱仪,北京北分瑞利分析仪器;X-4型数字显微熔点测定仪,北京福凯科仪科技有限公司;DF-101D集热式恒温加热磁力搅拌器、旋转蒸发器RE-2000B、SHD-D(Ⅲ)循环水式真空泵均为巩义市予华仪器有限责任公司;DZF-6020真空干燥箱,上海申贤恒温设备厂.
4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯(C18H21ClN4O4)(1,实验室自制);1-甲基哌嗪(C5H12N)、2-氯苄胺(C7H8ClN)、对甲氧基苯胺(C7H9NO)、L-苯丙氨醇(C9H13NO)、苄胺(C7H9N)、N-甲基苄胺(C8H11N)、L-亮氨醇(C6H15NO)、α-甲基苄胺(C8H11N)、1-乙基-3-(3-二甲基氨基丙基)碳化二亚胺盐酸盐(EDCI)和1-羟基苯并三唑水合物(HOBt)均购自阿拉丁试剂有限公司、二甲基亚砜(DMSO)、四氢呋喃(THF)、三乙胺(Et3N)等均为分析纯.
1.2 化合物的合成
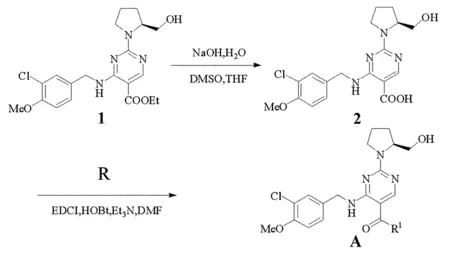
图2 阿伐那非类似物的合成路线
1.2.1 4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸(2)的合成
在50 mL圆底烧瓶中加入2.5 mmol 4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯(1),用体积比为VDMSO∶VTHF=1∶1的混合溶液溶解,再加入8 mL 10%的NaOH水溶液,室温下搅拌,反应结束后向混合物中加入25 mL 10%的柠檬酸水溶液,35 ℃下,减压蒸馏除去THF,析出白色固体,抽滤,滤饼用蒸馏水洗涤,真空干燥6 h,得到化合物2,白色粉末状固体.产物纯度较高,不需要提纯,直接进行下一步反应.
1.2.2 阿伐那非类似物的合成
在50 mL圆底烧瓶中加入0.5 mmol化合物2,用DMF溶解,再加入0.6 mmol R,依次加入0.6 mmol 1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDCI)、0.6 mmol 1-羟基苯并三唑水合物(HOBt)和1.0 mmol三乙胺(Et3N),磁力搅拌反应混合物,反应结束后把反应液倒入18 mL饱和NaHCO3溶液中,乙酸乙酯萃取,有机层用饱和食盐水洗涤,通过无水硫酸钠干燥,在减压旋蒸下除去溶剂,残留物通过硅胶柱色谱纯化,得到阿伐那非类似物.
2 结果与讨论
2.1 化合物1和2的结构表征
化合物1(实验室自制):m.p.:86~88 ℃;1H NMR(400 MHz,DMSO-d6)δ:8.53(q,J=6.4 Hz,1H,NH),8.48(d,J=6 Hz,1H,Pyrimidine-H),7.42(dd,J=2 Hz,J=4.4 Hz,1H,Ph-H),7.29(d,J=8.4 Hz,1H,Ph-H),7.08(d,J=8.4 Hz,1H,Ph-H),4.81(m,1H,OH),4.55(t,J=7.6 Hz,2H,Ph-CH2),4.21(q,J=6.8 Hz,2H,OCH2CH3),4.13~4.08(m,1H,Pyrrolidine-H),3.82(d,J=1.6 Hz,3H,OCH3),3.63-3.58(m,1H,Pyrrolidine-H),3.51~3.45(m,2H,Pyrrolidine-H),3.35~3.31(m,1H,Pyrrolidine-H),2.02~1.83(m,4H,Pyrrolidine-H),1.26(t,J=7.2 Hz,3H,OCH2CH3);1H NMR(400 MHz,DMSO-d6,D2O)δ:8.47(q,J=5.6 Hz,1H,NH),8.42(d,J=2.4 Hz,1H,Pyrimidine-H),7.35(t,J=1.5 Hz,1H,Ph-H),7.25(d,J=8.4 Hz,1H,Ph-H) 7.03(dd,J=2.5,8.4 Hz,1H,Ph-H),4.51(d,J=6.5 Hz,2H,Ph-CH2),4.17(q,J=7.1 Hz,2H,OCH2CH3),4.07(s,1H,Pyrrolidine-H),3.77(d,J=1.1 Hz,3H,OCH3),3.60~3.52(m,1H,Pyrrolidine-H),3.48~3.40(m,2H,Pyrrolidine-H),3.30(dd,J=7.5,10.3 Hz,1H,Pyrrolidine-H),1.95~1.81(m,4H,Pyrrolidine-H),1.22(t,J=7.1 Hz,3H,OCH2CH3); IR(KBr,cm-1)σ:3340,1674,1525,1257,804; ESI-MS(m/z):421.25 [M+H]+.
表1阿伐那非类似物汇总
Tab. 1Avanafilanaloguessummary

化合物2:产率95.1%,m.p.:202~204 ℃;1H NMR(400MHz,DMSO-d6,D2O)δ:8.37(s,1H,Pyrimidine-H),7.35(d,J=8.2 Hz,1H,Ph-H),7.24(s,1H,Ph-H),7.04(d,J=8.2 Hz,1H,Ph-H) 4.52(s,2H,Ph-CH2),4.06(s,1H,Pyrrolidine-H),3.78(s,3H,OCH3),3.57(d,J=10.4 Hz,1H,Pyrrolidine-H),3.45(s,2H,Pyrrolidine-H),3.32(t,J=9.0 Hz,1H,Pyrrolidine-H),1.91(s,2H,Pyrrolidine-H),1.82(s,2H,Pyrrolidine-H); ESI-MS(m/z):393.25 [M+H]+.
2.2 化合物2的合成条件
化合物1的水解是一个很简单的反应.化合物1经过水解得到4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸(化合物2)(如图2所示).本文参考蒋慧敏[8]学位论文中的水解方法,用四氢呋喃(THF)作溶剂对原料进行溶解,加入10%的NaOH水溶液后,发现混合物中有分层现象.因为有机相和水相无法充分混溶,不仅反应时间长,而且原料无法完全反应,产率较低.参考Yamada等人[9]专利文献的方法,用二甲基亚砜(DMSO)作溶剂,原料完全溶解后加入10%的NaOH水溶液,立刻有原料析出,即使在超声下也无法完全溶解,使得产品的纯度和产率较低.通过大量实验发现,采用混合溶剂法,即使用体积比为VDMSO∶VTHF=1∶1的混合溶液溶解原料,不仅原料可以充分溶解,而且反应得到的产品产率和纯度都较高.
在对水解得到的化合物2进行后处理时,如果处理不当也会使产率降低.实验中发现,反应结束后,如果先旋蒸除去四氢呋喃,加入一定量的10%的柠檬酸水溶液后,立刻有大量白色沉淀产生,而且有相当量的无须的淡黄色固体产生,附着在瓶壁上不易脱离下来,造成产品损失,而且在抽滤后滤液中会有少量白色悬浮物且不易回收,也会造成产品损失;反应结束后如果先加入一定量的10%的柠檬酸水溶液再进行旋蒸,随着溶液中四氢呋喃的慢慢减少,会有白色沉淀慢慢析出,四氢呋喃除尽进行抽滤,得到白色粉末状的固体而且滤液为无色透明的液体,最终得到的产品杂质较少,产率较高.产率为95.1%,产物纯度较高,无须提纯,直接进行下一步反应.
2.3 阿伐那非类似物的结构表征
化合物A-1:无色油状物,产率82.7%;1H NMR(400 MHz,DMSO-d6),δ:7.85(s,1H,Pyrimidine-H),7.54(s,1H,Ph-CH2NH),7.42(d,J=1.5 Hz,1H,Ph-H),7.30(d,J=8.4 Hz,1H,Ph-H),7.06(d,J=8.6 Hz,1H,Ph-H),4.86(m,1H,OH),4.48(d,J=3.6 Hz,2H,Ph-CH2),4.07(s,1H,Pyrrolidine-H),3.81(s,3H,OCH3),3.63(s,1H,Pyrrolidine-H),3.48(s,4H,Piperazine-H),3.43(d,J=8.3 Hz,2H,CH2OH),3.32(t,J=8.8Hz,1H,Pyrrolidine-H),2.28(t,J=4.3 Hz,4H,Piperazine-H),2.17(s,3H,CH3),1.94~1.83(m,4H,Pyrrolidine-H);13C NMR(100MHz,DMSO-d6)δ:167.8,160.1,159.9,156.2,153.7,134.0,129.8,128.1,121.0,112.9,101.0,62.3,59.3,56.4,55.0(2C),47.6,46.0(2C),45.2,42.8,28.1,23.1; ESI-MS(m/z):497.2 [M+Na]+.
化合物A-2:白色固体,产率72.3%,m.p.:146~149 ℃;1H NMR(400 MHz,DMSO-d6),δ:9.17(d,J=5.8 Hz,1H,C(O)NH),8.75(t,J=5.8 Hz,1H,Ph-CH2NH),8.54(d,J=4.9 Hz,1H,Pyrimidine-H),7.44~7.41(m,2H,Ph-H),7.35~7.25(m,4H,Ph-H),7.07(d,J=8.5 Hz,1H,Ph-H),4.88(m,1H,OH),4.52(s,2H,Ph-CH2),4.49(d,J=5.9 Hz,2H,Ph-CH2),4.12(s,1H,Pyrrolidine-H),3.81(s,3H,OCH3),3.65(s,1H,Pyrrolidine-H),3.54~3.46(m,2H,CH2OH),3.34(d,J=9.9 Hz,1H,Pyrrolidine-H),1.99~1.84(m,4H,Pyrrolidine-H);13C NMR(100 MHz,DMSO-d6)δ:167.7,161.2,160.3,156.8,153.8,137.1,133.7,132.3,129.8,129.6,129.5,128.8,128.1,128.0,127.6,121.1,113.0,98.5,62.4,59.4,56.4,47.8,42.7,28.1,23.1; ESI-MS(m/z):516.23 [M+H]+.
化合物A-3:白色固体,产率78.7%,m.p.:192~194 ℃;1H NMR(400 MHz,DMSO-d6),δ:9.77(s,1H,C(O)NH),9.03(d,J=5.7 Hz,1H,Ph-CH2NH),8.58(d,J=9.6 Hz,1H,Pyrimidine-H),7.56(dd,J=2.1 Hz,J=5 Hz,2H,Ph-H),7.43(s,1H,Ph-H),7.31(dd,J=2.1 Hz,J=6.4 Hz,1H,Ph-H),7.08(d,J=8.5 Hz,1H,Ph-H),6.89(dd,J=2.1 Hz,J=4.9 Hz,2H,Ph-H),4.88(m,1H,OH),4.55(s,2H,Ph-CH2),4.12(d,J=13.8 Hz,1H,Pyrrolidine-H),3.82(s,3H,OCH3),3.73(s,3H,OCH3),3.65(d,J=4.5 Hz,1H,Pyrrolidine-H),3.55~3.48(m,2H,CH2OH),3.35(t,J=6.6 Hz,1H,Pyrrolidine-H),1.99~1.85(m,4H,Pyrrolidine-H);13C NMR(100 MHz,DMSO-d6),δ:166.1,161.2,160.2,157.2,155.8,153.8,133.7,132.5,129.8,128.1,122.7(2C),121.1,114.1(2C),113.1,99.2,62.4,59.4,56.5,55.6,47.8,42.7,28.1,23.1; ESI-MS(m/z):498.24 [M+H]+.
化合物A-4:白色固体,产率74.8%,m.p.:98~100 ℃;1H NMR(400 MHz,DMSO-d6),δ:9.05(d,J=5.4 Hz,1H,C(O)NH),8.39(d,J=10.0 Hz,1H,Pyrimidine-H),7.88(d,J=7.0 Hz,1H,Ph-CH2NH),7.39(s,1H,Ph-H),7.27~7.24(m,5H,Ph-H),7.17~7.14(m,1H,Ph-H),7.07(d,J=8.5 Hz,1H,Ph-H),4.90(m,1H,OH),4.83(t,J=5.7 Hz,1H,OH),4.49(d,J=4.8 Hz,2H,Ph-CH2NH),4.10(d,J=4.6 Hz,2H,Pyrrolidine-H,C(O)NHCH),3.81(s,3H,OCH3),3.62(d,J=8.6 Hz,1H,Pyrrolidine-H),3.51~3.42(m,4H,CH2OH),3.33(t,J=9.8 Hz,1H,Pyrrolidine-H),2.92(dd,J=5.2Hz,J=8.4Hz,1H,Ph-CH2),2.75(dd,J=4.5 Hz,J=9.0 Hz,1H,Ph-CH2),1.93~1.82(m,4H,Pyrrolidine-H);13C NMR(100 MHz,DMSO-d6),δ:167.2,161.1,160.2,156.6,153.8,139.9,133.7,129.8,129.6(2C),128.5(2C),128.1,126.3,121.0,113.1,99.0,63.4,62.6,59.4,56.5,53.2,47.8,42.6,37.1,28.1,23.1; ESI-MS(m/z):548.2 [M+Na]+.
化合物A-5:白色固体,产率71.9%,m.p.:58 ℃~60 ℃;1H NMR(400 MHz,DMSO-d6),δ:9.22(t,J=7.0 Hz,1H,C(O)NH),8.74(t,J=6.0 Hz,1H,Ph-CH2NH),8.48(d,J=5.2 Hz,1H,Pyrimidine-H),7.41(s,1H,Ph-H),7.33~7.23(m,6H,Ph-H),7.08(d,J=8.5 Hz,1H,Ph-H),4.86(m,1H,OH),4.52(d,J=5.5 Hz,2H,Ph-CH2),4.41(d,J=5.9 Hz,2H,Ph-CH2),4.10(s,1H,Pyrrolidine-H),3.82(s,3H,OCH3),3.63(s,1H,Pyrrolidine-H),3.50~3.44(m,2H,CH2OH),3.33(s,1H,Pyrrolidine-H),1.97~1.84(m,4H,Pyrrolidine-H);13C NMR(100 MHz,DMSO-d6)δ:167.5,161.3,160.3,156.6,153.8,140.3,133.7,129.8,128.7(2C),128.1,127.5(2C),127.1,121.1,113.1,98.7,62.4,59.4,56.5,47.6,42.5,41.2,28.1,23.1; ESI-MS(m/z):482.29 [M+H]+.
化合物A-6:无定形,产率90.1%;1H NMR(400 MHz,DMSO-d6),δ:7.93(s,1H,Pyrimidine-H),7.70(s,1H,Ph-CH2NH),7.45(d,J=1.8 Hz,1H,Ph-H),7.38~7.25(m,6H,Ph-H),7.08(d,J=8.5 Hz,1H,Ph-H),4.83(m,1H,OH),4.59(s,2H,Ph-CH2),4.50(d,J=5.2 Hz,2H,Ph-CH2),4.05(t,J=4.7 Hz,1H,Pyrrolidine-H),3.82(s,3H,OCH3),3.62(d,J=7.8 Hz,1H,Pyrrolidine-H),3.43(s,2H,CH2OH),3.30(s,1H,Pyrrolidine-H),1.99~1.82(m,4H,Pyrrolidine-H);13C NMR(100MHz,DMSO-d6)δ:170.8,160.2,159.8,155.8,153.7,137.7,134.1,129.8,129.1(2C),128.1,127.6(2C),127.5,121.0,112.9,101.2,62.4,60.2,59.4,56.4,47.7,42.8,35.7,28.1,23.2; ESI-MS(m/z):496.47 [M+H]+.
化合物A-7:白色固体,产率72.1%,m.p.:136~139 ℃;1H NMR(400 MHz,DMSO-d6),δ:9.19(d,J=4.6 Hz,1H,C(O)NH),8.42(s,1H,Pyrimidine-H),7.69(d,J=8.2 Hz,1H,Ph-CH2NH),7.41(s,1H,Ph-H),7.29(dd,J=2.0 Hz,J=6.4 Hz,1H,Ph-H),7.08(d,J=8.5 Hz,1H,Ph-H),4.90(m,1H,OH),4.65(t,J=5.8 Hz,1H,OH),4.51(d,J=5.8 Hz,2H,Ph-CH2),4.09(s,1H,Pyrrolidine-H),3.99(d,J=5.0Hz,1H,C(O)NHCH),3.82(s,3H,OCH3),3.63(d,J=7.2 Hz,1H,Pyrrolidine-H),3.48(d,J=4.6 Hz,2H,CH2OH),3.40(t,J=5.6Hz,1H,Pyrrolidine-H),3.34-3.30(m,2H,CH2OH),1.93~1.82(m,4H,Pyrrolidine-H),1.63~1.57(m,1H,(CH3)2CH),1.41~1.35(m,2H,(CH3)2CH-CH2),0.87(dd,J=3.7 Hz,J=6.6 Hz,6H,(CH3)2);13C NMR(100 MHz,DMSO-d6),δ:167.2,161.2,160.1,156.6,153.8,133.8,129.8,128.1,121.0,113.1,99.1,64.4,62.6,59.4,56.5,49.3,47.8,42.6,40.4,28.1,24.9,23.8,23.1,22.4; ESI-MS(m/z):514.2 [M+Na]+.
化合物A-8:无定形,产率80.8%;1H NMR(400 MHz,DMSO-d6),δ:9.13(d,J=4.8 Hz,1H,C(O)NH),8.56(s,1H,Ph-CH2NH),8.46(d,J=7.7 Hz,1H,Pyrimidine-H),7.39(s,1H,Ph-H),7.36~7.25(m,5H,Ph-H),7.23~7.19(m,1H,Ph-H),7.06(d,J=9.1 Hz,1H,Ph-H),5.08(d,J=7.1 Hz,1H,Ph-CH),4.92(m,1H,OH),4.52~4.48(m,2H,Ph-CH2),4.12(s,1H,Pyrrolidine-H),3.81(s,3H,OCH3),3.63(d,J=6.1 Hz,1H,Pyrrolidine-H),3.48(t,J=8.0 Hz,2H,CH2OH),3.36(s,1H,Pyrrolidine-H),1.99~1.83(m,4H,Pyrrolidine-H),1.44(d,J=7.1 Hz,2H,CH3);13C NMR(100 MHz,DMSO-d6)δ:167.8,161.3,160.3,156.8,153.8,145.7,133.7,129.8,128.7(2C),128.1,126.9,126.4(2C),121.1,113.0,98.8,62.7,59.5,56.4,48.4,47.8,42.6,28.2,23.1,22.8; ESI-MS(m/z):496.32 [M+H]+.
3 结论
以4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯为原料,经过酯水解和酰胺缩合反应,合成了8种未见文献报道的阿伐那非类似物,其结构经1H NMR、13C NMR及ESI-MS确证.本文合成的阿伐那非类似物,支持其生物活性及毒理的研究,为筛选出更理想的PDE5i服务.
