基于丙烯酸的聚电解质与聚乙二醇溶液的粘度行为
2016-07-24徐丽娟石花蕾肖先森王正辉
徐丽娟,石花蕾,肖先森,王正辉
(华南农业大学材料与能源学院,广东广州510642)
基于丙烯酸的聚电解质与聚乙二醇溶液的粘度行为
徐丽娟,石花蕾,肖先森,王正辉*
(华南农业大学材料与能源学院,广东广州510642)
报道不同温度下PEG-PAA-C2H5OH-H2O体系的相图,以及质量分数、温度、PEG摩尔分数、NaCl和尿素对中和度分别为50%的PAA(DN-50%)和100%的PAANa及其与PEG构成的复合体系的粘度行为的影响.结果表明,PAA线团内氢键作用形成羧基“桥架”结构、柔性带疏水结构的PEG分子的缠绕作用以及乙醇分子对大分子间作用力的消弱作用共存;与PAANa比较,PAA(DN-50%)因受羧基“桥架”结构影响,质量分数对其比浓粘度影响较小;PEG分子对PAA(DN-50%)和PAANa的缠绕模式不同,在PEG摩尔分数小于0.5的情况下,复合体系的比浓粘度变化趋势不同;聚合物链段的内能随温度升高而增大,溶液的比浓粘度降低;主要由于同离子效应缘故,随NaCl质量分数增加,2种复合体系比浓粘度都降低;尿素分子在PAA(DN-50%)线团表面因氢键结合及水化,使得复合体系PEG+PAA(DN-50%)的比浓粘度在尿素质量分数低于0.25%时随质量分数增大有所增加;当质量分数超过0.25%后,进入聚合物线团的尿素分子因其氢键作用使得线团收缩,比浓粘度降低.
聚丙烯酸;聚乙二醇;相图;复合体系;粘度行为
水溶性大分子在溶液中的形态及其相互作用
一直是有关高分子基础理论的重要研究内容,研究方法主要有粘度法[1-3]、电势法[4-6]和荧光标记法[7-9]等.近年来,随着双水相聚合研究的兴起,增加了人们对水溶液中大分子间作用的研究兴趣[10-13].关于聚乙二醇(PEG)与聚丙烯酸(PAA)及其中和产物大分子在溶液中的作用已有一些报道.早年文献[1]研究了稀溶液体系中聚氧化乙烯与PAA间的相互作用,证实了稀溶液中分子间复合作用的存在.刘平等[14]用粘度法研究了浓溶液体系中PEG与PAA及其中和产物大分子间的相互作用,结果表明,在很宽的pH范围内都存在复合作用,在pH值小于3.5的浓溶液中会发生相分离而析出复合物沉淀,并将此归因于强的氢键作用.G.Staikos等[3]用粘度法研究了PEG与丙烯酸共聚物间的相互作用以及极稀溶液的比浓粘度与质量分数的关系,发现在低离子强度和低pH条件下PEG与PAA间因氢键作用形成紧密聚集体,而当PAA分子链上有一定的离子取代度后,因氢键作用减弱阻碍了分子间的缔合.C.W.Frank等[7,15]用荧光法研究了末端带有芘基的PEG与PAA和聚甲基丙烯酸(PMA)在水中的作用,发现PEG链上的氧能与PAA和PMA中的羧基形成氢键,PAA和PMA与PEG的缔合作用因甲基的疏水作用而加强,这种加强是通过众多羧基与PEG的协同络合作用实现的,PEG的疏水作用是氢键缔合的推动力.
虽然PAA和PEG的作用研究取得了一些有价值的研究成果,但也存在一些尚需进一步探讨的内容,比如:pH值小于3.5的情况下,刘平等[15]在低浓溶液中PAA和 PEG发生相分离与 G.Staikos等[3]在极稀溶液不发生相分离是否矛盾,在浓溶液中发生相分离能否全归因于强的氢键作用,质量分数、小分子物质等因素如何影响不同中和度的PAA和PEG的作用,等等.
本研究通过PEG-PAA-C2H5OH-H2O体系的相图考察了相分离的条件和PEG、PAA与C2H5OH之间的相互作用,同时也用粘度法研究了一定相对分子质量的PEG与不同中和度的丙烯酸聚合物体系的粘度行为,进而分析其大分子构象、线团尺寸与浓度、温度、PEG的质量分数以及小分子物质的关系.
1 实验部分
1.1 主要原料 聚乙二醇(PEG),分析纯,相对数均分子质量为6×103,Aldrich公司产品;聚丙烯酸(PAA),本实验室合成,相对粘均分子质量为3.8× 104;NaOH、NaCl和尿素(Urea),均为分析纯,广州化学试剂公司购买.
1.2 待测溶液的准备 先将PEG和PAA溶解配制成一定浓度的溶液,随即取2份PAA溶液并用NaOH溶液进行计量中和,分别得到中和度为50%的PAA(DN-50%)和中和度为100%的PAANa聚电解质溶液,最后分别用水稀释至预定浓度.在不同质量浓度的聚合物溶液中加入计量NaCl和Urea,得到不同NaCl和Urea质量浓度的聚合物溶液.复合溶液中PEG摩尔分数N(PEG)定义为n(PEG)/[n(PEG)+ nx],nx是PAA(DN-50%)或PAANa的结构单元的物质的量.
1.3 粘度测定 溶液的粘度用小球体积为5.4 mL、毛细管直径为0.59 mm的乌氏粘度计在精度为±0.1℃的恒温水槽中测定.
1.4 PEG-PAA-C2H5OH-H2O相图的绘制用浊度滴定法[13]可以得到不同温度下PEG-PAA-C2H5OH-H2O体系的相图.先取2 g质量分数为4%的PEG水溶液于试管中,置于恒温槽中,然后向试管中慢慢滴加质量分数已知的PAA水溶液,记录刚发生相分离出现浑浊时加入的PAA溶液质量,计算混合体系中PAA和PEG的组成.再慢慢加入一定量无水乙醇使体系变得澄清,再次滴加一定量PAA的水溶液直至出现浑浊,再加一定量无水乙醇使体系变得澄清,如此反复,可根据每个相分离点体系中的PAA、PEG和无水乙醇的组成绘制出PEG-PAA-C2H5OH-H2O体系的相图.
2 结果与讨论
2.1 不同温度下PEG-PAA-C2H5OH-H2O体系的相图 用质量分数为4%的PAA和PEG溶液进行浊度滴定法研究,实验发现,将PEG加入PAA中会立刻发生相分离而析出沉淀复合物,随即滴加乙醇,沉淀溶解,溶液变得澄清,再滴加PEG则不再发生相分离;将PAA加入PEG中也立刻析出沉淀复合物,随即滴加乙醇,溶液变得澄清,再滴加PAA又发生相分离,再滴加乙醇,溶液又变得澄清.因此,在相图研究中就采用后一种加料方式,不同温度下的测定结果见图1.从图1可见,随着温度升高,相分离的PAA含量增加,发生相转变(由两相变为单相)所需乙醇的量降低,亦即低温下较容易发生相分离.

在本研究的浓度范围内,PAA大分子形成缠结线团,线团内的羧基主要以氢键形式相互结合,线团外的羧基及其电离的极少羧酸根负离子的水化使得PAA表现出良好的水溶性.将PEG加入其中,由于十分柔顺的PEG分子链在醚结构的氢键作用下靠近缠结的PAA线团,其中的亚乙基也同时与PAA主链发生协同的疏水作用,由于强的疏水推动作用使PAA线团收缩、线团内外的水化作用减弱而导致相分离.向相分离体系中加入乙醇后,乙醇分子插入PEG链与PAA线团之间,从而减弱了疏水的协同作用,使PAA线团部分恢复到原来的水化状态而溶解.再向其中加入PEG,因新的PEG分子只能靠近环绕PAA线团周围具有弱作用的PEG分子而不能引起相分离.反之,将PAA加入PEG中发生相分离,加入乙醇后沉淀物溶解,原因与PAA第一次加入PEG中的相同.若再次加入PAA又立刻产生沉淀物,这是由于加入的PAA立刻受到体系中的PEG分子包围,在强疏水推动作用下PAA线团收缩、线团内外的水化作用减弱而导致相分离.由此可见,PAA和PEG发生相分离[15]的主要原因归因于强的协同疏水推动作用,而PEG和PAA间的氢键是促使2种分子靠近的重要因素.
随着体系温度升高,PAA大分子的羧基电离作用增强,大分子的构象因电荷排斥作用而变得更为伸展,缠结的大分子线团更为疏松,线团的水化作用更强,PEG在线团表面的氢键数减少,从而使PEG分子与PAA线团间的作用会因升高而减弱,因此使沉淀物溶解所需的乙醇量随之降低(尤其是在PAA含量较高的情况下).温度升高后,为了获得发生相分离的紧密疏水线团,就需要增加PAA用量,使线团内的氢键协同作用增强.G.Staikos等[3]在极稀溶液研究了PAA和PEG体系的特性粘数,说明在溶液浓度极稀的情况下是没有发生相分离,其原因是在极稀溶液中PAA电离度大,PAA以舒展的单分子线团存在,PEG与之的作用仅表现为分子之间的缔合,柔顺的PEG分子以氢键与PAA大分子缔合,这种缔合不会改变PAA的水化状态,因而不会发生相分离现象.由此可见,PAA的浓度、混合的方式是PEG与PAA作用发生相分离和相反转的前提条件,PEG分子与PAA线团间的氢键作用以及协同疏水作用是相分离和相转变的内在动力.
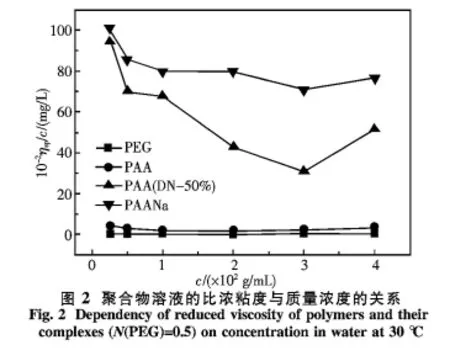
2.2 聚合物溶液的比浓粘度与质量浓度的关系聚合物溶液比浓粘度的变化可以反映出大分子的构象及其相互作用等信息,不同聚合物水溶液在30℃和质量分数为0.25%~4%之间的比浓粘度变化如图2所示.从图2可以看出,PEG和PAA溶液的比浓粘度在此质量浓度范围基本不变,表明它们的线团尺寸基本不变.PAANa侧基全是羧酸根阴离子,PAA(DN-50%)中侧基仍有近一半是羧基,前者的静电排斥作用更显著,表现出较大的线团尺寸和较高的比浓粘度.在质量分数大于3%后,随浓度增加,线团数增加,大分子的缠结加剧,使得溶液中的内摩擦增大,比浓粘度增大.
2.3 PEG的摩尔分数对复合体系的比浓粘度的影响 在聚合物总质量分数为2%和30℃的条件下,考察了PEG的摩尔分数对PEG+PAA(DN-50%)和PEG+PAANa两复合体系的比浓粘度变化,结果见图3.从图3看出,PEG+PAANa复合体系的粘度大于PEG+PAA(DN-50%)复合体系的粘度,表明前者的线团尺寸比后者大,这是由于PAA(DN-50%)未中和的羧基间氢键对线团扩张的限制作用所致.在N(PEG)小于0.5时出现2种相反的变化趋势.对于PEG+PAANa复合体系,N(PEG)为0.1~0.3之间比浓粘度的逐渐降低是由于PEG分子缠绕在PAANa松散线团的分子链上,使线团逐渐收缩造成的;N(PEG)为0.3~0.5之间比浓粘度的逐渐升高是由于缠绕在PAANa线团分子链的PEG中疏水力逐渐增大使线团又逐渐扩张,当N(PEG)为0.5时,可能是PAANa链被完全缠绕、疏水力最大的情形;N(PEG)为0.5的比浓粘度比小于N (PEG)为0.1的比浓粘度,是PAANa链被PEG分子缠绕的佐证;当N(PEG)>0.5以后,粘度的降低是由于较小相对分子质量的PEG含量逐渐增加,高相对分子质量的PAANa含量逐渐减少的缘故.对于PEG+PAA(DN-50%)复合体系,N(PEG)由0.1变到0.25左右,比浓粘度略有增加,这是由于PAA(DN-50%)中仍有50%结构单元中含有的羧基间的氢键阻碍了PEG分子的顺利缠结,PEG分子只能部分缠绕于PAA(DN-50%)分子链上羧酸根阴离子附近的链段上,由于链段疏水协同作用使PAA(DN-50%)线团略有增大;N(PEG)>0.25以后,体系粘度呈总体下降的原因与PEG+PAANa复合体系的N(PEG)>0.5后粘度下降原因相同.

2.4 温度对复合体系粘度的影响 在总质量分数为2%和N(PEG)为0.5的条件下,复合体系水溶液的粘度随温度的变化见图4.温度对PEG+PAA (DN-50%)复合体系粘度的影响小于对PEG+ PAANa体系粘度的影响.对于PEG+PAA(DN-50%)复合体系,由于PAA(DN-50%)线团内由氢键构建的稳定“桥架”结构抑制了链段的运动能力和线团尺寸的改变,因而表现出温度升高对体系粘度影响不大.对于PEG+PAANa体系,没有线团内羧基的“桥架”结构,温度升高使链段的运动能力增强,结果表现出随温度升高体系粘度显著降低.

2.5 小分子物质对复合体系粘度的影响 在聚合物总质量分数为2%、N(PEG)为0.5和30℃的条件下,研究了复合体系的粘度对无机、有机小分子物质浓度的依赖性,结果见图5.对于PEG+PAANa复合体系,NaCl的同离子效应降低PAANa的电离引起线团收缩而导致粘度降低,Urea分子钻入松散的PAANa线团与羧酸根离子发生氢键作用也引起线团收缩和粘度降低,由于同离子效应比Urea的氢键效应显著,表现出NaCl对体系粘度的降低比Urea对体系粘度的降低更为显著,尤其是在引入它们的初期.对于PEG+PAA(DN-50%)复合体系来说,NaCl的同离子效应同样降低PAA(DN-50%)的电离而引起线团收缩和粘度逐渐降低;加入Urea的情况显得较为复杂,在Urea质量分数(<0.25%)较低时,由于PAA(DN-50%)线团内的氢键作用使线团较为紧密,Urea分子通过氢键作用在线团表面,增加了线团的水化性,促使线团扩张和粘度增加;当Urea质量分数(>0.25%)较高时,Urea分子钻入PAA(DN-50%)线团并通过与羧酸根离子的氢键作用引起线团收缩,随Urea质量分数增加,氢键作用引起线团收缩逾显著,粘度降低逾多.
3 结论
1)PEG-PAA-C2H5OH-H2O体系的相图表明PAA线团内氢键作用形成羧基“桥架”结构、柔性带疏水结构的PEG分子的缠绕作用以及乙醇分子对分子间作用力的消弱作用共存.
2)与PAA(DN-50%)线团不同,PAANa线团内没有羧基“桥架”结构,因而质量浓度对其比浓粘度影响较大.
3)受羧基“桥架”结构影响,PEG分子只能部分缠绕在PAA(DN-50%)大分子链上,从而表现出其复合体系的比浓粘度与温度和N(PEG)<0.5时与PEG+PAANa不同的变化趋势.
4)NaCl的同离子效应使电离下降、线团收缩及复合体系比浓粘度降低;尿素小分子具有易水化和形成氢键的特点,在浓度较低时对2种复合体系的比浓粘度有不同的影响.
[1]BAILEY F E Jr,LUNDBERG R D,CALLARDR W.Some factors affecting the molecular association of poly(ethylene oxide)and poly(acrylic acid)in aqueous solution[J].J Polym Sci:Polym Chem,1964,A2(2):845-850.
[2]ILIOPOULOS I,HALARY J L,AUDEBERT R.Polymer complexes stabilized through hydrogen bonds.Influence of“structuredefects”on complex formation:Viscometry and fluorescence polarization measurements[J].J Polym Sci:Polym Chem,1988,A26(1):275-282.
[3]BOKIAS G,STAIKOS G,ILIOPOULOS I,et al.Interpolymer association between acrylic acid copolymers and polyethylene glycol:effects of the copolymer nature[J].Macromolecules,1994,27(2):427-431.
[4]STAIKOS G,BOKIAS G,KARAYAMI K.Interpolymer complexes of poly(acrylamide)and poly(N-isopropylacrylamide)with poly(acrylic acid):a comparative study[J].Polym Int,1996,41(3):345-350
[5]HEMKER D J,GARZA V,FRANK C W.Complexation of poly(acrylic acid)and poly(methacrylic acid)with pyrene-endlabeled poly(ethylene glycol):pH and fluorescence measurements[J].Macromolecules,1990,23(20):4411-4418.
[6]ILIOPOULOS I,AUDEBERT R.Polymer complexes stabilized through hydrogen bonds.Influence of“structure defects”on complex formation:Potentiometric study[J].Eur Polym J,1988,24(2):171-175.
[7]OYAMA H T,TANG W T,FRANK C W.Complex formation between poly(acrylic acid)and pyrene-labeled polyethylene glycol in aqueous solution[J].Macromolecules,1987,20(3):474-480.
[8]HEYWARD J J,GHIGGINO K P.Fluorescence polarization study of the poly(acrylic acid)/poly(ethylene oxide)interpolymer complex in aqueous solution[J].Macromolecules,1989,22(3):1159-1165.
[9]BEDNAR B,LI Z M,HUANG Y H,et al.Fluorescence study of factors affecting the complexation of poly(acrylic acid)with poly(oxyethylene)[J].Macromolecules,1985,18(10):1829-1833.
[10]吕挺,单国荣.粘度法研究聚丙烯酰胺与聚乙烯醇在水中的相互作用[J].高分子学报,2010(2):156-159.
[11]SONG B K,CHO M S,YOON K J,et al.Dispersion polymerization of acrylamide with quaternary ammonium cationic comonomer in aqueous solution[J].J Appl Polym Sci,2003,87:1101-1108.
[12]CHO M S,YOON K J,SONG B K.Dispersion polymerization of acrylamide in aqueous solution of ammonium sulfate:Synthesis and characterization[J].J Appl Polym Sci,2002,83(7):1397-1405.
[13]单国荣,曹志海,黄志明,等.丙烯酰胺双水相聚合体系稳定性研究[J].高分子学报,2005(5):784-788.
[14]刘平,黄展淑,谢志明,等.聚丙烯酸与聚乙烯醇在浓溶液中的复合作用[J].高分子材料科学与工程,1995,11(5):79-82.
[15]OYAMA H T,TANG W T,FRANK C W.Effect of hydrophobic interaction in the poly(methacrylic acid)/pyrene end-labeled poly(ethylene glycol)complex[J].Macromolecules,1987,20(8):1839-1847.
Viscosity Behavior of Solution of Acrylic-acid-based Polyelectrolyte and Poly(ethylene glycol)
XU Lijuan,SHI Hualei,XIAO Xiansen,WANG Zhenghui
(College of Materials and Energy,South China Agricultural University,Guangzhou 510642,Guangdong)
This paper reports the phase diagram of PEG-PAA-C2H5OH-H2O system at different temperatures and the effects of concentration,temperature,PEG molar ratio,NaCl and Urea on viscosity behavior of PAA(DN-50%),which are from PAA with 50% carboxyl group neutralized,PAANa and their composite with PEG.The results show that the relatively stable“carboxyl bridges”formed by the internal hydrogen bonding of PAA chain coils,the entanglement effect of PEG with hydrophobic structure in inflexible chain and the effect of ethanol on extinction of intermolecular forces are coexisting.Compared with PAANa,the effect of concentration of PAA(DN-50%)on its specific viscosity has less impact because of the“carboxyl bridges”effect.The change trends of specific viscosity of composites are different when PEG is below the molar ratio of 0.5 for the difference of the winding mode of PEG to PAA(DN-50%)and PAANa.The internal energy of the chain segments increases with the increase of temperature so that the specific viscosity of the solution decreases correspondingly.Mainly due to the same ion effect,the specific viscosities of the two kinds of composite solutions decrease with the increase of the NaCl concentration.Hydrogen bonding and hydration of urea molecules on the surface of PAA(DN-50%)coil lead to the increasing of the specific viscosity of composite PEG+PAA(DN-50%)with increasing the urea concentration when the urea concentration is below 0.25%.When the concentration of urea exceeds 0.25%,the polymer coils shrink and the specific viscosities decrease because of the hydrogen bonding interactions between urea molecules in the polymer coils and carboxyl group.
poly(acrylic acid);poly(ethylene glycol);phase diagram;composite;viscosity behavior
O631.4
A
1001-8395(2016)04-0566-05
10.3969/j.issn.1001-8395.2016.04.020
(编辑 余 毅)
2015-09-18
广州市科技计划项目(2013J4300041)
*通信作者简介:王正辉(1963—),男,教授,主要从事高分子理论及应用的研究,E-mail:zhwang@scau.edu.cn
