黄体酮阴道缓释凝胶配伍减量肌注黄体酮在体外受精-胚胎移植技术中的应用研究*
2016-07-22第四军医大学唐都医院妇产科西安710038黄剑磊马夜肥王晓红
第四军医大学唐都医院妇产科(西安710038) 巨 瑛 吴 静 黄剑磊 刘 芳 马夜肥 王晓红
黄体酮阴道缓释凝胶配伍减量肌注黄体酮在体外受精-胚胎移植技术中的应用研究*
第四军医大学唐都医院妇产科(西安710038)巨瑛吴静黄剑磊刘芳马夜肥王晓红▲
摘要目的:探讨在体外受精胚胎移植技术中黄体酮阴道缓释凝胶联合减量肌注黄体酮方案对妊娠结局的影响。方法:采用黄体酮阴道缓释凝胶联合减量肌注黄体酮方案(研究组)进行黄体支持的IVF-ET共1556个周期,与同期常规肌注黄体酮方案(对照组)进行黄体支持的IVF-ET共1553个周期,比较两种黄体支持方案的有效性。结果:在治疗效果中,<35岁组与35~39岁组两种治疗方案在着床率、临床妊娠率及异位妊娠率方面均无显著性差异(P>0.05);在早期流产中,<35岁研究组早期流产率为4.8%,对照组早期流产率为11.3%;35~39岁研究组早期流产率为4.5%,对照组早期流产率为23.7%,两组早期流产率比较均有显著性差异(P<0.05),且以年龄35~39岁差异更大(P<0.01)。结论:黄体酮阴道缓释凝胶联合减量肌注黄体酮方案与常规单用肌注黄体酮相比,在保持着床率及临床妊娠率的前提下,能够降低早期流产率的发生,是一种有效易行的黄体支持方案。
主题词受精,体外胚胎移植黄体保持妊娠结局
IVF-ET技术中黄体支持已成为必要步骤之一。对于黄体缺陷的理论依据,大部分学者认为在使用促性腺激素释放激素激动剂(GnRH-a)进行降调节中,GnRH-a引起垂体抑制,导致垂体功能恢复延迟引起。少数理论支持助孕中经阴道穿刺取卵的同时抽吸了部分颗粒细胞,引起妊娠早期黄体功能缺陷。虽其理论机制尚未十分明确,但是为提高最终妊娠结局,黄体支持已成为必然。目前黄体支持用药方法有多种,包括药物种类、给药方式、药物剂量及是否联合用药等,然而仍无统一标准。我中心采用黄体酮阴道缓释凝胶联合减量肌注黄体酮黄体支持方案,与常规肌注黄体酮方案进行回顾性对照研究,比较分析两种黄体支持方案在IVF-ET术中的助孕效果。
对象与方法
1研究对象本研究选取第四军医大学唐都医院妇产科生殖医学中心2010年1月至2012年7月采用GnRH-a长方案、女方年龄20~39岁、行IVF-ET的共3109个周期。其中:黄体酮阴道缓释凝胶联合减量肌注黄体酮方案为研究组1556个治疗周期;常规肌注黄体酮方案为对照组1553个治疗周期。
2研究方法患者均采用GnRH-a长方案,于前一周期的黄体中期(约月经周期第18~24d)皮下注射促性腺激素释放激素激动剂(GnRH-a)0.05mg~0.1mg/d(曲普瑞林),对垂体进行降调节,于卵泡期早期(月经周期第3~5d)根据患者年龄、基础卵泡数、血清激素水平等,适当给予卵泡刺激素(FSH或/FSH+hMG,100U~300U/d),阴道B超监测卵泡发育,当个主导卵泡径线≥18mm、同时至少3个卵泡直径≥17mm时,注射5000~10000U人绒毛膜促性腺激素(hCG),36h后于B超引导下行经阴道穿刺取卵术。所有患者自取卵日起肌注黄体酮20mg,根据受精日血中P水平给予黄体酮20~40mg/d。自移植前一天起黄体支持方案分成两种,研究组:阴道给予黄体酮缓释凝胶(雪诺同,默克雪兰诺)1枚同时肌注黄体酮注射液20~40mg/d。根据ET后每3d血中P水平调整黄体酮针剂用量,至ET后第15天,若血HCG(+),每5d复查1次血中P水平。若血中P浓度维持在30~50ng/ml以上,则每5d黄体酮针剂减量1次,每次减少剂量10~20mg/d,直至减完。一般情况,黄体酮针剂在ET后15d查HCG(+)后15~20d后停止使用。阴道黄体酮缓释凝胶放置至孕84d左右(ET后70d左右)。对照组:肌注黄体酮针剂60~80mg/d肌注至ET后30dB超见孕囊及胎心后,每5d复查一次P,若血中P浓度维持在30~50ng/ml以上,则每5d黄体酮针剂减量1次,每次减少剂量10~20mg/d,直至减完。
结果
两个年龄组不孕年限、促性腺激素(Gn)用量、 获卵数、移植胚胎数比较均无显著性差异(P>0.05 );黄体酮阴道缓释凝胶联合减量肌注黄体酮与单纯肌注黄体酮这两种黄体支持方案中,<35岁组与35~39岁组在着床率、临床妊娠率及异位妊娠率等方面均无显著性差异(P>0.05 );在早期流产中,<35岁研究组早期流产率为4.8%,对照组早期流产率为11.3%;35~39岁研究组早期流产率为4.5%,对照组早期流产率为23.7%,两组早期流产率比较均有显著性差异(P<0.05),且以年龄35~39岁差异更大(P<0.01)。详见表1~2 。

表1 两组年龄<35岁患者治疗效果比较
注:*与对照组比较,P<0.05
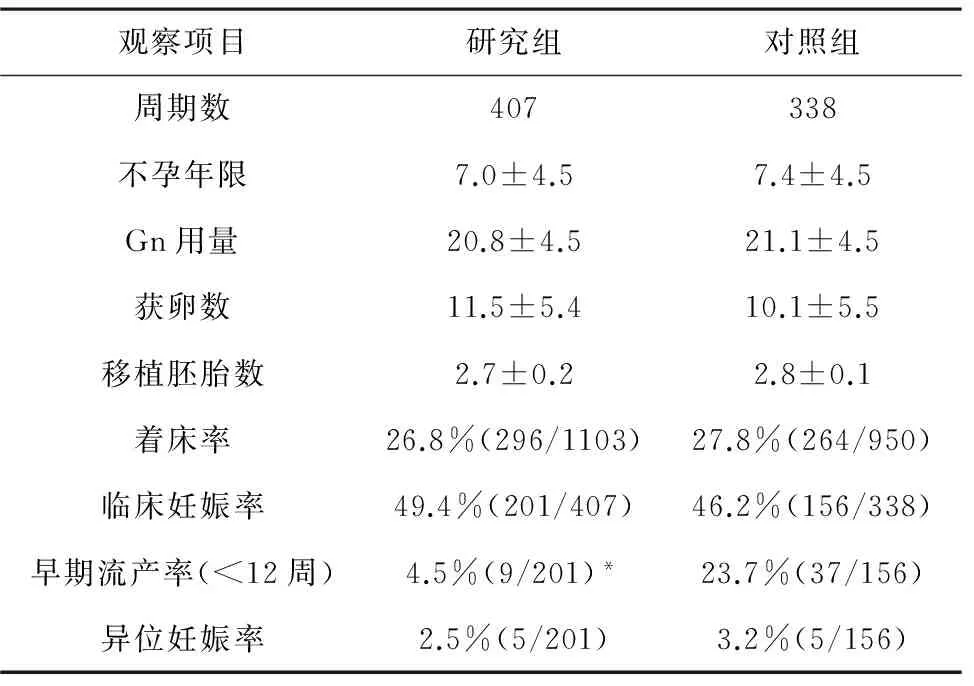
表2 两组年龄为35~39岁患者治疗效果比较
注:*与对照组比较,P<0.05
讨论
Edwards和Steptoe[1]早于1980年提出IVF-ET助孕必须进行黄体支持以达到满意的结局。但迄今为止,其理论机制仍未完全阐明。然而多数研究者将其归为以下两个因素:①IVF-ET超促排卵周期多使用GnRH激动剂对垂体降调节。垂体一旦被抑制,则需要在抑制停止后的2~3周才能缓慢恢复,取卵时垂体还在降调节的作用时间内,内源性的LH仍处在低水平,从而P水平低下; ②负压吸取卵泡时,可能使颗粒黄体细胞减少,进而引起黄体功能不足[2]。因此,为了改善由于IVF-ET导致的黄体功能缺陷,我们需要进行黄体支持。
目前黄体支持常见给药方式主要有三种:口服、肌注和经阴道给药[3]。三种方式各有优缺点。口服孕酮方便易行,但因肝脏首过效应后,生物利用度仅<10%,且其代谢产物可引起嗜睡、恶心及面色潮红等不良反应。目前很少单独采用口服制剂进行黄体支持。肌注黄体酮经济高效,不存在肝清机制,吸收快,2h可达血清浓度高峰,维持8h。而且肌注部位就像一个储存站,孕酮在脂肪组织堆积,并向母体外周血中缓慢释放。因此,肌注黄体酮是一种能够更加维持稳定孕酮血清浓度的给药方式,也是目前国内普遍采用的黄体支持方式。但IVF-ET后大剂量长时间肌注黄体酮可导致注射部位疼痛、瘙痒、甚至过敏反应及无菌脓肿形成,且油剂黄体酮半衰期长,通常需要数周才能恢复。阴道给药的黄体酮在子宫内膜产生明显的局部效应,即所谓的子宫首过效应,这种方法可以对子宫内膜直接作用,不参与全身循环。体外试验子宫放射性自显影显示:黄体酮经阴道给药后呈现时间依赖性从宫颈到宫底扩散,同时显示在给药后1h,黄体酮出现在子宫内膜,而之后开始扩散至子宫肌层,在给药5h后黄体酮聚集在整个子宫内膜和肌层,并达到稳定浓度;在体内试验中也可以得到相似的浓度积聚,但是肌注后没有。同时,黄体酮阴道给药可有效诱导子宫内膜完成分泌同步转化[4,5]。然而,有文献报道单纯使用黄体酮阴道缓释凝胶进行黄体支持时出现个别患者阴道少量出血的现象。
为采取上述给药方式优势的同时避免其劣势,并且使得药物在子宫局部产生的生物学效应最大化的同时不希望的全身作用最小化,我中心提出并且实施了以阴道给药为主,减量肌注黄体酮为辅的改良方案。
根据肌注及阴道给药不同的吸收特点,具体方案的设计如上所述。阴道黄体酮缓释凝胶联合减量肌注黄体酮方案一般约于HCG日后15~20d内黄体酮针剂减完,而此时单用肌注黄体酮组才开始减量。因此,这种改良方案不仅注射黄体酮剂量较少,约为常规方案的一半;且时间短,一般注射针剂时间为25d左右,而常规肌注黄体酮组,一般注射针剂时间为50d左右,肌肉注射黄体酮时间缩短一半。减少了患者因为长期肌肉注射黄体酮油剂引起的痛苦,依从性较好。且此改良方案显著降低了早期流产率及罕见单用黄体酮阴道缓释凝胶的点滴出血等副作用,这可能由于更稳定的血中P水平,晨起放置阴道黄体酮缓释凝胶,其在5h后达到稳定子宫浓度,12h降至较低水平,下午肌注黄体酮,正好处在阴道给药子宫P逐渐下降期间。黄体酮注射后2h达到最大P浓度,并且持续8h,在24h内,体内含有充足的P进行黄体支持,局部与全身的交替使用,药物作用产生的P水平更均衡。
近十几年中,不断有学者对黄体支持方案进行各种临床试验研究。Zarutskie等[6]2007年对于阴道给药及肌注黄体酮在持续妊娠及临床妊娠等方面的荟萃分析结果显示:对于辅助生殖技术周期中的黄体支持,阴道黄体酮的妊娠流产率显著低于肌注黄体酮。2008年Daya等[7]研究显示:使用雪诺同及肌注黄体酮两组患者间妊娠率、种植率、早期流产率等方面均无显著性差异,然而使用雪诺同的患者其副反应更少,满意度更高。2012年Kaser等[8]认为在冷冻胚胎移植周期中,与肌注黄体酮相比,单用雪诺同的临床妊娠率及活产率显著降低。而同年2月Kaylen等[9]对IVF周期中阴道用黄体酮及肌注黄体酮对比研究表明:在年轻女性中,阴道用黄体酮可明显提高妊娠率,而年长女性,则效果无明显差异。由此可见,助孕治疗中黄体支持方案效果仍存在争议。
目前,国内外对于ART中黄体支持方案随着不同新药、新剂型的引入,一直处于不断更新的状态。黄体酮阴道缓释凝胶联合减量肌注黄体酮方案用于IVF黄体支持不仅助孕效果良好,而且在一定程度上可避免患者因为长期肌注黄体酮产生的痛苦,更加人性化。然而,能否单一采用阴道给药完全取代肌注黄体酮对长方案取卵后患者进行黄体支持还有待进一步研究。
参考文献
[1]Edwards RG, Steptoe PC. Establishing full-term human pregnancies using cleaving embryos grown in vitro[J].Br J Obstet Gynaecol,1980,87(2):737-756.
[2]Ciampaglia W, Cognigni GE.Clinical use of progesterone in infertility and assisted reproduction[J]. Acta Obstet Gynecol Scand, 2015,94 (Suppl 161):17-27.
[3]Vaisbuch E, De-Ziegler D, Leong M,etal. Luteal-phase support in assisted reproduction treatment: real-life practices reported worldwide by an updated website-based survey[J]. Reprod Biomed Online,2014,28(3):330-335.
[4]Bulletti C, De Ziegler D, Flamigni C. Targeted drug delivery in gynaecology: the first uterine pass effect[J]. Human Reproduction,1997 ,12 (5):1073-1079.
[5]Beltsos AN,Sanchez MD,Doody KJ,etal. Patients' administration preferences: progesterone vaginal insert compared to intramuscular progesterone for Luteal phase support[J]. Reprod Health, 2014,11(1):78-79.
[6]Zarutskie PW, Phillips JA. RE-analysis of vaginal progesterone as luteal phase support (LPS) assisted reproductive teachnology (ART) cyckes[J]. Fertil Steril, 2007,88(Supl1): 113-115.
[7]Daya S, Gunby JL.Withdrawn:Luteal phase support in assisted reproduction cycles[J]. Cochrane Database Syst Rew, 2008,16(3):4830.
[8]Kaser DJ, Ginsburg ES, Missmer SA,etal. Intramuscular progesterone versus 8% Crinone vaginal gel for luteal phase support for day 3 cryopreserved embryo transfer[J]. Ferti and Steri, 2012, 97(2):1-6.
[9]Kaylen M,Silverberg MD,Thomas C,etal. Vaginal (Crinone 8%) gel vs intramuscular progesterone in oil for luteal phase support in vitro fertilization: a large prospective trial[J]. Ferti and Steri, 2012, 97(2):344-348.
(收稿:2015-12-20)
通讯作者▲
【中图分类号】R714.13
【文献标识码】A
doi:10.3969/j.issn.1000-7377.2016.05.003
The clinical research of progesterone vaginal gel associated with reductionof intramuscular progesterone protocol in vitrofertilization - embryo transfer
Department of Obstetrics and Gynecology,Tangdu Hospital of the Fourth Military Medical University(Xi’an710038)Ju YingWu JingHuang Jianleiet al
ABSTRACTObjective: To study the effects of progesterone vaginal gel associated with reduction of intramuscular progesterone luteal support protocol on pregnant outcomes with in vitro fertilization-embryo transfer. Methods: In this study, IVF-ET 1556 cycles from Jan. 2010 to Jul. 2012 with progesterone vaginal gel combined with reduction of intramuscular progesterone protocols(study group), and 1553 cycles with conventional intramuscular progesterone protocols(control group) were analyzed retrospectively. Results: In both <35y and 35~39y groups,there were no statistical differences between the two luteal support protocols in implantation rates, clinical pregnancy rates and ectopic pregnancy rates. But both of the early abortion rates, in <35y cycles study group 4.8 %, control group 11.3%, and in 35~39y cycles study group 4.5%, control group 23.7%, were significant difference. Conclusion: The luteal support protocol of progesterone vaginal gel combined with reduction of intramuscular progesterone not only has the same implantation rates, clinical pregnancy rates and ectopic pregnancy rates with conventional intramuscular progesterone protocol, but also could reduce the early abortion rate. It seemed to be more effective and convenient for pregnant outcomes.
KEY WORDSFertilization in vitro Embryo transferCorpus luteum maintenancePregnant outcome
*国家自然科学基金资助面上项目(81370710)