影响乳清分离蛋白和酪蛋白乳液物理稳定性因素研究
2016-07-14朱振宝王艳斐易建华
朱振宝, 王艳斐, 易建华
(1.陕西科技大学 食品与生物工程学院,陕西 西安 710021; 2.陕西科技大学 陕西省食品加工工程技术研究中心,陕西 西安 710021)
影响乳清分离蛋白和酪蛋白乳液物理稳定性因素研究
朱振宝1,2, 王艳斐1, 易建华1,2
(1.陕西科技大学 食品与生物工程学院,陕西 西安710021; 2.陕西科技大学 陕西省食品加工工程技术研究中心,陕西 西安710021)
摘要:以乳清分离蛋白(WPI)和酪蛋白(CS)为乳化剂、以核桃油为油相,制备出了水包核桃油(O/W)乳状液.研究了蛋白质浓度、盐离子种类及其强度、pH等因素对乳液物理稳定性的影响.结果表明,当蛋白质浓度为0.2~1.5 w/v%时,乳液物理稳定性随两种蛋白质浓度的增大而增强;pH对乳液稳定性影响较大,在蛋白质等电点(pI 4.6)附近,乳液失稳;CaCl2较NaCl更容易使两种蛋白乳液失稳.在pH7.0时,CS乳液在NaCl 300 mM时仍然稳定,而WPI乳液稳定的最大NaCl浓度为100 mM;在pH3.0时,WPI乳液为50 mM,而CS乳液为25 mM.在乳液加入CaCl2后,WPI乳液在pH分别为7.0和3.0时,稳定的最大Ca2+浓度均为2 500 μM;而CS乳液在pH7.0时为1 000 μM、pH3.0时为500 μM.
关键词:乳清分离蛋白;酪蛋白;乳状液;物理稳定性
0引言
水包油(O/W)乳状液,例如牛奶、婴幼儿食品、沙拉酱、乳饮料等是最常见的食品体系之一[1].但乳状液的稳定性易受到制备方法、乳化剂类型和用量、温度、电解质离子、以及介质pH等影响,在制备和贮存过程中容易出现聚结、分层、破乳等失稳现象[2].
蛋白质是天然两亲性大分子物质,常作为乳化剂和泡沫稳定剂而被广泛应用于食品乳状液体系中[3].它可以快速吸附到油水界面形成粘弹性界面层,并通过静电或空间立体排斥力提高乳液的稳定性[4].在乳滴界面上,酪蛋白(CS)拥有疏松开放的空间结构,而乳清分离蛋白(WPI)则是较紧凑的球状结构.这些吸附在乳滴界面的蛋白质的组织结构被认为是控制乳液及其相关产品的一个主要因素[3].
核桃油中富含多不饱和脂肪酸(PUFA).有研究表明,核桃油中的ω-3脂肪酸能预防因高血压而造成的动脉损伤[5],更重要的是核桃油中ω-6/ω-3脂肪酸比例符合联合国粮农组织和世界卫生组织推荐的膳食比例[6].
近年来,核桃油逐渐受到消费者的青睐.基于此,本课题用WPI和CS作为乳化剂,制备出了水包核桃油乳状液,研究了蛋白质浓度、盐离子及其浓度、pH等对乳液物理稳定性的影响,以期为乳液食品的开发及利用提供理论依据.
1材料与方法
1.1实验材料与仪器
1.1.1主要材料与试剂
乳清分离蛋白:DaviscWPI95,WPI蛋白质含量为97.6%,乳清分离蛋白中的主要蛋白成分为55%~61% β-LG,19%~22% α-LG,6%~8%牛血清白蛋白,上海福诺食品有限公司;酪蛋白(Casein),新疆伊犁特克斯县科瑞乳品开发有限公司;磷酸氢二钠、磷酸二氢钠、叠氮钠:分析纯,天津市科密欧化学试剂有限公司;无水氯化钙、氯化钠、石油醚:分析纯,天津市天力化学试剂有限公司;核桃油:实验室自制.
1.1.2主要仪器
精密pH计:PB-10型,赛多利斯科学仪器北京有限公司;电子天平:BS323S型,赛多利斯科学仪器北京有限公司;磁力搅拌器:84-1型,上海梅颖浦仪器仪表制造有限公司;超细匀浆器:F6/10-10G型,上海弗鲁克流体机械制造有限公司;超高压均质机:HP-4L科研型,喜高精密流体机械有限公司;激光粒度仪:Mastersizer2000 型,英国Malvern仪器有限公司;纳米粒度表面电位分析仪:ZetasizerNANO-ZS90型,英国Malvern仪器有限公司;正置式显微镜(目镜放大倍数10×,物镜放大倍数100×):DM2500M型,德国徕卡仪器有限公司.
1.2实验方法
1.2.1核桃油的制备
参考文献[7]进行制备,有所改动.将新鲜无病害核桃去壳后,用0.6 M的NaOH溶液于55 ℃的热水中浸泡核桃仁15 min,然后手工去皮;将去皮后的核桃仁置于40 ℃的烘箱中烘干,用粉碎机打成粉状,然后以核桃仁粉:石油醚为1∶6的比例加入石油醚,搅拌使其充分浸提核桃油,通过抽滤进行固液分离,旋转蒸发回收石油醚,即得到核桃油. [8]进行制备,略有改动.将乳清分离蛋白和酪蛋白按照一定浓度溶解于10 mM pH3.0或7.0的磷酸氢二钠-磷酸二氢钠缓冲液中,加入0.02%的叠氮钠防腐;室温下磁力搅拌2 h,放入4 ℃冰箱中冷藏过夜;将5%的油相与95%的水相通过手持式超细匀浆机搅拌混合形成粗乳,搅拌速率为20 000 r/min,搅拌时间为1 min;然后在50 MPa条件下高压均质3次,得到乳化均匀的乳状液.
1.2.2乳液的制备
1.2.3不同蛋白质及其浓度对乳液稳定性的影响
pH高于蛋白质的等电点pI时,乳滴带负电荷;pH低于pI时,乳滴带正电荷[9].而电荷的差异会对乳液的稳定性产生一定的影响,所以,本实验对带有两种不同电荷的乳液进行研究.
参照章节1.2.2所述方法,分别配制pH7.0不同浓度为0.2w/v%、0.3w/v%、0.5w/v%、0.7w/v%、0.9w/v%、1.0w/v%的WPI和CS溶液,制备乳液;pH3.0不同浓度为0.3w/v%、0.5w/v%、0.7w/v%、0.9w/v%、1.2w/v%、1.5w/v%的WPI和CS溶液,制备乳液.将乳液置于50 ℃的烘箱中放置15天,观察乳液是否分层,同时在0天、7天、14天时分别测定乳滴的粒径和ζ-电位[10],并用显微镜观察乳滴的形貌,以表征乳液的稳定情况,从而研究WPI和CS及其不同浓度对乳液稳定性的影响.
1.2.4pH对乳液稳定性的影响
将0.7%WPI和1.5%CS分别溶于pH7.0的缓冲液中,用0.1M的HCl溶液和NaOH溶液调节成多个pH梯度,最终为pH3、4、5、6、7、8,参照章节1.2.2所述方法,制备一系列乳液,其物理稳定性的表征如章节1.2.3所述,研究pH对乳液稳定性的影响.
1.2.5盐离子种类及其强度对乳液稳定性的影响
将0.3%WPI和0.9%CS溶于pH7.0缓冲液中;0.7%WPI和1.5%CS溶于pH3.0缓冲液中.pH7.0WPI和CS水相中NaCl浓度均为0mM、50mM、100mM、200mM、300mM、400mM;pH3.0WPI水相中NaCl浓度同上,CS水相中为0mM、10mM、25mM、50mM、100mM,在磁力搅拌时缓慢加入,参照章节1.2.2所述方法,制备一系列乳液.同样,WPI水相中CaCl2浓度在pH7.0和3.0时均为0 μM、100 μM、500 μM、1 000 μM、2 500 μM、5 000 μM,CS均为0 μM、100 μM、500 μM、1 000 μM、2 500 μM,制备一系列乳液.其物理稳定性的表征如章节1.2.3所述,研究Na+和Ca2+及其浓度对乳液稳定性的影响.
2结果与讨论
2.1WPI、CS及其浓度对乳液稳定性的影响
不同浓度的WPI和CS乳液在50 ℃的烘箱中放置15天,采用视觉、显微形貌观察以及测定微滴粒径、ζ-电位等,研究了蛋白质种类及其浓度对乳液稳定性的影响.乳状液油滴粒径大小并非均一,一般呈现一定的分布趋势,因此,常用粒径分布曲线来反映乳状液液滴的分布情况[11].研究发现,WPI与CS形成乳液,其乳滴的ζ-电位无显著性差异(数据未显示),这与Hu等[12]的研究结果一致.研究同时显示,蛋白质浓度对乳滴的ζ-电位也无明显影响.
乳液的视觉观察如图1所示.图1表明,WPI、CS浓度对乳液物理稳定性产生了影响,总体表现为随着蛋白质浓度的增大乳液稳定性增强.如当pH3.0时,WPI浓度<0.5w/v%,乳液存放15天时失稳;而WPI浓度≥0.5w/v%,乳液无分层现象;相同pH及存放时间,CS浓度<1.2w/v%,乳液失稳;而CS浓度≥1.2w/v%,乳液无分层现象.
图1同时显示,乳液pH较低时,乳液物理稳定性较差.当pH7.0时,WPI一系列浓度乳液无明显分层,而pH3.0时,制备稳定乳液WPI的最低浓度为0.5w/v%;同样,当pH7.0时,制备稳定乳液CS的最低浓度为0.5w/v%,当pH3.0时,CS浓度达1.2w/v%,才能获得稳定的乳液.对比图1(a)、1(b)、1(c)、1(d)可发现,WPI乳液的稳定性高于CS.
如果已完工工序任务集合中的最后一个工序任务pthk∈pts1∪pts2∪∪ptsc,则pts1,pts2,,ptsc的相对完成工时量可表示为

(a)pH7.0 WPI乳液稳定性 (b)pH7.0 CS乳液稳定性

(c)pH3.0 WPI乳液稳定性 (d) pH3.0 CS乳液稳定性图1 乳液存放15天的照片
粒径分布如图2~3所示.由图2可看出,经过15天高温存放,乳滴粒径无增大趋势,且随WPI浓度的提升,粒径趋于集中分布,表明乳液稳定性增强,与图1结果一致;由图3显示,CS浓度较低时,乳滴粒径分布疏散无规律,表明乳液已失稳.而浓度较大时,乳液粒径分布范围变窄,说明稳定性增强.对比图2和图3,同样可以看出,WPI乳液较CS乳液的稳定性更好,这进一步验证了图1的结果.
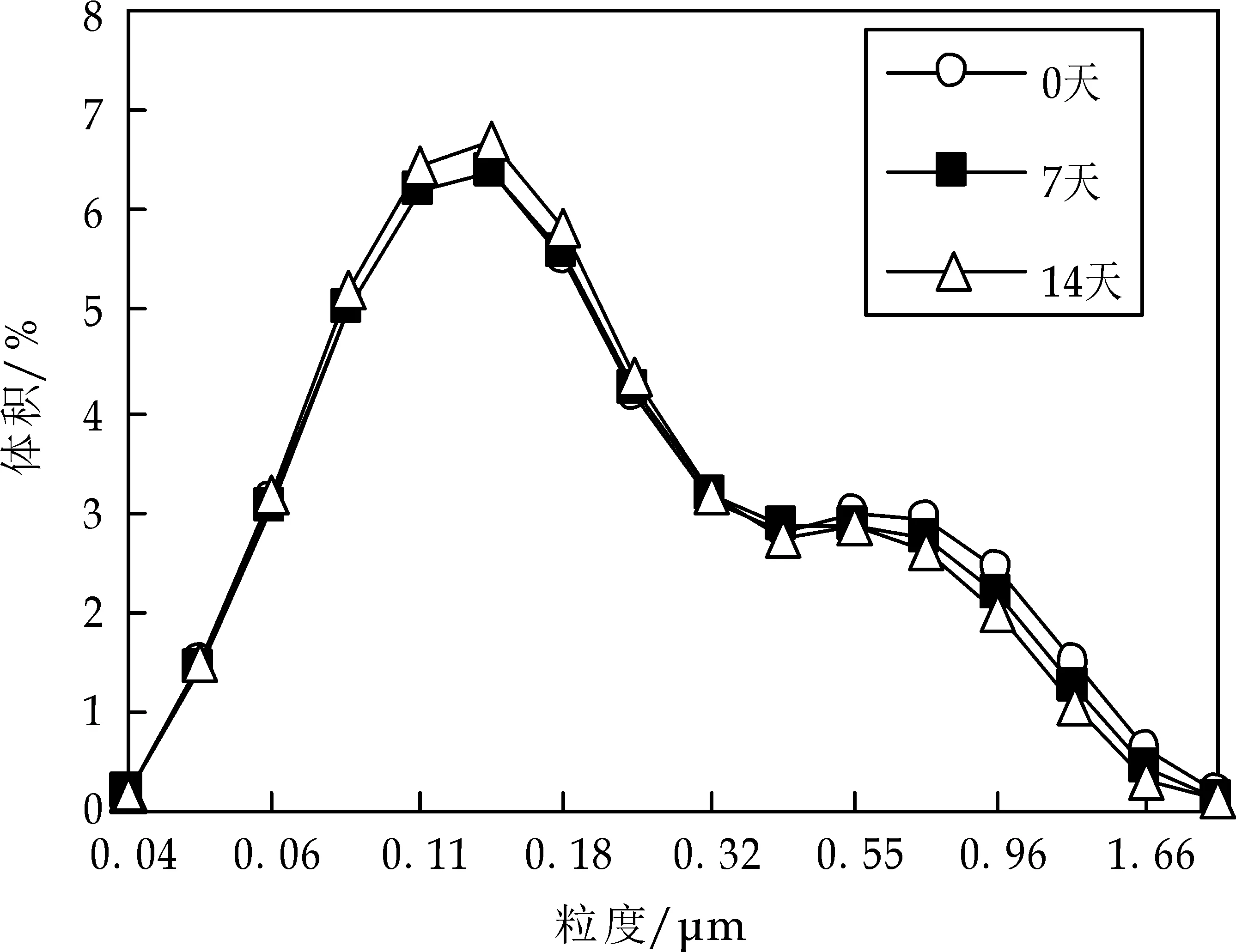
(a)pH7.0时0.2%WPI乳滴粒径的分布
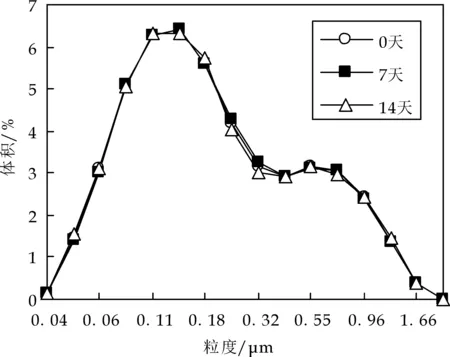
(b)pH7.0时0.3%WPI乳滴粒径的分布

(c)pH3.0时0.3%WPI乳滴粒径的分布

(d)pH3.0时0.7%WPI乳滴粒径的分布图2 WPI乳液存放15天后的粒径分布
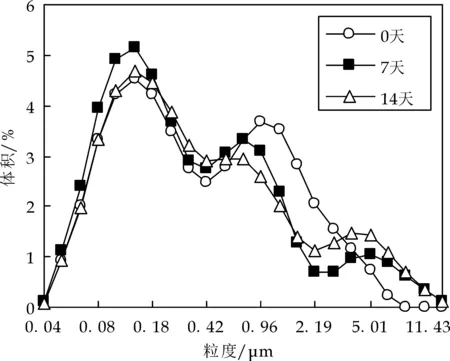
(a)pH7.0时0.7%CS乳滴粒径的分布
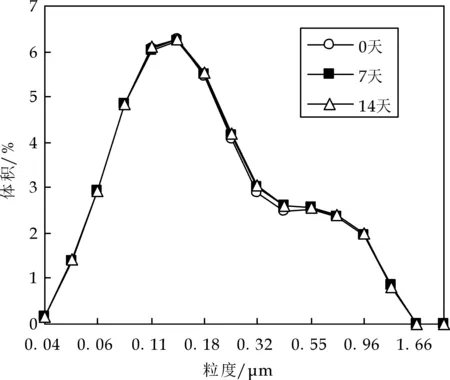
(b)pH7.0时0.9%CS乳滴粒径的分布

(c)pH3.0时1.2%CS乳滴粒径的分布
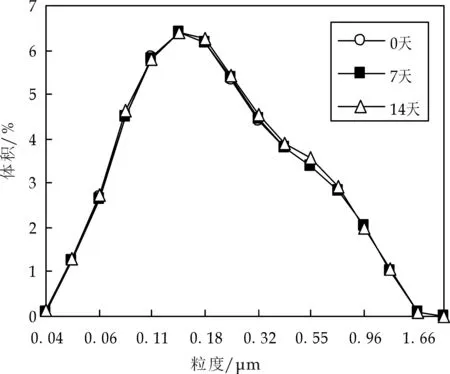
(d)pH3.0时1.5%CS乳滴粒径的分布图3 CS乳液存放15天后的粒径分布
显微形貌观察如图4~5所示.对比图4(a)、4(b)、4(c)、4(d)可以发现,当乳液为中性时,较低浓度的WPI可形成稳定的乳液,而乳液为酸性时,WPI浓度较低时,乳液微滴聚集成团,表明乳液稳定性较差(如图4(c)所示).分析图5,可获得与图4相同的结论,即提高乳液pH可提升乳液稳定性.图4~5同时显示,蛋白质浓度越大,乳化能力越高,在乳化过程中减少界面张力,可促进乳液的稳定性,这与Wan等[13]的研究一致.
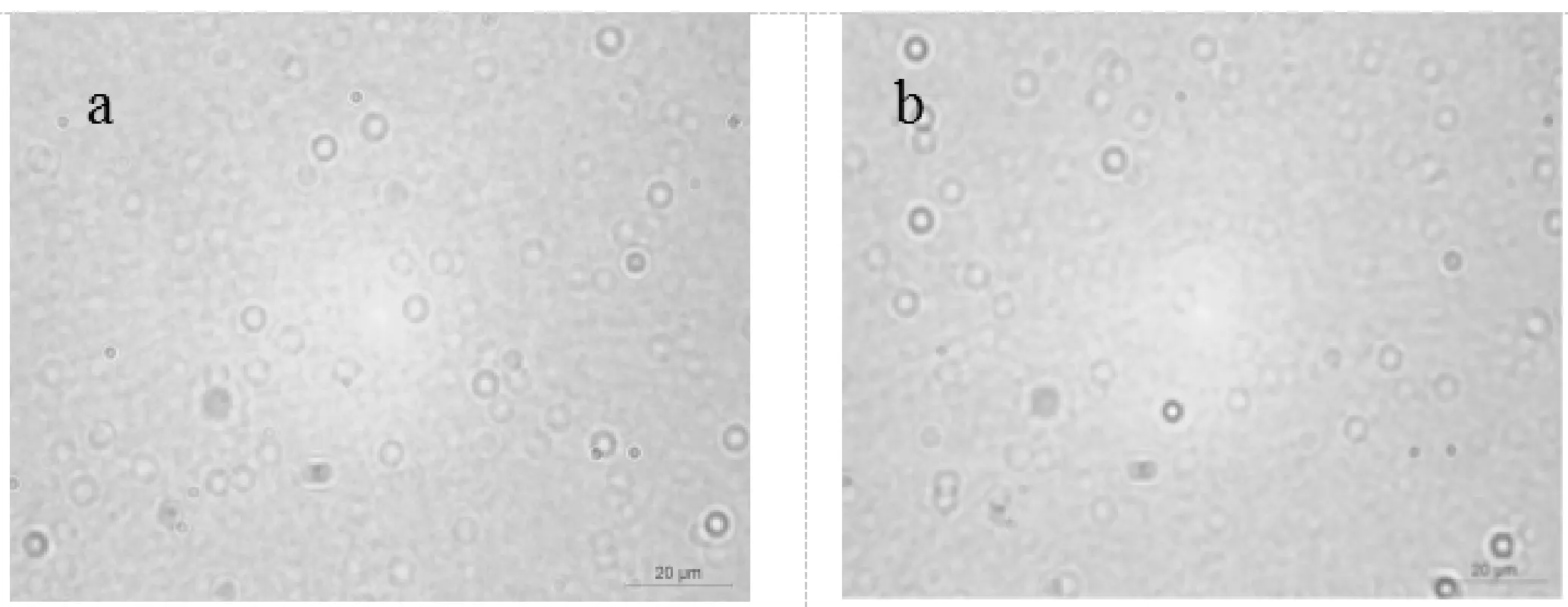
(a)pH7.0时0.2%WPI乳滴形貌 (b)pH7.0时0.3%WPI乳滴形貌
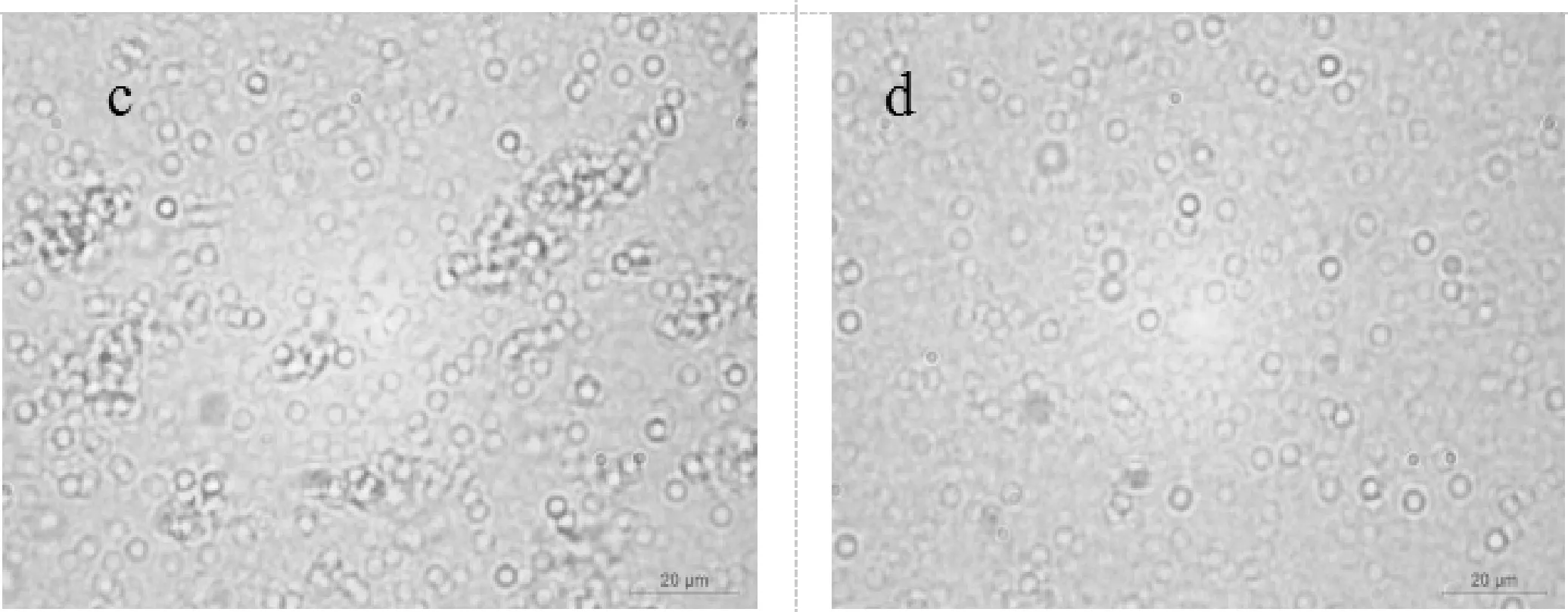
(c)pH3.0时0.3%WPI乳滴形貌 (d)pH3.0时0.7%WPI乳滴形貌图4 WPI乳液存放15天后的显微形貌观察
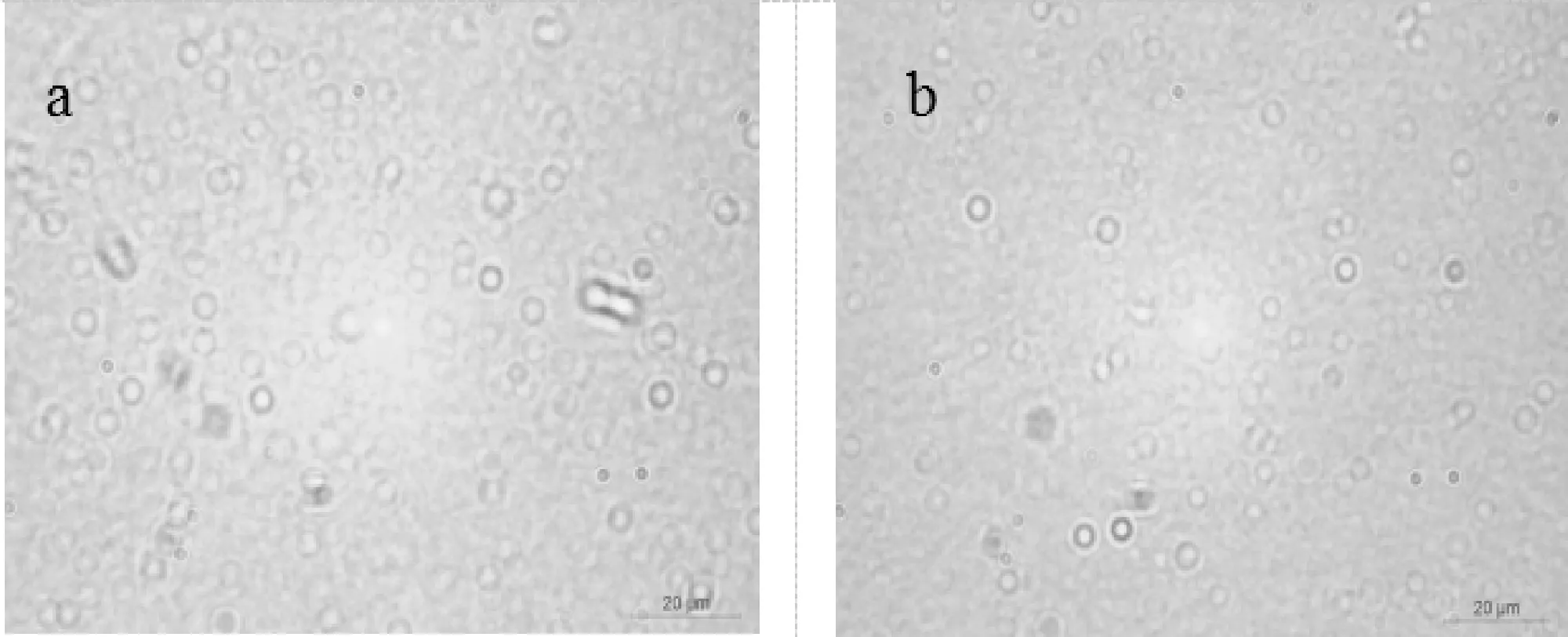
(a)pH7.0时0.7%CS乳滴形貌 (b)pH7.0时0.9%CS乳滴形貌
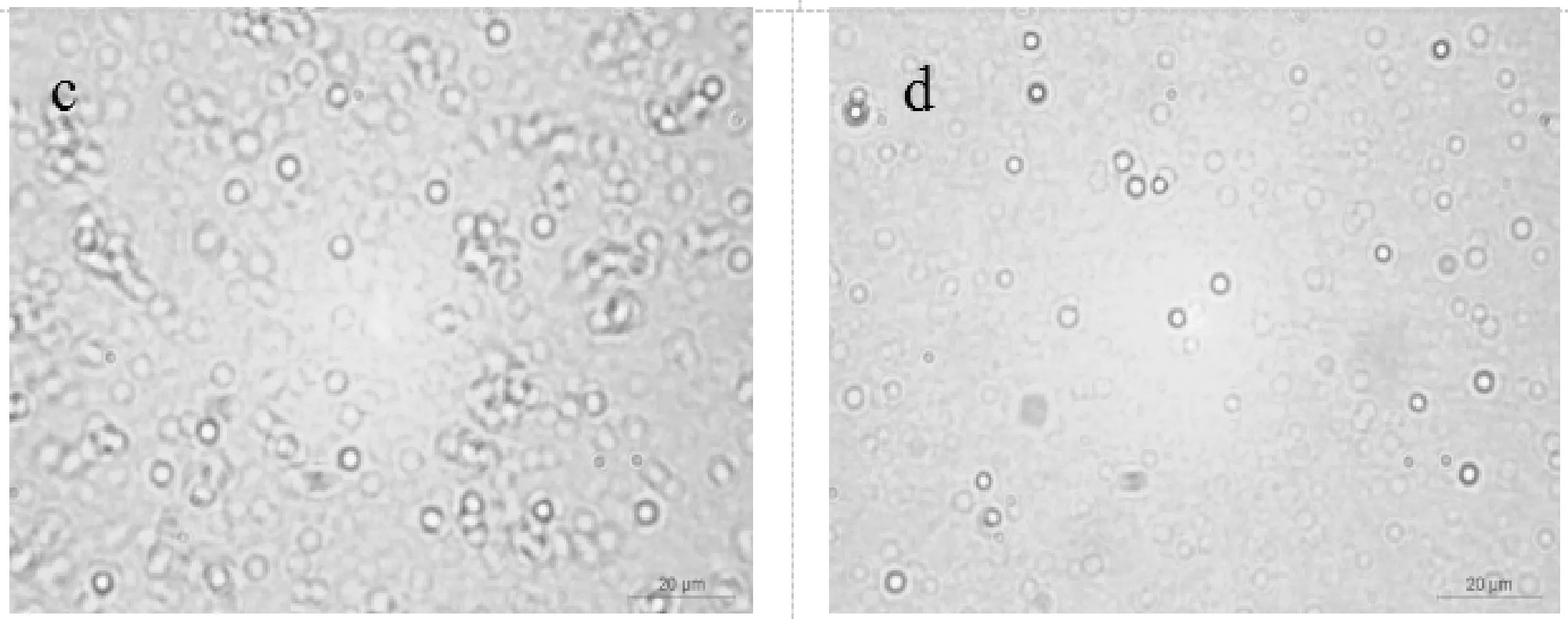
(c)pH3.0时1.2%CS乳滴形貌 (d)pH3.0时1.5%CS乳滴形貌图5 CS乳液存放15天后的显微形貌观察
2.2不同pH对乳液稳定性的影响
以上研究显示,pH可能影响乳液的稳定性.基于此,制备了一系列不同pH乳液,于50 ℃烘箱中放置15天,进一步探究pH对乳液稳定性的具体影响.视觉观察如图6所示,显微镜形貌观察如图7所示(部分图片),乳滴的ζ-电位如图8所示.
图6显示了WPI乳液分别在pH4.0、pH5.0时分层,CS乳液分别在pH4.0、pH5.0、pH6.0时分层,可见pH对CS乳液的影响大于WPI乳液;图7表明pH7.0时,WPI和CS乳液存放15天后乳滴均匀分布,乳液稳定;从图8可看出,当pH3.0、4.0时,乳滴带正电荷,当pH7.0、8.0时带负电荷,这与章节1.2.3所述相符合.
由于WPI和CS的等电点pI为4~6,在等电点附近,蛋白质的溶解度较小,形成乳状液的能力下降,而且此时蛋白质粒子表面电荷量较低,粒子间的静电排斥力降低,易发生絮凝或聚合,表现为乳状液乳滴粒径增大.但当pH远离等电点时,带电液滴间排斥力大于相互吸引的范德华力,液滴不会相互凝聚,乳状液具有高度的稳定性[14].

图6 乳液存放15天后的照片

(a)pH7.0 WPI乳滴形貌 (b)pH7.0 CS乳滴形貌图7 乳液存放15天后的显微形貌观察

(a)WPI

(b)CS图8 pH对乳液ζ-电位的影响
2.3盐离子种类及其强度对乳液稳定性的影响
在WPI和CS乳液中,加入不同浓度的Na+和Ca2+于50 ℃烘箱放置15天后,其视觉观察如图9~10所示,加入Na+后乳滴粒径的分布如图11所示.
图9显示,随着NaCl浓度的增大,乳液稳定性逐渐降低.对比图9(a)、9(b)可看出,当pH7.0时,WPI乳液含300mMNaCl已分层,而含一系列浓度NaCl的CS乳液尚未分层.这表明在中性条件下NaCl对WPI乳液的影响大于CS乳液;当pH3.0时,WPI乳液含300mMNaCl时出现分层现象,而CS乳液NaCl浓度为50mM已分层.这表明在酸性条件下NaCl对CS乳液的影响大于WPI乳液.对比图9(b)和9(d)可看出,若pH不同,NaCl对同一种蛋白乳液影响的差异较大,这表明pH与NaCl对蛋白质乳液的稳定性有影响.

(a)pH7.0时WPI乳液稳定性 (b)pH7.0时CS乳液稳定性

(c)pH3.0时WPI乳液稳定性 (d)pH3.0时CS乳液稳定性图9 NaCl对蛋白质乳液物理稳定性的影响

(c)pH3.0时WPI乳液稳定性 (d)pH3.0时CS乳液稳定性图10 CaCl2对蛋白质乳液物理稳定性的影响
预实验发现,WPI乳液的CaCl2浓度高于10mM时,乳液出现分层现象,而CS乳液的CaCl2浓度高于4mM时,乳液失稳,这表明CaCl2对乳液稳定性影响明显大于NaCl.pH与CaCl2对蛋白质乳液稳定性影响关系甚微,如图10(a)和10(c)所示,WPI乳液在相同浓度下均未分层.
pH7.0时WPI和CS乳液稳定最高钙盐浓度分别为2 500 μM和1 000 μM;pH3.0时分别为2 500 μM和500 μM(图未显示).Ca2+对乳液稳定性的影响比Na+大,更容易使乳液失稳.已有研究表明,增加离子强度可以提高乳状液中水相离子强度,可以在乳状液中产生静电屏蔽,从而降低粒子间静电排斥力,诱发粒子絮凝或者聚合[14].
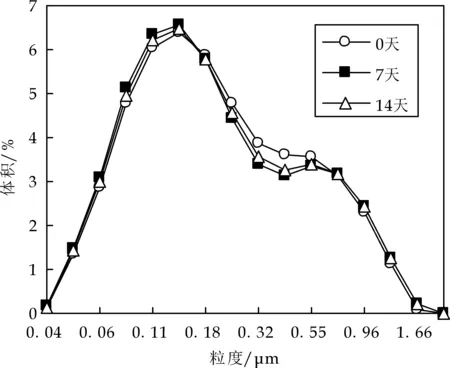
(a)pH7.0时NaCl浓度100 mM WPI乳滴粒径分布

(b)pH7.0时NaCl浓度300 mM CS乳滴粒径分布

(c)pH3.0时NaCl浓度50 mM WPI乳滴粒径分布
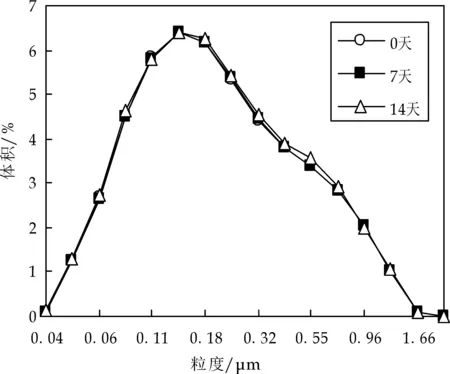
(d)pH3.0时NaCl浓度25 mM CS乳滴粒径分布图11 NaCl对乳液粒径分布的影响
3结论
以蛋白质为乳化剂制备了水包核桃油乳液,随着蛋白浓度的增大,乳液稳定性逐渐增大;pH对乳液稳定性具有较大影响,在蛋白质等电点附近,乳液出现失稳分层现象;二价Ca2+对乳液稳定性的影响大于一价Na+,pH7.0时WPI和CS乳液稳定的最高钠盐浓度分别为100mM和300mM,最高钙盐浓度分别为2 500 μM和1 000 μM;pH3.0时WPI和CS乳液稳定的最高钠盐浓度分别50mM和25mM,最高钙盐浓度分别为2 500 μM和500 μM.
[1]ThaddaoWaraho,D.JulianMcClements,EricA.Decker.Mechanismsoflipidoxidationinfooddispersions[J].FoodScienceandTechnology,2011,22:3-13.
[2] 冯建国,项盛,钱坤,等.乳状液稳定性表征方法及其在农药水乳剂研发中的应用[J].农药学学报,2015,17(1):15-26.
[3]LiDay,JialiZhai,MiXu,etal.Conformationalchangesofglobularproteinsadsorbedatoil-in-wateremulsioninterfacesexaminedbysynchrotronradiationcirculardichroism[J].FoodHydrocolloids,2012,12(15):1-10.
[4]SarahS.Kellerby,D.JulianMcClements,EricA.Decker.Roleofproteinsinoil-in-wateremulsionsonthestabilityoflipidhydroperoxides[J].JournalofAgriculturalandFoodChemistry,2006,54(20):7 879-7 884.
[5]CortsB,NezI,CofnM,etal.Acuteeffectsofhigh-fatmealsenrichedwithwalnutsoroliveoilonpostprandialendothelialfunction[J].JournaloftheAmericanCollegeofCardiology,2006,48(8):1 666-1 671.
[6] 易建华,程菁菁,董文宾.乳化剂类型、浓度及水相pH对水包核桃油乳状液物理稳定性的影响[J].食品工业科技,2015,36(13):266-270.
[7] 周慧江.核桃蛋白源ACE抑制剂肽的酶法制备及分离、纯化[D].西安:陕西科技大学,2013.
[8]YunShao,ChuanHeTang.Characteristicsandoxidativestabilityofsoyprotein-stabilizedoil-in-wateremulsions:Influenceofionicstrengthandheatpretreatment[J].FoodHydrocolloids,2014,37:149-158.
[9]MinHu,D.JulianMcClements,EricA.Decker.Impactofwheyproteinemulsifiersontheoxidativestabilityofsalmonoil-in-wateremulsions[J].JournalofAgriculturalandFoodChemistry,2003,51:1 435-1 439.
[10] 张芬芬,曾茂茂,何志勇,等.大豆分离蛋白乳状液稳定性的几种分析方法比较[J].食品科学,2012,33(17):44-47.
[11] 任晓芬,潘道东,曾小群,等.胞壁蛋白酶(CEP)酶解对酪蛋白结构及功能特性的影响[J].现代食品科技,2013,29(11):2 643-2 648.
[12]MinHu,D.JulianMcClements,EricA.Decker.Lipidoxidationincornoil-in-wateremulsionsstabilizedbycasein,wheyproteinisolate,andsoyproteinisolate[J].JournalofAgriculturalandFoodChemistry,2003,51:1 696-1 700.
[13]ZhiLiWan,LiYingWang,JinMeiWang,etal.Synergisticinterfacialpropertiesofsoyproteine-steviosidemixtures:Relationshiptoemulsionstability[J].FoodHydrocolloids,2014,39:127-135.
[14] 崔健,郦金龙,王盼,等.温度、pH和盐对乳清蛋白乳状液稳定性的影响[J].食品工业科技,2010,31(11):84-87.
【责任编辑:晏如松】
Factorsaffectingphysicalstabilityofemulsionsstabilizedbywheyproteinisolateandcasein
ZHUZhen-bao1,2,WANGYan-fei1,YIJian-hua1,2
(1.SchoolofFoodandBiologicalEngineering,ShaanxiUniversityofScience&Technology,Xi′an710021,China; 2.ShaanxiProvinceResearchCenterofFoodProcessEngineeringandTechnology,ShaanxiUniversityofScience&Technology,Xi′an710021,China)
Abstract:In the present study oil-in-water (O/W) emulsions were prepared with whey protein isolate (WPI) and casein (CS) as emulsifiers,and walnut oil as oil phase.The effects of protein concentration,salt ions and their concentrations,and pH on the physical stability of emulsions were investigated.The results showed that at the concentrations of 0.2~1.5 w/v%,the physical stability of emulsions increased with the increase of the concentration.pH had great effects on physical stability of emulsions with emulsions instability near the protein isoelectric point(PI 4.6).CaCl2 had greater effects on physical stability of emulsions than NaCl.At pH7.0,CS emulsions was stable at 300 mM NaCl,whereas WPI emulsions was stalble at 100 mM NaCl.At pH3.0,the highest concentrations of NaCl for stable emulsions containing WPI and CS were 50 mM and 25 mM,respectively.However,the highest concentration of CaCl2 for WPI emulsions was 2 500 μM at both pH7.0 and pH3.0,while they were 1 000 μM and 500 μM for CS emulsions at pH7.0 and pH3.0,respectively.
Key words:whey protein isolate;casein;emulsions;physical stability
*收稿日期:2016-03-21
基金项目:陕西省科技厅自然科学基金项目(2015JM3085)
作者简介:朱振宝(1971-),男,陕西商洛人,副教授,博士,研究方向:功能食品与人类营养
文章编号:1000-5811(2016)04-0125-06
中图分类号:TS202.3
文献标志码:A
