右美托咪啶对全麻下长时间腹部手术患者术后寒颤预防的临床观察
2016-07-12于宏标
于宏标
(辽宁省朝阳市中心医院麻醉科,辽宁 朝阳 122000)
右美托咪啶对全麻下长时间腹部手术患者术后寒颤预防的临床观察
于宏标
(辽宁省朝阳市中心医院麻醉科,辽宁 朝阳 122000)
【摘要】目的 评价右美托咪啶预防长时间全麻下腹部手术患者术后苏醒期寒战的临床效果。方法 选择择期腹部手术患者110例,ASA分级Ⅰ~Ⅱ级,随机分成两组,每组55例。一组应用右美托咪啶(D),一组应用生理盐水(C)作为对照组。两组手术时间皆>4 h。两组术前用药及诱导方法相同。术前应用咪达唑仑2 mg和阿托品0.5 mg静注。诱导采用丙泊酚1.5 mg/kg+舒芬太尼0.3 μg/kg或芬太尼2 μg/kg+顺苯磺酸阿曲库铵0.2 mg/kg。麻醉维持:吸入七氟烷1%~4%,静脉注射泵注入瑞芬太尼0.1 μg/(kg·min),间断给予顺苯磺酸阿曲库铵0.08 mg/(kg·h)。D组诱导前10 min开始给予右美托咪定0.5 μg/(kg·h),术中应用0.4~0.7 μg/(kg·h)维持,C组在相同时间段给予相同剂量的生理盐水。记录诱导前,插管即刻,麻醉后2 h,拔管前,拔管即刻,拔管后5、10 min生命指标;记录手术时间,苏醒时间,七氟烷用量,应用阿托品例数,输入液体量,腹腔冲洗液量;记录术毕患者拔管前,拔管后10 min寒战发生情况。结果 两组手术时间,输入液体量,腹腔冲洗量,苏醒时间,体温变化没有统计学差异;插管即刻,术毕拔管前,拔管即刻,拔管后5、10、30 min MAP,心率变化D组更稳定(P<0.05);D组七氟烷应用量少于C组,阿托品应用例数高于C组(P<0.05);术毕拔管前,拔管后10 min寒战发生率D组明显低于C组(P<0.05)。结论 全麻下长时间腹部手术患者应用右美托咪定能够显著预防术后寒战的发生;并能减少七氟烷的用量;减少插管、拔管期间血流动力学波动。
【关键词】右美托嘧啶;腹部手术;全身麻醉;术后寒战;保护作用
右旋美托嘧啶(dexmedetomidine,Dex)是选择性α2肾上腺素受体激动剂。和可乐定相比,右美托米啶是一种高选择性,高特异性α2肾上腺素受体激动剂。其受体选择性上α2/α1约为1600/1,约是可乐定α2/α1200/1与α2受体亲和力的8倍。其半衰期也较可乐定短,分布半衰期大约为6 min,消除半衰期大约为2 h,药代动力学方面的可预测性更强。Dex具有镇静、镇痛、抗焦虑等作用。因此,在临床上,Dex常被认为是一种很好的麻醉辅助用药。另Dex还具有抗寒颤的作用,国内在这方面的研究还很少,本文主要观察Dex在长期全麻患者术后寒颤的预防作用,以便为临床应用提供依据。
1 资料与方法
1.1一般情况:本研究患者均签署之情同意书。选择我院2012年5月至2014年5月择期腹部手术患者110例,年龄23~78岁,性别,身高,体质量等方面也没有明显差别。随机分成两组,对照组(C)和实验组(D),每组55例。术前两组ASA分级皆在Ⅰ-Ⅱ级,无合并明显的系统性疾病。如高血压,糖尿病,冠心病等。主要疾病包括:胃癌、直肠癌、十二指肠胰腺肿瘤等。手术时间4~8 h。
1.2 方法:所有患者均采用全麻,术前麻醉用药为阿托品0.5 mg+咪达唑仑2 mg,静脉注射,入手术室后诱导前给予。诱导用药为:丙泊酚1~2 mg/kg,顺阿曲库铵0.15~0.2 mg/kg,舒芬太尼0.2~0.5 μg/kg或芬太尼1~2 μg/kg,D组在诱导前10 min左右开始应用右美托米啶0.6 μg/kg注射泵静注,大约10 min注入,C组应用同等剂量的生理盐水。在麻醉维持期间,D组采用右美托米啶0.4~0.7 μg/(kg·h)加七氟烷吸入浓度1%~4%随麻醉深度调整,瑞芬太尼0.1 μg/(kg·h),在手术将结束前约30 min时开始停用右美托咪定。C组:麻醉维持采用七氟烷吸入,瑞芬太尼静脉泵注,浓度同D组,等量生理盐水同D组方法相应时间段注入。术前约30 min停用生理盐水注入。两组皆在手术结束前5 min停药,术后皆采用静脉PCA,主要药物为地佐辛0.8 mg/kg左右,于手术结束前约30 min给予地佐辛负荷量5 mg,静脉注射,之后接镇痛泵。术中心率<50次/分时应用阿托品纠正,剂量0.3~0.5 毫克/次。血压降低应用麻黄碱纠正,剂量6毫克/次,静脉注射。麻醉机监护仪皆是Drager系列产品。术中输液以平衡液及胶体为主:乳酸林格液,贺斯或万汶,根据出血情况决定是否输血,输液情况为8~10 mL/(kg·h)。所有液体皆没有采用加温措施。监测指标包括:血压、脉搏、呼吸、血氧饱和度、呼吸末二氧化氮分压、体温,CVP、术毕寒颤评分、镇静评分、苏醒时间,持续到术后半小时。
2 结 果
两组患者在年龄,性别,体质量,术前ASA分级方面没有统计学意义。麻醉期间平均动脉压(MAP),心率(HR)和体温(T)不同时间点变化见表1。诱导前,插管即刻,D组和C组相比无明显区别,麻醉2 h后,D组血压和心率和C组相比皆降低,二者具有统计学意义P<0.05;拔管之前,拔管即刻,拔管后5、10、30 min,D组与C组相比更趋于平稳,二者有统计学上意义P<0.05;体温方面两组间变化无明显区别。

表1 麻醉期间一般生命指标变化
手术中的一些情况见表2。由表2可知,D组和C组苏醒时间无明显统计学意义,而在七氟醚用量上,D组低于C组,但是D组阿托品应用例数多于C组,两组间有统计学意义。
寒颤评分情况见表3。表3可知,右美托咪定组寒颤发生率明显低于对照组。
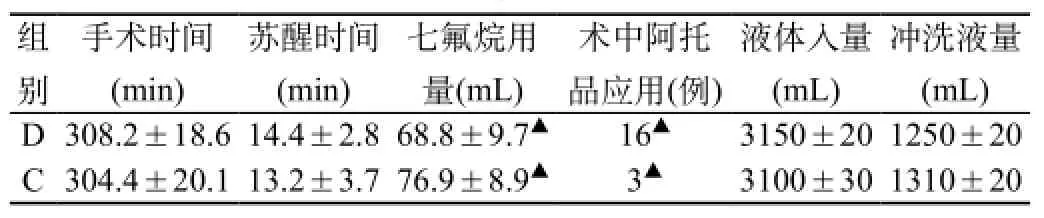
表2 术中一般情况
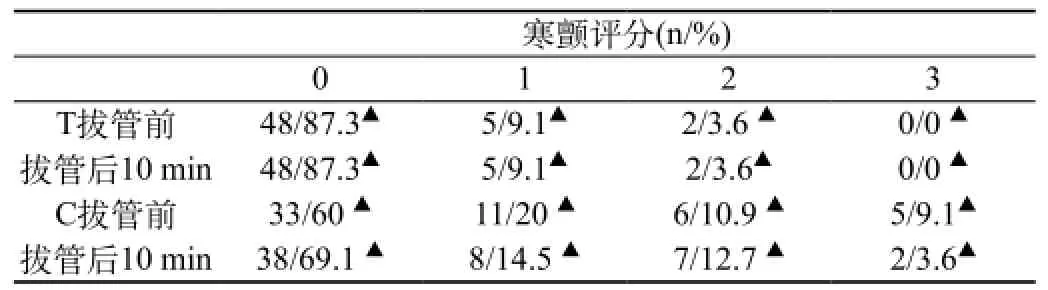
表3 寒颤评分情况
3 讨 论
腹部一些手术由于手术时间长,术中液体的需求量较大,再加上术中输液时,液体的温度难于控制一个理想的范围内,导致输入理想温度的液体要求技术较高,故多数以粗略估计液体温度为主,术中手术操作造成的内脏长时间暴露,术中大量冲洗液的应用,使得这类手术的术后寒颤的发生率一直很高。由于寒颤能够带来许多不良反应,有些甚至是致命性的。如除造成患者不适外,还可能增加眼内压、颅内压、加重伤口的疼痛,增加氧耗,对冠心病患者可能引起不良心血管事件。追求术毕寒颤发生率消失一直是临床理想的目标,最近几年在这方面已经取得了一定的进展,如输入加温液体,尽量减少手术对内脏不必要的暴露,保持手术室温度不要太低,尽量给患者保温,一些药物的预防应用等。但是并不是十分理想,如镇痛药(哌替啶和曲马多)及镇静药(咪达唑仑和丙泊酚)应用,这些药物确实能减少寒颤的发生,但是,他们引起的呼吸抑制一直是临床所顾虑。右美托咪啶的临床应用,可能为降低术后寒颤的发生率方面提供了一个很好的途径。右美托咪啶还有一个很好的优点:对呼吸影响较少。寒颤的评分,按照Crossley和Mahajan的方案进行寒颤分级:1级,为立毛征或外周血管收缩,无可见的寒颤;2级,为仅1组肌群寒颤;3级,为超过1组肌群寒颤但无全身肌群寒颤;4级,为全身寒颤。
右美托咪啶在降低寒颤发生率方面主要机制:右美托咪定预防寒战的具体机制不详,可能和下列机制有关:①Tobias等[1]认为此类药物主要作用于钾离子通道,使钾离子内流增加,神经细胞处于去极化状态,神经冲动传导减慢,导致体温中枢对体温的敏感性降低。②Phan等[2]人认为右美托咪定的抑制寒战的机制是通过抑制大脑体温调节中枢,降低寒战阈值,在脊髓水平抑制体温传入信息,从而抑制了寒战。一项对志愿者的研究[3]表明,靶血浆浓度为0.4 ng/mL的右美托咪咤,能够使寒战阑值降低2 ℃。本研究发现,体温降低二组皆没超过2℃,在此范围内右美托咪定抗寒颤作用显著。体温降低超过此值,右美托咪定是否仍旧有此功效尚不清楚。③温度信息从皮肤表面通过脊髓中缝核和中枢蓝斑核传到下丘脑,寒战中枢受到视交叉前的下丘脑部分的抑制性控制,这种控制可以被肾上腺素和去甲肾上腺素(NE)加强[4],右美托咪定作为高选择性α2肾上腺素能受体激动药作用于蓝斑核,抑制NE释放,调节中枢NE浓度,使体温趋于恒定,减轻寒战中枢对体温降低的防御反应而有效抑制寒战。本研究发现,应用右美托咪定确实能降低长时间手术患者的术后寒颤发生率。
右美托咪定可以减慢心率,对血压的影响呈剂量依赖性的双相变化,大剂量直接激动血管平滑肌的α2、β受体产生短暂高血压,小剂量则产生轻度低血压(较基础血压下降10%~20%),故心动过缓和低血压也是右美托咪定较常见不良反应。术毕时阿片类镇痛药的应用,不但影响苏醒时间,而且还增加呼吸抑制的担心。右美托咪定0.4~0.7 μg/(kg·min)应用能减少七氟醚的用量,这和Fragen等[5]研究相似。另有研究[6]表明,右美托咪啶在0.5 μg/(kg·min)剂量下具有镇痛封顶作用。并且右美托咪啶在0.4~1.5 μg/(kg·min)范围内应用镇静强度相似,大剂量仅能延长恢复时间。故应用右美托咪啶0.4~0.7 μg/(kg·min)剂量较适合,此剂量对循环影响较小。在本研究中也发现,右美托咪定的降血压,减慢心率的不良反应较明显,需用阿托品纠正的例数和对照组有明显统计学意义。但尚在可控范围内。本研究也证明了这观点。
总之,右美托咪啶0.4~0.7 μg/(kg·min)应用,在腹部长时间手术患者术后寒颤预防方面效果显著;更能维持麻醉诱导、苏醒期的血流动力学平稳。术毕前约30 min停药,并不影响患者的苏醒时间,亦无明显的呼吸抑制作用,并且能降低吸入麻醉药的用量,但其能引起心率减慢,血压降低,术中应引起注意。
参考文献
[1] Tobias JD.Bradycardia during dexmedetomidine and therapeutic hypothermia[J].J Intensive Care Med,2008,23(6):403-408.
[2] Phan H,Hnahata MC.Clinical uses of dexmedetomidine in pediatric patients[J].Paediatr Drugs,2008,10(1):49-69.
[3] Doufas AG,Lin CM,Suleman ML,et al.Dexmedetomidine and meperidine additively reduce the shivering threshold in humans [J].Stroke,2003,34:1218-1223.
[4] Alfonsi P.Postanaesthetic shivering;epidemiology,pathophysiolog y,and approachesto prevention and management,Drugs,2001,61(1 5):2193-2205.
[5] Jaakola ML,Salonen M,Lehtinen R,et al.The analgesic action of dexmedetomidine--a novel alpha2-adrenoceptor—agonist in healthy volunteers[J].Pain,1991,46(3):281-285.
[6] 李彦文,欧阳文,汪赛赢,等.不同剂量右旋美托咪啶的镇静效应[J].临床麻醉学杂志,2010,26(7):580-582.
The Clinical Observation of Prevention of Postoperative Shivering of Dexmedetomidine to the Long Time Abdominal Operation under Genenal Anesthesia
YU Hong-biao
(Department of Anesthesiology, Chaoyang Central Hospital, Chaoyang 122000, China)
[Abstract]Objective To investigate the effect of Dexmedetomidine prophylactic long time of abdominal operation in patients with postoperative shi-vering. Methods 110 cases with abdominal operation were randomly divided into dexmedetomidine (D) group and normal saline (C) group with 55 cases in each group.The operation,s time of the two groups were exceed 4 hours. Two groups method of premedication and induction was the same. midazolam of 2 mg and atropine of 0.5 mg injected by intravenous before operating. The methal of induction was that the dose of propofol 1.5 mg/kg and sulfentanyl 0.3 μg/ kg or fentanyl 2 μg/kg and Cisatracurium besilate 0.2 mg/kg injected by intravenous. Continuous anesthesia was Sevoflurane inhalation that potency was 1%~4%, and remifentanil intravenous infusion that potency was 0.1 μg/(kg·min) and Cisatracurium besilate intermittent intravenous of 0.08 mg/(kg·h). The group D pumped dexmedetomidine that the dose was 0.5 μg/(kg·h) for 10 minutes before anesthesia induce, the maintenance dose was 0.4~0.7 μg/(kg·h)in operating. The group C given the same dose of normal saline at the same time . Recorded contents include: life index in the following time points before induced, intubation, 2 hour after anesthesia, before extubation, the time of extubation, 5 minute after extubation, and 10 minute; recovery time, sevolflurane dosage, the case of atropine application, entering the amount of liquid, peritoneal lavage fluid, and the postoperative shivering case after before extubation and 10 minute after extubation postoperative. Results It was no statistically significant differences betweeen two groups in operation time, amount of input liquid, amount of peritoneal lavage, recovery time, and temperature change. But in terms of intubation time, before extubation, extubation immediately, 5,10, 30 minutes, the change of MAP and heart rate in group D was more stable than C(P<0.05). And the dosage of sevoflurane application of D group was less than that of C group (P<0.05), the cases of atropine application were higher than that of C group (P<0.05); and the incidence of shivering of D group was significantly lower than that of C group (P<0.05). Conclusion Dexmedetomidine can effectively reduce the postoperative shivering incidence,and the dosage of sevolflurane application, and the hemodynamic fluctuations in the period of intubation and extubation to the patients that went through long time abdominal opration under general anesthesia.
[Key words]Dexmedetomidine; Abdominal operation; General anesthesia; Prevention; Postoperative shivering
中图分类号:R614
文献标识码:B
文章编号:1671-8194(2016)05-0001-03
