原位合成四氧化三锰处理模拟核电厂含Co2+放射性废水
2016-06-22詹瑛瑛蒋博博黄光团
詹瑛瑛, 张 禛, 蒋博博, 黄光团
(华东理工大学资源与环境工程学院,上海 200237)
原位合成四氧化三锰处理模拟核电厂含Co2+放射性废水
詹瑛瑛,张禛,蒋博博,黄光团
(华东理工大学资源与环境工程学院,上海 200237)
摘要:在硼酸体系中,以59Co作为模拟非放射性同位素研究了原位合成四氧化三锰处理模拟核电厂放射性废水中Co2+的工艺条件。考察了反应时间、n(Mn2+)∶n(Co2+)、空气流量、反应温度以及pH对出水Co2+质量浓度的影响,并由正交试验L9(43)优化工艺条件。研究表明:在废水Co2+初始质量浓度10 mg/L,硼酸质量浓度(以B计)1 000 mg/L条件下,最佳工艺条件为反应时间105 min、n(Mn2+)∶n(Co2+)=25∶1、空气流量0.7 L/min、反应温度65 ℃以及pH 10.5,在此条件下出水Co2+质量浓度约为5.68 ng/L,去除效率大于99.99%,产物经XRD分析证明沉渣为Mn3O4和CoMn2O4混合物。
关键词:原位合成; 四氧化三锰; 放射性废水; 正交试验; Co2+
随着核工业的迅速发展,越来越多的放射性废物产生,60Co是核电厂中常见的放射性元素,其毒性大、半衰期长、γ射线能量高,会对人体产生严重的危害。因此,系统研究模拟核电厂含Co2+放射性废水的处理方法具有重要意义。目前,国内外处理含Co2+放射性废水的方法有吸附法[1]、离子交换法[2-3]、膜分离法[4-5]和铁氧体法[6]等。传统方法在处理放射性废水方面均有其局限性,经济、有效的放射性废水处理方法仍需进一步研究。
通常认为四氧化三锰是一种混合氧化物,即MnO·Mn2O3,可写成[Mn2+][Mn3+]2O4,是正常的尖晶石结构。Mn2+占据四面体位置,Mn3+占据八面体位置[7],具有顺磁性和吸附性。当重金属离子的半径大小与Mn2+或Mn3+接近时,可代替它们进入四氧化三锰晶格中,得到稳定的晶相[8]。目前,已有四氧化三锰在重金属离子处理方面的报道[9-12]。另外,国内外学者利用原位合成工艺去除重金属离子的方法已有所应用,并具有明显优势。俞志敏等[13-15]采用原位合成方法高效去除了废水中Pb、Cd、Ni和Cr等重金属离子。因此,研究四氧化三锰原位合成方法处理模拟核电厂含Co2+放射性废水具有可行性。
核电厂放射性废水中含有作为中子吸收剂的硼酸。因此,本文在硼酸体系下,以59Co作为模拟非放射性同位素,研究两步法原位合成四氧化三锰处理核电厂放射性废水的工艺。两步法即二价锰离子经加碱生成氢氧化锰,再加入氧化剂氧化生成四氧化三锰。原位合成四氧化三锰对重金属离子有很强的亲和力,具有强吸附性能,可同时去除多种重金属离子,重金属离子可进入四氧化三锰晶格中而不易浸出造成二次污染,为减小放射性物质危害提供参考价值。
1实验部分
1.1实验试剂及仪器
氯化钴(CoCl2·6H2O),氯化锰(MnCl2·4H2O),硼酸(H3BO3),氢氧化钠(NaOH)均为分析纯,购自上海凌峰化学试剂有限公司;实验用水均为去离子水。
原子吸收光谱仪(novAA400,德国耶拿分析仪器公司);X 射线粉末多晶衍射仪(D/MAX 2550 VB/PC,Japan Rigaku);电感耦合等离子体质谱仪(NexION 300X,Perkin Elmer);电热恒温水槽(HH-1,上海比朗仪器有限公司);电子分析天平(AB104-N,梅特勒公司);pH计(PHS-25,上海精密科学仪器有限公司);循环水式真空泵(SHZ-D(Ⅲ),上海科兴仪器有限公司);气泵(ACO-9610,广东海利集团有限公司)和真空干燥箱(DZF-6030A,上海一恒科学仪器有限公司)。
1.2实验方法
实验中的模拟核电厂放射性废水由CoCl2· 6H2O、硼酸和去离子水配制。模拟废水中Co2+质量浓度为10 mg/L,硼酸质量浓度(以B计)为1 000 mg/L。实验中,含Co2+模拟废水中按一定投料加入锰盐,搅拌均匀后用2 mol/L NaOH溶液调节废水的pH,然后用气泵通入一定空气曝气,在一定温度的恒温水浴槽中反应一定时间。反应完成后用0.45 μm 滤膜进行抽滤分离,测定滤液 Co2+质量浓度,并以净化因子 DF 评价去除效果(DFCo=C0/Ci,C0为Co2+初始浓度,Ci为Co2+残余浓度),固体干燥后进行XRD分析。
1.3测定与表征
滤液中Co2+质量浓度采用电感耦合等离子体质谱仪(样品质量浓度<5 μg/L)和原子吸收光谱仪(样品质量浓度≥5 μg/L)进行测定。抽滤所得固体用去离子水进行多次洗涤,于105 ℃真空干燥箱中干燥5 h,并用XRD仪对样品进行分析(采用Cu靶,Ka射线,管电压40 kV,管电流100 mA,在10°~80°连续扫描)。
2实验结果与讨论
2.1反应时间影响
模拟废水的Co2+初始质量浓度为10 mg/L,按n(Mn2+)∶n(Co2+)=20∶1加入Mn2+,pH调节至9,以1.4 L/min空气流量进行曝气,反应温度为50 ℃。考察了反应时间为0.5、1.0、1.5、2.0、2.5、5.0 h时对Co2+去除效果的影响,并确定最佳反应时间,结果如图1所示。

图1 反应时间对Co2+去除效果的影响
Mn2+在碱性条件下生成Mn(OH)2,而氢氧化锰是一个相当不稳定的锰氧化物,在空气中加热时就转化为Mn3O4[16]。生成四氧化三锰以及并合、吸附Co2+需要一定的时间。反应时间不充足,Mn(OH)2氧化不够充分,不能充分并合、吸附Co2+,去除效果不好。由图1可知,反应时间在0.5~2.0 h内,Co2+去除率呈正线性相关,此后,去除率基本呈平稳状态。这是因为在反应2.0 h以内时,Mn2+不断转化为Mn(OH)2,并在氧化形成Mn3O4过程中并合或吸附Co2+,从而溶液中Co2+逐渐降低。而在反应2.0 h以后,Co2+去除效率的变化不大,对Co2+的并合、吸附作用大致饱和,大部分Co2+已被去除,去除率不随反应时间的延长而进一步降低,产物稳定。综合考虑,选择最佳反应时间为2.0 h,此时Co2+的去除率可达到99.86%。
2.2n(Mn2+)∶n(Co2+)影响
模拟废水的Co2+初始质量浓度为10 mg/L,按n(Mn2+)∶n(Co2+)为1∶1~40∶1加入Mn2+,调节pH至9,并以1.4 L/min空气流量在反应温度为50 ℃时进行曝气2 h。实验考察n(Mn2+)∶n(Co2+)对Co2+去除效果的影响,并确定Mn2+与Co2+的物质的量之比,结果如图2所示。

图2 n(Mn2+)∶n(Co2+)对Co2+去除效果的影响
四氧化三锰具有吸附性能,可通过加大Mn2+的投加量增加四氧化三锰而提高对Co2+的去除率。同时,锰钴产生共沉淀会消耗部分Mn2+,故需加大Mn2+的投加量。由图2可知,随着n(Mn2+)∶n(Co2+)的增大,Co2+的去除效率也随之增加。这是由于n(Mn2+)∶n(Co2+)越大,形成的四氧化三锰晶体越多,Co2+越容易被并合进入四氧化三锰晶体。且随着四氧化三锰增多,其对Co2+的吸附、并合也会增强,从而得到较高的去除效率;而n(Mn2+)∶n(Co2+)较小时,理论可生成的四氧化三锰较少,其对Co2+并合、吸附效果较差,不能达到吸附、并合的平衡。结果表明:n(Mn2+)∶n(Co2+)>20∶1时,虽然去除率略有提高,但提高效果不大,同时造成材料浪费,增加沉渣固体废物量,处理成本增加,不利于实际工程应用。综合考虑,选择n(Mn2+)∶n(Co2+)最佳值为20∶1,此时Co2+去除率可达到99.86%。
2.3空气流量影响
模拟废水的Co2+初始质量浓度为10 mg/L,按n(Mn2+)∶n(Co2+)=20∶1加入Mn2+,pH调节至9,并以0.2~2.5 L/min空气流量在反应温度为50 ℃时进行曝气2 h。实验考察空气流量对Co2+去除效果的影响,并确定最佳空气流量,结果如图3所示。

图3 空气流量对Co2+去除效果的影响
四氧化三锰的合成过程中,在同样氧化时间下,空气流量在很大程度上决定了氢氧化锰的氧化程度。合适的空气通入量可获得更多的四氧化三锰,从而充分发挥其优越的吸附性能。由图3可知,随着空气流量的增加,Co2+去除效率虽呈先上升后下降的趋势,在0.7 L/min时达到最高,但在0.4~2.1 L/min范围对去除率的影响并不大。空气流量过低时,氧化速度慢,在同样时间内产生的四氧化三锰的量偏少,从而影响去除效率。而空气流量过大时,虽然氧化速率加大使四氧化三锰颗粒增多,但曝气力度加大,会导致形成的四氧化三锰颗粒被破坏或者使Co2+解吸,从而降低Co2+的去除率。另外,空气流量过大,会使Mn3O4向MnOOH转化[17],这样也会降低四氧化三锰的作用。综合考虑,最佳空气流量为0.7 L/min,此时对Co2+的去除率可达到99.86%。
2.4温度影响
模拟废水的Co2+初始质量浓度为10 mg/L,按n(Mn2+)∶n(Co2+)=20∶1加入Mn2+,pH调节至9,并以1.4 L/min空气流量在反应温度为25~70 ℃时进行曝气2 h。实验考察反应温度对Co2+去除效果的影响,并确定最佳反应温度,结果如图4所示。

图4 反应温度对Co2+去除效果的影响
由图4可知,随着反应温度的上升,Co2+去除率呈上升趋势,但在60~70 ℃时去除率趋于平缓。这可能是因为四氧化三锰生成反应是吸热过程,温度越高越有利于四氧化三锰的形成,且随着温度升高,扩散过程加速,有效地促进了晶粒长大,同时也使晶粒之间的吸附作用增强。但温度也直接影响颗粒的大小,温度越高则得到的粒度越大[18],团聚现象有所增加,颗粒的比表面积下降引起吸附作用降低。另外,温度越高、空气或氧气在溶液中的溶解度小、空气氧化能力下降,四氧化三锰量降低而影响去除效率。综合考虑,最佳反应温度为60 ℃,此时对Co2+的去除率可达到99.91%。
2.5pH影响
模拟废水的Co2+初始质量浓度为10 mg/L,按n(Mn2+)∶n(Co2+)=20∶1加入Mn2+,pH调节至8~12,并以1.4 L/min空气流量在反应温度为50 ℃时进行曝气2 h。实验考察pH对Co2+去除效果的影响,并确定最佳pH,结果如图5所示。

图5 pH对Co2+去除效果的影响
pH影响Mn(OH)2的形成过程,并对产物二次团聚颗粒有较大的影响。若pH控制不当,难以形成四氧化三锰,沉降效果也有所降低,影响Co2+去除效果。由图5可知,pH在8~10内变化时,Co2+去除率呈上升趋势。这可能是因为pH与Mn2+氧化速度呈正相关[19],而锰离子的氧化速度直接影响到Co2+的去除率,pH越大越好。但当pH>10时,Co2+去除率反而下降,这可能是因为pH的升高使Co2+在水溶液中的羟基配离子形式产生变化,生成Co(OH)3-、Co(OH)42-等水解产物[20],反而不容易被并合或吸附。另外,pH控制了Mn(OH)2在溶液中的过饱和度,从而影响晶体的成核与成长速度,对Co2+去除率产生一定制约作用。综合考虑,最佳pH为10,此时对Co2+的去除率可达到99.97%。
2.6正交试验及结果
通过单因素试验研究发现空气流量在较宽范围内对Co2+的去除率影响不大,且最佳空气流量附近Co2+去除率波动不大,故在试验条件优化时不考虑空气流量。本实验通过四因素三水平L9(34)正交表进行优化试验,在Co2+进水10 mg/L、硼酸质量浓度为1 000 mg/L、空气流量为0.7 L/min的条件下,考察了反应时间(A)、pH(B)、n(Mn2+)∶n(Co2+)(C)、温度(D)对原位生成四氧化三锰处理含Co2+放射性废水效果的影响。表1所示为四因素三水平正交表,正交试验结果及分析如表2所示。

表1 四因素三水平正交表
极差大小反映各因素对出水Co2+质量浓度的影响程度,R值越大影响越强烈。通过对正交试验结果进行极差分析知,4个因素对出水效果的影响大小为B>D>A>C,也就是pH>温度>反应时间>n(Mn2+)∶n(Co2+),得到最优组合可知pH 10.5,温度65 ℃,反应时间105 min以及n(Mn2+)∶n(Co2+)为25∶1。在此最佳工艺条件下,当进水质量浓度为10 mg/L,ρ(H3BO3)=1 000 mg/L时,Co2+出水质量浓度为5.68 ng/L,此时Co2+的去除率大于99.99%,净化因子(DFCo)达到1.761×106。由此可知,此方法确实可有效去除Co2+。
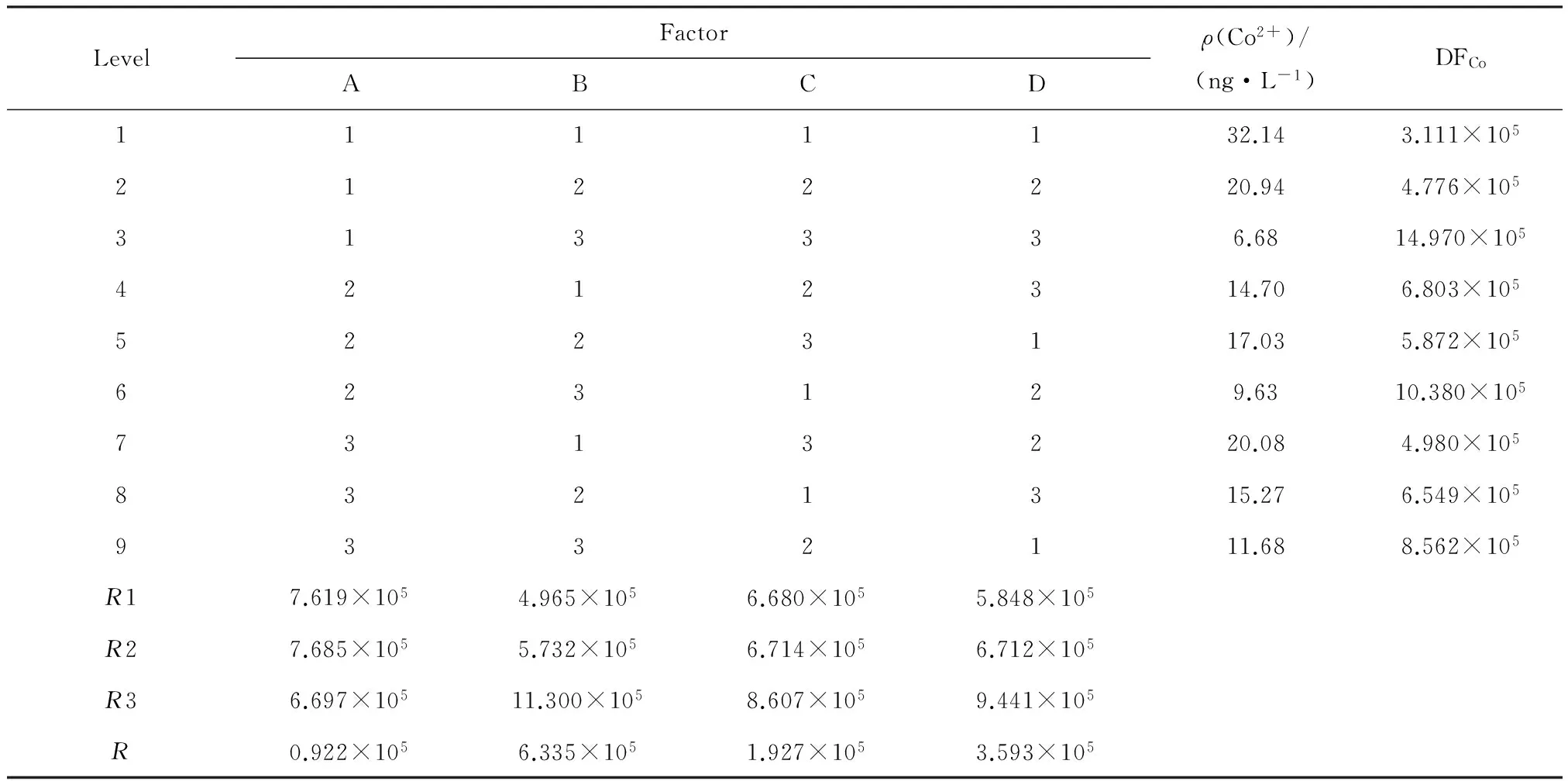
表2 正交试验结果
2.7XRD分析
为了确定产物是否为四氧化三锰或者钴锰氧化物,采用XRD分析了最佳反应条件下原位生成四氧化三锰沉渣中的成分。在所确定的最佳工艺条件为反应时间为105 min,空气通入量为0.7 L/min,pH为10.5,反应温度为65 ℃,n(Mn2+)∶n(Co2+)为25∶1条件下,处理10 mg/L含Co2+废水,抽滤并将固体多次洗涤,于105 ℃真空干燥箱中干燥5 h制得XRD样品。
由图6可知,样品 XRD图谱出峰明显,基线稳定,结晶度好。经过与标准卡片对比,该图谱与Mn3O4和CoMn2O4(Mn3O4、CoMn2O4对应的卡片号分别为PDF24-0734、PDF01-1126)相符合。由固体产物XRD图谱可看出,虽然两种物质衍射峰接近,但由峰形可区分两者衍射峰,故可认为沉渣是Mn3O4和CoMn2O4混合物。说明在实验过程中不仅产生了Mn3O4,并有部分Co2+可能进入晶格形成CoMn2O4,因此可利用此过程去除模拟放射性元素钴。

图6 固体产物XRD图
3结论
(1)在硼酸体系采用原位合成四氧化三锰法处理含Co2+放射性废水效果良好,反应时间、pH、温度以及n(Mn2+)∶n(Co2+)对处理效果影响较大,且影响大小为pH>温度>反应时间>n(Mn2+)∶n(Co2+)。
(2)在废水中Co2+质量浓度10 mg/L,硼酸质量浓度(以硼计)1 000 mg/L条件下,最佳工艺条件为反应时间105 min、n(Mn2+)∶n(Co2+)=25∶1、空气流量0.7 L/min、反应温度65 ℃以及pH=10.5,在此条件下出水中Co2+质量浓度约为5.68 ng/L,去除效率大于99.99%,净化因子DFCo达到1.761×106。在最佳工艺条件下,经XRD分析沉渣组成为Mn3O4和CoMn2O4的混合物。
参考文献:
[1]NISHAD P A,BHASKARAPILLAI A,VELMURUGAN S,etal.Cobalt (Ⅱ) imprinted chitosan for selective removal of cobalt during nuclear reactor decontamination[J].Carbohydrate Polymers,2012,87(4):2690-2696.
[2]PLECAS I,PAVLOVIC R,PAVLOVIC S.Leaching behavior of 60 Co and 137 Cs from spent ion exchange resins in cement-bentonite clay matrix[J].Journal of Nuclear Materials,2004,327(2):171-174.
[3]MUSTAFA Y A,ZAITER M J.Treatment of radioactive liquid waste (Co-60) by sorption on Zeolite Na-A prepared from Iraqi kaolin[J].Journal of Hazardous Materials,2011,196(30):228-233.
[4]CHMIELEWSKI A G,HARASIMOWICZ M,ZAKRZEWS-KA-TRZNADEL G.Membrane technologies for liquid radioactive waste treatment[J].Czechoslovak Journal of Physics,1999,49(1):979-985.
[5]王欣鹏,蒯琳萍,车俊霞.反渗透技术处理模拟核电站放射性废水中的钴[J].核化学与放射化学,2011,33(2):114-118.
[6]陈希飞.铁氧体原位共沉淀法处理核电厂放射性废液技术研究[D].上海:华东理工大学,2014.
[7]杨秀梅.四氧化三锰的制备工艺及机理探讨[D].贵阳:贵州大学,2008.
[8]匡莉莉.掺杂锰氧化物微纳米结构的制备及其性能研究[D].南宁:广西大学,2013.
[9]FENG X H,ZHAI L M,TAN W F,etal.Adsorption and redox reactions of heavy metals on synthesized Mn oxide minerals[J].Environmental Pollution,2007,147(2):366-373.
[10]PARSONS J G,LOPEZ M L,PERALTA-VIDEA J R,etal.Determination of arsenic(Ⅲ) and arsenic(V) binding to microwave assisted hydrothermal synthetically prepared Fe3O4,Mn3O4and MnFe2O4nanoadsorbents[J].Microchemical Journal,2009,91(1):100-106.
[11]SILVA G C,ALMEIDA F S,FERREIRA A M,etal.Preparation and application of a magnetic composite (Mn3O4/Fe3O4) for removal of As(Ⅲ) from aqueous solutions[J].Materials Research,2012,15(3):403-408.
[12]CANTU Y,REMES A,REYNA A,etal.Thermodynamics,kinetics,and activation energy studies of the sorption of chromium(Ⅲ) and chromium(VI) to a Mn3O4nanomaterial.[J].Chemical Engineering Journal,2014,254(7):374-383.
[13]QIN Q,WANG Q,FU D,etal.An efficient approach for Pb (II) and Cd (II) removal using manganese dioxide formed in situ[J].Chemical Engineering Journal,2011,172(1):68-74.
[14]俞志敏,刘景丽,陈天虎,等.原位合成层状双氢氧化物处理含镍废水[J].硅酸盐学报,2007,34(11):1420-1424.
[15]TU C H,HUANG Y J,TSAI C H,etal.InsituXANES study of removal of heavy metals from laboratory wasteliquid by the ferrite process[J].Journal of Electron Spectroscopy and Related Phenomena,2007,156:228-231.
[16]BASTAMI T R,ENTEZARI M H.Sono-synthesis of Mn3O4nanoparticles in different media without additives[J].Chemical Engineering Journal,2010,164(1):261-266.
[17]KIRILLOV S A,ALEKSANDROVA V S,LISNYCHA T V,etal.Oxidation of synthetic hausmannite to manganite[J].Journal of Molecular Structure,2009,928(1):89-94.
[18]索鎏敏,华宁,韩英,等.氧化沉淀法制备纳米级Mn3O4粉体及影响因素[J].微纳电子技术,2009,46(1):23-28.
[19]邹兴,孙宁磊,王国承.用空气直接氧化游离二价锰离子制备高纯四氧化三锰[J].北京科技大学学报,2008,29(12):1250-1253.
[20]田庆华,辛云涛,郭学益,等.Co2+-H2O 体系羟基配离子配位平衡[J].中国有色金属学报,2014,24(7):1901-1906.
Treatment of Simulated Radioactive Wastewater Containing Co2+in Nuclear Power Plant by In-situ Synthesis Process of Mn3O4
ZHAN Ying-ying,ZHANG Zhen,JIANG Bo-bo,HUANG Guang-tuan
(School of Resources and Environmental Engineering,East China University of Science and Technology,Shanghai 200237,China)
Abstract:Using59Co as the simulated radioactive isotopes,the removal of Co2+from the simulated radioactive wastewater with boric acid in nuclear power plant by in-situ synthesis of Mn3O4 was studied.The effects of reaction time,n(Mn2+)∶n(Co2+),air flow,reaction temperature and pH on the Co2+concentration in the effluent were investigated.An orthogonal experiment table L9(43) was used to optimize the process parameters.When the wastewater contained 10 mg/L Co2+and 1 000 mg/L boric acid (as B),the optimal process was as follows:the reaction time 105 min,n(Mn2+)∶n(Co2+)=25∶1,air flow 0.7 L/min,reaction temperature 65 ℃ and pH 10.5.Under the optimal condition,the effluent concentration of Co2+was 5.68 ng/L,the removal rate was more than 99.99%.XRD analysis proved that the sediment was the mixture of Mn3O4 and CoMn2O4.
Key words:in-situ synthesis; Mn3O4; radioactive wastewater; orthogonal experiment; cobalt ion
收稿日期:2015-08-06
作者简介:詹瑛瑛(1990-),女,浙江杭州人,硕士生,研究方向为水污染控制。E-mail:wuyyz2010@163.com 通信联系人:黄光团,E-mail:gthuang@ecust.edu.cn
文章编号:1006-3080(2016)02-0210-06
DOI:10.14135/j.cnki.1006-3080.2016.02.009
中图分类号:X591
文献标志码:A
